文档内容
2.3化学反应的方向(分层作业)
1.已知凡气体分子总数增多的反应一定是熵增大的反应。一定条件下,下列反应不能自发进行的是
A.2O(g)=3O(g) ΔH<0 B.2CO(g)=2C(s)+O (g) ΔH>0
3 2 2
C.N(g)+3H(g)⇌2NH (g) ΔH<0 D.CaCO (s)=CaO(s)+CO (g) ΔH>0
2 2 3 3 2
2.氢气可用于制备HO 已知:①H(g)+A(l)=B(l) ΔH;②O(g)+B(l)=A(l)+HO(l) ΔH,其中A、B均为
2 2. 2 1 2 2 2 2
有机物,两个反应均为自发反应,则反应H(g)+O(g)=HO(l)的ΔH
2 2 2 2
A.大于0 B.小于0
C.等于0 D.无法判断
3.下列变化的熵变大于零的是
A.2HO(l)=2H O(l)+O(g)
2 2 2 2
B.CO(g)→CO (s)
2 2
C.NaOH(aq)+HCl(aq)=NaCl(aq)+HO(l)
2
D.NH (g)+HCl(g)=NH Cl(s)
3 4
4.下列关于自发反应的叙述中,正确的是
A.自发反应的逆过程在相同条件下也必定是自发的
B.铁在潮湿的空气中生锈属于非自发反应
C.自发过程可以是物理过程,不一定是自发反应,而自发反应一定是自发过程
D.自发反应与外界条件无关
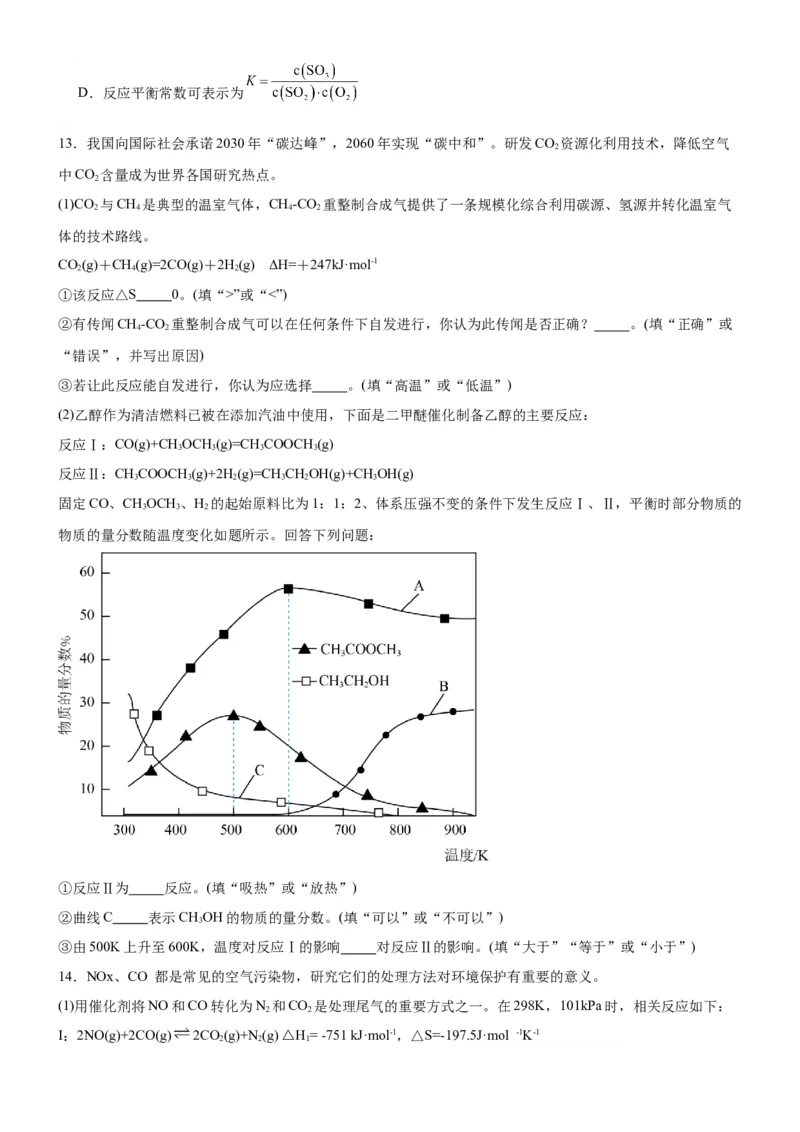
5.我国科学家在碳资源化利用方面取得突破性进展,如合成 的反应为
,其能量变化示意图如下。下列有关该反应的叙述错误的是
A.该反应在任何温度下都能自发进行
B.该反应的自发性与焓变和熵变都有关
C.该反应的焓变和熵变与物质的聚集状态都有关
D.使用催化剂能加快反应速率,但焓变不会变化6.下列说法正确的是。
A.常温常压下, 、 的溶解焓变相近, ;
,则
B.
C.非自发进行的反应一定不可能发生
D.需要加热才能进行的过程肯定不是自发过程
7.已知甲烷隔绝空气在不同温度下有可能发生如下两个反应:①CH(g)=C(s)+2H(g),②2CH(g)=C H(g)+
4 2 4 2 2
3H(g)。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆查到了如下热力学数据:
2
①的ΔH(298 K)=74.848 kJ·mol-1,ΔS(298 K)=80.674 J·mol-1·K-1
②的ΔH(298 K)=376.426 kJ·mol-1,ΔS(298 K)=220.211 J·mol-1·K-1
已知焓变和熵变随温度变化很小。请帮助这位同学考虑如下问题:
(1)判断②反应是高温自发还是低温自发: (填“高温”或“低温”)。
(2)通过计算判断①反应在常温下能否自发进行: 。
(3)求算制取炭黑的允许温度范围: 。
(4)为了提高甲烷的碳化程度,你认为下面四个温度中最合适的是___________(填字母)。
A.905.2 K B.927 K
C.1 273 K D.2 000 K
8.已知甲烷隔绝空气在不同温度下有可能发生如下两个裂解反应:①CH(g)→C(s)+2H (g);
4 2
②2CH(g)→C H(g)+3H(g)某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆中查到了
4 2 2 2
如下热力学数据:
反应①的ΔH(298K)=+74.848kJ·mol-1,ΔS(298K)=+80.674J·mol-1·K-1。
反应②的ΔH(298K)=+376.426kJ·mol-1,ΔS(298K)=+220.211J·mol-1·K-1。
已知焓变和熵变随温度变化很小。请参考上述信息,回答下列问题:
(1)这两个反应在 (填“高温”或“低温”)下自发进行。
(2)反应①在常温下 (填“能”或“不能”)自发进行。
(3)制取炭黑的允许温度范围为 。
(4)为了提高甲烷的炭化程度,下面四个温度中最合适的是___________(填字母)
A.905.2K B.927K C.1273K D.2000K
9.回答下列问题。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO,发生反应:2CO(g)=2CO(g)+O(g),该反应的
2 2 2
ΔH (填“>”“<”或“=”)0,ΔS (填“>”“<”或“=”)0,在低温下,该反应 (填“能”或“不能”)自发进行。
(2)已知在100kPa、298K时石灰石分解反应CaCO (s)=CaO(s)+CO(g)的ΔH>0,ΔS>0,则:
3 2
①该反应常温下 (填“能”或“不能”)自发进行。
②据本题反应数据分析,温度 (填“能”或“不能”)成为反应方向的决定因素。
(3)已知下列数据:CaO(s)+SO (g)=CaSO (s) ΔH=-401.9 kJ·mol-1
3 4
CaSO(s) CaO(s) SO (g)
4 3
S/J·mol-1·K-
107.0 39.75 256.65
1
用CaO(s)吸收高炉废气中的SO 气体 (填“能”或“不能”)防止SO 污染环境。
3 3
10.在相同条件下研究催化剂Ⅰ、Ⅱ对反应 的影响,各物质浓度c随反应时间t的变化的部分曲线如图,
下列说法正确的是
A.对于不能自发发生的反应,可寻找高效催化剂使其发生
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅰ时X的浓度随t的变化
D.使用催化剂时,能提高产物的产率
11.下列关于化学反应方向的叙述不正确的是
A.化学反应的方向受焓变、熵变、温度影响
B.将氯化铵晶体与氢氧化钡晶体置于小烧杯中混合,产生刺激性气体,说明该反应低温自发,高温非自发
C.常温下很容易发生反应4Fe(OH) (s)+O(g)+2HO(l)=4Fe(OH) (s),说明该反应ΔH< 0
2 2 2 3
D.NaHCO (s) + HCl(aq) = NaCl(aq) + CO (g) + HO(l) ΔH = +31.4 kJ·mol-1,反应能自发进行的原因是体系
3 2 2
有自发地向熵增方向转变的倾向
12.下列关于反应2SO (g)+O(g) 2SO (g)说法正确的是
2 2 3
A.该反应的△S>0
B.将部分SO 分离出来,v(正)将增大
3
C.使用适当催化剂能降低反应的活化能D.反应平衡常数可表示为
13.我国向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。研发CO 资源化利用技术,降低空气
2
中CO 含量成为世界各国研究热点。
2
(1)CO 与CH 是典型的温室气体,CH-CO 重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气
2 4 4 2
体的技术路线。
CO(g)+CH(g)=2CO(g)+2H(g) ΔH=+247kJ·mol-1
2 4 2
①该反应△S 0。(填“>”或“<”)
②有传闻CH-CO 重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确? 。(填“正确”或
4 2
“错误”,并写出原因)
③若让此反应能自发进行,你认为应选择 。(填“高温”或“低温”)
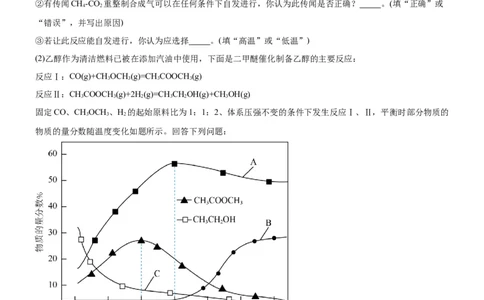
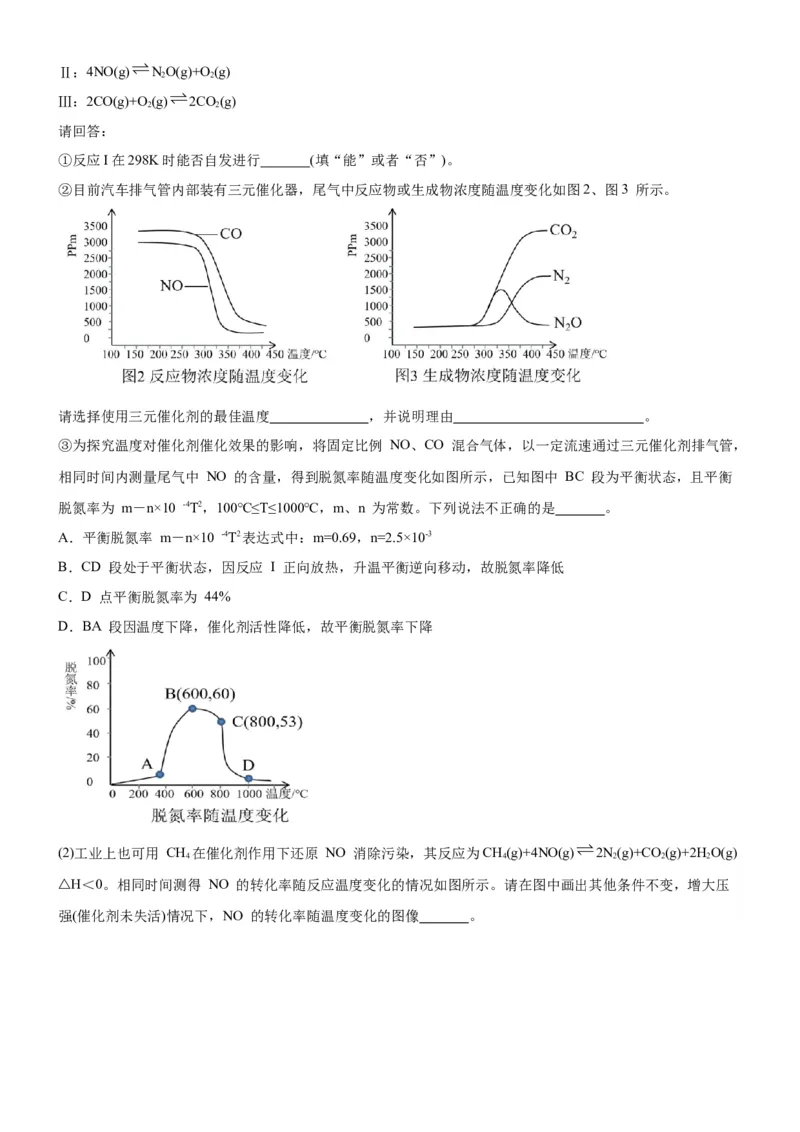
(2)乙醇作为清洁燃料已被在添加汽油中使用,下面是二甲醚催化制备乙醇的主要反应:
反应Ⅰ:CO(g)+CHOCH (g)=CH COOCH (g)
3 3 3 3
反应Ⅱ:CHCOOCH (g)+2H(g)=CH CHOH(g)+CH OH(g)
3 3 2 3 2 3
固定CO、CHOCH 、H 的起始原料比为1:1:2、体系压强不变的条件下发生反应Ⅰ、Ⅱ,平衡时部分物质的
3 3 2
物质的量分数随温度变化如题所示。回答下列问题:
①反应Ⅱ为 反应。(填“吸热”或“放热”)
②曲线C 表示CHOH的物质的量分数。(填“可以”或“不可以”)
3
③由500K上升至600K,温度对反应Ⅰ的影响 对反应Ⅱ的影响。(填“大于”“等于”或“小于”)
14.NOx、CO 都是常见的空气污染物,研究它们的处理方法对环境保护有重要的意义。
(1)用催化剂将NO和CO转化为N 和CO 是处理尾气的重要方式之一。在298K,101kPa时,相关反应如下:
2 2
I:2NO(g)+2CO(g) 2CO(g)+N(g) △H = -751 kJ·mol-1,△S=-197.5J·mol -1K-1
2 2 1Ⅱ:4NO(g) NO(g)+O (g)
2 2
Ⅲ:2CO(g)+O(g) 2CO(g)
2 2
请回答:
①反应I在298K时能否自发进行 (填“能”或者“否”)。
②目前汽车排气管内部装有三元催化器,尾气中反应物或生成物浓度随温度变化如图2、图3 所示。
请选择使用三元催化剂的最佳温度 ,并说明理由 。
③为探究温度对催化剂催化效果的影响,将固定比例 NO、CO 混合气体,以一定流速通过三元催化剂排气管,
相同时间内测量尾气中 NO 的含量,得到脱氮率随温度变化如图所示,已知图中 BC 段为平衡状态,且平衡
脱氮率为 m-n×10 -4T2,100℃≤T≤1000℃,m、n 为常数。下列说法不正确的是 。
A.平衡脱氮率 m-n×10 -4T2表达式中:m=0.69,n=2.5×10-3
B.CD 段处于平衡状态,因反应 I 正向放热,升温平衡逆向移动,故脱氮率降低
C.D 点平衡脱氮率为 44%
D.BA 段因温度下降,催化剂活性降低,故平衡脱氮率下降
(2)工业上也可用 CH 在催化剂作用下还原 NO 消除污染,其反应为CH(g)+4NO(g) 2N(g)+CO (g)+2HO(g)
4 4 2 2 2
△H<0。相同时间测得 NO 的转化率随反应温度变化的情况如图所示。请在图中画出其他条件不变,增大压
强(催化剂未失活)情况下,NO 的转化率随温度变化的图像 。(3)一种焦炭催化 CO 还原 NO 反应的历程如下,请补充完整相关基元反应(“*”表示吸附态):
A.NO NO*
B.2NO* ON-NO*
C.
D.ON-NO-CO* ON-N*+CO
2