文档内容
第六章 化学反应与能量
第一节 化学反应的速率与限度 课时作业
第一课时 化学反应的速率
基础达标
1.下列关于化学反应速率的说法不正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示
C.在同一个反应中,各物质的反应速率之比等于反应方程式中对应物质的化学计量
数之比
D.化学反应速率的常用单位有 mol·L-1·s-1和 mol·L-1·min-1
2.下列关于化学反应速率的说法正确的是( )
A.对于任何化学反应来说,反应速率越大,反应现象就越明显
B.化学反应速率通常表示一定时间内任何一种反应物浓度的减少或任何一种生成物
浓度的增加
C.化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1
D.根据化学反应速率的大小可以知道化学反应进行的快慢
3.下列说法正确的是( )
A.镁与盐酸反应的速率一定比铝快
B.比较Mg和Al与盐酸的反应速率时,必须在相同的条件下进行
C.镁与盐酸的反应,可以用单位时间内镁的物质的量的变化表示镁的反应速率
D.只有在溶液中的反应才能计算化学反应速率
4.在氧化钕(Nd O)等稀土催化剂的作用下可发生反应:4CO+2NO N +4CO ,
2 3 2 2 2
若该反应的反应速率分别用v(CO)、v(NO )、v(N )、v(CO)表示,则下列关系正确的是(
2 2 2
)
A. v(N )=v(CO) B. v(NO )=v(CO) C. v(N )=v(CO) D. v(CO)=
2 2 2 2 2
v(NO )
2
5.在t℃,在4个均为 的密闭容器中分别进行合成氨反应:N(g)+3H(g)
2 2
2NH (g)。根据在相同时间内测定的结果,判断反应进行快慢的顺序为( )
3
a. b.c. d.
A.a>c>b>d B.a>c=d>b C.a>b>c>d D.
a>d>c>b
6.反应4A(s)+3B(g) 2C(g)+D(g),经过2 min后B的浓度减小0.6 mol/L。下列说
法正确的是( )
A.用D表示的反应速率是0.1 mol·L-1·min-1
B.用A、B、C、D分别表示反应的速率,其比值是4∶3∶2∶1
C.在2 min末,物质B的反应速率是0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的反应速率的值都是逐渐增大的
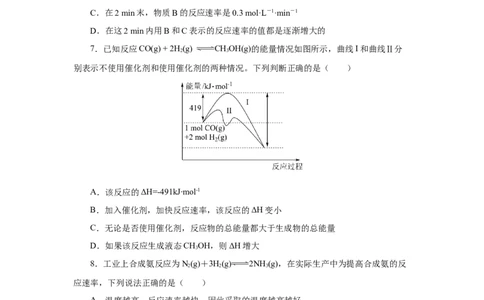
7.已知反应CO(g) + 2H (g) CHOH(g)的能量情况如图所示,曲线І和曲线Ⅱ分
2 3
别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
A.该反应的ΔH=-491kJ‧mol-1
B.加入催化剂,加快反应速率,该反应的ΔH变小
C.无论是否使用催化剂,反应物的总能量都大于生成物的总能量
D.如果该反应生成液态CHOH,则ΔH增大
3
8.工业上合成氨反应为N(g)+3H(g) 2NH (g),在实际生产中为提高合成氨的反
2 2 3
应速率,下列说法正确的是( )
A.温度越高,反应速率越快,因此采取的温度越高越好
B.压强越高,反应速率越快,因此采取的压强越高越好
C.催化剂能加快反应速率,因此可选用适当的催化剂
D.可向容器中加入一定量的水蒸气,使氨气溶解以提高反应速率
9.下表中是各组反应的反应物和温度,反应刚开始时,放出H 速率最快的是
2
( )
金属(粉末状)/mol 酸的浓度及体积 反应温度A Mg 0.1 6mol•L﹣1硝酸 10mL 60℃
B Mg 0.1 3mol•L﹣1盐酸 10mL 60℃
C Fe 0.1 3mol•L﹣1盐酸 10mL 60℃
D Mg 0.1 3mol•L﹣1硫酸 10mL 60℃
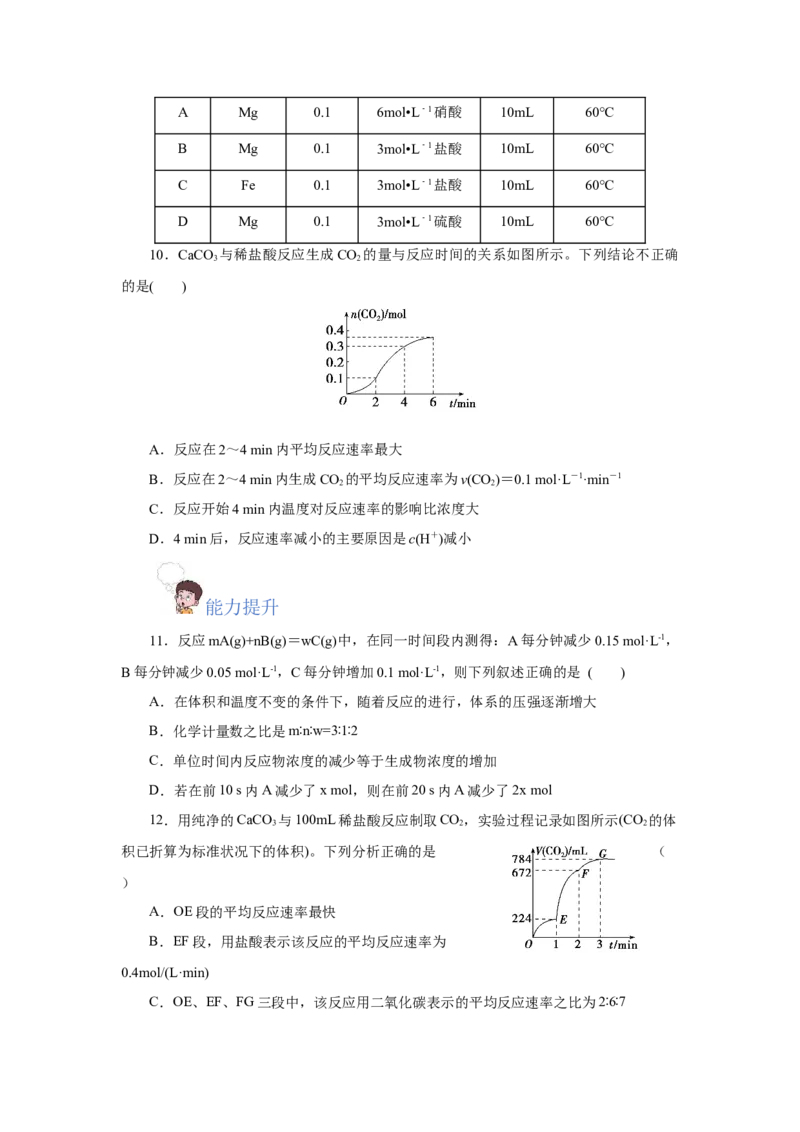
10.CaCO 与稀盐酸反应生成CO 的量与反应时间的关系如图所示。下列结论不正确
3 2
的是( )
A.反应在2~4 min内平均反应速率最大
B.反应在2~4 min内生成CO 的平均反应速率为v(CO)=0.1 mol·L-1·min-1
2 2
C.反应开始4 min内温度对反应速率的影响比浓度大
D.4 min后,反应速率减小的主要原因是c(H+)减小
能力提升
11.反应mA(g)+nB(g)=wC(g)中,在同一时间段内测得:A每分钟减少0.15 mol·L-1,
B每分钟减少0.05 mol·L-1,C每分钟增加0.1 mol·L-1,则下列叙述正确的是 ( )
A.在体积和温度不变的条件下,随着反应的进行,体系的压强逐渐增大
B.化学计量数之比是m∶n∶w=3∶1∶2
C.单位时间内反应物浓度的减少等于生成物浓度的增加
D.若在前10 s内A减少了x mol,则在前20 s内A减少了2x mol
12.用纯净的CaCO 与100mL稀盐酸反应制取CO,实验过程记录如图所示(CO 的体
3 2 2
积已折算为标准状况下的体积)。下列分析正确的是 (
)
A.OE段的平均反应速率最快
B.EF段,用盐酸表示该反应的平均反应速率为
0.4mol/(L·min)
C.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2∶6∶7D.F点收集到的CO 的量最多
2
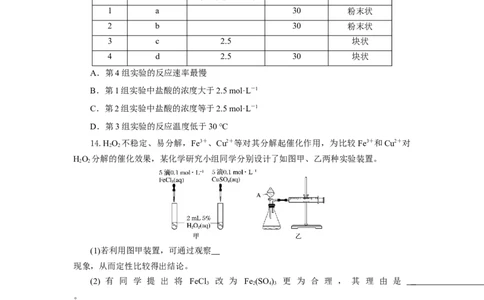
13.等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生
气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法一定不正确的是( )
组别 对应曲线 c(HCl)/(mol·L-1) 反应温度/℃ 铁的状态
1 a 30 粉末状
2 b 30 粉末状
3 c 2.5 块状
4 d 2.5 30 块状
A.第4组实验的反应速率最慢
B.第1组实验中盐酸的浓度大于2.5 mol·L-1
C.第2组实验中盐酸的浓度等于2.5 mol·L-1
D.第3组实验的反应温度低于30 ℃
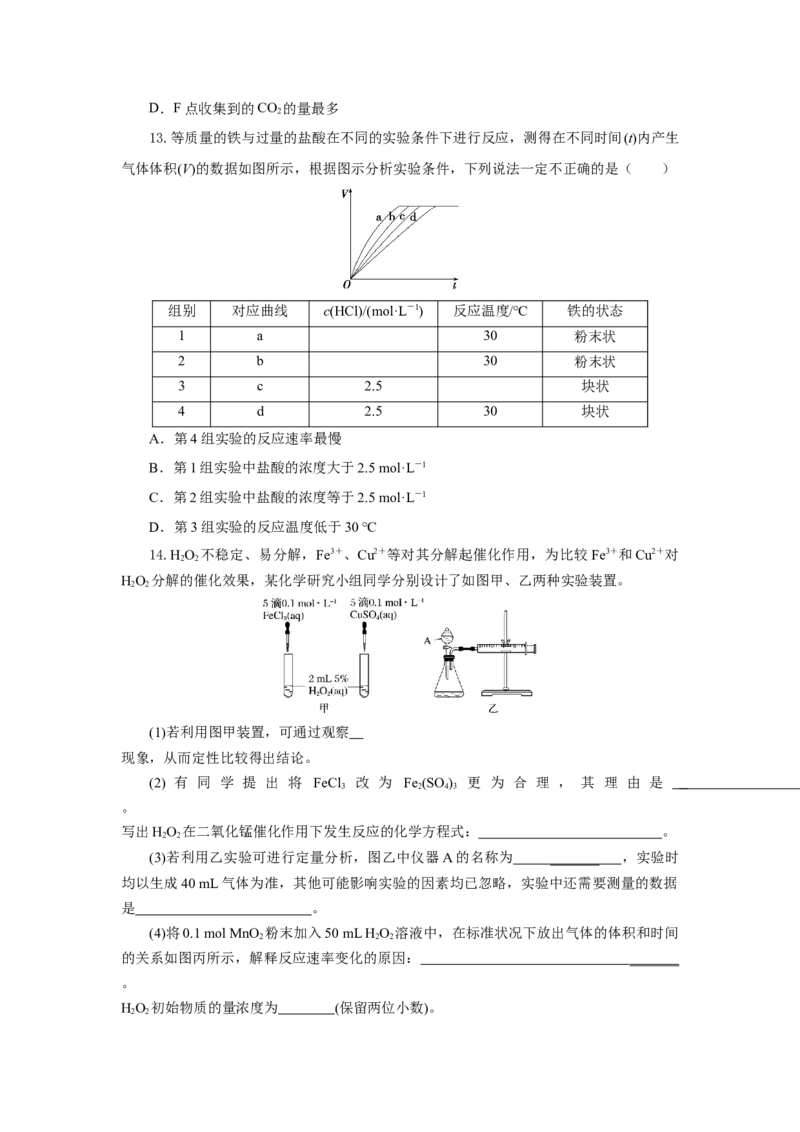
14.HO 不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对
2 2
HO 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
2 2
(1)若利用图甲装置,可通过观察
现象,从而定性比较得出结论。
(2) 有 同 学 提 出 将 FeCl 改 为 Fe (SO ) 更 为 合 理 , 其 理 由 是
3 2 4 3
。
写出HO 在二氧化锰催化作用下发生反应的化学方程式: 。
2 2
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为 ______ _ ,实验时
均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据
是 。
(4)将0.1 mol MnO 粉末加入50 mL H O 溶液中,在标准状况下放出气体的体积和时间
2 2 2
的关系如图丙所示,解释反应速率变化的原因: ______ _
。
HO 初始物质的量浓度为 (保留两位小数)。
2 2丙
直击高考
15.实验探究HO 分解速率影响因素。HO 浓度在不同条件下随时间变化的曲线如图
2 2 2 2
所示。实验分组及反应条件分别为:
分组 温度/°C pH c(Mn2+)/mol·L-1
① 60 ≈7 0.00002
② 60 12 0
③ 60 13 0
④ 60 11 0.00002
⑤ 70 13 0
下列说法不正确的是( )
A.实验①、④说明中性条件下,少量Mn2+对HO 分解的影响不大
2 2
B.实验②、③说明其他条件相同时,溶液碱性越强,HO 分解速率越大
2 2
C.实验③、⑤说明温度升高可以增大HO 分解速率
2 2
D.实验④反应到40min时的化学反应速率为0.0225mol·L-1·min-1
16.某研究性学习小组利用HC O 溶液和酸性KMnO 溶液之间的反应来探究“外界
2 2 4 4
条件改变对化学反应速率的影响”,实验如下:(不考虑溶液混合引起的体积变化)
参加反应的物质
溶液颜色褪
实验 实验温 KMnO 4 溶液(含硫酸) H 2 C 2 O 4 溶液 H 2 O 至无色时所
序号
度/K
需时间/s
V/mL c/mol·L-1 V/mL c/mol·L-1 V/mL
A 293 2.0 0.02 4.0 0.1 0 6
B T 2.0 0.02 3.0 0.1 V 8
1 1C 313 2.0 0.02 V 0.1 1.0 t
2 1
(1)通过实验A、B,可探究出浓度的改变对反应速率的影响,其中V=___________,
1
T1=___________,通过实验___________可探究出温度变化对化学反应速率的影响。
(2)C组实验中溶液褪色时间t1___________(填“>”或“<”或“=”)8s,C组实验的
反应速率v(KMnO)=___________。(用含有t 的式子表示)
4 1
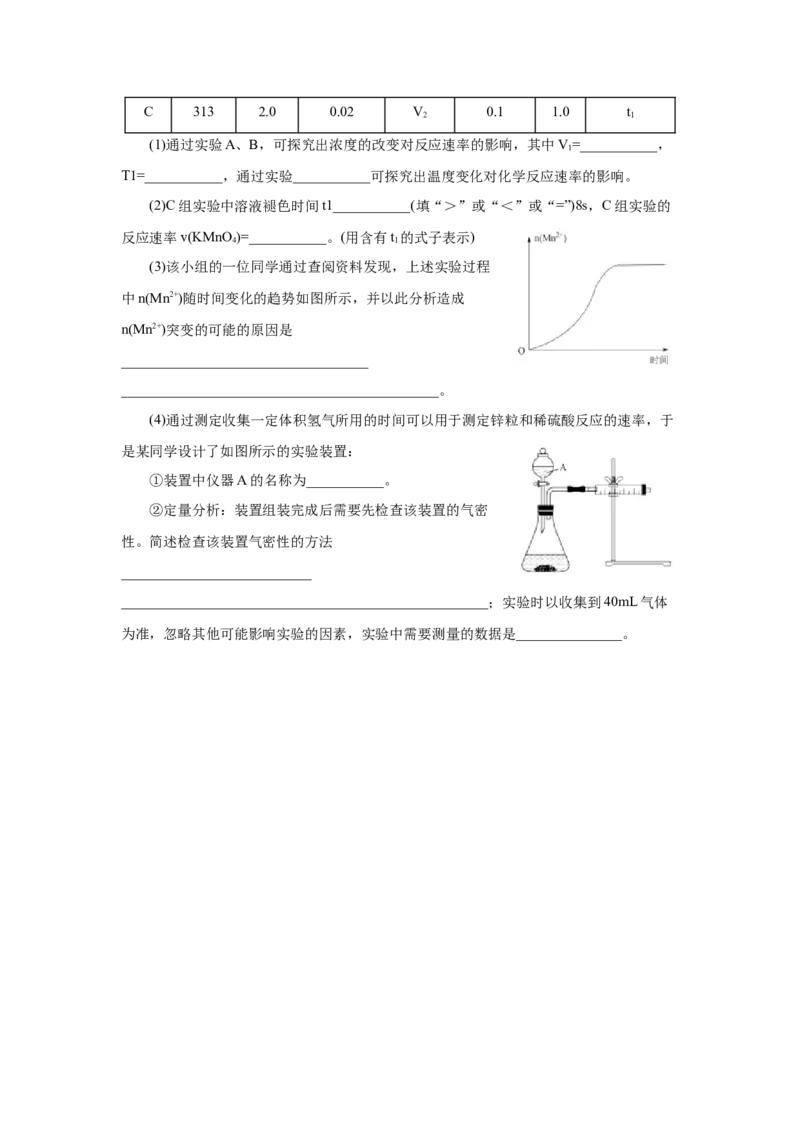
(3)该小组的一位同学通过查阅资料发现,上述实验过程
中n(Mn2+)随时间变化的趋势如图所示,并以此分析造成
n(Mn2+)突变的可能的原因是
___________________________________
_____________________________________________。
(4)通过测定收集一定体积氢气所用的时间可以用于测定锌粒和稀硫酸反应的速率,于
是某同学设计了如图所示的实验装置:
①装置中仪器A的名称为___________。
②定量分析:装置组装完成后需要先检查该装置的气密
性。简述检查该装置气密性的方法
___________________________
____________________________________________________;实验时以收集到40mL气体
为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_______________。