文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第一课时 化学反应与热能
【学习目标】1.通过实验探究、讨论交流,感受化学反应中的能量变化,知道常见的吸热反应和放
热反应,树立物质变化中伴随着能量变化的观念。
2.通过思考讨论、微观分析,能从反应物和生成物具有的能量、化学键变化两个角度理解化学反应中
能量变化的主要原因。
3.通过阅读思考、实例分析,从本质上认识物质变化与能量变化的关系,了解人类利用的主要能源及
新能源,分析能源的利用对自然环境及社会发展的影响。
【学习重点】化学键与化学反应能量变化的关系、吸热反应和放热反应
【学习难点】理解化学反应中能量变化的主要原因
【课前预习】
旧知回顾:1.请举例说明什么是放热反应和吸热反应?
2.什么是化石燃料?请举例说明人类对化学反应中能量的利用情况有哪些?
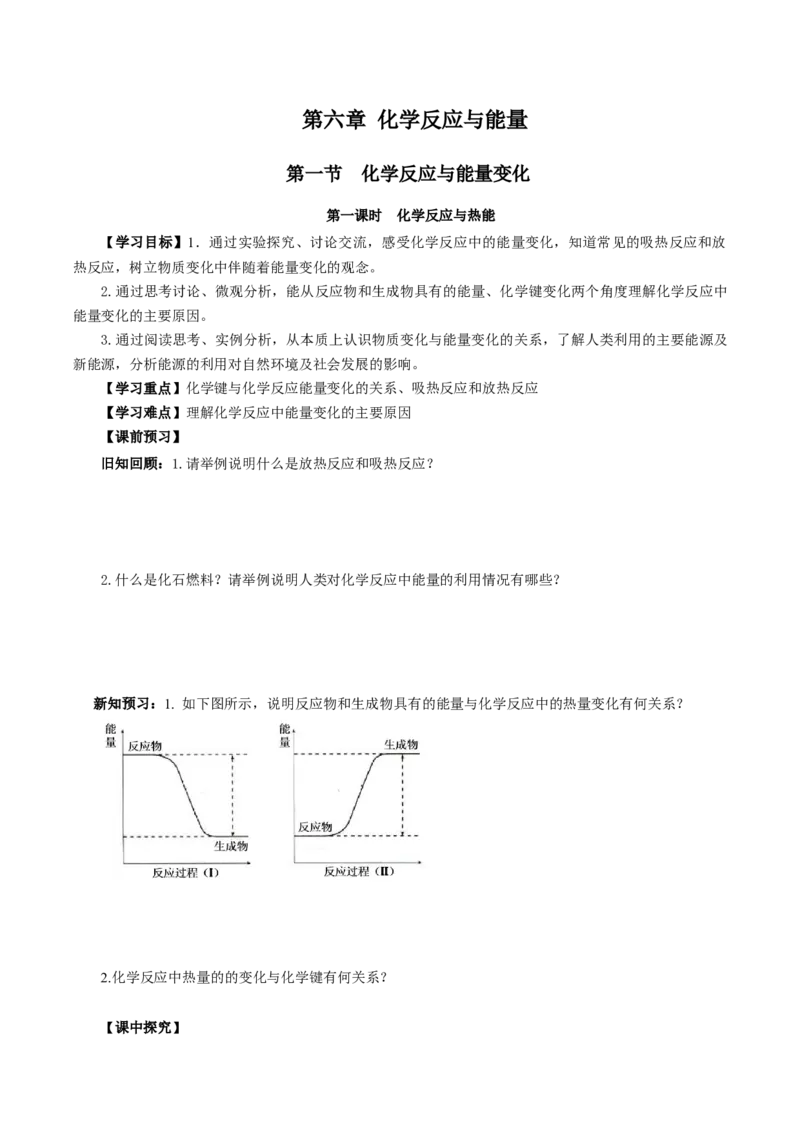
新知预习:1. 如下图所示,说明反应物和生成物具有的能量与化学反应中的热量变化有何关系?
2.化学反应中热量的的变化与化学键有何关系?
【课中探究】情景导入:能源、材料,信息被称为现代社会发展的三大支柱。能源是人类赖以生存和发展的重要资
源。我们在生产、生活中所使用的能量绝大部分是由化学反应提供的,特别是煤、石油、天然气以及它们
的制品燃烧所产生。随着社会的发展,人类活动对能源的消耗逐渐增多,尽管一些新能源被不断开发和利
用,但是,由于对资源的不合理开发和利用从而引发了不可回避的能源危机已成为制约一个国家发展的瓶
颈,今天我们以化学的眼光来研究有关能源问题。(见PPT图片)
一、化学反应中的热量变化
活动一、放热反应和吸热反应
任务一、讨论交流:结合已有知识思考化学反应的本质和特征分别是什么?
(1)本质:
(2)特征:
任务二、阅读思考:阅读教材P33页第二自然段,结合初中所学知识,思考什么是吸热反应和放热反
应?并列举你知道的常见吸热反应和放热反应。
【对应训练】1.下列说法正确的是 ( )
A.物质发生化学变化都伴随着能量变化 B.任何反应中的能量变化都表现为热量变化
C.伴有能量变化的物质变化都是化学变化 D.即使没有物质的变化,也可能有能量的变化
2.将盛有NH HCO 粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧
4 3
烈,醋酸逐渐凝固。由此可知( )
A.NH HCO 和盐酸的反应是放热反应
4 3
B.该反应中,热能转化为化学能
C.醋酸与NH HCO 发生了复分解反应,该反应为吸热反应
4 3
D.该反应的离子方程式为:CO+2H+===CO ↑+HO
2 2
活动二、实验探究放热反应和吸热反应
任务一、实验探究:结合教材P32-33页【实验6-1】、【实验6-2】,完成相关实验,观察实验现象,
思考实验原理,填写表格内容:在一只试管中加入2 mL 2 mol/L 将20g Ba(OH)•8H O晶体研细后与10g NHCl在烧
2 2 4
盐酸,并用温度计测量其温度。 杯中混合,并将烧杯放在滴有几滴水的木片上,用
实验操作 再向试管中放入用砂纸打磨光亮 玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧
的镁条 杯,用手触摸烧杯下部,试着用手拿起烧杯
实验装置
实验现象
实验原理
实验结论
任务二、问题探究:(1)放热反应和吸热反应与反应条件是否需要加热有何关系?
(2)NaOH固体或浓硫酸溶于水,溶液温度均会升高,则NaOH固体、浓硫酸溶于水是放热反应,对
吗?
(3)你认为实验【6-2】成功的关键是什么?该实验中能量是如何转化的?
【对应训练】1.下列关于化学反应与能量变化的说法中,不正确的是( )
A.化学反应必然伴随着能量变化
B.Na与HO的反应属于吸热反应
2
C.Ba(OH) ·8H O与NH Cl的反应属于吸热反应
2 2 4
D.化学变化中的能量变化主要是由化学键变化引起的
2.下列说法正确的是( )
①需要加热才能发生的反应一定是吸热反应 ②放热反应在常温下一定很容易发生 ③反应是放出能
量还是吸收能量必须看反应物和生成物所具有的总能量的相对大小 ④有的放热反应加热到一定温度引发
后,停止加热反应也能继续进行A.只有③④ B.只有①② C.①②③④ D.②③④
二、化学反应中能量变化的原因
活动一、探究化学反应中热量的变化与化学键的关系—微观角度
任务一、阅读思考:阅读教材P33页内容,思考化学反应中化学键与能量有何关系?
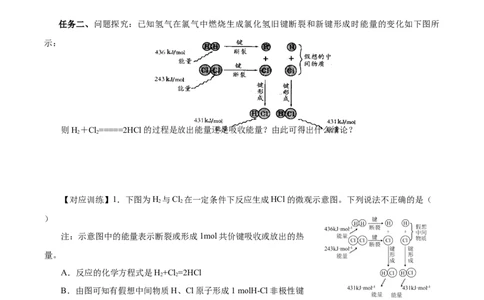
任务二、问题探究:已知氢气在氯气中燃烧生成氯化氢旧键断裂和新键形成时能量的变化如下图所
示:
则H+Cl=====2HCl的过程是放出能量还是吸收能量?由此可得出什么结论?
2 2
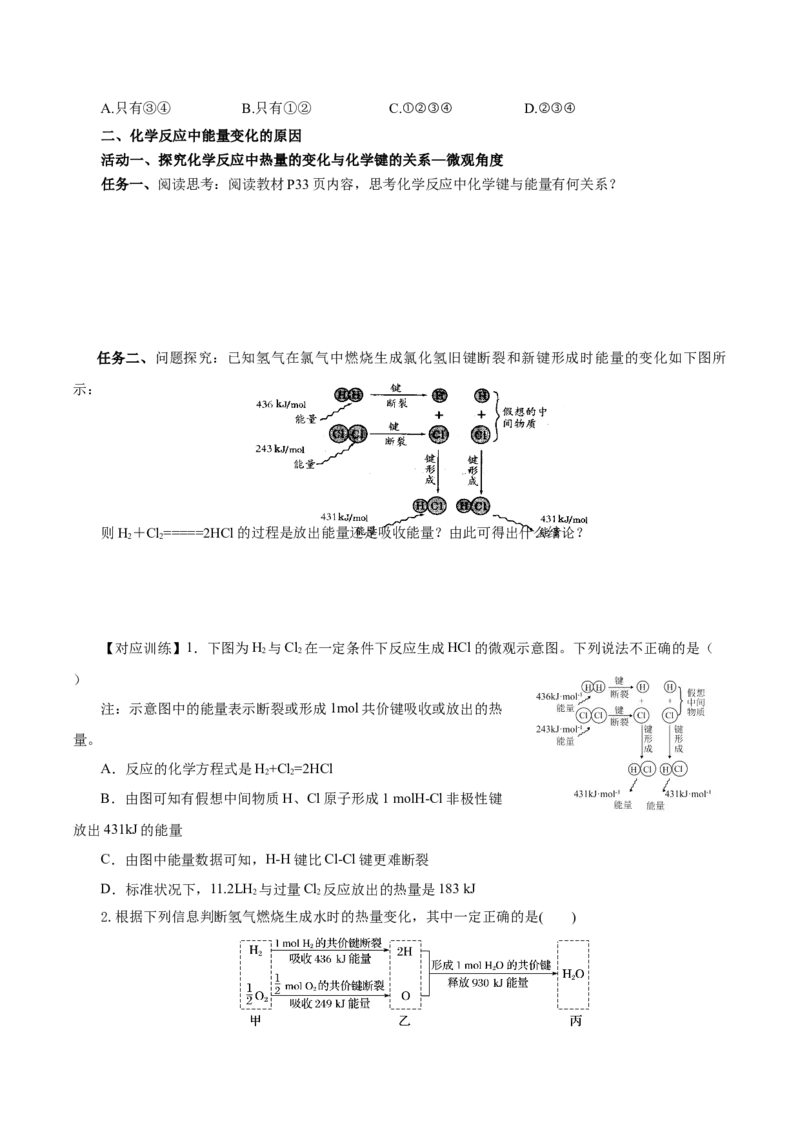
【对应训练】1.下图为H 与Cl 在一定条件下反应生成HCl的微观示意图。下列说法不正确的是(
2 2
)
注:示意图中的能量表示断裂或形成1mol共价键吸收或放出的热
量。
A.反应的化学方程式是H+Cl=2HCl
2 2
B.由图可知有假想中间物质H、Cl原子形成1 molH-Cl非极性键
放出431kJ的能量
C.由图中能量数据可知,H-H键比Cl-Cl键更难断裂
D.标准状况下,11.2LH 与过量Cl 反应放出的热量是183 kJ
2 2
2.根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )A.HO分解为H 与O 时放出热量 B.生成1 mol H O时吸收热量245 kJ
2 2 2 2
C.甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙 D.氢气和氧气的总能量小于水的能量
活动二、探究化学反应中热量的变化与反应物和生成物具有的能量高低的关系—宏观角度
任务一、阅读思考:阅读教材P34内容,并结合图6-3,思考物质的能量与反应放出、吸收能量有何关
系?由此可得出什么结论?
宏观解释 放热反应示意图 吸热反应示意图
化学反应放出热量
化学反应吸收热量
结 论
注意:
任务二、归纳总结:比较放热反应与吸热反应,完成表格内容。
类型
放热反应 吸热反应
比较
定义
形成原因
与化学键
的关系
反应过程
图示
任务三、问题探究:结合所学知识,思考如何判断吸热反应和放热反应?
【对应训练】1.下列说法正确的是( )
A.物质发生化学反应时都伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.在一个确定的化学反应体系中,反应物的总能量与生成物的总能量一定相同
D.在一个确定的化学反应体系中,反应物的总能量总是高于生成物的总能量
2.已知反应NO (g)+CO(g)=NO(g)+CO (g)的能量变化如图所示,下列说法中正确的是( )
2 2
A.图中A→B的过程为放热过程B.该反应为氧化还原反应
C.断开1 mol NO 和1 mol CO的化学键吸收的热量总和大于
2
生成1 mol NO和 1 mol CO 时放出的热量总和
2
D.1 mol NO (g)和1 mol CO(g)的总能量小于1 mol NO(g) 和
2
1 mol CO (g)的总能量
2
活动三、化学能与热能转化的应用
任务一、阅读思考:阅读教材P34-35页内容,思考现阶段人类获取热能的主要途径是什么?化石燃料
获取能量面临哪些问题?
任务二、讨论交流:为了改善人类的生存环境,促进社会可持续发展,有哪些节能减排的措施?
【对应训练】1.液态储氢技术就是在常温常压下将氢气融入到一种化合物“储油”中,形成“氢
油”,便于储存和运输。下列有关说法错误的是( )
A.“氢油”不稳定
B.氢能源属于可再生能源
C.该技术实现了常温常压下储氢技术的新突破
D.液态储氢项目有利于发展氢能源电动机,从而带来新能源汽车的升级
2.下列关于能源和作为能源使用的物质的叙述中错误的是( )
A.化石能源物质内部蕴含着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在一定条件下转化为热能、电能,为人类所利用
D.吸热反应没有利用价值
【课后巩固】1.下列说法不正确的是( )
A.当今社会人们所需的能量绝大部分是由化学反应产生的
B.目前,全球仍处于化石能源时代
C.人体生命活动所需要的能量,是由氧化还原反应提供的
D.凡是放出热量的化学反应均可用来造福人类
2.下列说法中正确的是( )
A.物质发生化学反应时都伴随能量变化,伴随能量变化的过程也一定是化学变化的过程B.需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应
C.因为3O=2O 是吸热反应,所以臭氧比氧气的化学性质更活泼
2 3
D.吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化
学键形成时放出的能量多
3.下列说法中不正确的是 ( )
A.化学键的断裂与形成是化学反应过程的本质
B.化学键的断裂与形成是化学反应中能量变化的主要原因
C.从能量的角度看,断开化学键要吸收能量,形成化学键要放出能量
D.若化学反应吸收能量时,其断键吸收的能量小于成键放出的能量
4.下列实验现象或图像信息不能说明相应的化学反应是放热反应的是( )
A.反应物总能量大于生成物总能量 B.反应开始后,甲处液面低于乙处液面
C.反应开始后,针筒活塞向右移动 D.反应开始后,饱和石灰水变浑浊
5.由NO和NO反应生成N 和NO 的能量变化如图所示。下列说法不正确的是( )
2 2 2
A.反应生成1 mol N 时转移4 mol e-
2
B.反应物能量之和大于生成物能量之和
C.1 molNO(g)和1 molNO如图中完全反应放出139kJ能量
2
D.断键吸收能量之和小于成键释放能量之和
6.如图关于下列说法不正确的是( )
A.1 mol I (s)与1 mol H (g)化合生成2 mol HI(g)时,需要吸收5 kJ的能量
2 2
B.2 mol HI(g)分解生成1 mol I (g)与1 mol H (g)时需要吸收12 kJ的能量
2 2
C.1 mol I (s)变为1 mol I (g)时需要吸收17 kJ的能量
2 2
D.I(g)与H(g)生成HI(g)的反应是吸热反应
2 2
7.已知2SO +O =2SO 为放热反应,对该反应的下列说法中正确的是( )
2 2 3
A.SO 和O 的总能量一定高于SO 的总能量
2 2 3
B.为了提高SO 的转化率,应使用催化剂
2C.此反应达到平衡时,SO 的浓度与SO 的浓度一定相等
2 3
D.因该反应为放热反应,故不必加热就可发生
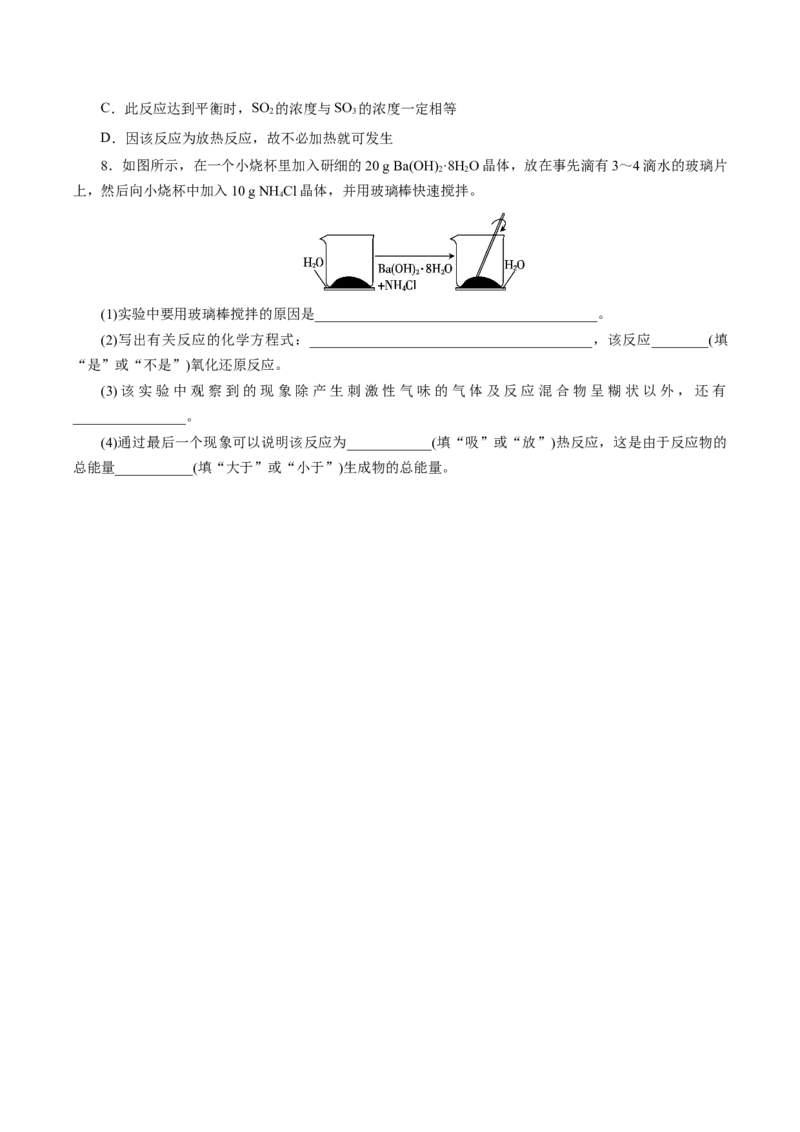
8.如图所示,在一个小烧杯里加入研细的20 g Ba(OH) ·8H O晶体,放在事先滴有3~4滴水的玻璃片
2 2
上,然后向小烧杯中加入10 g NH Cl晶体,并用玻璃棒快速搅拌。
4
(1)实验中要用玻璃棒搅拌的原因是________________________________________。
(2)写出有关反应的化学方程式:________________________________________,该反应________(填
“是”或“不是”)氧化还原反应。
(3)该实验中观察到的现象除产生刺激性气味的气体及反应混合物呈糊状以外,还有
________________。
(4)通过最后一个现象可以说明该反应为____________(填“吸”或“放”)热反应,这是由于反应物的
总能量___________(填“大于”或“小于”)生成物的总能量。