文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化 课时作业
第二课时 化学反应与电能
基础达标
1.下列关于原电池的叙述正确的是 ( )
A.构成原电池的正极和负极的材料必须是两种不同的金属
B.原电池是将化学能转化为电能的装置
C.在原电池中,电子流出的一极是正极
D.原电池工作时,电路中的电流是从负极到正极
【答案】B
【解析】A.构成原电池的电极可以是金属与金属,也可以是金属与非金属,A项错
误;B.原电池是将化学能转化为电能的装置,B项正确;C.原电池中电子流出的一极是
负极,C项错误;D.原电池工作时,电流是从正极到负极,D项错误。故选:B。
2.下列说法不正确的是( )
A.电能属于一次能源
B.太阳能电池的能量转化方式为光能→电能
C.植物及其加工品所储存的能量为生物质能
D.芒硝晶体(Na SO ·10H O)白天在阳光下曝晒后失水、溶解吸热,夜里重新结晶放
2 4 2
热,实现太阳能转化为化学能继而转化为热能
【答案】A
【解析】A. 电能是用风能、水能、太阳能等制取的能源,属于二次能源,故A错
误;B. 太阳能电池直接把太阳能转化为电能,故B正确;C. 生物质能是绿色植物将太阳
能转化为化学能而储存在生物质内部的能量,故C正确;D. Na SO •10H O结晶属于化学
2 4 2
变化,能量转换形式为化学能和热能的转化,白天在阳光下曝晒后失水,转换形式为太阳
能和化学能的转化,故D正确;选A。
3.原电池产生电流的本质原因是( )
A.原电池中,电解质溶液能电离出自由移动的离子
B.有两个活泼性不同的电极
C.导线将电极、电解质溶液连接,形成了闭合回路
D.原电池中发生了氧化还原反应
【答案】D
【解析】原电池中,外电路中,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流向正极;内电路中,电解质溶液中的阴离子向负极移动,阳离
子向正极移动,所以形成了闭合回路,产生了电流,所以在原电池中发生氧化还原反应是
原电池产生电流的本质原因。故选:D。
4.钢铁不是纯净的铁,通常含有少量的碳,在潮湿的空气中易形成原电池而腐蚀,下
列说法正确的是 ( )
A.铁为正极,发生还原反应 B.铁为负极,发生氧化反应
C.碳为正极,发生氧化反应 D.碳为负极,发生还原反应
【答案】B
【解析】钢铁在潮湿的空气中易形成原电池而发生吸氧腐蚀。在钢铁发生吸氧腐蚀
时,铁作负极发生氧化反应,碳作正极,氧气在正极发生还原反应。A.铁为负极,发生
氧化反应,故A错误;B.铁为负极,发生氧化反应,故B正确;C.碳为正极,发生还原
反应,故C错误;D.碳为负极,发生还原反应,故D错误;故答案为:B。
5.如图所示,为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家
提出了利用太阳能制取氢能的构想。下列说法不正确的是( )
A.过程①将太阳能转换成化学能
B.电能属于一次能源
C.能量利用率:燃料电池比H 直接燃烧高
2
D.过程②将化学能转换为电能
【答案】B
【解析】A.化学物质中存在化学能,过程①是水在太阳能的作用下转化为氢气和氧
气,是太阳能转换成化学能,故A正确;B.电能是经过人为加工获得的,为二次能源,
故B错误;C.燃料电池的能量利用率要比燃料直接燃烧的能量利用率高,故C正确;D.
过程②是燃料电池,是将化学能转换为电能,故D正确;
故选B。
6.下列有关装置的说法正确的是( )A.装置Ⅰ中 为原电池的负极 B.装置Ⅱ为一次电池
C.装置Ⅲ可构成原电池 D.装置Ⅳ工作时,电子由锌通过导线流向碳
棒
【答案】D
【解析】A.镁与氢氧化钠溶液不反应,铝能够与氢氧化钠溶液反应,装置Ⅰ中铝为
负极,镁为正极,故A错误;B.铅蓄电池是二次电池,可以放电充电,故B错误;C.装
置Ⅲ中的两个材料相同、都是Zn,不能构成原电池,故C错误;D.装置Ⅳ为干电池,锌
为负极,碳棒为正极,工作时,原电池中电子由负极沿导线流向正极,因此电子由锌通过
导线流向碳棒,故D正确;故选D。
7.一种锂水电池以锂和钢板为电极,LIOH为电解质,使用时加入水即可放电,总反
应为:2Li+2HO==2LiOH+H ↑。下列有关该电池的说法错误的是( )
2 2
A.锂极为负极 B.OH-移向正极
C.H 为正极产物 D.电子由锂经导线流向钢板
2
【答案】B
【解析】A.由方程式可知,Li失去电子,发生氧化反应,做负极,则钢板做正极,A
项正确;B.负极上的电极方程式为:Li-e-+OH-==LiOH,可知OH-移向负极,B项错误;
C.正极上的电极方程式为:2Li+2HO==2LiOH+H ↑,可知氢气为正极产物,C项正确;
2 2
D.电子会从负极流向正极,即电子由锂经导线流向钢板,D项正确;答案选B。
8.下列四个常用电化学装置的叙述错误的是( )
A.图Ⅰ所示电池中,电子从锌片流出
B.图Ⅱ所示干电池中锌作负极
C.图Ⅲ所示电池为二次电池,放电时正极的电极反应式为Pb-2e-+SO2-==PbSO
4 4
D.图Ⅳ所示电池中通入氧气的电极是正极
【答案】C
【解析】A.图I构成原电池,锌比铜活泼,锌作负极,电子由锌片流出,故A正确;B.图II为锌锰干电池,其中锌作负极,故B正确;C.图III为铅蓄电池,放电时正
极二氧化铅得电子生成硫酸铅,电极反应式为:PbO +2e- +SO 2-+4H+==PbSO +2H O,故C
2 4 4 2
错误;D.图Ⅳ为氢氧燃料电池,氢气失电子,a为负极;氧气在b电极得电子,b电极为
正极,故D正确;故选:C。
9.碱性锌锰电池获得了广泛的应用,根据电池的电极反应,下列判断正确的是(
)
A.碱性锌锰电池是二次电池
B.Zn为负极,MnO 为正极
2
C.工作时电子由MnO 经外电路流向Zn极
2
D.Zn电极发生还原反应,MnO 电极发生氧化反应
2
【答案】B
【解析】A. 碱性锌锰电池是一次电池,不可重复使用,故A错误;B. Zn失电子
发生氧化反应,为负极,MnO 为正极,故B正确;C. 工作时电子由经Zn极外电路流向
2
MnO ,故C错误;D. Zn电极发生氧化反应,MnO 电极发生还原反应,故D错误;故
2 2
选B。
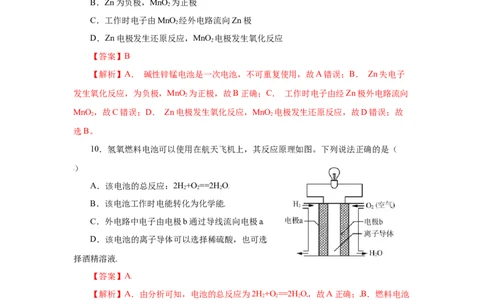
10.氢氧燃料电池可以使用在航天飞机上,其反应原理如图。下列说法正确的是(
)
A.该电池的总反应:2H+O ==2H O
2 2 2
B.该电池工作时电能转化为化学能
C.外电路中电子由电极b通过导线流向电极a
D.该电池的离子导体可以选择稀硫酸,也可选
择酒精溶液
【答案】A
【解析】A.由分析可知,电池的总反应为2H+O ==2H O,故A正确;B.燃料电池
2 2 2
工作时,将化学能转化为电能,故B错误;C.燃料电池工作时,外电路中电子由负极电
极a通过导线流向正极电极b,故C错误;D.若离子导体选择酒精溶液,酒精是非电解
质,不能形成闭合回路,不能构成原电池,故D错误;故选A。
能力提升
11.X、Y、Z、M、N代表五种金属,有以下反应:
①Y与M用导线连接放入稀硫酸中,M上冒气泡;②M、N为电极,与N的盐溶液组成原电池,电子从M极流出,经过外电路,流入N
极;
③Z+2HO(冷水)=Z(OH) +H ↑;
2 2 2
④水溶液中,X+Y2+=X2++Y。
则这五种金属的活动性由强到弱的顺序为( )
A.Z>X>Y>M>N B.Z>Y>X>M>N
C.Z>X>Y>N>M D.X>Y>M>N>Z
【答案】A
【解析】①Y与M用导线连接放入稀硫酸中,M上冒气泡,说明M作为原电池的正
极,活泼性MN;
③Z+2H O(冷水)=Z(OH) +H ↑,Z的化学性质非常活泼;④水溶液中,X+Y2+=X2++Y,X可
2 2 2
以置换出Y的盐溶液中的Y,所以活泼性X>Y,所以五种金属活动性由强到弱的顺序为:
Z>X>Y>M>N,答案选A。
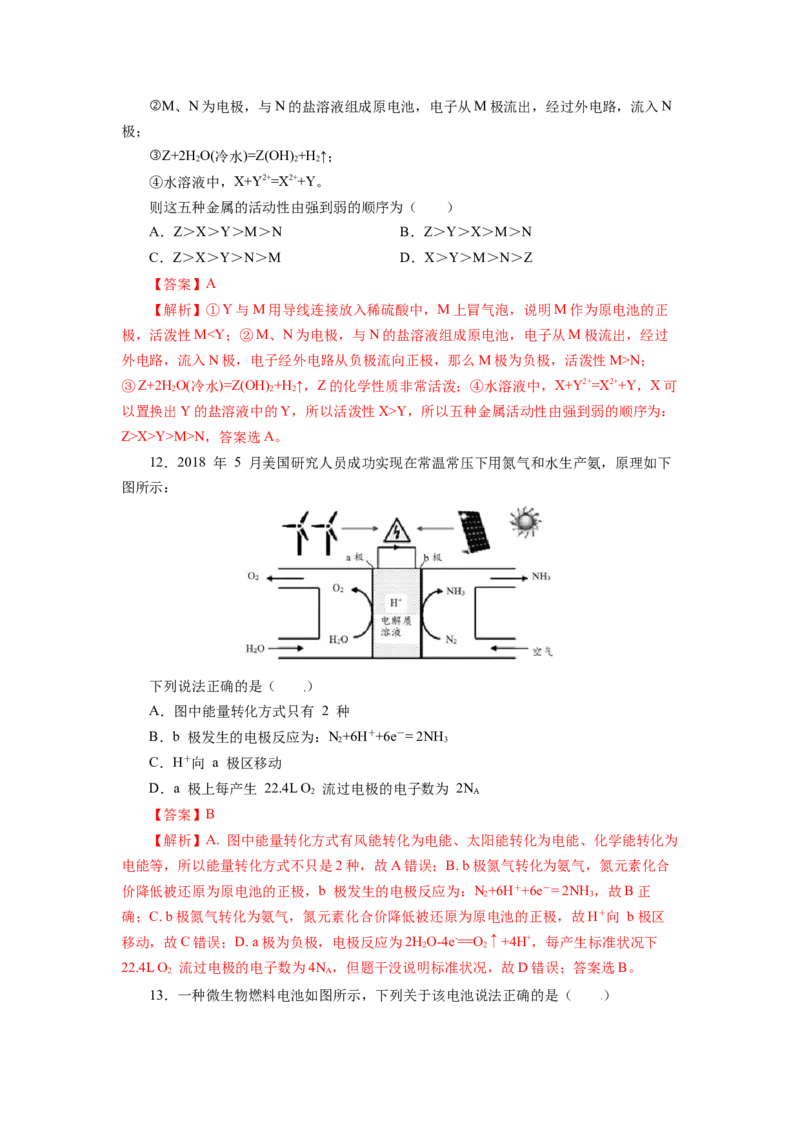
12.2018 年 5 月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下
图所示:
下列说法正确的是( )
A.图中能量转化方式只有 2 种
B.b 极发生的电极反应为:N+6H++6e-= 2NH
2 3
C.H+向 a 极区移动
D.a 极上每产生 22.4L O 流过电极的电子数为 2N
2 A
【答案】B
【解析】A. 图中能量转化方式有风能转化为电能、太阳能转化为电能、化学能转化为
电能等,所以能量转化方式不只是2种,故A错误;B. b极氮气转化为氨气,氮元素化合
价降低被还原为原电池的正极,b 极发生的电极反应为:N+6H++6e-= 2NH ,故B正
2 3
确;C. b极氮气转化为氨气,氮元素化合价降低被还原为原电池的正极,故H+向 b极区
移动,故C错误;D. a极为负极,电极反应为2HO-4e-==O ↑+4H+,每产生标准状况下
2 2
22.4L O 流过电极的电子数为4N ,但题干没说明标准状况,故D错误;答案选B。
2 A
13.一种微生物燃料电池如图所示,下列关于该电池说法正确的是( )A.a电极为正极,发生还原反应
B.H+由右室通过质子交换膜进入左室
C.当b电极上产生lmolN 时,溶液中将有l0mole—通过
2
D.b电极反应式为:2NO +10e—+12H+=N ↑+6HO
2 2
【答案】D
【解析】A.由分析可知,电极a为燃料电池的负极,故A错误;B.燃料电池工作
时,氢离子向正极移动,由左室通过质子交换膜进入右室,故B错误;C.由分析可知,
电极b为正极,硝酸根离子在正极得到电子发生还原反应生成氮气和水,则当b电极上产
生lmolN 时,导线中将有lmol×5×2=l0mole—通过,故C错误;D.由分析可知,电极b为
2
正极,硝酸根离子在正极得到电子发生还原反应生成氮气和水,电极反应式为2NO +10e
—+12H+=N ↑+6HO,故D正确;故选D。
2 2
14.高一台山市华侨中学校考期中)原电池原理的发现是储能和供能技术的巨大进
步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:
A.NaOH+HCl==NaCl+H O; B.Zn+H SO ==ZnSO +H ↑。
2 2 4 4 2
判断能否设计成原电池A,B(填“能”或“不能”)。
(2)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答
下列问题:
①下列说法正确的是。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的 均
增大
②在相同时间内,两烧杯中产生气泡的速度:甲乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:。构成原电池的电池工作时,溶液中
向极移动;电池工作完成后,溶液中 浓度(填“增大”或“减小”或“不变”)。
④当乙中产生1.12L 标准状况 气体时,将锌、铜片取出,再将烧杯中的溶液稀释至
1L,测得溶液中 设反应前后溶液体积不变 。试确定原稀硫酸的物质的
量浓度为。
(3)当甲中产生1.12L 标准状况 气体时,理论上通过导线的电子数目为。
【答案】(1) 不能 能
(2) BD > Zn-2e-==Zn2+ 负 不变 1mol/L
(3)0.1N
A
【解析】(1)原电池的构成条件之一为自发的氧化还原反应,A.
NaOH+HCl═NaCl+H2O不是氧化还原反应,不能设计成原电池;B.
Zn+H2SO4═ZnSO4+H2↑是氧化还原反应,能设计成原电池;
(2)①A.甲构成原电池,将化学能转变为电能,乙中铜锌没有用导线连接,乙没有
形成原电池,乙不能将化学能转变为电能,故A错误;B.乙没有形成原电池,乙装置中
铜片不反应,所以铜片上没有明显变化,故B正确;C.甲、乙中都是锌失电子生成锌离
子,铜片不反应,锌片质量都减少、铜片质量不变,故C错误;D.两个烧杯中都产生氢
气,氢离子浓度都降低,所以溶液的pH均增大,故D正确;选BD;
②甲构成原电池,所以甲的腐蚀速度>乙的腐蚀的速度;
③甲构成原电池,负极是锌失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+;原电
池的电池工作时阴离子移向负极,则溶液中SO向负极移动,该原电池的总反应式为:
Zn+2H+=Zn2++H2↑,SO不参与反应,电池工作完成后,溶液中SO浓度不变;
④稀释后氢离子的物质的量为1L×0.1mol•L-1=0.1mol,生成氢气的氢离子的物质的量
为1.12L/22.4L/mol×2=0.1mol,所以原溶液中氢离子的物质的量为0.2mol,硫酸的物质的量为0.1mol,原溶液中硫酸的浓度为0.1mol/0.1L=1mol/L;
(3)甲中正极反应式为2H++2e-=H2↑,产生1mol氢气时转移2mol电子,产生标准状
况1.12L气体即物质的量为1.12L/22.4L/mol=0.05mol时转移0.1mol电子,理论上通过导线
的电子数目为0.1N 。
A
直击高考
15.尿素燃料电池既能去除城市废水中的尿素,又能发电。尿素燃料电池结构如下图所
示,甲电极上发生如下反应:CO(NH)+H O-6e-==CO +N +6H+,则下列说法正确的是(
2 2 2 2 2
)
A.甲电极是正极 B.每1.5molO 理论上可净化1molCO(NH )
2 2 2
C.H+从乙电极附近向甲电极附近迁移 D.电解质溶液可以是NaOH溶液
【答案】B
【解析】A.甲电极电极反应式为:CO(NH)+H O-6e-==CO +N +6H+,是氧化反应,
2 2 2 2 2
甲电极是负极,A错误;B.由电荷守恒知:2CO(NH)~12e-~3O,则每1.5molO 理论上
2 2 2 2
可净化1molCO(NH ),B正确;C.阳离子移向正极,甲电极为负极、乙电极为正极,则
2 2
H+从甲电极附近向乙电极附近迁移,C错误;D. 从甲电极电极反应式CO(NH)+H O-6e-
2 2 2
==CO +N +6H+知,电解质溶液不可以是NaOH溶液,D错误;答案选B。
2 2
16.现代生产、生活和国防中大量使用电池,各种电池应运而生。请回答下列问题。
(1)碱性锌锦干电池是应用广泛的一次电池。总反应Zn+2MnO +2H O=2MnO(OH)+
2 2
Zn(OH) 该电池的负极材料是__________,负极电极反应式是
2
_________________________。
(2)铅蓄电池工作时的总反应为Pb+PbO+2H SO =2PbSO+2H O,电池在工作时,
2 2 4 4 2
PbO 电极附近溶液的酸性将__________(填“增强”、“减弱,'或“不变”);若该电池反
2
应转移了0.2mol电子,则正极电极理论上增重_______g。(3)氢氧燃料电池是一种将化学能转化为电能的高效、环境友好的发电装置。该电池
的构造如图所示,请回答:
电极a为该电池_______(填“正极”或“负极”),电极b的电极反应为
___________________。
(4)某实验小组依据氧化还原反应:_______(用离子方程式表示)设计的原电池装置
如图,反应前,两电极质量相等,一段时间后,两电极质盘相差12g,导线中通过
_______mol电子。
【答案】(1)Zn Zn-2e-+2OH-=Zn(OH)
2
(2)减弱 6.4 g
(3)负极 O+4e-+2H O=4OH-
2 2
(4)Fe+Cu2+=Fe2++Cu 0.2
【解析】(1)碱性锌锦干电池总反应Zn+2MnO +2H O=2MnO(OH)+Zn(OH) ,反应中还
2 2 2
原剂是锌,失电子发生氧化反应,该电池的负极材料是Zn,负极电极反应式是Zn-2e-
+2OH-=Zn(OH) 。故答案为:Zn;Zn-2e-+2OH-=Zn(OH) ;
2 2
(2)铅蓄电池工作时的总反应为Pb+PbO+2H SO =2PbSO+2H O,电池在工作时,正极
2 2 4 4 2
反应式为PbO +SO+4H++2e-=PbSO+2H O,消耗氢离子,PbO 电极附近溶液的酸性将减弱
2 4 2 2
(填“增强”、“减弱,'或“不变”);由电池反应可知消耗2mol酸转移2mol电子,正极电
极理论上增重64g,若该电池反应转移了0.2mol电子,则正极电极理论上增重6.4g。故答
案为:减弱;6.4;
(3)电极a上氢气失电子,发生氧化反应,为该电池负极(填“正极”或“负极”),电极b氧气得电子,发生还原反应,电极反应为O+4e-+2H O=4OH-。故答案为:负极;
2 2
O+4e-+2H O=4OH-;
2 2
(4)Fe为负极,发生:Fe-2e-=Fe2-,石墨为正极,发生Cu2++2e-=Cu,总反应式为
Fe+Cu2+═Fe2++Cu;一段时间后,两电极质量相差12g,
导线中通过0.2mol电子。故答案为:Fe+Cu2+=Fe2++Cu;0.2。