文档内容
5.3 无机非金属材料(精练)
题组一 硅
1.(2021·湖北·华中师大一附中高一期中)碳、硅及其化合物常用做性能优异的无机非金属材料。比如氮
化硅,其熔点高、硬度大,电绝缘性好,化学性质稳定。有关碳、硅及其化合物的说法正确的是
①硅在自然界中主要以单质形式存在,硅是应用最广泛的半导体材料
②硅是构成一些岩石和矿物的基本元素
③石墨烯是一种新型的纳米化合物
④氮化硅的化学式为Si N,其可制作坩埚,制作切削刀具
3 4
⑤光导纤维的通信容量大,导电性强
⑥水玻璃可用于生产黏合剂和防火剂
A.①③⑤ B.①③⑥ C.②④⑤ D.②④⑥
【答案】D
【解析】①硅是亲氧元素,在自然界中以化合态的形式存在,不能以单质形式存在,①错误;
②硅元素是地壳中大量存在的元素,是许多种岩石和矿物的基本构成元素之一,②正确;
③石墨烯是碳单质,不属于化合物,③错误;
④氮化硅的化学式为Si N,氮化硅硬度大、熔点高可以用来制作坩埚;熔点高、化学性质稳定可制作耐高
3 4
温轴承,切削刀具等,④正确;
⑤二氧化硅晶体对光具有全反射作用,能传递光信号,可以用二氧化硅晶体制备光导纤维,无导电性,⑤
错误;
⑥水玻璃具有黏性,不易燃烧,可用于生产黏合剂和防火剂,⑥正确;
综上所述,正确的是②④⑥,故选D。
2.(2021·福建省南安市侨光中学高一月考)芯片是中美经贸摩擦的焦点之一、制造芯片的高纯硅(Si)可以
用下述方法制取(反应条件略)。下列说法不正确的是
A.SiO 和SiCl 中Si的化合价均为+4
2 4
B.反应①、②、③均为氧化还原反应C.SiO 和CO都属于酸性氧化物,均能与NaOH溶液反应
2
D.利用产物的沸点不同实现由粗硅到高纯硅的提纯
【答案】C
【解析】A.SiO 中氧元素-2价,Si为+4价,SiCl 中Cl是-1价,Si为+4,A正确;
2 4
B.反应①SiO 被C还原、反应②Si被Cl 氧化、反应③SiCl 被H 还原,均为氧化还原反应,B正确;
2 2 4 2
C.SiO 属于酸性氧化物,能与NaOH溶液反应,CO属于不成盐氧化物,C错误;
2
D.SiCl 常温下是气体,沸点低易从粗硅杂质中分离,产物HCl易挥发,从高纯硅中分离,均是利用产物
4
的沸点不同,实现由粗硅到高纯硅的提纯,D正确;
故答案选C。
3.(2021·黑龙江·牡丹江市第十五中学高一期中)下列关于硅的说法不正确的是
A.硅在地壳中的含量仅次于氧
B.硅在自然界中既有化合态,又有游离态
C.高纯度的硅可用于制造计算机芯片
D.硅单质的导电能力介于导体和绝缘体之间
【答案】B
【解析】A.地壳中元素含量由大到小为:氧、硅、铝、铁、钙等,故A不符合题意;
B.硅在自然界中只有化合态,没有游离态的硅,故B符合题意;
C.硅是半导体材料,常用于制造计算机芯片,故C不符合题意;
D.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料,故D不符合题意;
故答案为:B。
4.(2021·广东·仲元中学高一期中)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工
业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
(1)工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为_______。当有 1molC参与
反应时,该反应转移的电子数是_______。
(2)有关物质的熔沸点数据如下表,提纯SiHCl 的主要工艺操作依次是沉降、冷凝和_______。
3物质 Si SiCl SiHCl SiHCl SiHCl HCl SiH
4 3 2 2 3 4
熔点/℃ 1410 -70.4 -126.5 -122 -118 -114.2 -185
沸点/℃ 2355 57.6 31.8 8.2 -30.4 -84.9 -111.9
(3)还原炉中发生的化学反应方程式为:_______。
(4)上述工艺生产中循环使用的物质除Si、SiHCl 外,还有_______。
3
(5)关于硅及其相关化合物的叙述正确的是_______。
A.自然界中存在天然游离的硅单质
B.已知C与Si属于主族元素,由于CO+H O=HCO,用类比法得知,SiO+H O=HSiO
2 2 2 3 2 2 2 3
C.硅酸钠的水溶液俗称水玻璃,具有粘性和耐高温,可以作为木材的粘合剂和防火材料
D.硅元素在金属与非金属的分界线处,因此具有弱的导电性,一般可用于作为半导体材料
E.光导纤维的主要成分是SiO
2
F.玻璃、水泥、陶瓷都是传统的硅酸盐产品
【答案】
(1) 2N
A
(2)蒸馏
(3)
(4)H、HCl
2
(5)CDEF
【解析】(1)工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为
,C的化合价从0升高为+2价,故当有 1molC参与反应时,该反应转移的电子数
是2N 。
A
(2)比较SiCl 、SiHCl 、SiHCl、SiHCl等物质的沸点,可得常温下SiCl 、SiHCl 为液体,SiHCl、
4 3 2 2 3 4 3 2 2
SiHCl为气体,沉降除去产物中的固体后,冷凝得到SiCl 、SiHCl 的混合液体,再进行蒸馏可分离二者。
3 4 3
(3)还原炉中氢气还原SiHCl 得到纯硅,发生的化学反应方程式为: 。
3
(4)粗硅与HCl发生反应 ,生成氢气,还原炉中氢气还原SiHCl 得到纯硅,发生
3反应: ,则上述工艺生产中循环使用的物质除Si、SiHCl 外,还有H、HCl。
3 2
(5)A.硅元素为亲氧元素,在自然界中主要以硅的氧化物和硅酸盐存在,故A错误;
B.SiO 难溶于水,也不与水反应,故B错误;
2
C.硅酸钠的水溶液俗称水玻璃,具有粘性和耐高温,可以作为木材的粘合剂和防火材料,故C正确;
D.硅元素在金属与非金属的分界线处,因此具有弱的导电性,一般可用于作为半导体材料,故D正确;
E.光导纤维的主要成分是SiO,故E正确;
2
F.玻璃、水泥、陶瓷都是传统的硅酸盐产品,故F正确;故选CDEF。
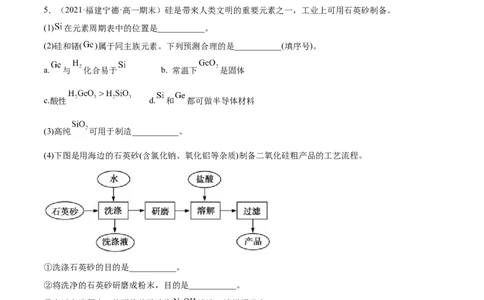
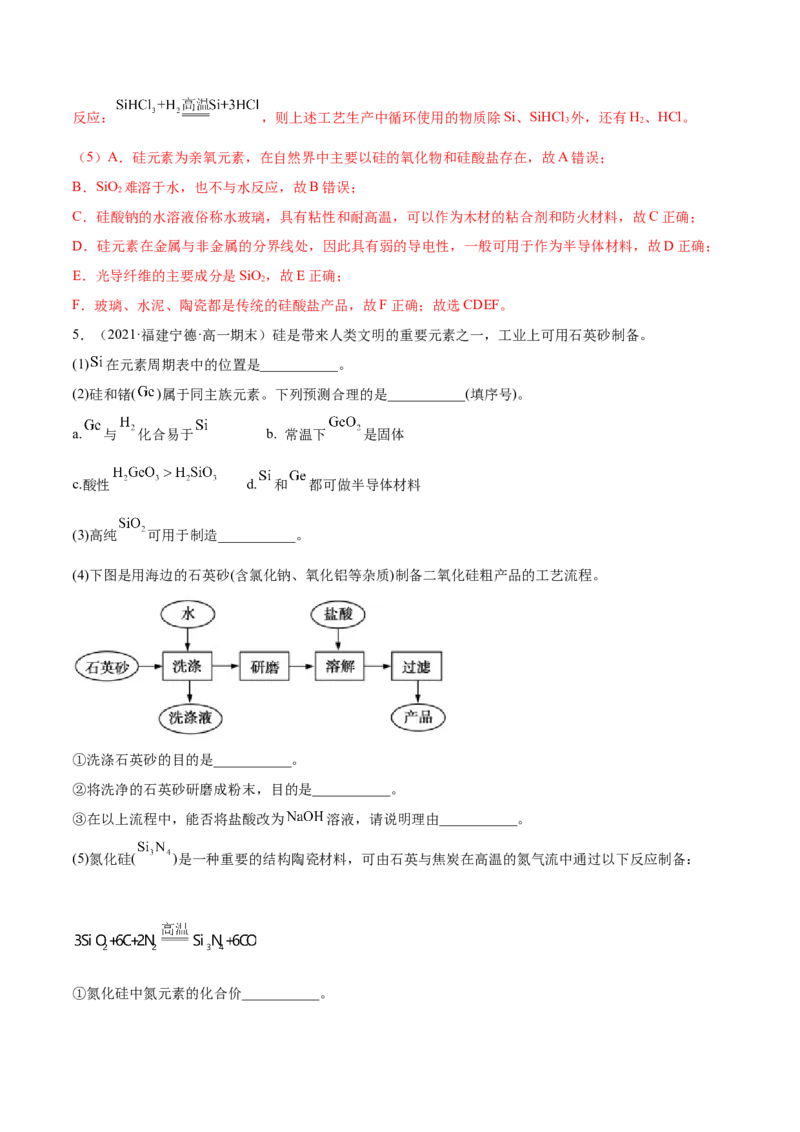
5.(2021·福建宁德·高一期末)硅是带来人类文明的重要元素之一,工业上可用石英砂制备。
(1) 在元素周期表中的位置是___________。
(2)硅和锗( )属于同主族元素。下列预测合理的是___________(填序号)。
a. 与 化合易于 b. 常温下 是固体
c.酸性 d. 和 都可做半导体材料
(3)高纯 可用于制造___________。
(4)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
①洗涤石英砂的目的是___________。
②将洗净的石英砂研磨成粉末,目的是___________。
③在以上流程中,能否将盐酸改为 溶液,请说明理由___________。
(5)氮化硅( )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气流中通过以下反应制备:
①氮化硅中氮元素的化合价___________。②若生成 (标准状况),则生成氮化硅的质量是___________ (保留一位小数)。
【答案】(1)第3周期ⅣA族
(2)bd
(3)光导纤维
(4)①除去石英砂中的 杂质 ②增大反应物之间的接触面积,从而增大反应速率,提高生产效率
③不能,因二氧化硅能与 溶液反应
(5) −3 11.7
【解析】(1) 是14号元素,在元素周期表中的位置是第3周期ⅣA族;故答案为:第3周期ⅣA族。
(2)a.同主族从上到下非金属性逐渐减弱,因此 与 化合难于 ,故a不符合题意;b. 常温下SiO 是固
2
体,因此 是固体,故b符合题意;c.同主族从上到下非金属性逐渐减弱,最高价氧化物对应水化物酸
性逐渐减弱,因此酸性 ,故c不符合题意;d. 和 再金属和非金属交界处,因此两者
都可做半导体材料,故d符合题意;综上所述,答案为bd。
(3)高纯 可用于制造光导纤维;故答案为:光导纤维。
(4)①石英砂(含氯化钠、氧化铝等杂质),氯化钠易溶于水,氧化铝难溶于水,因此洗涤石英砂的目的是除
去石英砂中的 杂质;故答案为:除去石英砂中的 杂质。
②将洗净的石英砂研磨成粉末,目的是增大反应物之间的接触面积,从而增大反应速率,提高生产效率;
故答案为:增大反应物之间的接触面积,从而增大反应速率,提高生产效率。
③在以上流程中,用盐酸将氧化铝溶液,而二氧化硅不与盐酸反应,因此溶解后过滤得到二氧化硅,因此
不能将盐酸改为 溶液,二氧化硅能与 溶液反应;故答案为:不能,因二氧化硅能与 溶
液反应。
(5)①氮化硅中硅化合价为+4价,因此氮元素的化合价−3价;故答案为:−3。
②若生成 (标准状况)即物质的量为0.5mol,根据化学方程式得到氮化硅物质的量为
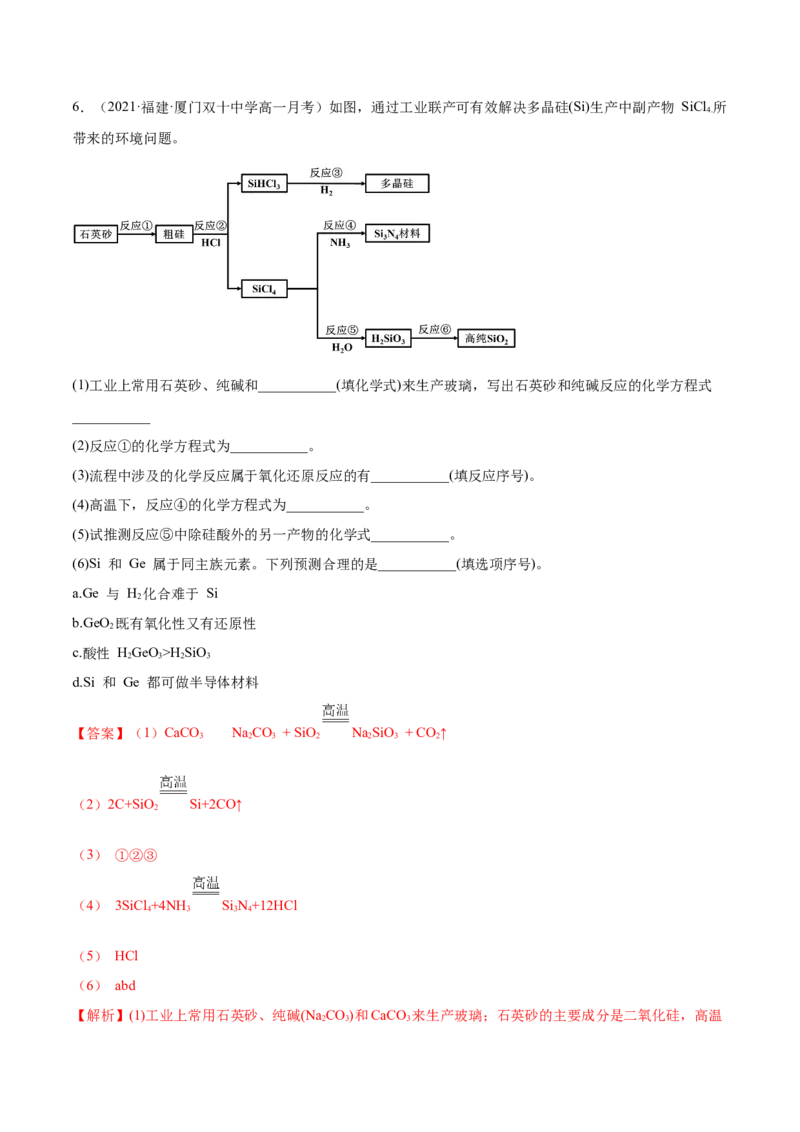
,则生成氮化硅的质量是 ;故答案为:11.7。6.(2021·福建·厦门双十中学高一月考)如图,通过工业联产可有效解决多晶硅(Si)生产中副产物 SiCl 所
4.
带来的环境问题。
(1)工业上常用石英砂、纯碱和___________(填化学式)来生产玻璃,写出石英砂和纯碱反应的化学方程式
___________
(2)反应①的化学方程式为___________。
(3)流程中涉及的化学反应属于氧化还原反应的有___________(填反应序号)。
(4)高温下,反应④的化学方程式为___________。
(5)试推测反应⑤中除硅酸外的另一产物的化学式___________。
(6)Si 和 Ge 属于同主族元素。下列预测合理的是___________(填选项序号)。
a.Ge 与 H 化合难于 Si
2
b.GeO 既有氧化性又有还原性
2
c.酸性 HGeO >H SiO
2 3 2 3
d.Si 和 Ge 都可做半导体材料
【答案】(1)CaCO Na CO + SiO NaSiO + CO↑
3 2 3 2 2 3 2
(2)2C+SiO Si+2CO↑
2
(3) ①②③
(4) 3SiCl +4NH Si N+12HCl
4 3 3 4
(5) HCl
(6) abd
【解析】(1)工业上常用石英砂、纯碱(Na CO)和CaCO 来生产玻璃;石英砂的主要成分是二氧化硅,高温
2 3 3条件下可以和纯碱反应生成硅酸钠和二氧化碳,化学方程式为NaCO + SiO NaSiO + CO↑;
2 3 2 2 3 2
(2)反应①是碳和二氧化硅高温条件下反应生成硅和一氧化碳,化学方程式为2C+SiO Si+2CO↑;
2
(3)反应①中Si、C元素化合价发生变化,为氧化还原反应;反应②、③中Si、H元素化合价发生变化,为
氧化还原反应;其余反应中没有元素化合价发生变化,不是氧化还原反应,故答案为①②③;
(4)根据元素守恒可知SiCl 和NH 在高温条件下反应生成Si N 和HCl,化学方程式为3SiCl +4NH
4 3 3 4 4 3
Si N+12HCl;
3 4
(5)该反应不是氧化还原反应,Cl元素的化合价仍为-1价,所以另一产物应为HCl;
(6) a.Si和Ge属于同主族元素,同主族元素从上到下非金属性逐渐减弱,单质的氧化性逐渐减弱,与氢
气化合越来越难,Ge与H 化合难于Si,故a正确;
2
b.Si和Ge属于同主族元素,GeO 中Ge的化合价为+4价,处于最高价态,可以被还原,氧元素的化合
2
价为-2价,处于最低价态,既有氧化性又有还原性,故b正确;
c.碳和硅位于同一主族,同主族元素从上到下非金属性逐渐减弱,最高价氧化物对应的水化物的酸性减
弱,酸性HGeO <HSiO,故c错误;
2 3 2 3
d.Si和Ge都位于金属区和非金属区的分界区,既有金属性又有非金属性,Si和Ge都可做半导体材料,
故d正确;答案选abd。
题组二 二氧化硅
1.(2021·江苏淮安·高一月考)光纤通信是一种现代化的通讯手段,光纤通信容量大,一对光纤上可同时
传送3万门电话。制造光导纤维的主要原料是SiO,则SiO 属于
2 2
A.酸 B.碱 C.盐 D.氧化物
【答案】D
【解析】SiO 酸性氧化物,故答案为D。
2
2.(2021·四川·成都市郫都区成实外教育培训学校有限公司高一开学考试)“我是碳家族的大女儿,让大
地充满生机、让地球因我而温暖;我调皮可爱,钻进石灰水,搅得人家不安宁;我藏在汽水里,小朋友喝
了直打隔。”这里叙述中的“我”是指
A.二氧化碳 B.氧气 C.氮气 D.一氧化碳
【答案】A【解析】二氧化碳能参与植物的光合作用,让大地充满生机;二氧化碳能产生温室效应,让地球变暖;二
氧化碳能与氢氧化钙反应生成碳酸钙和水,搅得石灰水不安宁;汽水中含有溶有CO,进入体内后,当温
2
度升高时,CO 的溶解度随温度的升高而减小会从体内逸出,因此喝了汽水以后,常常会打嗝,则“我”
2
是指二氧化碳,故选A。
3.(2021·吉林·长春市第二十九中学高一期末)下列物品中含有二氧化硅的是
①陶瓷②金刚砂③普通玻璃④有机玻璃⑤水晶项链⑥光导纤维⑦计算机芯片⑧玛瑙⑨硅太阳能电池⑩石英
坩埚
A.①③④⑤⑥⑧ B.②③⑤⑥⑧⑩ C.③④⑤⑥⑧⑩ D.①③⑤⑥⑧⑩
【答案】D
【解析】①陶瓷材料属于硅酸盐材料,一般主要成分是二氧化硅,氧化铝,①符合题意;
②金刚砂为SiC,不含二氧化硅,②不符合题意;
③普通玻璃的化学组成是NaSiO、CaSiO 、SiO,③符合题意;
2 3 3 2
④有机玻璃为有机物,不含二氧化硅,④不符合题意;
⑤水晶的主要成分为二氧化硅,⑤符合题意;
⑥光导纤维主要成分为二氧化硅,⑥符合题意;
⑦计算机芯片的主要成分是硅单质,⑦不符合题意;
⑧玛瑙的主要成分为二氧化硅,⑧符合题意;
⑨硅太阳能电池主要成分为硅单质,⑨不符合题意;
⑩石英的主要成分为二氧化硅,⑩符合题意;
综上所述答案为D。
4.(2021·广东·东莞市新世纪英才学校高一月考)下列说法正确的是
A.二氧化硅溶于水显酸性
B.二氧化碳通入水玻璃可以得到原硅酸
C.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸比碳酸强
D.二氧化硅是酸性氧化物,它不溶于任何酸
【答案】B
【解析】A.二氧化硅不溶于水,A错误;
B.二氧化碳和硅酸钠反应生成原硅酸和碳酸钠,B正确;
C.不能通过高温下的反应比较酸性强弱,C错误;
D.二氧化硅是酸性氧化物,但能溶于氢氟酸,D错误;
故选B。
5.(2021·云南省通海县第二中学高一期中)二氧化硅与二氧化碳组成相似,结构不同。下列反应原理不同的是
A.SiO+2C Si+2CO↑与NaCl+K KCl+Na
2
B.SiO+CaCO CaSiO +CO ↑与NaSiO+CO +H O=Na CO+H SiO↓
2 3 3 2 2 3 2 2 2 3 2 3
C.SiO+2OH-= +H O与CO+2OH-= +H O
2 2 2 2
D.SiO+2C Si+2CO↑与SiO+Na CO NaSiO+CO
2 2 2 3 2 3 2
【答案】B
【解析】A.都是高温下同主族元素单质间的置换反应,生成气体使反应趋于完全,原理相同,故A不符
合题意;
B.前者是高温下的固体反应,生成的二氧化碳气体使反应趋于完全,后者是溶液中的强酸制弱酸的复分
解反应,原理不同,故B符合题意;
C.二者都是酸性氧化物与碱的反应,原理相同,故C不符合题意;
D.前者是氧化还原反应,后者是非氧化还原反应,但本质上两个反应都是高温固相反应,生成气体使反
应趋于完全,原理相同,故D不符合题意;
故答案为:B
6.(2021·甘肃·民勤县第四中学高一期中)我国科学家成功研制SiO 超分子纳米管,其微观结构如图,下
2
列叙述不正确的是
A.该超分子性质稳定,不与任何酸发生反应
B.SiO 是酸性氧化物
2
C.SiO 在工业上可用于制造光导纤维
2
D.SiO 是水晶项链的主要成分
2
【答案】A
【解析】A.二氧化硅能与氢氟酸发生反应,A错误;
B.SiO 能与碱反应生成盐和水,属于酸性氧化物,B正确;
2C.SiO 制成的纤维能够传导光波和各种光信号,在工业上可用于制造光导纤维,C正确;
2
D.水晶的成分是SiO,D正确。
2
故选A。
7.(2021·山东邹城·高一期中)由粗 制备纯的 流程如图所示,下列说法不正确的是
A. 属于酸性氧化物
B.二氧化硅是将太阳能转变为电能的常用材料
C.若在实验室中完成步骤Ⅲ,应该在坩埚中进行
D.步骤Ⅱ反应的离子方程式为
【答案】B
【解析】A.SiO 能和碱反应生成盐和水,属于酸性氧化物,A正确;
2
B.二氧化硅为光导纤维的常用材料,将太阳能转变为电能的常用材料为硅单质,B错误;
C.灼烧时所用温度较高,应在坩埚中进行,C正确;
D.步骤Ⅱ中CO 过量,所以得到硅酸沉淀和碳酸氢钠,离子方程式为
2
,D正确;
综上所述答案为B。
题组三 硅酸
1.(2020·全国·高一课时练习)由反应NaSiO+2HCl===2NaCl+HSiO↓制取硅酸,不可能的反应原理
2 3 2 3
是( )
A.强酸制取弱酸的原理
B.可溶性酸制取难溶性酸的原理
C.溶液中离子结合生成沉淀的原理
D.氧化还原反应的原理
【答案】D
【解析】A.该反应是由可溶性的强酸(盐酸)与硅酸钠溶液反应,反应得到的硅酸属于弱酸,故A正确,但不符合题意;
B.用盐酸制取难溶性的硅酸,即可溶性酸制取难溶性酸的原理,故B正确,但不符合题意;
C.盐酸与硅酸钠反应生成难溶的硅酸,硅酸还是一种弱酸,反应的实质是溶液中的氢离子与硅酸根离子结
合生成难溶性或难电离的硅酸,故C正确,但不符合题意;
D.该反应是复分解反应,无化合价变化,所以不是氧化还原反应,故D错误,符合题意。
故选D。
2.(2021·全国·高一课时练习)下列关于硅酸的说法正确的是( )
A.硅酸是一种不溶于水的含氧酸 B.硅酸不溶于水,是一种非电解质
C.硅酸的酸性比碳酸强 D.硅酸可由二氧化硅与水反应制得
【答案】A
【解析】A. 硅酸是一种不溶于水的含氧酸,A正确;
B. 硅酸不溶于水,是一种电解质,B错误;
C. 硅酸的酸性比碳酸弱,C错误;
D. 二氧化硅与水不反应,不能制备硅酸,D错误;
答案选A。
3.(2021·山东省)能证明碳酸比硅酸酸性强的实验事实是
A.CO 是气体,而SiO 是固体 B.高温下能反应 NaCO+SiO=Na SiO+CO↑
2 2 2 3 2 2 3 2
C.CO 溶于水生成碳酸,而SiO 却不溶于水D.CO 通入NaSiO 溶液中有胶状沉淀生成
2 2 2 2 3
【答案】D
【解析】A、氧化物的状态不能决定氧化物水化物的酸性强弱,故A错误;B、反应原理是高沸点制低沸
点气体,之所以能发生是因为生成了挥发性的气体二氧化碳,故B错误;C、氧化物的水溶性不能决定其
水化物的酸性强弱,故C错误;D、CO+H O+Na SiO═Na CO+H SiO↓,强酸能制弱酸,所以酸性:碳酸
2 2 2 3 2 3 2 3
>硅酸,故D正确。故选D。
4(2021·江苏)某同学设计如图装置,探究非金属性质变化规律.
(1)已知硅酸(H SiO)是一种难溶于水的弱酸,呈白色.现有硝酸、碳酸钙、澄清石灰水、硅酸钠溶液,选
2 3
择试剂并用如图装置证明N、C、Si的非金属性强弱顺序.①A中试剂为________;B中试剂为__________________.
②C中反应的离子方程式为________.
③该实验方案中明显不合理之处是________.
(2)利用上图装置证明氯气的氧化性强于碘单质的氧化性.
①A 中装浓盐酸,B 中装入高锰酸钾粉末,C 中试剂为______________;.
a.碘水 b.碘化钾溶液 c.碘的四氯化碳溶液 d.碘酸钾溶液
②C 中反应的离子方程式为________.
③该实验装置有明显不足,改进的方法是________.
(3)如果C 中装氢硫酸(H S 溶液),A 中装浓盐酸,B 中装高锰酸钾粉末,反应开始后观察到的现象是 C
2
中产生淡黄色沉淀,C 中反应的化学方程式_________________,该实验________;(填“能”或“不
能”)证明氯的非金属性比硫强。
【答案】(1)①硝酸 碳酸钙 ② CO+SiO 2﹣+H O=HSiO↓+CO 2﹣
2 3 2 2 3 3
③ 硝酸易挥发,硝酸进入 C 中与硅酸钠反应生成硅酸
(2)①b ②2I﹣+Cl═I +2Cl﹣ ③增加装有氢氧化钠溶液的尾气吸收装置
2 2
(3) Cl+H S═S↓+2HCl 能
2 2
【解析】(1)①现有硝酸、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用题中装置证明:酸性:
HNO>H CO>H SiO,根据强酸制弱酸可知,A中试剂是硝酸、B中物质是碳酸钙;
3 2 3 2 3
②硝酸和碳酸钙反应生成二氧化碳,二氧化碳通入硅酸钠溶液生成硅酸沉淀,装置C中离子反应是:
CO+SiO 2-+H O=HSiO↓+CO 2-;
2 3 2 2 3 3
③硝酸易挥发,硝酸进入C中与硅酸钠反应生成硅酸,所以不能确定C中反应物是二氧化碳还是硝酸,故
该实验方案中明显不合理之处是:硝酸易挥发,硝酸进入C中与硅酸钠反应生成硅酸;
(2)①利用题中装置证明氯气氧化性强于碘单质的氧化性,C中发生的是氯气和碘离子的反应,生成碘单质,
碘单质遇淀粉变蓝,所以C中加入碘化钾溶液;
② C中发生的是氯气和碘离子的反应,离子方程式为:2I-+Cl═I +2Cl-;
2 2
③生成的氯气有毒,需要尾气吸收处理,该实验装置的明显不足是没有尾气处理装置,改进的方法是在C
后增加装有氢氧化钠溶液的尾气吸收装置;
(3)如果C中装氢硫酸(H S溶液),A 中装浓盐酸,B中装高锰酸钾粉末,反应开始后观察到的现象是C中
2
产生淡黄色沉淀,C中反应的化学方程式为:Cl+H S═S↓+2HCl,说明氯气氧化硫化氢为硫单质,在氧化
2 2
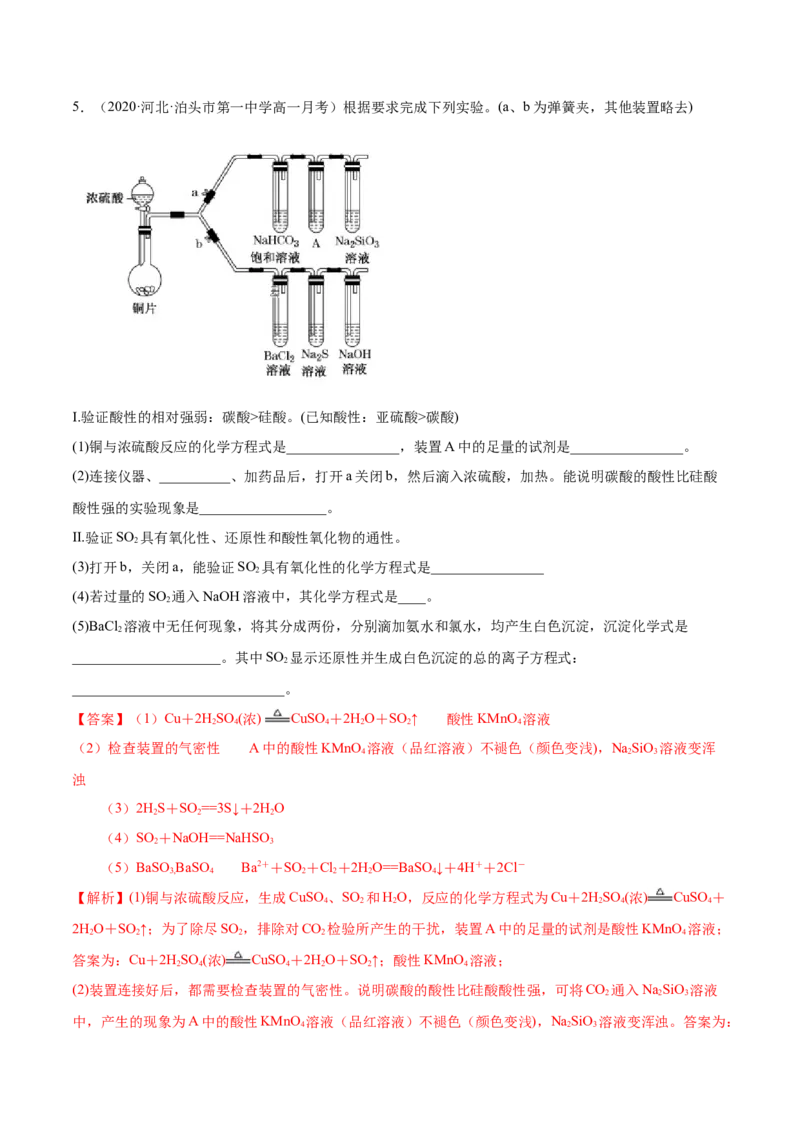
还原反应中,氧化剂的氧化性大于氧化产物的氧化性,因此能判断氯的非金属性比硫强。5.(2020·河北·泊头市第一中学高一月考)根据要求完成下列实验。(a、b为弹簧夹,其他装置略去)
Ⅰ.验证酸性的相对强弱:碳酸>硅酸。(已知酸性:亚硫酸>碳酸)
(1)铜与浓硫酸反应的化学方程式是________________,装置A中的足量的试剂是________________。
(2)连接仪器、__________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。能说明碳酸的酸性比硅酸
酸性强的实验现象是__________________。
Ⅱ.验证SO 具有氧化性、还原性和酸性氧化物的通性。
2
(3)打开b,关闭a,能验证SO 具有氧化性的化学方程式是________________
2
(4)若过量的SO 通入NaOH溶液中,其化学方程式是____。
2
(5)BaCl 溶液中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀化学式是
2
_____________________。其中SO 显示还原性并生成白色沉淀的总的离子方程式:
2
______________________________。
【答案】(1)Cu+2HSO (浓) CuSO +2HO+SO ↑ 酸性KMnO 溶液
2 4 4 2 2 4
(2)检查装置的气密性 A中的酸性KMnO 溶液(品红溶液)不褪色(颜色变浅),NaSiO 溶液变浑
4 2 3
浊
(3)2HS+SO ==3S↓+2HO
2 2 2
(4)SO +NaOH==NaHSO
2 3
(5)BaSO BaSO Ba2++SO +Cl+2HO==BaSO ↓+4H++2Cl-
3, 4 2 2 2 4
【解析】(1)铜与浓硫酸反应,生成CuSO 、SO 和HO,反应的化学方程式为Cu+2HSO (浓) CuSO +
4 2 2 2 4 4
2HO+SO ↑;为了除尽SO ,排除对CO 检验所产生的干扰,装置A中的足量的试剂是酸性KMnO 溶液;
2 2 2 2 4
答案为:Cu+2HSO (浓) CuSO +2HO+SO ↑;酸性KMnO 溶液;
2 4 4 2 2 4
(2)装置连接好后,都需要检查装置的气密性。说明碳酸的酸性比硅酸酸性强,可将CO 通入NaSiO 溶液
2 2 3
中,产生的现象为A中的酸性KMnO 溶液(品红溶液)不褪色(颜色变浅),NaSiO 溶液变浑浊。答案为:
4 2 3检查装置的气密性;A中的酸性KMnO 溶液(品红溶液)不褪色(颜色变浅),NaSiO 溶液变浑浊;
4 2 3
(3)验证SO 具有氧化性,应与还原剂HS发生反应,反应的化学方程式为2HS+SO ==3S↓+2HO。答案
2 2 2 2 2
为:2HS+SO ==3S↓+2HO;
2 2 2
(4)过量的SO 通入NaOH溶液中,最终生成NaHSO,反应的化学方程式为SO +NaOH==NaHSO 。答案
2 3 2 3
为:SO +NaOH==NaHSO ;
2 3
(5)溶有SO 的BaCl 溶液中滴加氨水时,会发生反应,生成BaSO 等;滴加氯水,会发生氧化还原反应,
2 2 3
生成BaSO。SO 显示还原性并生成白色沉淀时,SO 被氧化生成硫酸,最后转化为BaSO,而Cl 转化为
4 2 2 4 2
HCl,反应的离子方程式为Ba2++SO +Cl+2HO==BaSO ↓+4H++2Cl-。答案为:BaSO、BaSO;Ba2+
2 2 2 4 3 4
+SO +Cl+2HO==BaSO ↓+4H++2Cl-。
2 2 2 4
6.(2020·全国·高一单元测试)设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶
液、硅酸溶液的酸性强弱顺序是:CHCOOH>H CO>H SiO
3 2 3 2 3
(1)利用如图所示仪器可以组装实验装置,则仪器的连接顺序为:______接_____, _____接_____,
_____接_____。
(2)写出实验步骤、现象和有关的化学方程式。_____________
【答案】(1)A D E B C F
(2)第一步:打开分液漏斗止水阀;现象:锥形瓶中产生气泡;化学方程式:
。
第二步:打开导管上的止水夹;现象:试管中产生白色沉淀;化学方程式:
。
【解析】(1)证明三种酸的酸性强弱顺序,应运用强酸制弱酸的原理:证明醋酸酸性大于碳酸酸性,应
让醋酸与碳酸钠反应故A接D;证明碳酸酸性大于硅酸酸性,应用二氧化碳与硅酸钠溶液反应,故E接
B,C接F;
故答案为:A;D;E;B;C;F;
(2)第一步:醋酸制取二氧化碳;现象:锥形瓶中产生气泡;化学方程式:;
第二步:碳酸制取硅酸;现象:试管中产生白色沉淀;化学方程式:
。
故答案为:第一步:打开分液漏斗止水阀;现象:锥形瓶中产生气泡;化学方程式:
。第二步:打开导管上的止水夹;现象:试管中产生
白色沉淀;化学方程式: 。
题组四 硅酸盐材料
1.(2021·湖北·高一期中)下列关于硅酸盐的叙述中,不正确的是
A.硅酸盐是由硅、氧和金属组成的混合物
B.硅酸盐结构较为复杂,大多不溶于水,化学性质很稳定
C.硅氧四面体中,硅原子与氧原子都是以共价键结合
D.水泥与玻璃的共同原料是石灰石,水泥与陶瓷的共同原料是黏土
【答案】A
【解析】A.硅酸盐是由硅、氧和金属组成的化合物,属于纯净物,故A错误;
B.硅酸盐除硅酸钠、硅酸钾可溶外,大多不溶于水,则不易和其它物质反应,所以化学性质很稳定,故
B正确;
C.硅氧四面体中,硅原子与氧原子都是以共价键结合,故C正确;
D.石灰石是制备玻璃、水泥等物质的工业原料之一,陶瓷原料主要是黏土,故D正确;
故选:A。
2.(2021·浙江·高一月考)下列不属于硅酸盐材料的是
A.陶瓷 B.水泥 C.玻璃 D.光导纤维
【答案】D
【解析】硅酸盐产品主要有陶瓷、玻璃、水泥等,光导纤维的主要成分为二氧化硅,是氧化物,不是硅酸
盐,故选D。
3.(2021·浙江·丽水外国语实验学校高一月考)“九秋枫露越窑开,夺得千峰翠色来”是藏誉越窑青瓷的
诗句,描绘我国古代精美的青瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法正确的是
A.水泥是人类最早使用的硅酸盐制品B.制陶瓷的原料为纯碱、石灰石、和石英砂
C.玻璃属于硅酸盐制品,通常性质稳定、熔点较高
D.沙子和水晶的主要成分均为硅酸盐
【答案】C
【解析】A. 陶瓷是人类最早使用的硅酸盐制品,不是水泥,故A错误;
B. 制陶瓷的原料是黏土,为纯碱、石灰石、和石英是制造玻璃的原料,故B错误;
C. 玻璃属于硅酸盐制品,通常性质稳定,熔点较高,故C正确;
D. 沙子和水晶的主要成分是二氧化硅,是氧化物,不是硅酸盐,故D错误;
故选C。
4.(2021·广东海丰·高一期中)《青花瓷》一歌中有这样一句歌词:“瓶身描绘的牡丹一如你初妆”,青
花瓷瓶身上的图案让人赏心悦目。但古瓷中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,
如蓝紫色的硅酸铜钡(BaCuSi O)。下列说法不正确的是
2 6
A.硅酸铜钡是一种硅酸盐
B.硅酸铜钡性质稳定,不易脱色
C.水晶、玛瑙的主要成分也是硅酸盐
D.制造陶瓷的原材料也可用于制造水泥
【答案】C
【解析】A.根据题干可知,蓝紫色的硅酸铜钡(BaCuSi O)属于硅酸盐,A正确;
2 6
B.由古瓷能长时间保存可知,硅酸铜钡性质稳定,不易脱色,B正确;
C.水晶、玛瑙的主要成分是二氧化硅,C错误;
D.黏土是制造陶瓷和水泥的共同原料,D正确;故选C。
5.(2021·吉林·乾安县第七中学高一月考)化合物A、D、F是中学化学中常见的物质,化合物B、C、E
中含有两种相同的元素,这些化合物之间存在如图所示的反应关系,其中A和B的反应是一种硅酸盐工业
生产中的主要反应之一。
(1)在A、C、F中含有的相同元素是_______。
(2)化合物C的化学式是_______。
(3)C的水溶液和D能否发生反应?_______,其理由是_______。如能反应,请写出离子反应方程式:_______。
【答案】(1)钠或钾 (2) NaSiO 或KSiO
2 3 2 3
(3)能 C的水溶液和D(CO )反应生成酸性更弱的硅酸 SiO +CO +H O=HSiO↓+CO
2 2 2 2 3
【解析】(1)由于A和C可以和盐酸反应,所以分别应该是碳酸钠和硅酸钠,而钠和钾是物理化学性质相近
的金属,故A和C也可以是碳酸钾和硅酸钾,而F则是氯化钠或者氯化钾,故相同元素为钠或钾;
(2)已知C可以和盐酸反应,所以一定是硅酸盐,故为NaSiO 或KSiO;
2 3 2 3
(3)C的水溶液中有SiO ,和二氧化碳溶于水形成的碳酸发生反应,由于硅酸酸性小于碳酸,符合强酸生
弱酸的化学原理,故反应能发生,反应离子方程式为:SiO +CO +H O=HSiO↓+CO ;
2 2 2 3
6.(2021·辽宁·清原满族自治县第二高级中学高一期中)氮化硅高温陶瓷材料是现代重要的结构陶瓷,因
其具有硬度大、熔点高、化学性质稳定等特点而受到广泛关注。工业上普遍用图所示流程进行生产:
(1)SiO 和C反应除了得到粗硅外,还有可能得到一种硬度也很大的物质,是生成粗硅还是生成该物质
2
主要是由_______决定的。
(2)反应①的条件是_______。
(3)写出反应②的化学方程式:_______。
(4)A中可能的杂质有_______。
(5)现在用四氯化硅、氮气、氢气在稀有气体保护下加强热,得到纯度较高的氮化硅,其反应的化学方
程为_______。
【答案】(1)C的用量
(2)高温、隔绝空气
(3)3CuO+2NH 3Cu+N +3H O
3 2 2
(4)NH 及水蒸气
3(5)3SiCl +2N +6H Si N+12HCl
4 2 2 3 4
【解析】(1)在高温下SiO 与C混合,发生反应产生Si、CO。如果碳足量,生成的Si与C继续反应生成
2
硬度也很大的物质SiC,所以C的用量决定生成物是Si单质还是SiC。
(2)H 还原SiCl 需在高温条件下进行,由于H 是可燃性气体,与空气混合加热会发生爆炸,所以发生反
2 4 2
应条件是高温条件下、隔绝空气。
(3)氨气还原氧化铜生成单质铜、氮气和水,根据原子守恒、电子守恒、电荷守恒,可得该反应的化学
方程式为:3CuO+2NH 3Cu+N +3H O。
3 2 2
(4)在加热条件下,NH 还原CuO制取N 时可能不能完全发生反应,因此制取得到的N 中往往含有过量
3 2 2
的NH 及水蒸气。
3
(5)SiCl 与N、H 在稀有气体保护下加强热,得到纯度较高的氮化硅,根据原子守恒、电子守恒,可得
4 2 2
该反应的化学方程为:3SiCl +2N +6H Si N+12HCl。
4 2 2 3 4
题组五 新型无机非金属
1.(2021·云南·峨山彝族自治县第一中学高一期中)华为麒麟芯片是一种半导体材料,下列可用作麒麟芯
片材料的是
A.铝 B.硅 C.碳 D.铁
【答案】B
【解析】硅的性质是可以做半导体,芯片的材质主要是硅,故正确答案为:B
2.(2021·河南·信阳高中高一月考)化学与生产、生活、科技息息相关,下列叙述错误的是
A.华为首款5G手机搭载了7nm制程的麒麟980芯片,此芯片的主要成分是Si
B.国产飞机C919用到氮化硅陶瓷是新型无机非金属材料
C.“司南之杓(勺),投之于地,其柢(勺柄)指南”中“杓”的材质是FeO
D.小苏打是制作面包等糕点的膨松剂,也可用于治疗胃酸过多
【答案】C
【解析】A.硅属于半导体材料,可用于制造芯片,所以麒麟980芯片的主要成分是Si,故A正确;
B.氮化硅陶瓷是由非金属元素形成的化合物,具有耐高温、抗氧化、耐腐蚀等优良性能,是新型无机非金属材料,故B正确;
C.“司南之杓(勺),投之于地,其柢(勺柄)指南”,结合以上信息分析可知该物质具有磁性,四氧化三铁
为磁性氧化铁,具有磁性,因此“杓”的材质是Fe O,故C错误;
3 4
D.碳酸氢钠受热分解生成二氧化碳气体,能够使面团疏松多孔,可做膨松剂;碳酸氢钠能够与盐酸反应,
且碱性较弱,可以用来治疗胃酸过多,故D正确;
故选C。
3.(2021·安徽·高一月考)近年来,我国在无机非金属材料领域的发展受到世界瞩目。下列叙述正确的是
A.石墨烯是电阻率高的新型材料
B.氮化硅陶瓷属于传统无机非金属材料
C.二氧化硅导电性良好
D.陶瓷是以黏土为原料制成的
【答案】D
【解析】A.石墨烯能导电,是电阻率低的新型材料,A错误;
B. 新型材料是具有传统材料所不具备的优异性能和特殊功能的材料材料,氮化硅陶瓷属于新型无机非金
属材料,B错误;
C. 二氧化硅适合做光导纤维,因为对光的全反射,不是利用导电性,C错误;
D. 陶瓷是以黏土为原料经过高温烧制而成的硅酸盐材料,D正确;
答案选D。
4.(2021·辽宁·大连市一0三中学高一月考)《厉害了,我的国》展示了中国五年来探索太空,开发深海,
建设世界第一流的高铁、桥梁、码头,5G技术联通世界等取得的举世瞩目的成就。它们与化学有着密切联
系。下列说法正确的是:
A.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料,主要成分是硅酸
盐
B.我国发射的“嫦娥三号”卫星中使用的碳纤维,是一种新型无机非金属材料
C.C 是富勒烯的代表物,与石墨烯互称为同位素
60
D.SiO 制备粗硅发生反应的化学方程式为:SiO+C Si+CO
2 2 2
【答案】B
【解析】A.高温结构陶瓷是新型无机非金属材料,而硅酸盐是传统无机非金属材料,A不正确;
B.碳纤维属于无机物,且不属于传统无机非金属材料,所以是一种新型无机非金属材料,B正确;
C.C 和石墨烯都属于碳单质,二者互称为同素异形体,C不正确;
60D.用焦炭还原SiO 制备粗硅时,还生成一氧化碳气体,发生反应的化学方程式为:SiO+2C
2 2
Si+2CO↑,D不正确;
故选B。
5.(2021·湖南省常德芷兰实验学校高一期中)化学与生活息息相关,下列有关说法不正确的是
A.国产飞机C919用到的氮化硅陶瓷是新型有机非金属材料
B.硫酸钡不溶于水、不溶于酸且不能被X射线透过,可用作X射线检测的“钡餐”
C.彩色玻璃是制玻璃过程中会加入一些金属氧化物或盐制得的,可用于建筑物和装饰
D.熟石膏与水混合成糊状物会很快凝固,医疗上可用来制作石膏
【答案】A
【解析】A.氮化硅陶瓷是新型无机非金属材料,故A错误;
B.硫酸钡不溶于水、不溶于酸且不能被X射线透过,可用作X射线检测的“钡餐”,故B正确;
C.彩色玻璃是制玻璃过程中加入一些金属氧化物或盐制得的,如加入Co O 玻璃呈蓝色,故C正确;
2 3
D.熟石膏与水混合成糊状后会很快凝固,转化为坚硬的生石膏,利用石膏的这一性质,医疗上可用来制
作石膏绷带,故D正确。
故选A。
6.(2021·吉林·乾安县第七中学高一月考)下列关于无机非金属材料的说法不正确的是
A.传统无机非金属材料是指:玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的缺点,具有极大强度
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
【答案】D
【解析】A.硅酸盐材料是传统的无机非金属材料,主要包括:玻璃、水泥、陶瓷,故A正确;
B.新型无机非金属材料不但克服了传统的无机非金属材料的缺点,而且同时还具有了如能承受高温、强
度较高,故B正确;
C.高温结构材料属于新型的无机非金属材料,具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优
点,故C正确;
D.新型无机非金属材料如高温结构陶瓷(Si N 陶瓷、SiC陶瓷)的主要成分不是硅酸盐,只有传统无机非金
3 4
属材料才是硅酸盐,故D错误;
故答案选:D。7.(2021·海南·琼中中学高一期中)近年来新型无机非金属材料种类众多、应用广泛,下列说法错误的是
A.高纯硅可用作光伏电池和电脑芯片
B.二氧化硅可用作生产光导纤维
C.新型陶瓷碳化硅(SiC)可作耐高温结构材料
D.富勒烯、石墨烯都是有机化合物
【答案】D
【解析】A.高纯硅广泛应用于光伏电池和电脑芯片,选项A正确;
B.光导纤维的成分是二氧化硅,选项B正确;
C.碳化硅(SiC)陶瓷基复合材料是一种新型热结构材料,可作耐高温结构材料,选项C正确;
D.富勒烯、石墨烯都是碳形成的单质,不属于有机化合物,选项D错误;
答案选D。
8.(2021·浙江浙江·高一期中)《厉害了,我的国》展示了中国制造的重点工程,下列所涉及的材料不属
于无机非金属材料的是
A.“中国天眼”的钢铁圈梁“眼眶”
B.中国第一艘深海载人潜水器“蛟龙号”使用的氮化硅陶瓷发动机
C.“嫦娥四号”月球探测器使用的晶体硅芯片
D.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷
【答案】A
【解析】A.“中国天眼”的钢铁圈梁“眼眶”属于金属材料,故A符合;
B.氮化硅陶瓷发动机属于新型无机非金属材料,故B不符合;
C.晶体硅芯片成分为硅单质,属于无机非金属材料,故C不符合;
D.高温结构陶瓷属于新型无机非金属材料,故D不符合;
故选A。
9.(2021·河北邢台·高一月考)“中国名片”“中国制造”的发展举世瞩目,它们与化学有着密切联系。
下列说法不正确的是
A.北斗卫星导航系统由中国自主研发、独立运行,其所用芯片的主要成分为Si
B.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
C.石墨烯液冷散热技术是我国首创的,所使用的材料石墨烯是一种无机非金属材料
D.抗击新型冠状病毒过程中用到的“84”消毒液的有效成分是NaClO
【答案】B
【解析】A.北斗卫星导航系统其所用芯片的主要成分为Si,是良好的半导体,故A正确;
B.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷,新型无机非金属材料在性能上比传统无机非金属材料有了很大的提高,可适用于不同的要求,如高温结构陶瓷、压电陶瓷、透明陶瓷、超导陶瓷
等都属于新型无机非金属材料,不属于传统的硅酸盐材料,故B错误;
C.石墨烯液冷散热技术是我国首创的,所使用的材料石墨烯是一种无机非金属材料,具有良好的热传导
性能,故C正确;
D.抗击新型冠状病毒过程中用到的“84”消毒液的有效成分是NaClO,可以起到消毒杀菌的作用,故D正
确;
故选B。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育