文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第二课时 化学反应与电能
【学习目标】1.通过查阅资料、阅读思考,能举出化学能转化为电能的实例,辨识简单原电池的正
负极及正负极上发生的化学反应类型。
2.通过实验探究、讨论交流,知道原电池概念及原电池工作原理是利用氧化还原反应将化学能转化
为电能的装置,知道构成原电池的条件。
3.通过观察现象、原理分析,会判断原电池的正极、负极,能正确书写简单原电池的电极反应式,了
解常见的化学电源,感受化学能转化为电能的奇妙。
【学习重点】原电池概念、原理、组成及应用
【学习难点】原电池工作原理及构成条件
【课前预习】
旧知回顾:1.氧化还原反应的特征和本质分别是什么?
2.化学反应中物质变化和能量变化有何特点?
新知预习:1.火力发电过程中能量是如何转化的?火力发电存在哪些问题?
① 火力发电过程中能量是转化:
②火力发电的缺点:
2.构成原电池的条件是什么?在原电池中电子、电流的流向有何特点?
【课中探究】
情景导入:电能是现代社会中应用最广泛,使用最方便、污染最小的一种二次能源,又称电力。小到
日常生活中使用的手提电脑、手机、相机、摄像机……大到火箭上天、神州六号宇宙飞船遨游太空,这一
切都依赖于电池的应用。播放电池的发展史(见PPT视频)一、原电池原理及构成条件
活动一、探究化学能与电能的转化
任务一、阅读思考:阅读教材P36页内容,思考生活中人们使用的电能来自于哪里?火力发电中化学能
是如何转化为电能的?有何优缺点?
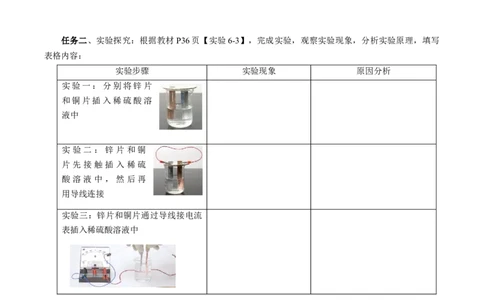
任务二、实验探究:根据教材P36页【实验6-3】,完成实验,观察实验现象,分析实验原理,填写
表格内容:
实验步骤 实验现象 原因分析
实验一:分别将锌片
和铜片插入稀硫酸溶
液中
实验二:锌片和铜
片先接触插入稀硫
酸溶液中,然后再
用导线连接
实验三:锌片和铜片通过导线接电流
表插入稀硫酸溶液中
任务三、讨论交流:结合【实验6-3】,以铜锌稀硫酸原电池为例,思考什么是原电池?有何特点?
你认为构成原电池的条件是什么?并填写表格内容。
①原电池的概念及工作原理:
概念
装置示意图
电极材料 电极名称 电子转移 电极反应式 反应类型锌片
铜片
电子的流向
反应本质
总反应式
②构成原电池的条件:
【对应训练】1.下列叙述不正确的是( )
A.用天然气火力发电时,每一步都需要化学反应来完成
B.利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境
C.原电池反应一定为氧化还原反应
D.在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化
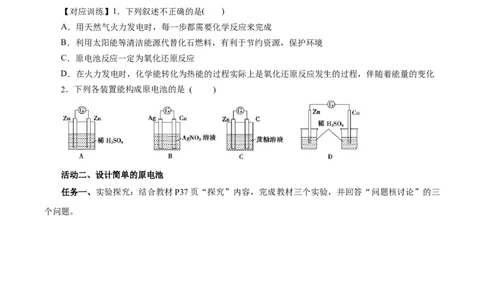
2.下列各装置能构成原电池的是 ( )
活动二、设计简单的原电池
任务一、实验探究:结合教材P37页“探究”内容,完成教材三个实验,并回答“问题核讨论”的三
个问题。
原电池的设计方法:
任务二、归纳小结:请画出原电池的工作原理示意图,思考如何判断原电池的正负极?
①原电池的工作原理:注意:
②原电池正、负极的判断方法:
注意:
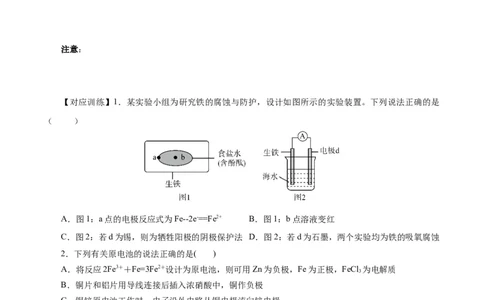
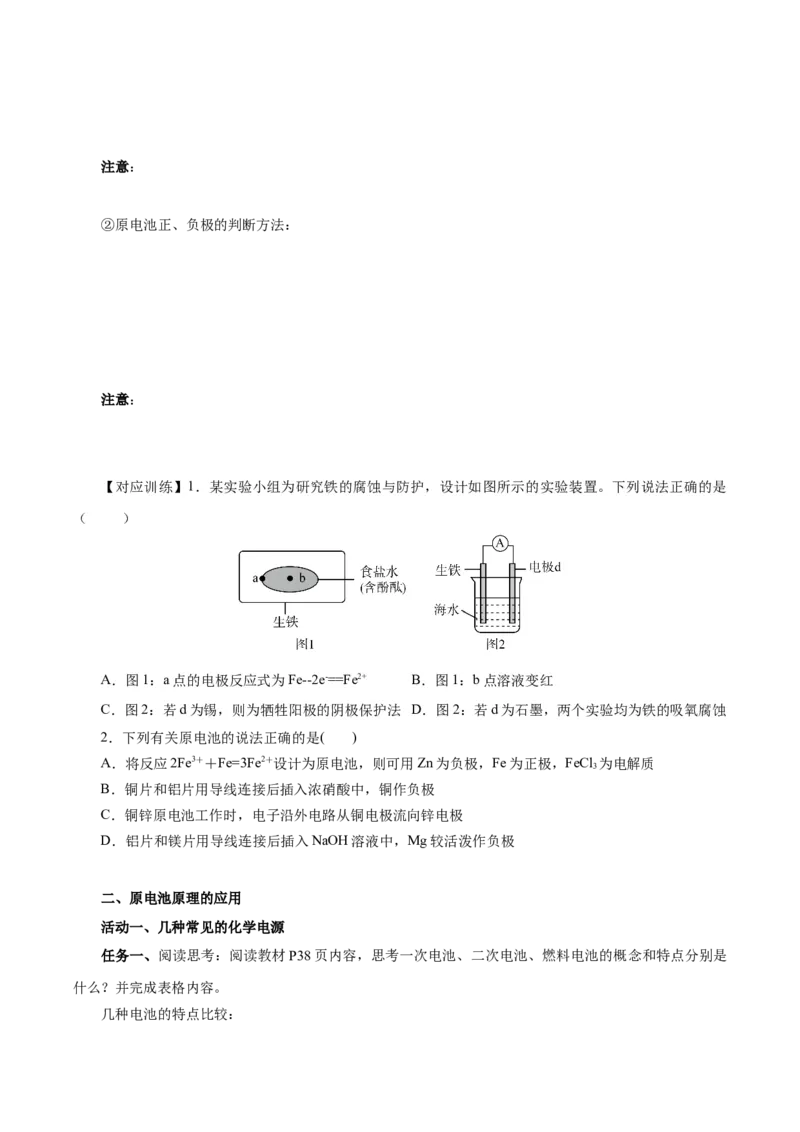
【对应训练】1.某实验小组为研究铁的腐蚀与防护,设计如图所示的实验装置。下列说法正确的是
( )
A.图1:a点的电极反应式为Fe--2e-==Fe2+ B.图1:b点溶液变红
C.图2:若d为锡,则为牺牲阳极的阴极保护法 D.图2:若d为石墨,两个实验均为铁的吸氧腐蚀
2.下列有关原电池的说法正确的是( )
A.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用Zn为负极,Fe为正极,FeCl 为电解质
3
B.铜片和铝片用导线连接后插入浓硝酸中,铜作负极
C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
D.铝片和镁片用导线连接后插入NaOH溶液中,Mg较活泼作负极
二、原电池原理的应用
活动一、几种常见的化学电源
任务一、阅读思考:阅读教材P38页内容,思考一次电池、二次电池、燃料电池的概念和特点分别是
什么?并完成表格内容。
几种电池的特点比较:名称 干电池(一次电池) 充电电池(二次电池) 燃料电池
特点
举例
任务二、讨论交流:原电池原理在化学上有哪些应用?
【对应训练】1.化学电源在日常生活和高科技领域中都有广泛应用。下列说法错误的是( )
A.图甲:通入O 的一极为正极
2
B.图乙:锌锰干电池属于一次电池
C.图乙:在使用锌锰干电池的过程中,MnO 被还原
2
D.图丙:正极的电极反应式为PbO -2e- +SO2-+4H+==PbSO +2H O
2 4 4 2
2.把A、B、C、D四块金属泡在稀HSO 中,用导线两两相连可以组成各种原电池。若A、B相连
2 4
时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极。则四
种金属的活泼性顺序由大到小排列为 ( )
A.A>C>D>B B.A>C>B>D C.B>D>C>A D.A>B>C>D
活动二、探究发展中的燃料电池
任务一、阅读思考:结合教材P39页“科学·技术·社会—发展中的燃料电池”内容,思考燃料电池的概念是什么?有何优点?
①概念:
②优点:
任务二、讨论交流:以氢氧燃料电池和甲烷燃料电池为例,思考如何书写电极反应式?
①氢氧燃料电池:
电解质溶液 负极 正极
酸性(H+)
中性(Na SO )
2 4
碱性(OH-)
②甲烷燃料电池:
电解质溶液 负极 正极
酸性(H+)
碱性(OH-)
③原电池电极反应式的书写步骤:
【对应练习】1.可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝
合金为负极,空气电极为正极。下列说法正确的是 ( )
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为O+2HO+4e-===4OH-
2 2
B.以NaOH溶液为电解液时,负极反应为Al+3OH--3e-===Al(OH) ↓
3
C.以NaOH溶液为电解液时,电池在工作过程中电解液的碱性保持不变
D.电池工作时,电子通过外电路从正极流向负极
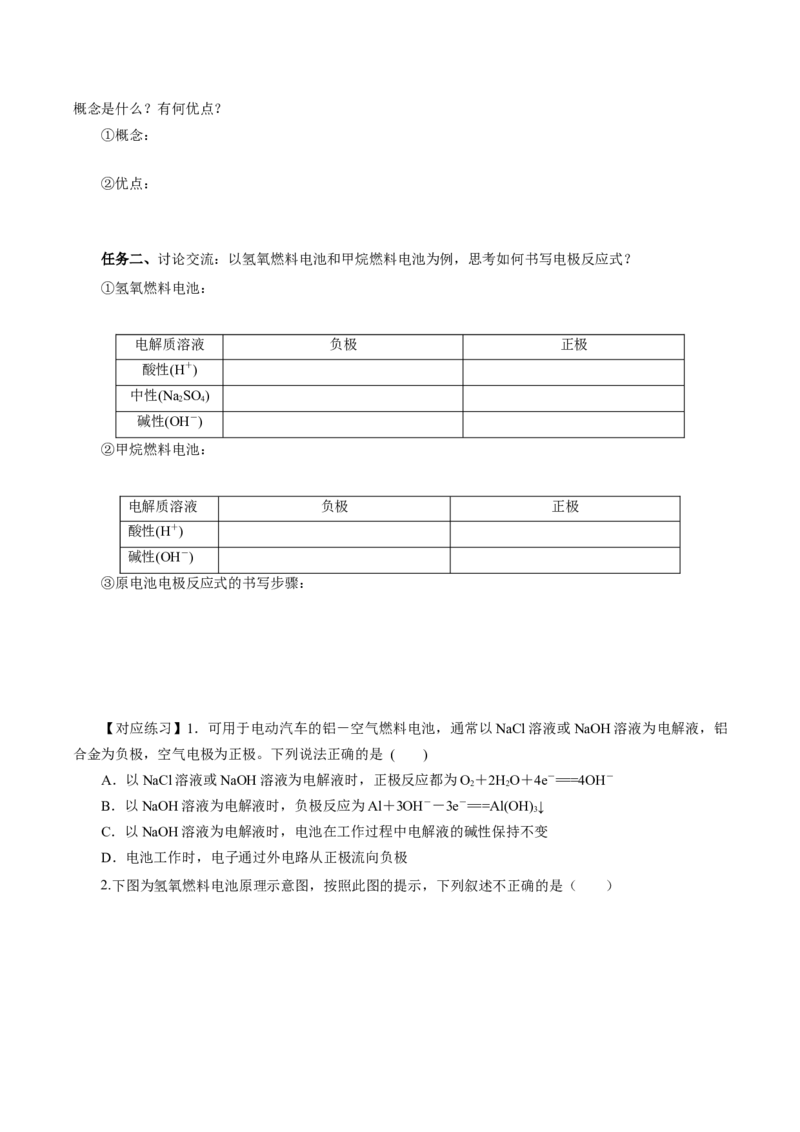
2.下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )A.b电极是正极
B.总反应方程式为2H+O ==2H O
2 2 2
C.a电极每消耗2.24LH ,转移电子0.2mol
2
D.氢氧燃料电池是一种具有广泛应用前景的绿色电源
【课后巩固】1.下列有关原电池的说法中正确的是( )
A.在外电路中,电子由负极经导线流向正极 B.在内电路中,电子由正极经电解质溶液流向负极
C.原电池工作时,正极表面一定有气泡产生 D.原电池工作时,一定不会伴随着热能变化
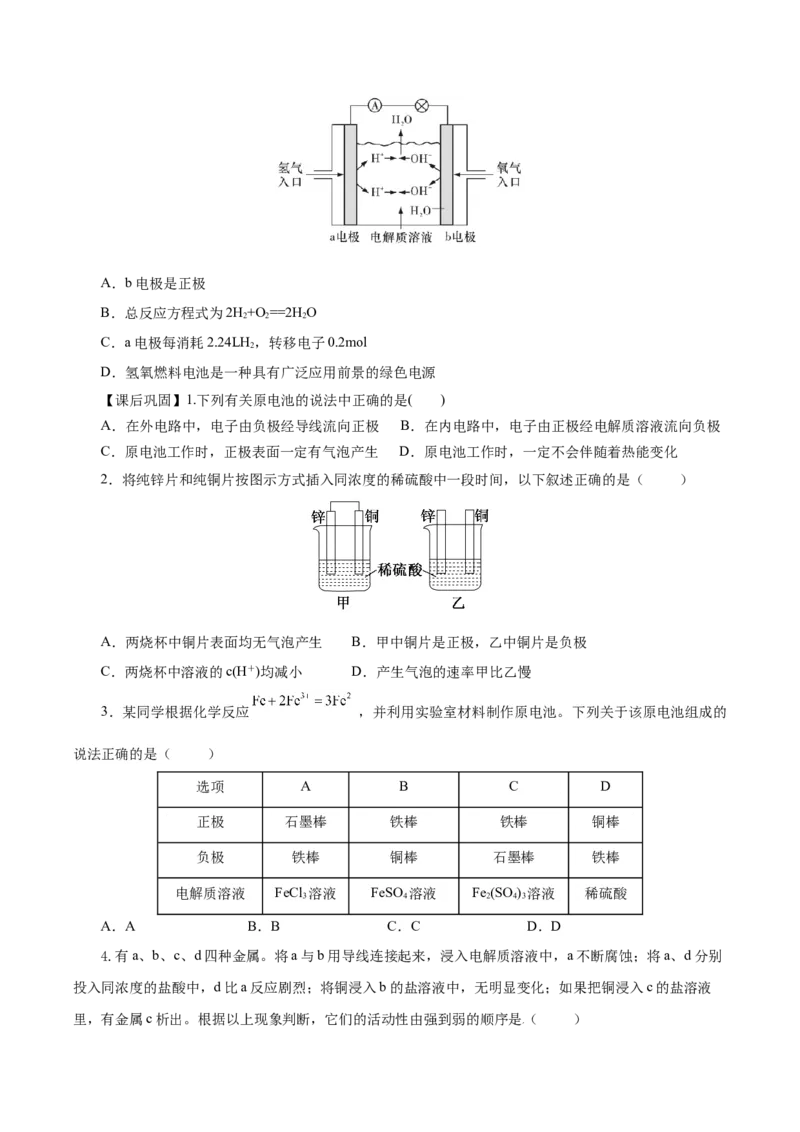
2.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的c(H+)均减小 D.产生气泡的速率甲比乙慢
3.某同学根据化学反应 ,并利用实验室材料制作原电池。下列关于该原电池组成的
说法正确的是( )
选项 A B C D
正极 石墨棒 铁棒 铁棒 铜棒
负极 铁棒 铜棒 石墨棒 铁棒
电解质溶液 FeCl 溶液 FeSO 溶液 Fe (SO ) 溶液 稀硫酸
3 4 2 4 3
A.A B.B C.C D.D
4.有a、b、c、d四种金属。将a与b用导线连接起来,浸入电解质溶液中,a不断腐蚀;将a、d分别
投入同浓度的盐酸中,d比a反应剧烈;将铜浸入b的盐溶液中,无明显变化;如果把铜浸入c的盐溶液
里,有金属c析出。根据以上现象判断,它们的活动性由强到弱的顺序是( )A.d c a b B.d a b c C.d b a c D.b a d c
5.有关如图所示四个常用电化学装置的叙述中,正确的是( )
图Ⅰ碱性锌锰电池 图Ⅱ铅-硫酸蓄电池 图Ⅲ原电池 图Ⅳ银锌纽扣电池
A.图Ⅰ所示电池属一次电池, 是作催化剂
B.图Ⅱ所示电池放电过程中,负极被氧化,质量不断增加
C.图Ⅲ所示装置工作过程中,电子由铜极经导线流向铁极
D.图Ⅳ所示电池属一次电池,正极的电极反应式为Ag O+2e-+2H+==2Ag+H O
2 2
6.氢氧燃料电池反应为: ,电解液为KOH,反应能保持在较高温度,使生成的
蒸发,下列叙述正确的是
A.该电池转移4mol电子时, 消耗22.4L
B.该电池是化学环境友好电池
C.电池工作过程中,化学能100%的转化成了电能
D.电极反应为:负极 ;正极
7.某化学兴趣小组,使用相同的铜片和锌片为电极,探究水果电池水果的种类和电极间距离对电流
的影响,实验装置图和所得实验所得数据如下:
水果种
实验编号 电极间距离/cm 电流/
类
Ⅰ 番茄 1 98.7
Ⅱ 番茄 2 72.5
Ⅲ 苹果 2 27.2电池工作时,下列说法不正确的是( )
A.负极的电极反应为Zn-2e-==Zn2+ B.水果种类和电极间距离对电流数值的大小均有影响
C.电子从锌片经水果流向铜片 D.若用石墨电极代替铜片进行实验,电流数值会发生变化
8.根据化学能转化电能的相关知识,回答下列问题:
Ⅰ.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设
计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_________,发生_________(填“氧化”或“还原”)反应,电解质溶液是
_____________。
(2)正极上出现的现象是_____________________________________________________________。
(3)若导线上转移电子1 mol,则生成银_________g。
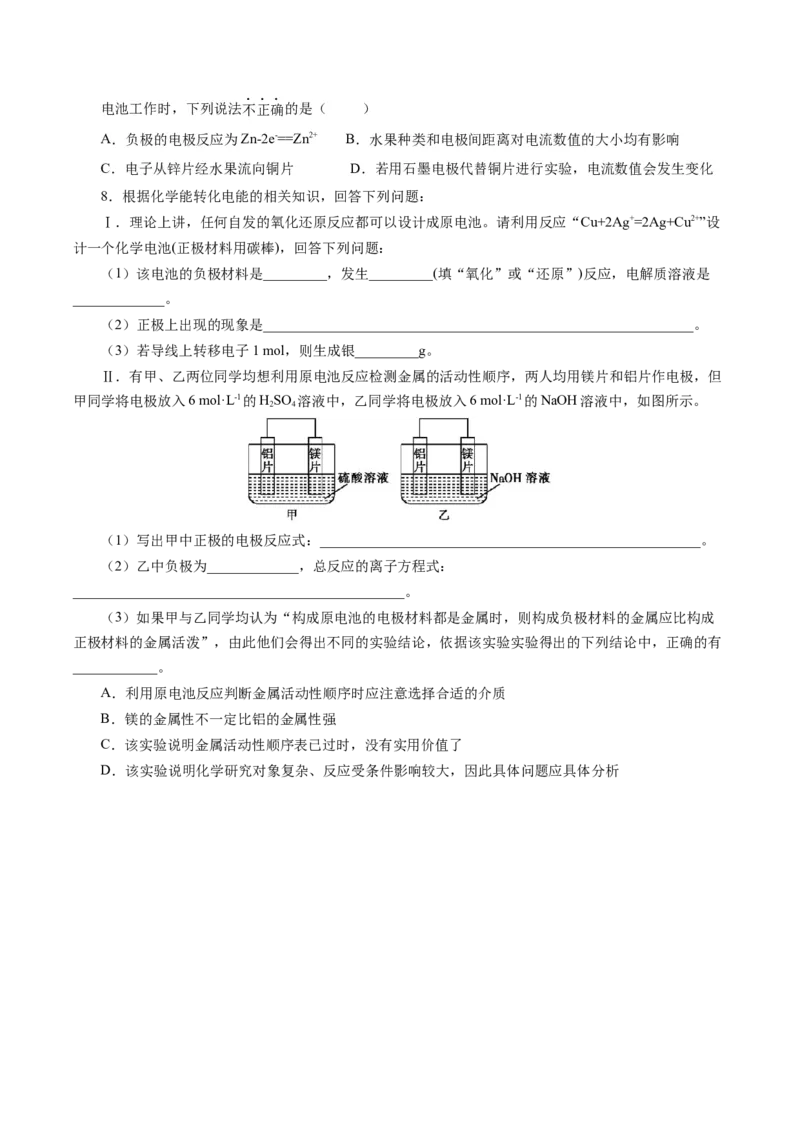
Ⅱ.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但
甲同学将电极放入6 mol·L-1的HSO 溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
2 4
(1)写出甲中正极的电极反应式:______________________________________________________。
(2)乙中负极为_____________,总反应的离子方程式:
_______________________________________________。
(3)如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成
正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验实验得出的下列结论中,正确的有
____________。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析