文档内容
第六章 化学反应与能量
第一节 化学反应的速率与限度 课时作业
第二课时 化学反应的限度及条件控制
基础达标
1.下列不属于可逆反应的是( )
A.氯气与水反应生成HC1与HClO
B.N 与H 在一定条件下可以生成NH ,同时NH 又可分解为N 和H
2 2 3 3 2 2
C.电解水生成H 和O,氢气和氧气燃烧生成HO
2 2 2
D.SO 溶于水生成HSO
2 2 3
2.对化学反应速率与化学反应限度的叙述,不正确的是( )
A.当化学反应达到最大限度时反应速率为0
B.同一化学反应,若反应条件不同,限度可能不同
C.化学反应达到限度时,正、逆反应速率相等
D.化学反应的限度与时间的长短无关
3.化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如果设法提
高化学反应的限度,下列说法错误的是( )
A.能够节约原料和能源 B.能够提高产品的产量
C.能够提高经济效益 D.能够提高化学反应速率
4.在一定条件下,使 NO 和 O 在一密闭容器中进行反应 2NO(g)+O(g)
2 2
2NO (g),下列说法中不正确的是( )
2
A.反应开始时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后为零
C.随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大
D.随着反应的进行,逆反应速率逐渐增大,最后与正反应速率相等
5.已知反应:NO (g)+SO (g) SO (g)+NO(g),起始时向某密闭容器中通入1 mol
2 2 3
NO 、2 mol S18O,反应达到平衡后,下列有关说法正确的是( )
2 2
A.NO 中不可能含18O
2
B.有1 mol N18O生成
C.S18O 的物质的量不可能为0.8 mol
2D.SO 、SO 、NO、NO 均含18O时,说明该反应达到平衡
2 3 2
6. 一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) Y(g)+Z(s),下列叙
述不能说明该反应达到化学平衡状态的是( )
A.混合气体的密度不再变化
B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等
D.单位时间内生成1 mol Y的同时生成2 mol X
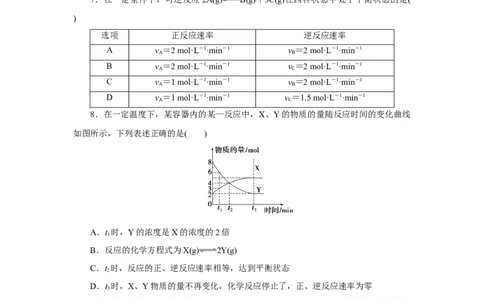
7.在一定条件下,可逆反应2A(g) B(g)+3C(g)在四种状态中处于平衡状态的是(
)
选项 正反应速率 逆反应速率
A v =2 mol·L-1·min-1 v =2 mol·L-1·min-1
A B
B v =2 mol·L-1·min-1 v =2 mol·L-1·min-1
A C
C v =1 mol·L-1·min-1 v =2 mol·L-1·min-1
A B
D v =1 mol·L-1·min-1 v =1.5 mol·L-1·min-1
A C
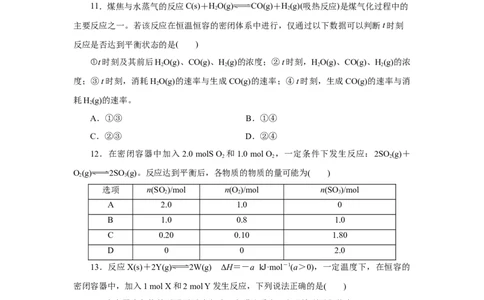
8.在一定温度下,某容器内的某一反应中,X、Y的物质的量随反应时间的变化曲线
如图所示,下列表述正确的是( )
A.t 时,Y的浓度是X的浓度的2倍
1
B.反应的化学方程式为X(g) 2Y(g)
C.t 时,反应的正、逆反应速率相等,达到平衡状态
2
D.t 时,X、Y物质的量不再变化,化学反应停止了,正、逆反应速率为零
3
9.恒温恒容条件下,发生化学反应:H(g)+I(g) 2HI(g),下列选项中不能作为达
2 2
到化学平衡状态的标志的是( )
A.混合气体颜色不再变化
B.单位时间内形成n mol H—H的同时断裂2n mol H—I
C.若该反应在隔热密闭体积恒定的容器中进行反应,体系的温度不再变化
D.2v(H ) =v(HI)
2 正 逆
10.化学反应速率和限度的研究对日常生活和工业生产有着重要意义。下列有关说法错误的是( )
A.向炉膛内鼓风,用煤粉代替煤块可以使炉火更旺
B.将肉类食品进行低温冷藏,能使其永远不会腐败变质
C.工业合成氨时,要同时考虑反应速率和反应限度两个方面
D.我国西周时期已发明用“酒曲”酿酒,原理是利用催化剂改变反应速率
能力提升
11.煤焦与水蒸气的反应C(s)+HO(g) CO(g)+H(g)(吸热反应)是煤气化过程中的
2 2
主要反应之一。若该反应在恒温恒容的密闭体系中进行,仅通过以下数据可以判断t时刻
反应是否达到平衡状态的是( )
①t时刻及其前后HO(g)、CO(g)、H(g)的浓度;②t时刻,HO(g)、CO(g)、H(g)的浓
2 2 2 2
度;③t时刻,消耗HO(g)的速率与生成CO(g)的速率;④t时刻,生成CO(g)的速率与消
2
耗H(g)的速率。
2
A.①③ B.①④
C.②③ D.②④
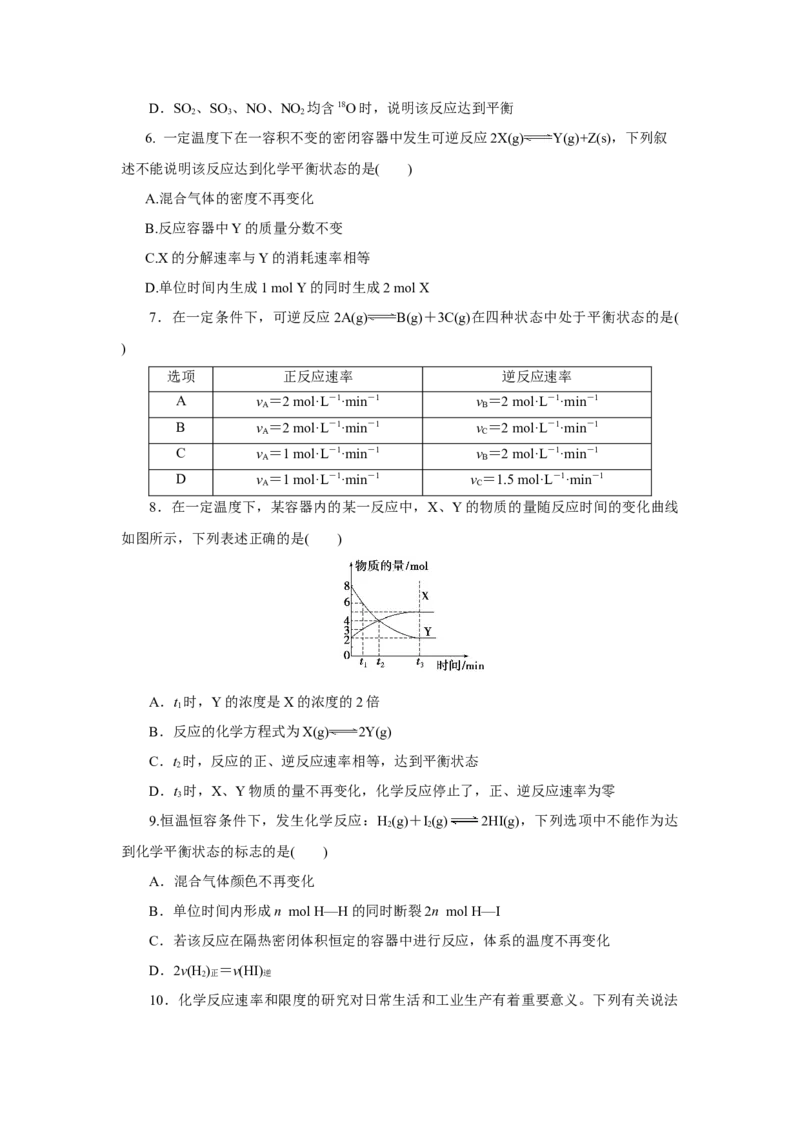
12.在密闭容器中加入 2.0 molS O 和1.0 mol O ,一定条件下发生反应:2SO (g)+
2 2 2
O(g) 2SO (g)。反应达到平衡后,各物质的物质的量可能为( )
2 3
选项 n(SO )/mol n(O )/mol n(SO )/mol
2 2 3
A 2.0 1.0 0
B 1.0 0.8 1.0
C 0.20 0.10 1.80
D 0 0 2.0
13.反应X(s)+2Y(g) 2W(g) ΔH=-a kJ·mol-1(a>0),一定温度下,在恒容的
密闭容器中,加入1 mol X和2 mol Y发生反应,下列说法正确的是( )
A.当容器中气体的压强不再改变时,表明该反应一定已达到平衡状态
B.当达到平衡状态时,X和Y的转化率之比为1∶2
C.当Y与W的物质的量浓度之比为1∶1时,表明该反应一定已到达平衡状态
D.当容器内气体的密度不再改变时,表明该反应一定已达到平衡状态
14.向某容积固定的密闭容器中加入0.3 mol A、0.1 mol C和一定量(未知)的B三种气
体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体
的平均相对分子质量没有变化。请回答下列问题:(1)密闭容器的容积是 L。
(2)若 t =15 s,则 0~t 阶段以 C 物质浓度变化表示的反应速率为 v(C)=
1 1
。
(3)写出反应的化学方程式: 。
(4)B的起始物质的量是 。
(5)判断该反应达到平衡状态的依据是 (填字母)。
a.t 时,正、逆反应速率均为零 b.混合气体的密度不再变化
2
c.v ∶v ∶v =3∶1∶2 d.t 时,c =0.06 mol·L-1,并保持不变
A B C 2 A
直击高考
15.已知可逆反应:N(g)+3H(g) 2NH (g) ΔH=-92 kJ·mol-1,下列关于此反应
2 2 3
的说法中错误的是( )
A.压缩反应容器使气体体积减小,可使该反应的反应速率变大
B.该反应中反应物的总能量比生成物的总能量高
C.单位时间内生成1 mol N ,同时消耗3 mol H ,说明该反应达到平衡状态
2 2
D.将1 mol N 和3 mol H 混合进行反应,共放出的热量为92 kJ
2 2
16.CH、CHOH、CO等都是重要的能源,也是重要的化工原料。
4 3
(1)已知25℃、101kPa时,1g甲烷燃烧生成CO和液态水时放出38kJ热量,则该条
件下反应2CH(g)+3O(g)=2CO(g)+4HO(l)的 =________________。
4 2 2
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO 的含量,有效地开发利用
2
CO,工业上可以用CO 来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO 和
2 2 2
3molH ,一定条件下发生反应:CO(g)+3H(g) CHOH(g)+H O(g)。经测得CHOH和
2 2 2 3 2 3
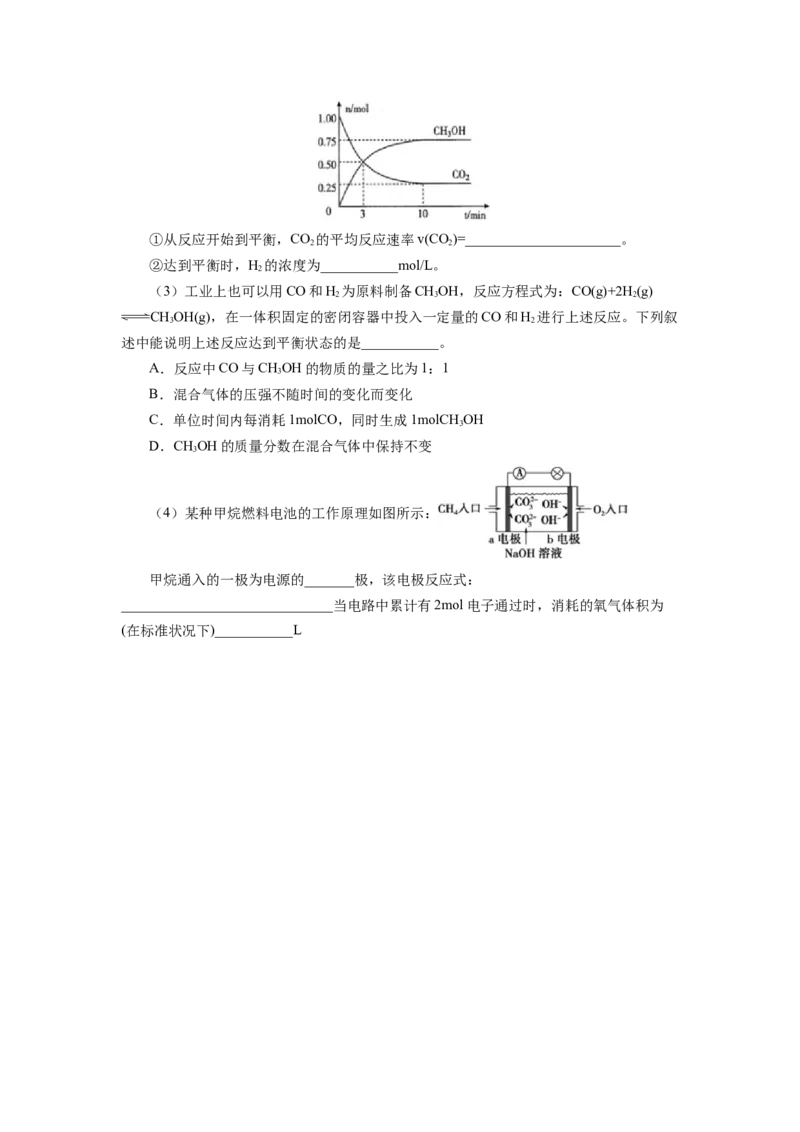
CO 的物质的量随时间变化如图所示。
2①从反应开始到平衡,CO 的平均反应速率v(CO)=______________________。
2 2
②达到平衡时,H 的浓度为___________mol/L。
2
(3)工业上也可以用CO和H 为原料制备CHOH,反应方程式为:CO(g)+2H(g)
2 3 2
CHOH(g),在一体积固定的密闭容器中投入一定量的CO和H 进行上述反应。下列叙
3 2
述中能说明上述反应达到平衡状态的是___________。
A.反应中CO与CHOH的物质的量之比为1:1
3
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH OH
3
D.CHOH的质量分数在混合气体中保持不变
3
(4)某种甲烷燃料电池的工作原理如图所示:
甲烷通入的一极为电源的_______极,该电极反应式:
______________________________当电路中累计有2mol电子通过时,消耗的氧气体积为
(在标准状况下)___________L