文档内容
4.3电化学腐蚀与防护(分层作业)
1.化学与生产、生活和社会息息相关,下列有关说法错误的是
A.合成氨的反应塔与外加电源的正极相连,并维持一定的电压可以钝化防腐
B.药用泡腾片中含有碳酸氢钠,遇水产生大量气泡加速药物分散和溶解
C.运动员剧烈运动后,补充的运动饮料中含有糖类和一定浓度的 等
D.开发利用新能源,减少化石燃料的使用是实现“碳中和”目标的有效途径
2.下列反应与电化学反应原理无关的是
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.市售“暖贴”中含有铁粉、炭粉、木屑、少量氯化钠和水等,揉搓后释放热量
C.纯银器表面变黑
D.用电镀法将镍、铬等金属外衣“披”在塑料制品上
3.下列说法错误的是
A.原电池中,负极一定是活动性较强的金属
B.其他条件相同时,粗锌与硫酸反应比纯锌与硫酸反应速率快
C.在镀件上电镀锌,用锌作阳极
D.为延长锅炉的使用寿命,常在其内壁焊上锌片
4.化学知识无处不在,下列说法中正确的是
A.垃圾分类时,废旧电池是可回收垃圾
B.铜在酸雨中发生吸氧腐蚀
C.问天实验舱的太阳翼是一种将太阳能转化为电能的原电池装置
D.工业上用电解熔融的 的方法冶炼Al
5.北京冬奥会火种灯的外形设计灵感来自于西汉的“长信宫灯”。下列说法正确的是
A.青铜的熔点大于纯铜B.铜锈的主要成分是Cu(OH)
2
C.镏金层破损后,金作负极可以继续保护破损处的铜,此法称为牺牲阳极的阴极保护法
D.铝合金表面氧化物薄膜可保护内部金属不被腐蚀
6.下列变化中,涉及氧化还原反应的是
①燃料的燃烧 ②绿色植物的光合作用 ③钢铁的锈蚀 ④食物的腐败
A.①②③④ B.①②③ C.②③④ D.①③④
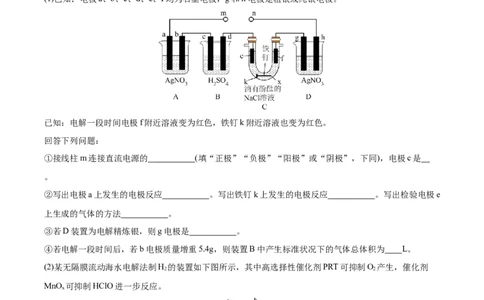
7.某化学兴趣小组的同学,组装了如下电化学装置。
(1)已知:电极a、b、c、d、e、f均为石墨电极,g和h电极是粗银或纯银电极。
已知:电解一段时间电极f附近溶液变为红色,铁钉k附近溶液也变为红色。
回答下列问题:
①接线柱m连接直流电源的 (填“正极”“负极”“阳极”或“阴极”,下同),电极c是
。
②写出电极a上发生的电极反应 。写出铁钉k上发生的电极反应 。写出检验电极e
上生成的气体的方法 。
③若D装置为电解精炼银,则g电极是 。
④若电解一段时间后,若b电极质量增重5.4g,则装置B中产生标准状况下的气体总体积为 L。
(2)某无隔膜流动海水电解法制H 的装置如下图所示,其中高选择性催化剂PRT可抑制O 产生,催化剂
2 2
MnO 可抑制HClO进一步反应。
x
①b电极是 (填“正极”“负极”“阳极”或“阴极”)。
②写出放电时钛网上发生的电极反应 。③电解一段时间后,海水的pH将 (填“增大”“减小”或“不变”)。
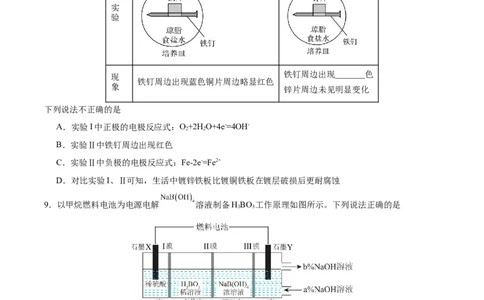
8.化学小组研究金属的电化学腐蚀,实验如下:
序
实验I 实验Ⅱ
号
实
验
铁钉周边出现_______色
现
铁钉周边出现蓝色铜片周边略显红色
象
锌片周边未见明显变化
下列说法不正确的是
A.实验I中正极的电极反应式:O+2H O+4e-=4OH-
2 2
B.实验Ⅱ中铁钉周边出现红色
C.实验Ⅱ中负极的电极反应式:Fe-2e-=Fe2+
D.对比实验I、Ⅱ可知,生活中镀锌铁板比镀铜铁板在镀层破损后更耐腐蚀
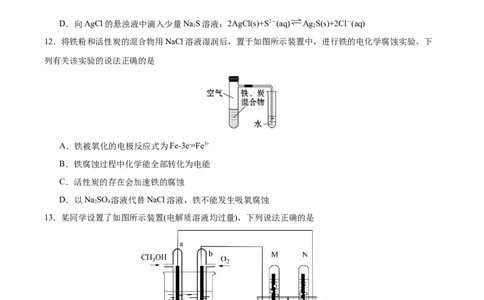
9.以甲烷燃料电池为电源电解 溶液制备HBO 工作原理如图所示。下列说法正确的是
3 3
A.N室中:
B.燃料电池通入氧气的电极接电解池的Y电极
C.I、Ⅲ膜为阴离子交换膜,Ⅱ膜为阳离子交换膜
D.理论上每生成 产品,需消耗甲烷的体积为 (标准状况)
10.下列事实中,能用勒夏特列原理解释的是
A.用牺牲阳极的阴极保护法保护船舶的外壳B.压缩氢气与碘蒸气的平衡混合体系,气体颜色变深
C.夏天打开冰镇啤酒,把啤酒倒入玻璃杯中,杯中立即泛起大量泡沫
D.500℃左右比常温下更有利于N 和H 反应生成NH
2 2 3
11.下列方程式不正确的是
A.吸氧腐蚀正极反应式: O+4e-+2H O=4OH-
2 2
B.NaHS水解:HS-+H O S2-+H O+
2 3
C.电解CuSO 溶液:2CuSO +2H O 2Cu+O ↑+2H SO
4 4 2 2 2 4
D.向AgCl的悬浊液中滴入少量NaS溶液:2AgCl(s)+S2-(aq) Ag S(s)+2Cl-(aq)
2 2
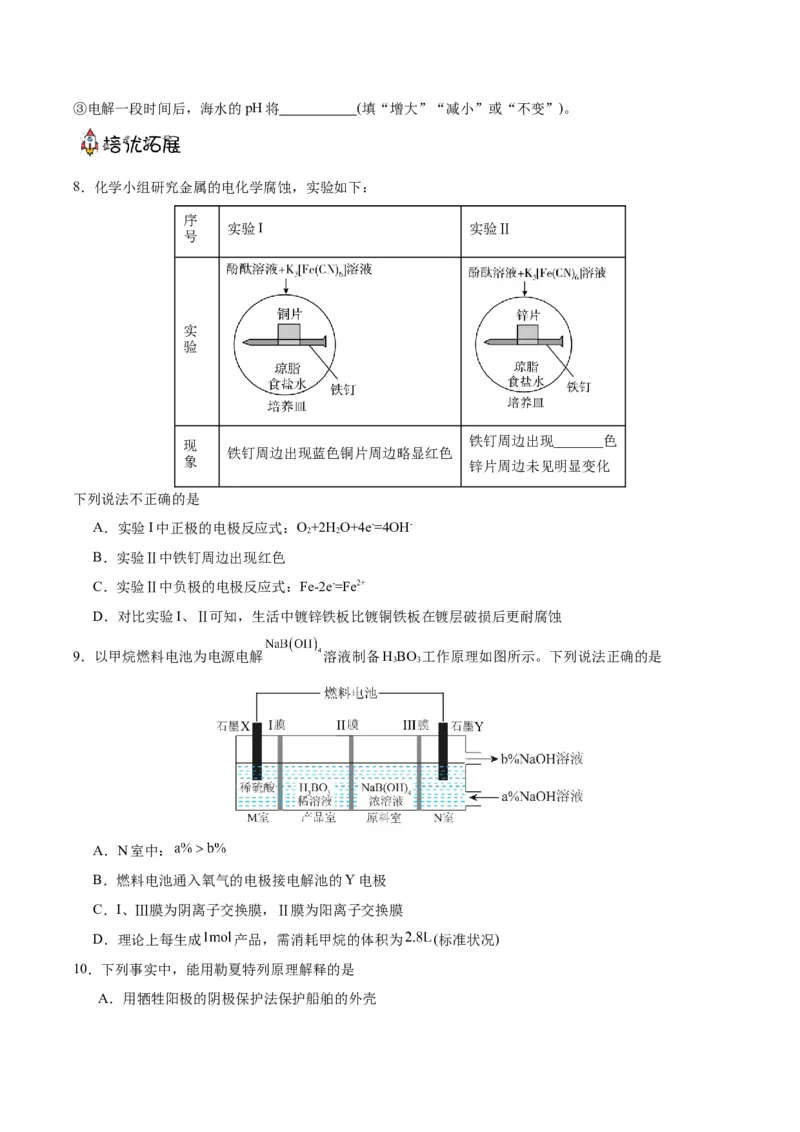
12.将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下
列有关该实验的说法正确的是
A.铁被氧化的电极反应式为Fe-3e-=Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以NaSO 溶液代替NaCl溶液,铁不能发生吸氧腐蚀
2 4
13.某同学设置了如图所示装置(电解质溶液均过量),下列说法正确的是
A.a极的电极反应为CHOH-6e-+H O=CO↑+6H+
3 2 2
B.N试管收集到黄绿色的气体
C.电路中每转移2 电子,理论上乙池阴极区生成2
D.甲池b极消耗的气体与乙池阴极产生的气体的体积比为2∶114.下列说法不正确的是
A.图①:进行化学实验时,需要佩戴护目镜,以保护眼睛
B.图②:可用于分离植物油和水的混合液
C.图③:可用于硫酸钠的焰色试验
D.图④:牺牲阳极法保护钢铁设备的示意图
15.电池是日常生活中最常见的一种提供电能的装置,研究各种新型电池成为新能源研究的一种方向。
(1)如图是一种甲烷燃料电池的装置。
①铂电极a是 (填“正极”“负极”“阳极”或“阴极”),发生 (填“氧化”或
“还原”)反应。
②电子从 (填“a”或“b”)电极流出,该电极的电极反应式是 。
③盐桥中的 向 (填“稀硫酸”或“稀氢氧化钾”)溶液移动。
(2)白铁是日常生活中常见的一种金属材料,俗称“锌包钢”,一旦划破后就会发生电化学反应,此时负极
材料是 ,在潮湿的碱性或中性环境中,铁电极上发生反应的电极反应式是 。金属铁被保
护而不易腐蚀,这种防腐的方法叫 (填名称)。
(3)一种水性电解液 离子选择双隔膜电池如图所示:已知:KOH溶液中, 以 存在。
①a离子选择性隔膜是 (填“阳离子”或“阴离子”)交换膜。
②写出MnO 电极上发生的电极反应 。
2
③写出该原电池总反应的离子方程式 。