文档内容
第五章 化工生产中的重要非金属元素
第一节 硫及其化合物 课时作业
第四课时 不同价态含硫物质的转化
基础达标
1.下列关于硫的叙述中不正确的是( )
A.在自然界中既有化合态的硫又有游离态的硫
B.游离态的硫存在于火山喷口附近或地壳的岩层里
C.实验室常用酒精除去附着在试管壁上的硫黄
D.硫是黑火药的主要成分之一
【答案】C
【解析】硫在自然界中既能以化合态(主要为硫化物和硫酸盐)又能以游离态(火山喷口
附近或地壳岩层)的形式存在。硫单质俗称硫黄,是一种黄色或淡黄色固体,难溶于水,微
溶于酒精,易溶于二硫化碳,常用二硫化碳除去试管内壁附着的硫单质。
2.下列转化不能一步实现的是 ( )
A.S→H S B.S→SO
2 3
C.H SO →SO D.Na SO →SO
2 4 2 2 3 2
【解析】选B。H+S=====HS,A不选;S和O 反应只能生成SO ,B选;浓硫酸和还原性
2 2 2 2
物质反应生成SO ,C不选;Na SO 与浓HSO 反应生成SO ,D不选。
2 2 3 2 4 2
3.含硫元素物质间发生转化:S SO SO HSO Al (SO ),其中硫元素化合
2 3 2 4 2 4 3
价发生变化的是( )
A.①② B.③④ C.①③ D.②④
【答案】A
【解析】①S单质与O 在点燃时反应转化为SO ,S元素化合价由0价变为+4价,反
2 2
应前后S元素化合价发生了变化,①符合题意;②SO 与O 在一定条件下反应产生SO ,S
2 2 3
元素化合价由+4价变为+6价,S元素化合价升高,可见在反应前后S元素化合价发生了变
化,②符合题意;③SO 被水吸收得到HSO ,S元素化合价都是+6价,因此S元素化合
3 2 4
价未发生变化,③不符合题意;④HSO 可以与Al O 发生反应产生Al (SO ) 和水,S元素
2 4 2 3 2 4 3
化合价都是+6价,反应前后S元素化合价未发生变化,④不符合题意;综上所述可知:在
物质转化中硫元素化合价发生变化的序号是①②,故合理选项是A。
4.下列关于硫及其化合物的说法正确的是( )A.向BaCl 溶液中通入SO 产生白色沉淀
2 2
B.SO 具有还原性,可使酸性高锰酸钾溶液褪色
2
C.CuS可以通过两种单质直接化合制得
D.硫在过量纯氧中燃烧生成三氧化硫
【答案】B
【解析】A项,氯化钡和二氧化硫不反应,向BaCl 溶液中通入SO 不产生白色沉淀,
2 2
错误;B项,SO 具有还原性,可以和强氧化剂高锰酸钾反应,可使酸性高锰酸钾溶液褪
2
色,正确;C项,硫的氧化性较弱,铜和硫反应生成硫化亚铜,错误;D项,硫在过量纯
氧中燃烧生成二氧化硫,错误。
5.HS是无色有恶臭味的有毒气体,空气中含0.1%的HS就会迅速引起头痛、晕眩等
2 2
症状,吸入大量HS会造成昏迷或死亡。是一种神经毒剂。亦为窒息性和刺激性气体。其
2
毒作用的主要靶器是中枢神经系统和呼吸系统,亦可伴有心脏等多器官损害,下列有关
HS的性质和用途说法不正确的是
2
A.硫化氢能被氧气、氯气、碘、溴等单质氧化成硫单质
B.将HS通入Pb(NO ) 溶液得到黑色沉淀,再加双氧水,沉淀会转化为白色
2 3 2
C.将HS气体通入CuSO 溶液中得到CuS沉淀,通入FeSO 溶液会产生FeS沉淀
2 4 4
D.HS通入到FeCl 溶液中,溶液酸性增强
2 3
【答案】C
【解析】A.硫化氢中的硫处于最低价态,能被氧气、氯气、碘、溴等单质氧化成硫
单质,故A正确;B.将HS通入Pb(NO ) 溶液中,发生反应
2 3 2
Pb(NO )+H S=PbS↓+2HNO ,生成黑色沉淀PbS ,PbS 经过过氧化氢处理发生反应
3 2 2 3
PbS+4HO=PbSO↓+4H O,生成白色沉淀PbSO ,故B正确;C.FeS相对于CuS溶解度
2 2 4 2 4
较大,会溶于稀硫酸,所以将HS气体通入FeSO 溶液中得不FeS沉淀,故C错误;D.
2 4
HS通入到FeCl 溶液中,Fe3+将S2-氧化,发生反应:HS+2Fe3+=S↓+2Fe2++2H+,氢离子浓
2 3 2
度增大,酸性增强,故D正确;故选C。
6.如图是实验室制取SO 并验证SO 某些性质的装置图。若观察到装置④中有淡黄色
2 2
沉淀生成,⑤中的溴水褪色,下列说法错误的是( )A.①中发生反应的离子方程式是SO +2H+=H O+SO ↑
2 2
B.②中溶液变为红色
C.③的品红溶液褪色,证明SO 有漂白性
2
D.④中SO 作还原剂
2
【答案】D
【解析】亚硫酸钠与硫酸反应生成二氧化硫,二氧化硫能够使石蕊溶液变红(体现酸
性氧化物性质),使品红溶液褪色(体现漂白性),与氢硫酸溶液反应生成黄色沉淀(体
现氧化性),使溴水褪色(体现还原性),最后尾气被碱液吸收。A.亚硫酸钠与硫酸反
应生成二氧化硫,①中发生反应的离子方程式是SO +2H+=H O+SO ↑,故A正确;B.
2 2
②中溶液变为红色,SO 溶于水生成亚硫酸,石蕊遇到酸变红,故B正确;C.二氧化硫能
2
够使品红褪色,③的品红溶液褪色,证明SO 有漂白性,故C正确;D.④中为二氧化硫
2
与氢硫酸反应生成单质硫,反应中SO 作氧化剂,被还原,故D错误;故选D。
2
7.X为一种常见气体(常温下),a、b、c是中学化学常见物质,均由常见元素组成,
转化关系如图所示,下列说法不正确的是( )
A.若a、b、c焰色反应均呈黄色,水溶液均呈碱性,
则a中可能既含有离子键又含有共价键
B.若X为O,a为一种固态单质,则c可能为CO 和SO
2 2 3
C.若b为固态非金属单质,b与X所含元素同主族,则a、b、c均能与X反应
D.若a为固态非金属单质,a与X所含元素同周期,常温常压下c为白色固体,则X
与a所含元素原子的核电荷数相差2
【答案】B
【解析】从框图分析,常见气体X可以为CO 、O 、Cl 等。符合各个选项的框图情况
2 2 2
如图所示。B项看似a为C、S均符合,但由于S与氧气化合不能直接生成SO ,符合条件的只有
3
C及其氧化物的转化。
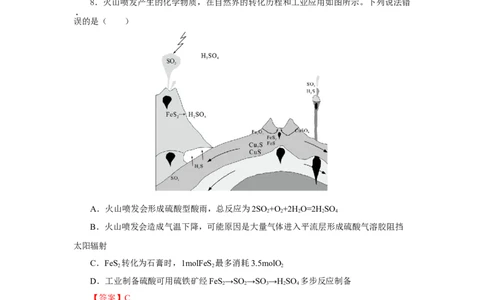
8.火山喷发产生的化学物质,在自然界的转化历程和工业应用如图所示。下列说法错
误的是( )
A.火山喷发会形成硫酸型酸雨,总反应为2SO +O +2H O=2HSO
2 2 2 2 4
B.火山喷发会造成气温下降,可能原因是大量气体进入平流层形成硫酸气溶胶阻挡
太阳辐射
C.FeS 转化为石膏时,1molFeS 最多消耗3.5molO
2 2 2
D.工业制备硫酸可用硫铁矿经FeS→SO →SO →HSO 多步反应制备
2 2 3 2 4
【答案】C
【解析】A.硫酸型酸雨的形成可以近似看做排放到空气中的二氧化硫气体,与潮湿
空气中水蒸气、氧气在空气粉尘的催化作用下生成硫酸或空气中粉尘做催化剂,氧气氧化
二氧化硫生成三氧化硫,三氧化硫溶于水生成硫酸,总反应为2SO +O +2H O=2HSO ,故
2 2 2 2 4
A正确;B.火山喷发产生大量二氧化硫,进入大气中形成硫酸气溶胶阻挡太阳辐射,造
成气温下降,故B正确;C.FeS 转化为石膏时,Fe元素由+2价升高为+3价,S元素由-1
2
价升高为+6价,1molFeS2最多失去1mol×{(3-2)+2×[6-(-1)]}=15mol,根据电子转移守恒,
可 消 耗 O2 为 15mol/4=3.75mol , 故 C 错 误 ; D . 工 业 制 备 硫 酸 的 反 应 是 :
4FeS+11O ═2Fe O+8SO , 2SO +O ═2SO , SO +H O═H SO , 可 用 硫 铁 矿 经
2 2 2 3 2 2 2 3 3 2 2 4FeS→SO →SO →HSO 多步反应制备硫酸,故D正确;故选:C。
2 2 3 2 4
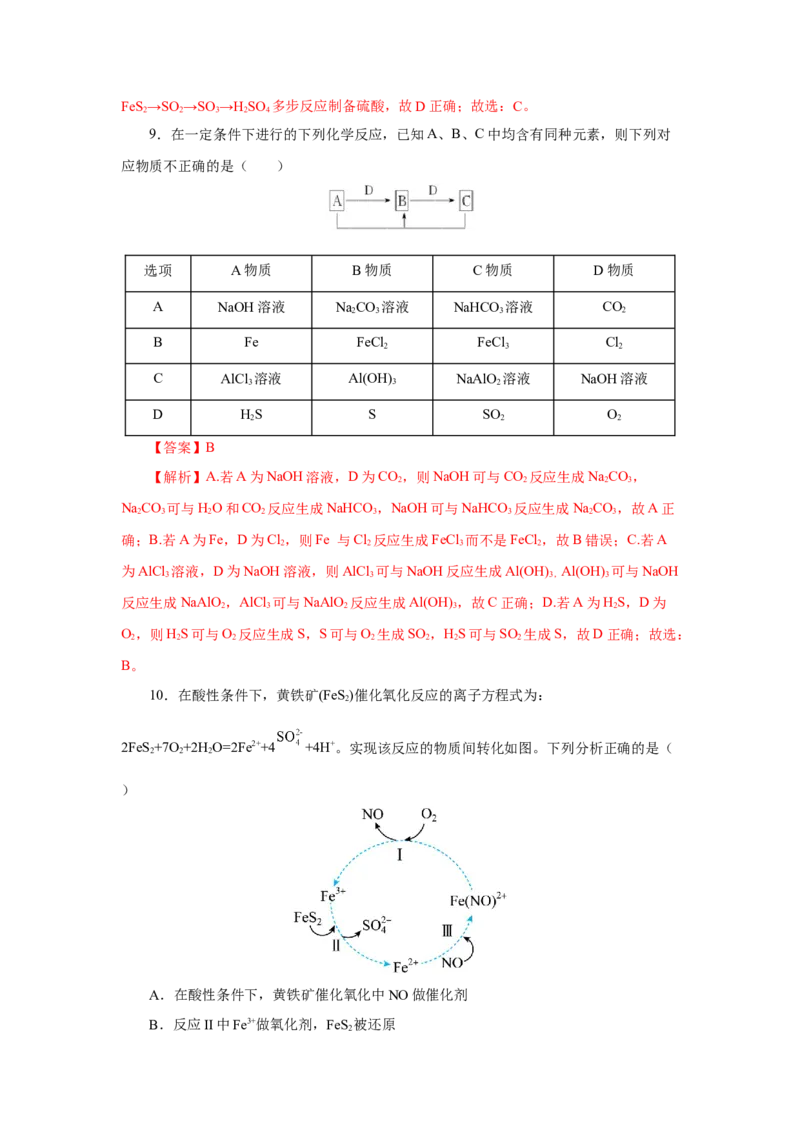
9.在一定条件下进行的下列化学反应,已知A、B、C中均含有同种元素,则下列对
应物质不正确的是( )
选项 A物质 B物质 C物质 D物质
A NaOH溶液 NaCO 溶液 NaHCO 溶液 CO
2 3 3 2
B Fe FeCl FeCl Cl
2 3 2
C AlCl 溶液 Al(OH) NaAlO 溶液 NaOH溶液
3 3 2
D HS S SO O
2 2 2
【答案】B
【解析】A.若A为NaOH溶液,D为CO,则NaOH可与CO 反应生成NaCO,
2 2 2 3
NaCO 可与HO和CO 反应生成NaHCO ,NaOH可与NaHCO 反应生成NaCO,故A正
2 3 2 2 3 3 2 3
确;B.若A为Fe,D为Cl,则Fe 与Cl 反应生成FeCl 而不是FeCl ,故B错误;C.若A
2 2 3 2
为AlCl 溶液,D为NaOH溶液,则AlCl 可与NaOH反应生成Al(OH) Al(OH) 可与NaOH
3 3 3, 3
反应生成NaAlO ,AlCl 可与NaAlO 反应生成Al(OH) ,故C正确;D.若A为HS,D为
2 3 2 3 2
O,则HS可与O 反应生成S,S可与O 生成SO ,HS可与SO 生成S,故D正确;故选:
2 2 2 2 2 2 2
B。
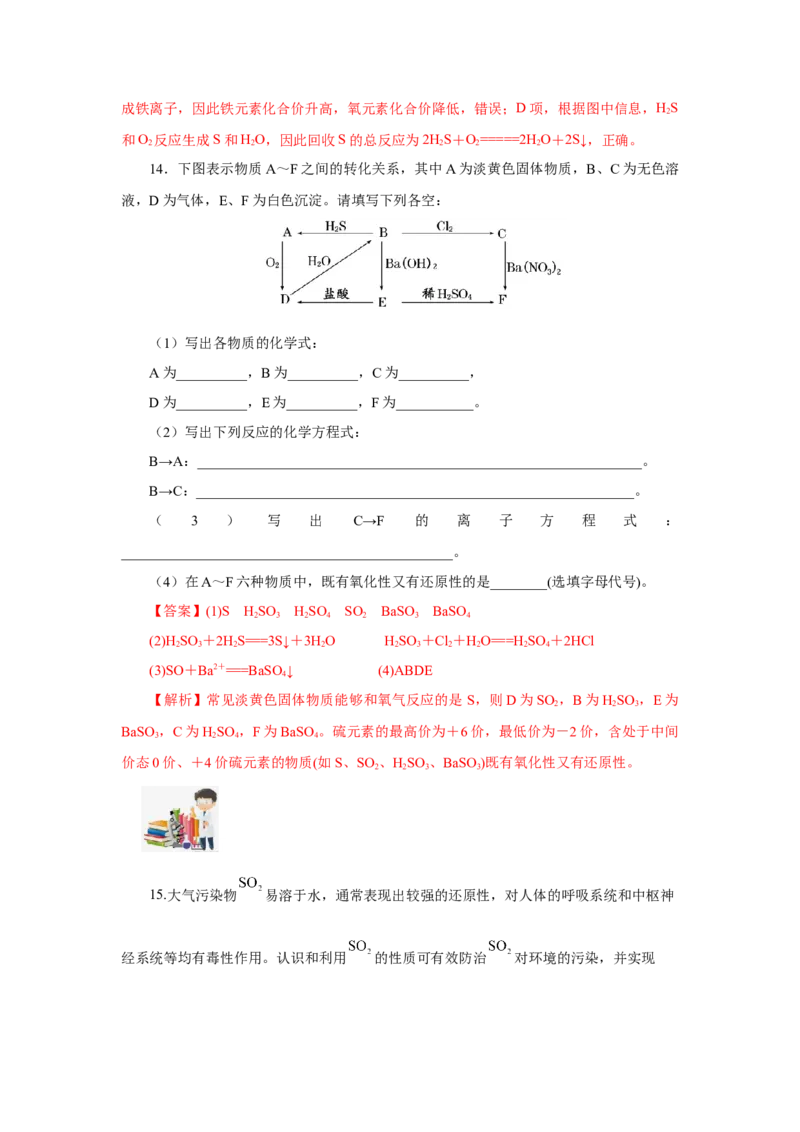
10.在酸性条件下,黄铁矿(FeS )催化氧化反应的离子方程式为:
2
2FeS+7O +2H O=2Fe2++4 +4H+。实现该反应的物质间转化如图。下列分析正确的是(
2 2 2
)
A.在酸性条件下,黄铁矿催化氧化中NO做催化剂
B.反应II中Fe3+做氧化剂,FeS 被还原
2C.反应I的离子方程式为4Fe(NO)2++O +4H+=4Fe3++4NO+2HO,其中Fe(NO)2+做氧化
2 2
剂
D.反应III的离子方程式为Fe2++NO=Fe(NO)2+,该反应是氧化还原反应
【答案】A
【解析】A.由总反应2FeS+7O +2H O=2Fe2++4SO+4H+可知,一氧化氮未参加反应,
2 2 2
但转化图上参与了反应,说明NO反应前后性质和质量不变,符合催化剂概念,A正确;
B.反应Ⅱ中Fe3+由+3价变成+2价,FeS 中S硫元素化合价升高,所以反应Ⅱ的氧化剂是
2
Fe3+,FeS 被氧化,B错误;C.由图可知:反应Ⅰ中Fe(NO)2+中铁由+2价变+3价,氧气中
2
氧由0价变成﹣2价,根据得失电子守恒,反应的离子方程式为:4Fe(NO)2++O +4H+=
2
4Fe3++4NO+2HO,Fe(NO)2+作还原剂,C错误;D.反应Ⅲ的离子方程式为Fe2++NO=
2
Fe(NO)2+,无元素化合价变化,所以反应Ⅲ是非氧化还原反应,D错误。答案选A。
能力提升
11.某微型实验装置(夹持仪器已省略)如图所示,其中a棉球蘸有品红溶液,b棉球蘸
有含酚酞的NaOH溶液, 棉球蘸有 与淀粉的混合溶液。实验时将 滴入装有
固体的培养皿中。下列说法错误的是( )
A.a棉球会变白,微热后变红
B.b棉球变为白色,离子反应为:SO +2OH-==SO+2H O
2 2
C.c棉球变为白色,说明SO 具有漂白性
2
D.若将试剂改为浓HCl和Ca(ClO) 固体,a、b处棉球也会变白色
2
【答案】C
【解析】A.SO 与品红反应生成无色不稳定物质,遇热分解又生成SO 和品红,又恢
2 2
复红色, a棉球会变白,微热后变红,故A正确;B.氢氧化钠遇到酚酞也是红色的,二
氧化硫能和氢氧化钠反应,溶液的碱性减弱,导致红色消失,反应原理是:SO +2OH-
2==SO+2H O、SO +OH-=HSO -,故B正确;C. 碘单质遇到淀粉变为蓝色,二氧化硫能将
2 2 3
碘单质还原为碘离子,SO +I +2H O=HSO +2HI,从而使蓝色消失,c棉球变为白色,说明
2 2 2 2 4
SO 具有还原性,故C错误;D. 若将试剂改为浓HCl和Ca(ClO) 固体,反应生成氯气,
2 2
潮湿的氯气也具有漂白性,氯气也能与碱反应,过量的氯气溶于水呈酸性,a、b处棉球也
会变白色,故D正确;故选C。
12.如图所示是一系列含硫化合物的转化关系(反应中生成的水已略去),其中说法正
确的是( )
A.反应①说明SO 具有氧化性,反应②说明SO 具有酸性
2 2
B.反应②中生成物n(Na SO )∶n(NaHSO)=1∶1时,则反应物n(SO )∶n(NaOH)=1∶2
2 3 3 2
C.反应③④⑤均属于氧化还原反应
D.工业上可利用反应②和反应④回收SO
2
【答案】D
【解析】A项,反应①中先变蓝后褪色,说明KIO 先转化为I 后转化为I-,SO 体现
3 2 2
还原性,错误;B项,根据原子守恒,当n(Na SO )∶n(NaHSO)=1∶1时,n(SO )∶n(NaOH)=
2 3 3 2
2∶3,错误;C项,反应④不是氧化还原反应,错误;D项,利用反应②④,可以吸收SO
2
并回收利用,正确。
13.硫化氢的转化是资源利用和环境保护的重要研究课题。将HS和空气的混合气体
2
通入FeCl 、FeCl 和CuCl 的混合溶液中回收S,其转化如下图所示(CuS不溶于水)。下列
3 2 2
说法中,不正确的是( )
A.过程①中,生成CuS的反应为HS+Cu2+=CuS↓+2H
2
+
B.过程②中,Fe3+作氧化剂
C.过程③中,各元素化合价均未改变
D.回收S的总反应为2HS+O=====2HO+2S↓
2 2 2
【答案】C
【解析】A项,过程①是铜离子和硫化氢反应生成氢离子和硫化铜,离子方程式为
HS+Cu2+=CuS↓+2H+,正确;B项,过程②中,铁离子和硫化铜反应生成亚铁离子,
2
铁离子化合价降低,因此Fe3+作氧化剂,正确;C项,过程③中,氧气和亚铁离子反应生成铁离子,因此铁元素化合价升高,氧元素化合价降低,错误;D项,根据图中信息,HS
2
和O 反应生成S和HO,因此回收S的总反应为2HS+O=====2HO+2S↓,正确。
2 2 2 2 2
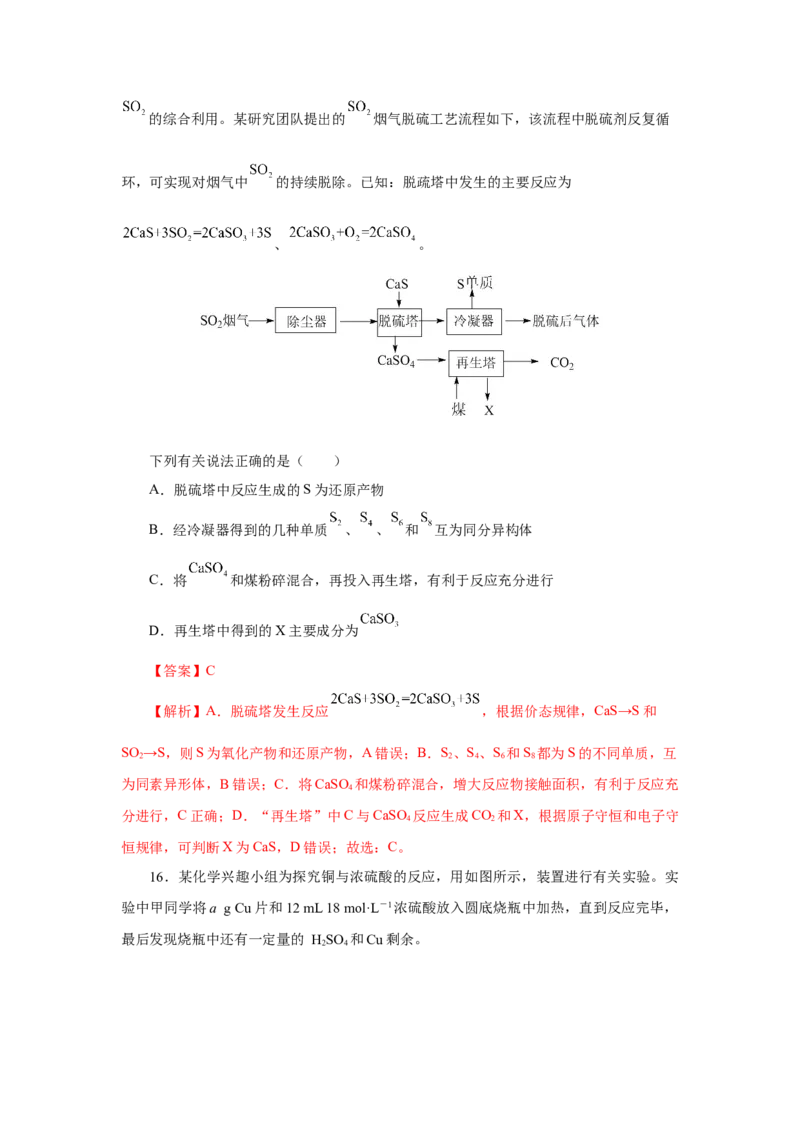
14.下图表示物质A~F之间的转化关系,其中A为淡黄色固体物质,B、C为无色溶
液,D为气体,E、F为白色沉淀。请填写下列各空:
(1)写出各物质的化学式:
A为__________,B为__________,C为__________,
D为__________,E为__________,F为___________。
(2)写出下列反应的化学方程式:
B→A:_______________________________________________________________。
B→C:______________________________________________________________。
( 3 ) 写 出 C→F 的 离 子 方 程 式 :
_______________________________________________。
(4)在A~F六种物质中,既有氧化性又有还原性的是________(选填字母代号)。
【答案】(1)S HSO HSO SO BaSO BaSO
2 3 2 4 2 3 4
(2)H SO +2HS===3S↓+3HO HSO +Cl+HO===H SO +2HCl
2 3 2 2 2 3 2 2 2 4
(3)SO+Ba2+===BaSO ↓ (4)ABDE
4
【解析】常见淡黄色固体物质能够和氧气反应的是 S,则D为SO ,B为HSO ,E为
2 2 3
BaSO ,C为HSO ,F为BaSO 。硫元素的最高价为+6价,最低价为-2价,含处于中间
3 2 4 4
价态0价、+4价硫元素的物质(如S、SO 、HSO 、BaSO)既有氧化性又有还原性。
2 2 3 3
直击高考
15.大气污染物 易溶于水,通常表现出较强的还原性,对人体的呼吸系统和中枢神
经系统等均有毒性作用。认识和利用 的性质可有效防治 对环境的污染,并实现的综合利用。某研究团队提出的 烟气脱硫工艺流程如下,该流程中脱硫剂反复循
环,可实现对烟气中 的持续脱除。已知:脱疏塔中发生的主要反应为
、 。
下列有关说法正确的是( )
A.脱硫塔中反应生成的S为还原产物
B.经冷凝器得到的几种单质 、 、 和 互为同分异构体
C.将 和煤粉碎混合,再投入再生塔,有利于反应充分进行
D.再生塔中得到的X主要成分为
【答案】C
【解析】A.脱硫塔发生反应 ,根据价态规律,CaS→S和
SO →S,则S为氧化产物和还原产物,A错误;B.S、S、S 和S 都为S的不同单质,互
2 2 4 6 8
为同素异形体,B错误;C.将CaSO 和煤粉碎混合,增大反应物接触面积,有利于反应充
4
分进行,C正确;D.“再生塔”中C与CaSO 反应生成CO 和X,根据原子守恒和电子守
4 2
恒规律,可判断X为CaS,D错误;故选:C。
16.某化学兴趣小组为探究铜与浓硫酸的反应,用如图所示,装置进行有关实验。实
验中甲同学将a g Cu片和12 mL 18 mol·L-1浓硫酸放入圆底烧瓶中加热,直到反应完毕,
最后发现烧瓶中还有一定量的 HSO 和Cu剩余。
2 4请回答下列问题:
( 1 ) 写 出 Cu 与 浓 硫 酸 反 应 的 化 学 方 程 式 :
_______________________________________。
(2)装置 D 内盛品红溶液,当 C 中气体集满后,D 中有可能观察到的现象是
__________________________________________________________。实验装置中有可能造
成 环 境 污 染 , 试 用 最 简 单 的 方 法 解 决 ( 实 验 用 品 自
选)___________________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒
精灯,但由于 余热 的作用, A 处仍 有气体产生,此时 B 装置 中的现 象是
_____________________。
(4)F中应放置的液体是________(填字母)。
A.饱和NaSO 溶液 B.酸性KMnO 溶液
2 3 4
C.浓溴水 D.饱和NaHSO 溶液
3
(5)为什么有一定量的余酸,但未能使 Cu 完全溶解,你认为原因是
__________________。
(6)下列足量药品能够用来证明反应结束后的烧瓶中确有余酸的是________(填字
母)。
A.Fe粉 B.BaCl 溶液
2
C.Ag D.NaCO 溶液
2 3
(7)甲同学向A中反应后的溶液中通入一种气体单质,使铜片全部溶解且仅生成硫
酸 铜 溶 液 , 请 问 该 气 体 单 质 是 ________( 填 名 称 ) , 化 学 反 应 方 程 式 是
_______________________。
【答案】(1)Cu+2HSO (浓)=====CuSO +SO ↑+2HO(2)品红溶液褪色 将浸有NaOH
2 4 4 2 2
溶液的棉花团塞在D试管口 (3)F中液面下降,长颈漏斗中液面上升
(4)D (5)随着反应的进行,浓硫酸的浓度不断减小,稀硫酸与Cu不反应 (6)AD(7)氧气 2Cu+2HSO +O===2CuSO+2HO
2 4 2 4 2