文档内容
2024-2025 江苏省名校协作体 12 月高一联考
化学试题
(本卷满分100分 考试时间75分钟)
一、单选题
1. 化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述不正确的是
A. 水果罐头中添加维生素C作抗氧化剂, 是因为维生素C易被氧化
B. 漂白粉露置于空气中变质,该过程未涉及化学变化
C. 洁厕灵(主要成分为 )与“84”消毒液不能混合使用,因为会产生有毒气体
D. 区别氯化钾和氯化钠可以利用焰色反应原理
【答案】B
【解析】
【详解】A.水果罐头中添加维生素C作抗氧化剂,是因为维生素C具有还原性易被氧化,故A正确;
B.漂白粉露置于空气中变质,该过程中涉及次氯酸钙和二氧化碳反应生成碳酸钙和次氯酸、次氯酸分解
为盐酸和氧气,次氯酸分解反应为氧化还原反应,故B错误;
C.洁厕灵(主要成分为 )与“84”消毒液不能混合使用,因为次氯酸钠和盐酸反应会产生有毒气体 ,
故C正确;
D.钠、钾的焰色不同,区别氯化钾和氯化钠可以利用焰色反应原理,故D正确;
选B。
2. 已知 可用于联合制碱。相关微粒的化学用语或性质
表述正确的是
A. 俗名:纯碱 B. 的结构示意图:
C. 该反应属于非氧化还原反应 D. 的电离方程式:
【答案】C
【解析】【详解】A.NaHCO 俗名小苏打,NaCO 俗名纯碱,A错误;
3 2 3
B.氯元素原子序数为17,Cl−核外有18个电子,故Cl−的结构示意图为 ,B错误;
C.题中所给反应,反应前后没有元素化合价发生变化,不是氧化还原反应,C正确;
D.碳酸氢根是弱酸的酸式酸根,电离方程式中不拆,正确的电离方程式为NaHCO =Na++ ,D错误;
3
本题选C。
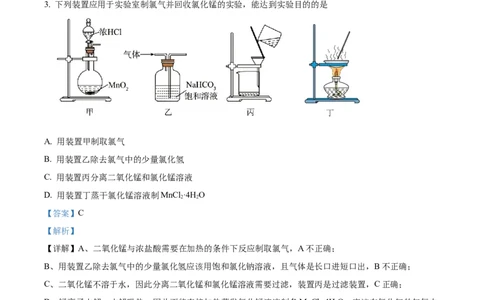
3. 下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是
A. 用装置甲制取氯气
B. 用装置乙除去氯气中的少量氯化氢
C. 用装置丙分离二氧化锰和氯化锰溶液
D. 用装置丁蒸干氯化锰溶液制MnCl ·4H O
2 2
【答案】C
【解析】
【详解】A、二氧化锰与浓盐酸需要在加热的条件下反应制取氯气,A不正确;
B、用装置乙除去氯气中的少量氯化氢应该用饱和氯化钠溶液,且气体是长口进短口出,B不正确;
C、二氧化锰不溶于水,因此分离二氧化锰和氯化锰溶液需要过滤,装置丙是过滤装置,C正确;
D、锰离子水解,水解吸热,因此不能直接加热蒸发氯化锰溶液制备MnCl ·4H O,应该在氯化氢的气氛中
2 2
进行,D不正确。
答案选C。
4. 下列物质的性质与用途具对应关系错误的是
A. 能吸收 产生 ,可用作潜水艇的供氧剂
B. 有碱性,可用于制胃酸中和剂C. 具有漂白性,可用于漂白纸浆
D. 明矾溶于水形成胶体,可用于净水
【答案】B
【解析】
【详解】A.NaO 能吸收二氧化碳生成碳酸钠和氧气,所以可用作呼吸面具中的供氧剂,故A正确;
2 2
B.碳酸钠溶液呈碱性,但其碱性过强,不能用于治疗胃酸过多,可以用碳酸氢钠,故B错误;
C.SO 可以用于纸浆、毛、丝、草帽辫的漂白,是因为SO 具有漂白性,故C正确;
2 2
D.明矾溶于水产生氢氧化铝胶体,胶体具有吸附性,可用作净水剂,故D正确;
故选B。
5. 室温下,下列各组离子在指定溶液中能大量共存的是
A. 饱和氯水: 、 、 、
B. 无色透明溶液中: 、 、 、
C. 能使酚酞变红的溶液: 、 、 、
D. 溶液: 、 、 、
【答案】C
【解析】
【详解】A.氯水能把 、 分别氧化为 、 ,饱和氯水中还含有H+,能与 反应,因此
该条件下,该组不能大量共存,故A错误;
B.含有 的溶液为蓝色,不符合条件,故B错误;
C.能使酚酞变红的溶液说明为碱性,含有大量的 ,该组离子均不发生反应,可以大量共存,故C正
确;
D. 与 在 条件下发生反应产生氯气,不能大量共存,故D错误;
故答案选C。
阅读下列材料,完成下面小题:
海水晒盐后精制得到NaCl,电解饱和NaCl溶液得到 和NaOH,两者在较低温度下反应可制得“84消毒液”(有效成分为NaClO),“84消毒液”应密封避光保存;以NaCl、 、 等为原料可得到 ;
向海水晒盐得到的卤水中通 可制溴;从海水中还能提取镁。
6. 下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是
A. 原子半径大小:r(Br)>r(Cl)>r(Na) B. 碱性强弱:NaOH>
C. 最外层电子数:Br>Cl>Mg D. 热稳定性大小:HBr>HCl
7. 在指定条件下,下列选项所示的物质间转化均能实现的是
A. NaCl(aq) (g) (s)
B. NaCl(aq)
C. NaBr(aq)
D. Mg(s)
8. 下列化学反应表示正确的是
A. 与NaOH溶液在较低温度下反应:
B. NaClO溶液受热易分解成 和NaCl:
C. NaClO溶液与 反应生成 :
D. HClO见光分解:
【答案】6. B 7. C 8. C
【解析】
【6题详解】
A.电子层数越多,原子半径越大,同周期主族元素原子半径随原子序数的增大而减小,所以半径:
r(Br)>r(Na)>r(CI),A错误;
B.由于元素金属性越强,其最高价氧化物对应水化物的碱性越强,金属性:Na>Mg,故碱性:
NaOH>Mg(OH) ,B正确;
2
C.原子最外层电子数n的关系为n(Br)=n(Cl),C错误;D.稳定性与氢与卤素离子之间的作用力,半径越大,二者的作用力逐渐越小,越不稳定,半径:
r(Br)>r(CI),所以热稳定性:HBrC
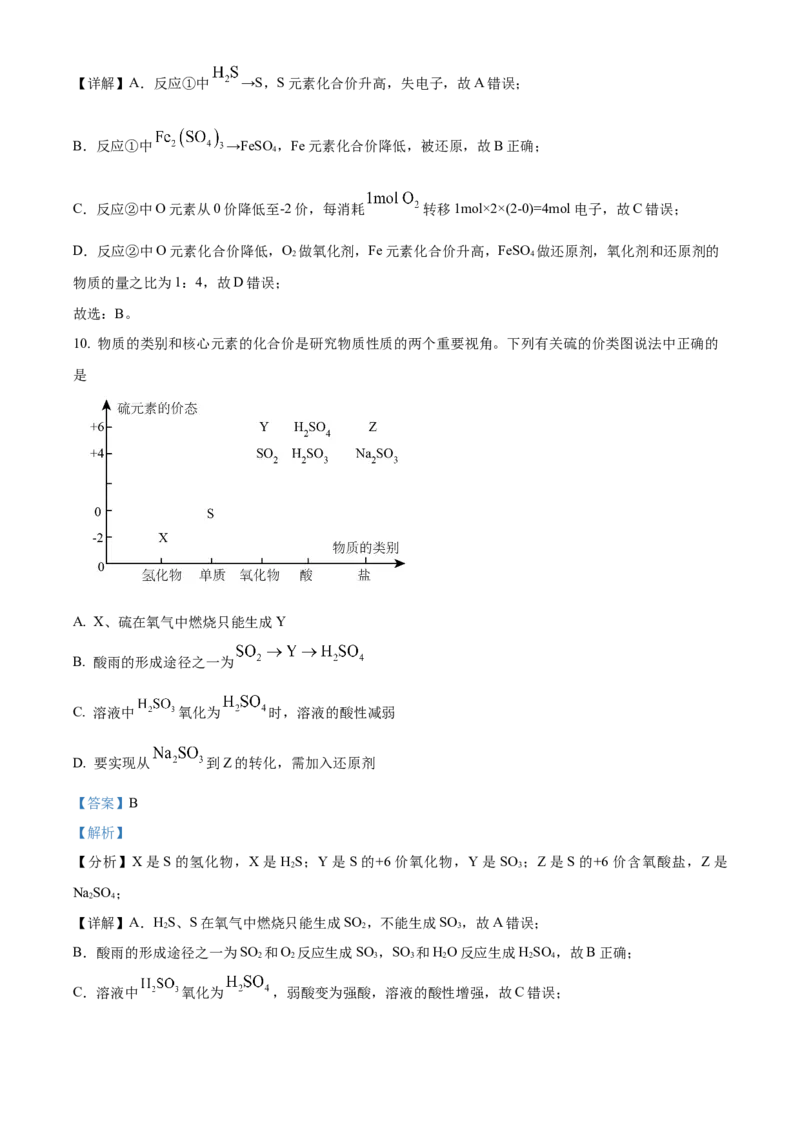
二氧化硫具有漂白
C 将 通入酸性高锰酸钾溶液中 紫红色褪去
性
该溶液中一定有
向某溶液中加入稀盐酸产生无色气体,将气
D 澄清石灰水变浑浊
体通入澄清石灰水中
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.蔗糖固体加入浓硫酸,浓硫酸使蔗糖脱水碳化,溶液温度升高,浓硫酸与碳反应生成二氧化
硫和二氧化碳,出现“黑面包现象”,A正确;
B.比较非金属性强弱,要比较最高价含氧酸的酸性,盐酸不是氯元素的最高价含氧酸,故无法比较 Cl和
C的非金属性强弱,B错误;
C.将 通入酸性高锰酸钾溶液中,二氧化硫具有还原性,与酸性高锰酸钾溶液发生氧化还原反应而使
之褪色,与漂白性无关,C错误;
D.向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,澄清石灰水变浑浊,则该溶液中可
能含有 、 、 、 ,D错误;
故选A 。
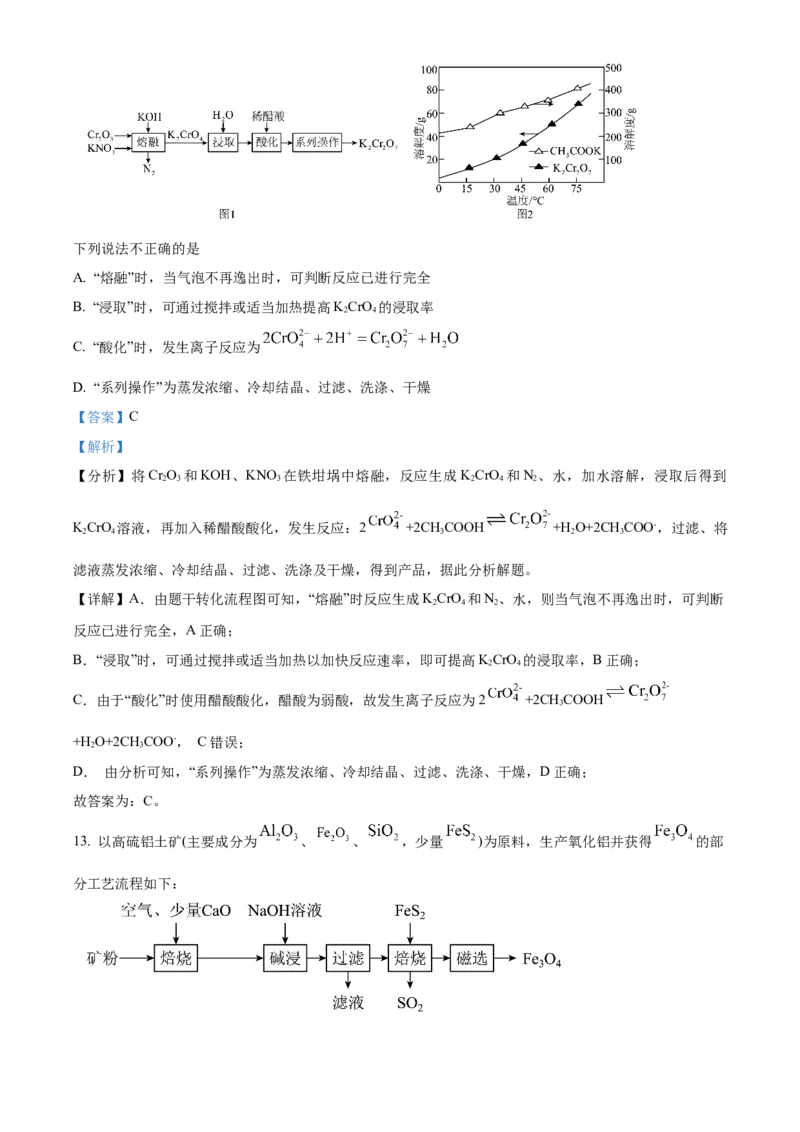
12. 重铬酸钾(K Cr O)是一种重要的化工原料。实验室以氧化铬(CrO)为原料制备重铬酸钾的实验流程如
2 2 7 2 3
图1。KCr O 与CHCOOK的溶解度随温度变化曲线如图2。
2 2 7 3下列说法不正确的是
A. “熔融”时,当气泡不再逸出时,可判断反应已进行完全
B. “浸取”时,可通过搅拌或适当加热提高KCrO 的浸取率
2 4
C. “酸化”时,发生离子反应为
D. “系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
【答案】C
【解析】
【分析】将Cr O 和KOH、KNO 在铁坩埚中熔融,反应生成KCrO 和N 、水,加水溶解,浸取后得到
2 3 3 2 4 2
KCrO 溶液,再加入稀醋酸酸化,发生反应:2 +2CH COOH +H O+2CHCOO-,过滤、将
2 4 3 2 3
滤液蒸发浓缩、冷却结晶、过滤、洗涤及干燥,得到产品,据此分析解题。
【详解】A.由题干转化流程图可知,“熔融”时反应生成KCrO 和N、水,则当气泡不再逸出时,可判断
2 4 2
反应已进行完全,A正确;
B.“浸取”时,可通过搅拌或适当加热以加快反应速率,即可提高KCrO 的浸取率,B正确;
2 4
C.由于“酸化”时使用醋酸酸化,醋酸为弱酸,故发生离子反应为2 +2CH COOH
3
+H O+2CHCOO-, C错误;
2 3
D. 由分析可知,“系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,D正确;
故答案为:C。
13. 以高硫铝土矿(主要成分为 、 、 ,少量 )为原料,生产氧化铝并获得 的部
分工艺流程如下:下列说法错误的是
A. “焙烧”产生的 可用 溶液吸收
B. “碱浸”时适当提高 溶液浓度可加快反应速率
C. 向“过滤”得到滤液中通入过量 ,将 转化为 离子反应为:
D. 与 混合后在缺氧条件下焙烧生成 和 ,理论上完全反应消耗的
【答案】D
【解析】
【分析】高硫铝土矿主要成分为Al O、Fe O、SiO,少量FeS,通入空气、加入氧化钙焙烧,其中氧化
2 3 2 3 2 2
钙和二氧化硫反应生成亚硫酸钙,和二氧化硅反应生成硅酸钙,得到产物加入氢氧化钠溶液碱浸其中氧化
铝溶解生成四羟基合铝酸钠溶液(偏铝酸钠),经过滤得到的固体中含大量的Fe O,Fe O 与FeS 混合后在
2 3 2 3 2
缺氧条件下焙烧生成Fe O 和SO ,以此解答该题。
3 4 2
【详解】A.“焙烧”产生的SO 可用NaOH溶液吸收转化为亚硫酸钠和水,A正确;
2
B.根据增大反应物浓度,可以加快化学反应速率,“碱浸”时适当提高NaOH溶液浓度可加快反应速率,B
正确;
C.向“过滤”得到滤液中通入过量CO,将 转化为Al(OH) 离子反应为:
2 3
,C正确;
D.无氧焙烧的方程式为FeS+16Fe O 2SO +11Fe O,理论上消耗的n(FeS ):n(Fe O)=1:16;D错误;
2 2 3 2 3 4 2 2 3
故选D。
二、解答题(共4小题 满分61分)
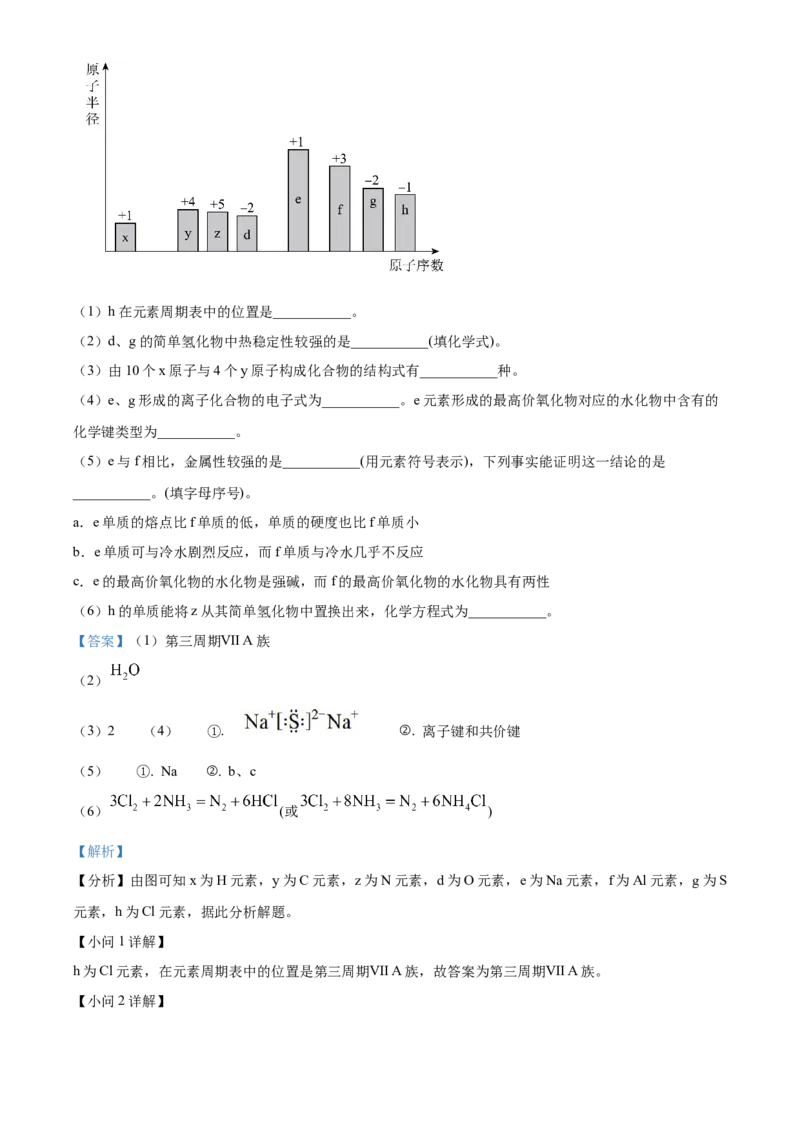
14. 随着原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合
价的变化如下图所示:(1)h在元素周期表中的位置是___________。
(2)d、g的简单氢化物中热稳定性较强的是___________(填化学式)。
(3)由10个x原子与4个y原子构成化合物的结构式有___________种。
(4)e、g形成的离子化合物的电子式为___________。e元素形成的最高价氧化物对应的水化物中含有的
化学键类型为___________。
(5)e与f相比,金属性较强的是___________(用元素符号表示),下列事实能证明这一结论的是
___________。(填字母序号)。
a.e单质的熔点比f单质的低,单质的硬度也比f单质小
b.e单质可与冷水剧烈反应,而f单质与冷水几乎不反应
c.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
(6)h的单质能将z从其简单氢化物中置换出来,化学方程式为___________。
【答案】(1)第三周期ⅦA族
(2)
(3)2 (4) ①. ②. 离子键和共价键
(5) ①. Na ②. b、c
(6) (或 )
【解析】
【分析】由图可知x为H元素,y为C元素,z为N元素,d为O元素,e为Na元素,f为Al元素,g为S
元素,h为Cl元素,据此分析解题。
【小问1详解】
h为Cl元素,在元素周期表中的位置是第三周期ⅦA族,故答案为第三周期ⅦA族。
【小问2详解】d为O元素,g为S元素, 的热稳定性比 ,故答案为 。
【小问3详解】
由10个x原子与4个y原子构成化合物为丁烷,可能的结构式有正丁烷和异丁烷,故答案为2。
【
小问4详解】
e、g形成的离子化合物为N S,电子式为 ,e元素形成的最高价氧化物对应的水化
a2
物为NaOH,含有的化学键类型为离子键和共价键,故答案为 ;离子键和共价键。
【小问5详解】
e为Na元素,f为Al元素,金属性强的是Na;
a.单质的熔点和硬度不能证明金属性强弱,故a不符合题意;
b.e单质可与冷水剧烈反应,而f单质与冷水几乎不反应,说明Na的金属性更强,故b符合题意;
c.最高价氧化物的水化物的碱性越强,金属性强,所以Na的金属性更强,故c符合题意;
故答案为Na;b、c。
【小问6详解】
h的单质能将z从其简单氢化物中置换出来,即Cl 可以从NH 中置换出N,化学方程式为
2 3 2
(或 ),故答案为 (或
)。
15. 海水中有丰富的化学资源,可利用海水制盐和提溴。
I海水晒盐获得 的粗盐中含有其他盐 和难溶性杂质,某兴趣小组在实验室
中进行粗盐精制的模拟实验。实验过程如下:称取一定质量的粗盐,加水充分溶解,过滤;向滤液中依次
加入稍过量的甲溶液、 溶液、乙溶液,过滤;向滤液中加入足量盐酸,蒸发结晶,制得精盐。
(1)加水溶解粗盐时,需控制所加入的水的质量。加入水的适宜用量是___________。
(2)乙溶液为___________溶液(填化学式)。实验中不取样出来进行分析,判断 溶液加入量已“稍过
量”的实验方法及现象是___________。
(3)某同学认为,若粗盐中含 的质量为 ,正确进行上述实验操作制得精盐的质量将大于 。判断其观点是否合理,并说明理由___________。
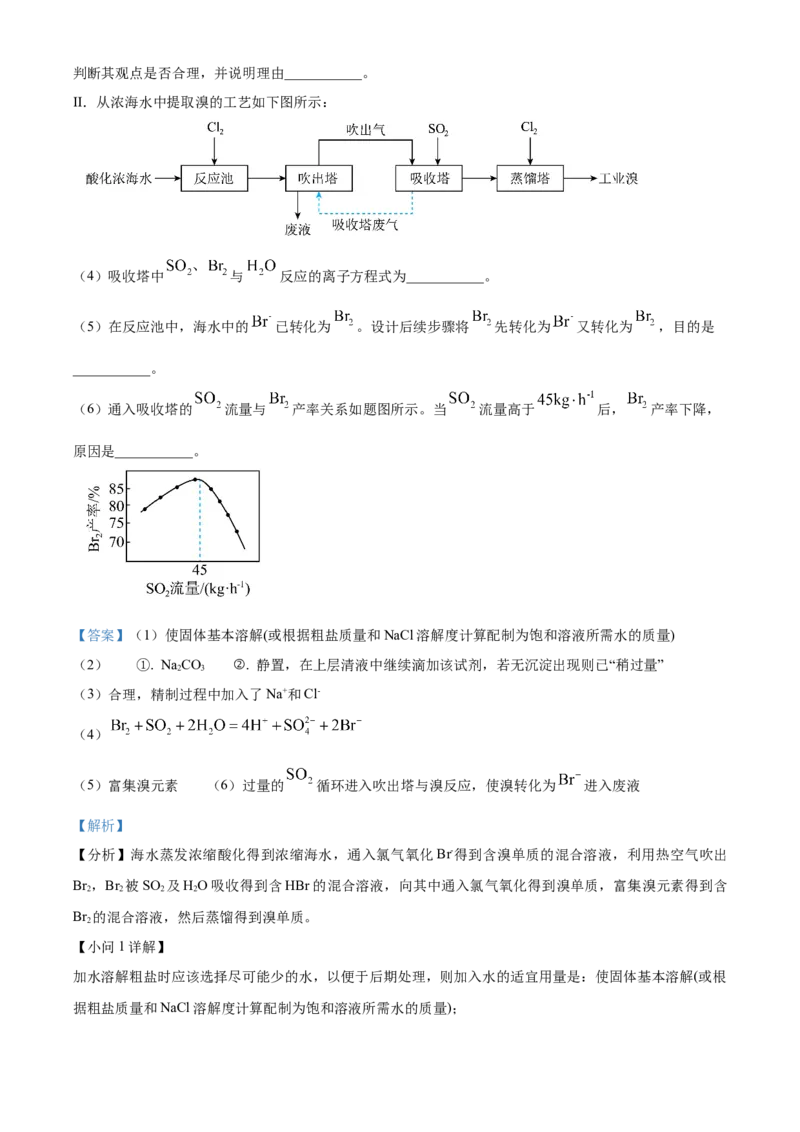
II.从浓海水中提取溴的工艺如下图所示:
(4)吸收塔中 与 反应的离子方程式为___________。
(5)在反应池中,海水中的 已转化为 。设计后续步骤将 先转化为 又转化为 ,目的是
___________。
(6)通入吸收塔的 流量与 产率关系如题图所示。当 流量高于 后, 产率下降,
原因是___________。
【答案】(1)使固体基本溶解(或根据粗盐质量和NaCl溶解度计算配制为饱和溶液所需水的质量)
(2) ①. NaCO ②. 静置,在上层清液中继续滴加该试剂,若无沉淀出现则已“稍过量”
2 3
(3)合理,精制过程中加入了Na+和Cl-
(4)
(5)富集溴元素 (6)过量的 循环进入吹出塔与溴反应,使溴转化为 进入废液
【解析】
【分析】海水蒸发浓缩酸化得到浓缩海水,通入氯气氧化Br-得到含溴单质的混合溶液,利用热空气吹出
Br ,Br 被SO 及HO吸收得到含HBr的混合溶液,向其中通入氯气氧化得到溴单质,富集溴元素得到含
2 2 2 2
Br 的混合溶液,然后蒸馏得到溴单质。
2
【小问1详解】
加水溶解粗盐时应该选择尽可能少的水,以便于后期处理,则加入水的适宜用量是:使固体基本溶解(或根
据粗盐质量和NaCl溶解度计算配制为饱和溶液所需水的质量);【小问2详解】
利用沉淀法除去粗盐中可溶性杂质:Mg2+、Ca2+、 ,先加入过量的NaOH溶液,生成Mg(OH) 沉淀,
2
以除去Mg2+,此时引入了OH-杂质,再加入过量BaCl 溶液,生成BaSO 沉淀,以除去 ,此时引入了
2 4
Ba2+杂质,再加入过量NaCO 溶液,生成BaCO 沉淀和CaCO 沉淀,以除去Ba2+、Ca2+,则乙溶液为
2 3 3 3
NaCO;加入氯化钡的目的是通过沉淀的方法除去溶液中的硫酸根离子,则检验其是否稍过量的方法是:
2 3
静置,在上层清液中继续滴加该试剂,若无沉淀出现则已“稍过量”;
【小问3详解】
由第2问可知,在除杂过程中加入的试剂中含有钠离子和氯离子,则最终会转化为氯化钠,故答案为:合
理;精制过程中加入了Na+和Cl-;
【小问4详解】
在吸收塔中单质溴、二氧化硫和水反应生成溴化氢和硫酸,离子方程式为:
;
【小问5详解】
Cl 将Br-氧化为Br 而自身还原为Cl-反应为Cl + 2Br-=2Cl-+ Br,再利用空气将Br 吹入吸收塔。吸收塔中
2 2 2 2 2
SO 将Br 还原为HBr反应为SO + Br + 2H O = HSO + 2HBr。蒸馏塔中Cl 将Br-氧化为Br ,经历反复
2 2 2 2 2 2 4 2 2
的氧化再还原后又氧化实则将溴进行富集,故答案为:富集溴元素;
【小问6详解】
根据吹出时,Br 吹出率与吸收塔中SO 流量的关系图可知:如果SO 流量过大,Br 吹出率反而下降,故
2 2 2 2
答案为:过量的 循环进入吹出塔与溴反应,使溴转化为 进入废液。
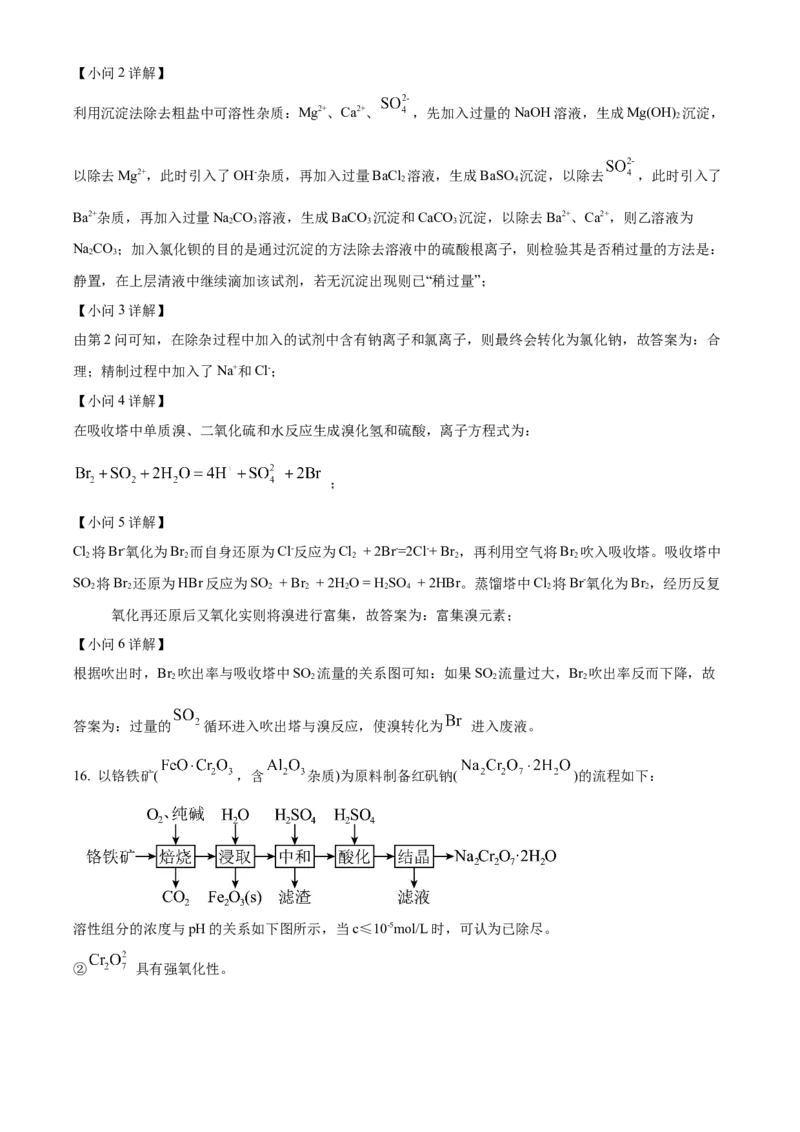
16. 以铬铁矿( ,含 杂质)为原料制备红矾钠( )的流程如下:
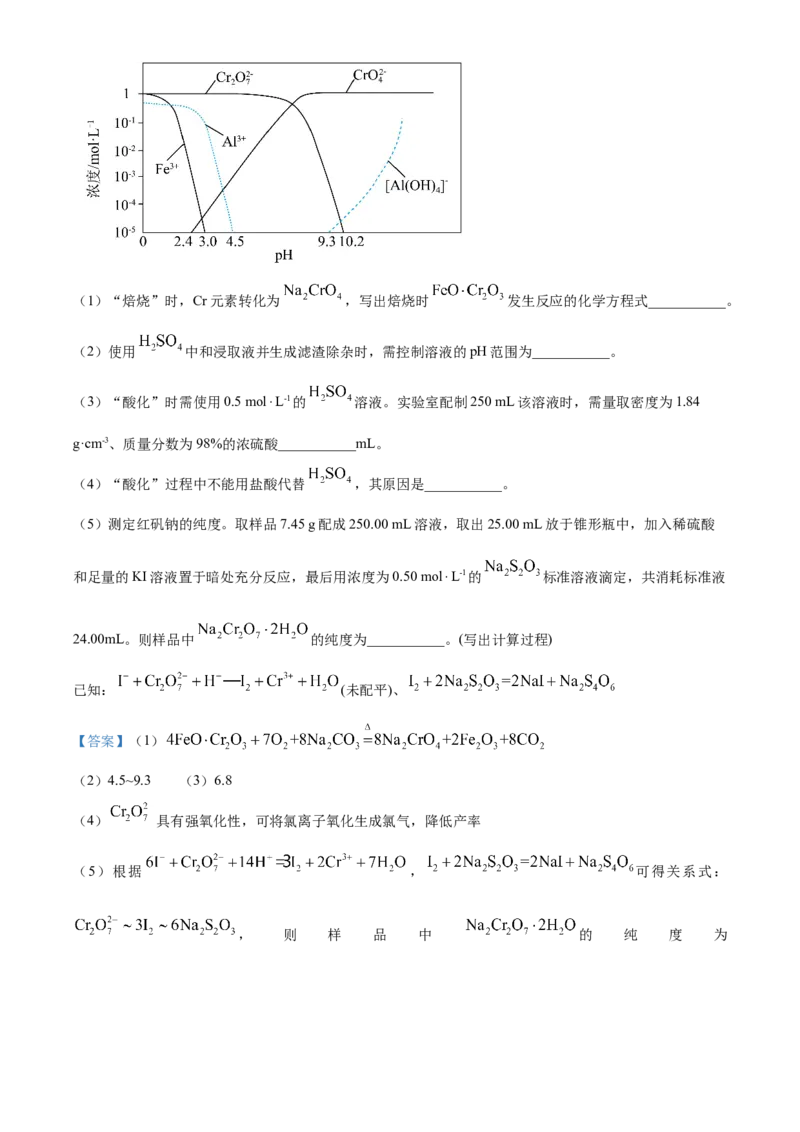
溶性组分的浓度与pH的关系如下图所示,当c≤10-5mol/L时,可认为已除尽。
② 具有强氧化性。(1)“焙烧”时,Cr元素转化为 ,写出焙烧时 发生反应的化学方程式___________。
(2)使用 中和浸取液并生成滤渣除杂时,需控制溶液的pH范围为___________。
(3)“酸化”时需使用0.5 mol⋅L-1的 溶液。实验室配制250 mL该溶液时,需量取密度为1.84
g·cm-3、质量分数为98%的浓硫酸___________mL。
(4)“酸化”过程中不能用盐酸代替 ,其原因是___________。
(5)测定红矾钠的纯度。取样品7.45 g配成250.00 mL溶液,取出25.00 mL放于锥形瓶中,加入稀硫酸
和足量的KI溶液置于暗处充分反应,最后用浓度为0.50 mol⋅L-1的 标准溶液滴定,共消耗标准液
24.00mL。则样品中 的纯度为___________。(写出计算过程)
已知: (未配平)、
【答案】(1)
(2)4.5~9.3 (3)6.8
(4) 具有强氧化性,可将氯离子氧化生成氯气,降低产率
(5)根据 , 可得关系式:
, 则 样 品 中 的 纯 度 为=80%
【解析】
【分析】铬铁矿主要成分FeO·Cr O,含Al O、SiO 等杂质。铬铁矿和纯碱、氧气焙烧生成NaCrO、偏
2 3 2 3 2 2 4
铝酸钠、硅酸钠、氧化铁,“水浸”除去氧化铁,滤液中加硫酸“中和”生成氢氧化铝、硅酸沉淀,过滤,滤
液中加硫酸酸化把 完全转化为 ,蒸发浓缩,冷却结晶析出NaCr O·2H O。
2 2 7 2
【小问1详解】
焙烧时FeO·Cr O、碳酸钠、氧气反应生成NaCrO、氧化铁、二氧化碳气体,发生反应的化学方程式为
2 3 2 4
;
【小问2详解】
使用 中和的目的是以氢氧化铝沉淀、硅酸沉淀的形式除去 元素, 根据图示,pH的理论范
围为4.5~9.3;
【小问3详解】
密度为1.84 g·cm-3、质量分数为98%的浓硫酸浓度为
,根据稀释前后硫酸的物质的量不变,需量取浓硫
酸的体积为 ≈6.8mL;
【小问4详解】
“酸化”过程中不能用盐酸代替 ,其原因是 具有强氧化性,可将氯离子氧化生成氯气,降低
产率;
【小问5详解】
根 据 , 可 得 关 系 式 :
, 则 样 品 中 的 纯 度 为=80%。
17. 自然界中含硫物质不断发生转化和转移,形成了硫元素的循环。利用这些转化可以制备重要的化工产
品,过程中产生的 等会污染环境,需要加以治理。
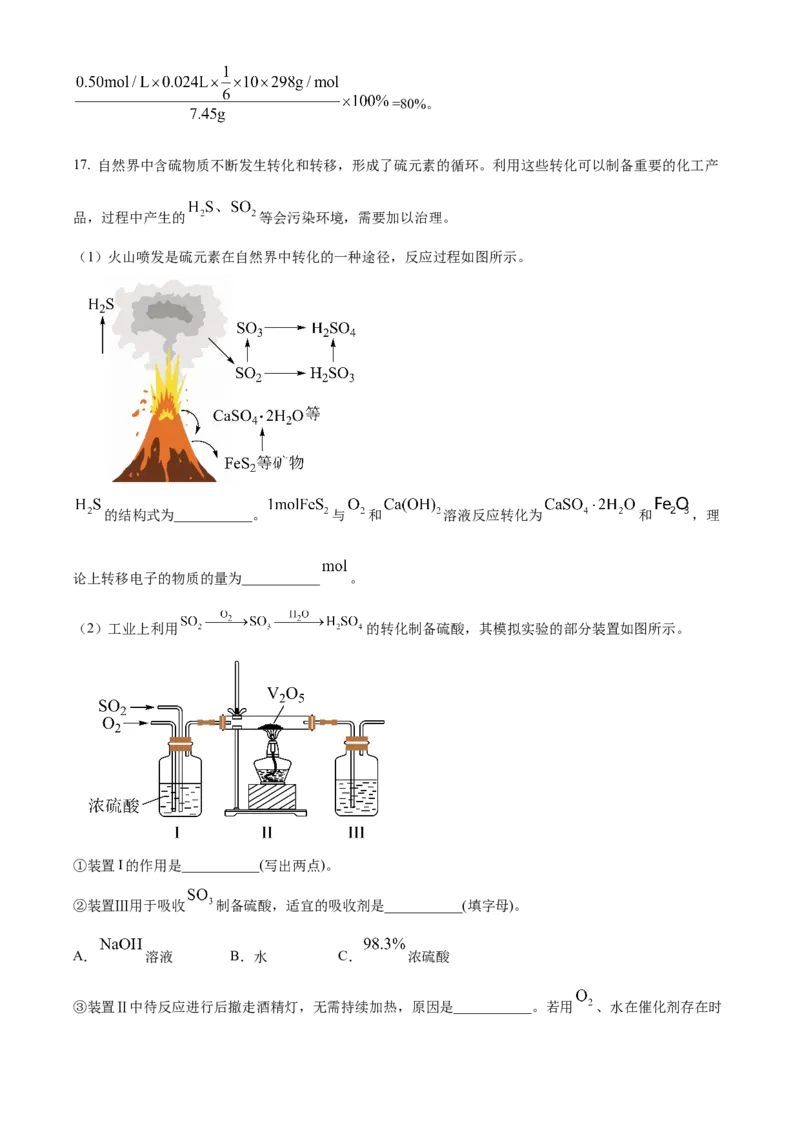
(1)火山喷发是硫元素在自然界中转化的一种途径,反应过程如图所示。
的结构式为___________。 与 和 溶液反应转化为 和 ,理
论上转移电子的物质的量为___________ 。
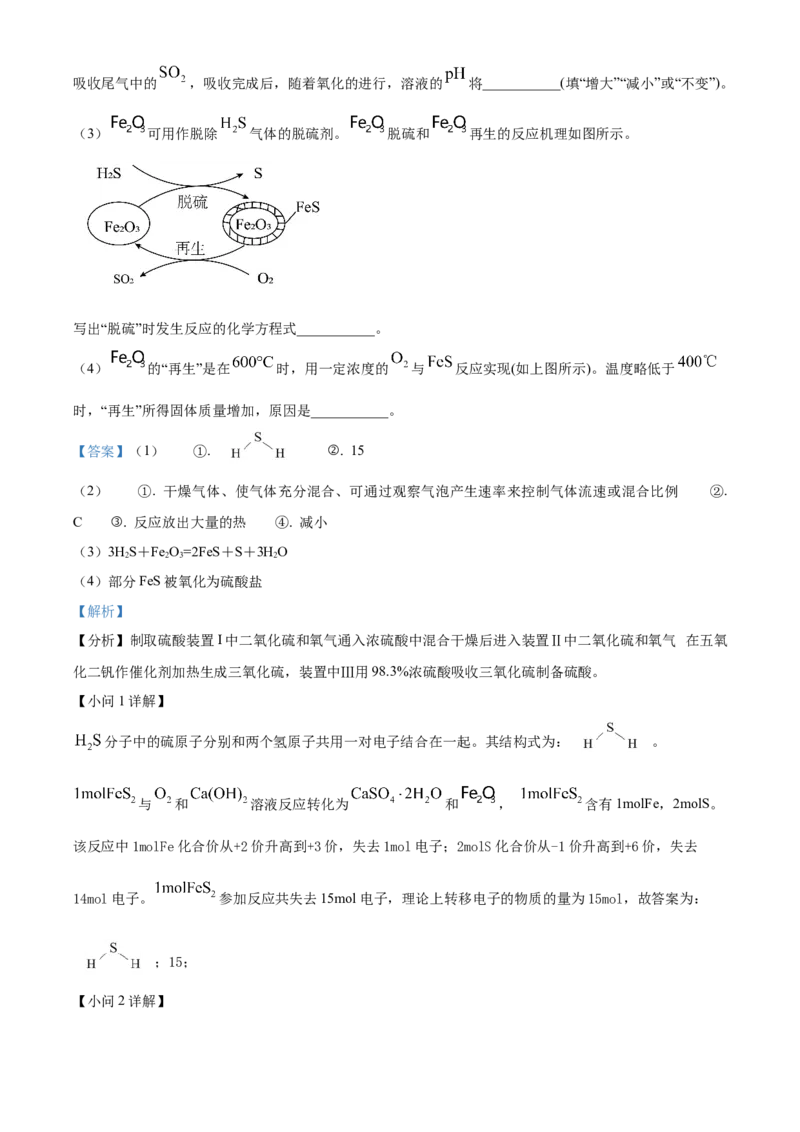
(2)工业上利用 的转化制备硫酸,其模拟实验的部分装置如图所示。
①装置I的作用是___________(写出两点)。
②装置Ⅲ用于吸收 制备硫酸,适宜的吸收剂是___________(填字母)。
A. 溶液 B.水 C. 浓硫酸
③装置Ⅱ中待反应进行后撤走酒精灯,无需持续加热,原因是___________。若用 、水在催化剂存在时吸收尾气中的 ,吸收完成后,随着氧化的进行,溶液的 将___________(填“增大”“减小”或“不变”)。
(3) 可用作脱除 气体的脱硫剂。 脱硫和 再生的反应机理如图所示。
写出“脱硫”时发生反应的化学方程式___________。
(4) 的“再生”是在 时,用一定浓度的 与 反应实现(如上图所示)。温度略低于
时,“再生”所得固体质量增加,原因是___________。
【答案】(1) ①. ②. 15
(2) ①. 干燥气体、使气体充分混合、可通过观察气泡产生速率来控制气体流速或混合比例 ②.
C ③. 反应放出大量的热 ④. 减小
(3)3HS+Fe O=2FeS+S+3HO
2 2 3 2
(4)部分FeS被氧化为硫酸盐
【解析】
【分析】制取硫酸装置I中二氧化硫和氧气通入浓硫酸中混合干燥后进入装置Ⅱ中二氧化硫和氧气 在五氧
化二钒作催化剂加热生成三氧化硫,装置中Ⅲ用98.3%浓硫酸吸收三氧化硫制备硫酸。
【小问1详解】
分子中的硫原子分别和两个氢原子共用一对电子结合在一起。其结构式为: 。
与 和 溶液反应转化为 和 , 含有1molFe,2molS。
该反应中1molFe化合价从+2价升高到+3价,失去1mol电子;2molS化合价从-1价升高到+6价,失去
14mol电子。 参加反应共失去15mol电子,理论上转移电子的物质的量为15mol,故答案为:
;15;
【小问2详解】①装置I中二氧化硫和氧气通入浓硫酸中,浓硫酸可以干燥气体、使气体充分混合、可通过观察气泡产生
速率来控制气体流速或混合比例,故答案为:干燥气体、使气体充分混合、可通过观察气泡产生速率来控
制气体流速或混合比例;
②装置Ⅲ中吸收 制备硫酸。三氧化硫不能用水进行吸收,否则将形成大量酸雾,应采用 98.3%硫酸作
吸收剂,故答案为:C;
③二氧化硫和氧气生成三氧化硫的反应为放热反应,所以装置Ⅱ中待反应进行后撤走酒精灯,无需持续加
热。用水在催化剂存在时吸收尾气中的 ,发生反应 ,吸收完成后,随着氧化的进
行 ,溶液的 将减小,故答案为:减小;
【小问3详解】
分析机理图可知脱硫时,部分 Fe O 转化成FeS,HS被氧化成S,发生反应:HS+Fe O=2FeS+S+
2 3 2 2 2 3
3HO,故答案为:HS+Fe O=2FeS+S+3HO;
2 2 2 3 2
【小问4详解】
400℃条件下,氧气将FeS中的S氧化成+6价,脱硫剂中除Fe、O元素外,引入了S元素,即氧气将FeS
氧化生成硫酸盐,“再生”所得固体质量增加,故答案为:部分FeS被氧化为硫酸盐。