文档内容
第五章 化学生产中的重要非金属元素
第一节 硫及其化合物
第四课时 不同价态含硫物质的转化
【学习目标】1.通过阅读教材“资料卡片—自然界中硫的存在和转化”内容,了解含硫物质进入大气
的主要途径,知道二氧化硫进入大气能形成酸雨危害环境,增强环保意识,培养社会责任感。
2.根据硫元素的不同价态,了解硫元素不同价态间的转化及反应条件的控制,理解硫及其化合物的相
互转化原理,熟悉常见的化学方程式
3.通过实验探究,知道含不同价态硫元素的物质可以相互转化,并能设计实验进行探究或验证,知道
二氧化硫进入大气能形成酸雨危害环境,增强环保意识,培养社会责任感。
【学习重点】不同价态含硫物质的转化及实验探究
【学习难点】不同价态含硫物质的转化原理
【课前预习】
旧知回顾:1.若将等物质的量的SO 和Cl 同时通入品红溶液中,溶液的漂白性会更强吗?为什么?
2 2
【答案要点】不是。若将等物质的量的 SO 和 Cl 相混合后,在溶液中发生反应:SO +Cl +
2 2 2 2
2HO===H SO +2HCl,从而失去漂白能力。
2 2 4
2.若设计实验鉴别SO 和CO 应注意哪些问题?
2 2
【答案要点】①鉴别SO 和CO ,不能用澄清的石灰水,因为二者通入澄清石灰水时,现象相同:开
2 2
始产生白色沉淀,后来沉淀又逐渐溶解。
②要检验SO 、CO 混合气体中的CO ,必须先除去SO (一般用溴水或KMnO 酸性溶液),再通入澄
2 2 2 2 4
清的石灰水。
新知预习: 1.简述硫元素在自然界的存在?
【答案要点】自然界中游离态的硫存在于火山喷口附近或地壳的岩层里,化合态的硫主要以硫化物和
_硫酸盐形式存在。
2.从氧化还原反应的视角分析不同价态硫元素之间如何进行相互转化?
【答案要点】不同价态硫元素之间的相互转化主要通过氧化还原反应实现。如下图所示:
上述转化中,从左到右,硫元素化合价升高,需加入氧化剂;从右到左,硫元素化合价降低,需加入
还原剂。【课中探究】
情景导入:视频播放—自然界中不同含硫物质的转化(见PPT)
一、不同价态含硫物质的转化关系
活动一、自然界中硫的存在和转化
任务一、阅读教材P7页“资料卡片”内容,思考硫元素在自然界的存在形态及转化关系分别什么?
【答案要点】①硫元素在自然界中的转化可用下图表示:
自然界中硫的转化
②硫在自然界以游离态(存在于火山喷口附近或地壳的岩层里,煤中也含有少量硫。)和化合态(主
要以硫化物和硫酸盐的形式存在)两种形态存在。例如黄铁矿(FeS )、黄铜矿(CuFeS)、石膏
2 2
(CaSO·2H O)、芒硝(Na SO ·10H O)。火山口附近的硫单质会被大气中是氧气氧化成二氧化硫,二氧化硫
4 2 2 4 2
可被进一步氧化成三氧化硫,二氧化硫和三氧化硫遇水分别形成亚硫酸和硫酸。如图:
任务二、讨论交流:根据硫元素在自然界的转化关系,思考硫及其化合物的转化原理有哪些?
【答案要点】①不同价态硫元素之间的相互转化主要通过氧化还原反应实现,如:
2HS+3O=2SO+2H O、2HSO +O =2H SO 等。
2 2 2 2 2 3 2 2 4
②相同价态硫元素之间的转化主要根据酸、碱、盐及其氧化物的性质实现。如SO +H O=HSO 、
3 2 2 4
SO +2NaOH=Na SO +H O等。
2 2 3 2
【对应训练】1.硫磺在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,乙溶液褪
色变成丙。甲、乙、丙均含有硫元素,则它们正确的顺序是( )
A.SO 、HSO 、HSO B.SO 、HSO 、HSO
3 2 4 2 3 2 2 3 2 4
C.SO 、HSO 、HSO D.SO 、HSO 、HSO
3 2 3 2 4 2 2 4 2 3
【答案】B
【解析】硫磺在空气中燃烧生成气体甲SO ,甲SO 溶于水得溶液乙HSO ,向乙HSO 溶液中滴加溴
2 2 2 3 2 3水,乙溶液褪色变成丙HSO ,则甲、乙、丙分别为SO 、HSO 、HSO ,答案B。
2 4 2 2 3 2 4
2.关于反应HSO +NaSO =Na SO +SO ↑+HO所涉及的物质,下列说法错误的是( )
2 4 2 3 2 4 2 2
A.浓HSO 能与SO 发生氧化还原反应 B.NaSO 容易被空气中的O 氧化变质
2 4 2 2 3 2
C.浓硫酸与铜在常温下反应生成SO D.SO 是导致酸雨的主要有害污染物
2 2
【答案】A
【解析】A.反应中元素化合价不变,属于非氧化还原反应,故A错误; B. NaSO 具有还原性,
2 3
容易被空气中的O 氧化为 NaSO ,故B正确;C. 浓硫酸具有强氧化性与铜在常温下反应生成SO ,故
2 2 4 2
C正确;D. SO 能和水反应生成HSO ,是导致酸雨的主要有害污染物,故D正确;选A。
2 2 3
活动二、建构含硫物质的价类二维图
任务一、讨论交流:如何根据氧化还原反应原理构建含硫物质的价类二维图?
【答案要点】①价态与性质:a.-2价硫处于最低价态,只有还原性,可被O、Cl 等氧化剂氧化为
2 2
S;
b.0价、+4价硫处于中间价态,既有氧化性又有还原性;c.+6价硫处于最高价态,只有氧化性。
②价态规律:a.当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态(化合价只靠拢不交
叉),即台阶式升降,可用下图表示:
b.相邻价态的同种元素的微粒间不发生氧化还原反应,如S和HS、S和SO 、SO 和浓硫酸之间不发生
2 2 2
氧化还原反应。
c.不同价态硫元素间的转化,均属于氧化还原反应,需要选择合适的氧化剂或者还原剂。证明硫单质、
SO 具有还原性要选择氧化剂,如酸性KMnO 溶液、氯水等;证明浓硫酸具有氧化性要选择还原剂,如金
2 4
属单质、硫单质、HS等;证明SO 具有氧化性要选择还原剂,如HS、NaS等。
2 2 2 2
③根据以上分析,含硫物质的价类二维图如下:
任务二、问题探究:根据含硫物质的价类二维图,不同价态硫元素间转化的思维模型是什么?结合所学知识,思考含硫物质有哪些不同转化关系?
【答案要点】①转化的思维模型:
②转化类型:
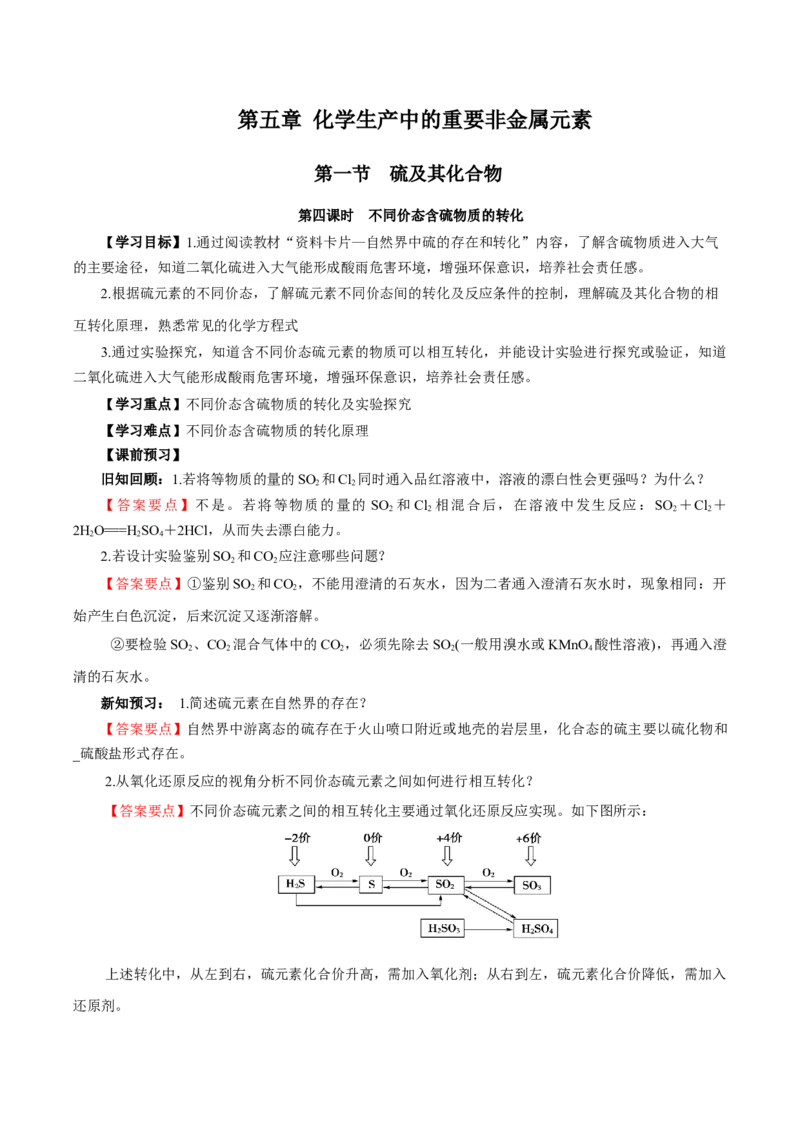
a,直线型转化关系:S(固体)――→SO ――→SO ――→HSO
2 3 2 4
或HS――→S(固体)――→SO ――→SO ――→HSO
2 2 3 2 4
b.交叉型转化关系:
c,三角型转化关系:
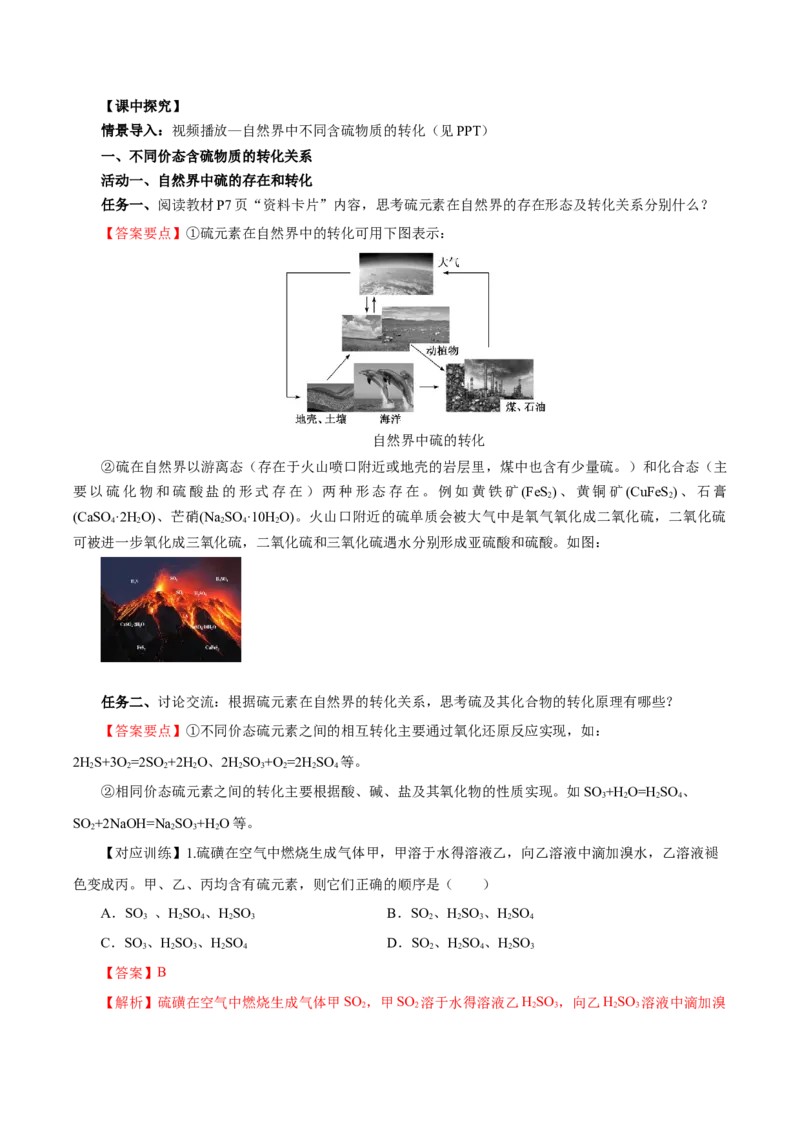
【对应训练】1.下图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.操作Ⅱ发生反应的离子方程式为:2Fe2++4H++O =2Fe3++2H O
2 2
B.溶液b中阳离子只有Fe2+
C.溶液a转化为溶液b的反应中,SO 被氧化
2
D.加入FeO可以使溶液c转化为溶液a
【答案】C
【解析】Fe3+有氧化性,SO 有还原性,Fe (SO ) 被SO 还原为FeSO ,溶液b主要溶质为FeSO 、
2 2 4 3 2 4 4
HSO ,可能含Fe (SO ) 或SO ,空气中氧气将FeSO 及可能存在的SO 氧化得溶液a循环使用。A.电荷
2 4 2 4 3 2 4 2
不守恒,操作Ⅱ发生反应的离子方程式为:4Fe2++4H++O = 4Fe3++2H O,A错误;B.操作I中发生反应的
2 2
离子方程式为:2Fe3++SO+2H O = 2Fe2++SO+4H+,溶液中阳离子有Fe2+、H+,若SO 少量,则还有Fe3+,B
2 2 2
错误;C.溶液a转化为溶液b的反应中,SO 被Fe3+氧化,C正确;D.溶液c中含有 Fe (SO )、HSO 等
2 2 4 3 2 4物质,加入FeO后会生成FeSO ,D错误。答案选C。
4
2.物质类别和核心元素的价态是学习元素及其化合物性质的重要认识视角。如图是某元素的“价类
二维图”,其中单质b是黄色固体,f、h均为正盐,且焰色都是黄色。下列说法不正确的是( )
A.a和c反应可以生成b B.用BaCl 溶液可以鉴别f和h的溶液
2
C.e的浓溶液可用铝槽车运输 D.c能使品红溶液褪色
【答案】B
【解析】单质b是黄色固体,所以b是硫,f、h均为正盐,且焰色都是黄色,根据示意图可知a是
HS,c是SO ,d是SO ,e是硫酸,f是硫酸钠,g是亚硫酸,h是亚硫酸钠,据此解答。A. 二氧化硫具
2 2 3
有氧化性,能氧化硫化氢,二者反应可以生成单质硫,A正确;B. 亚硫酸钠和硫酸钠均能与氯化钡反应生
成白色沉淀,不用BaCl 溶液鉴别二者,B错误;C. 常温下铝在浓硫酸中钝化,因此e的浓溶液可用铝槽
2
车运输,C正确;D. 二氧化硫具有漂白性,能使品红溶液褪色,D正确;
二、实验探究不同价态含硫物质的转化
活动一、实验室中研究不同价态含硫物质的转化原理
任务一、根据教材P8页“探究”内容,思考硫元素常见价态及其转化关系是什么?
【答案要点】①硫元素常见价态及转化:S S S S
②通过氧化还原反应实现不同价态含硫物质的相互转化,低价态的硫向高价态转化时需加入氧化剂,
高价态的硫向低价态转化时需加入还原剂。
任务二、讨论交流:阅读检测P9页“方法导引”栏目内容,你是如何理解化学实验设计及探究不同
价态含硫物质的转化关系的?并填写表格内容。
【答案要点】①化学实验设计是指实验者在实施化学实验之前,根据一定的实验目的,运用化学知识
与技能,按照一定的实验方法,对实验的原理、试剂、仪器与装置、步骤和方法等所进行的规划。
②设计实验实现不同价态硫转化,遵循的原则是科学性、可行性、安全性和绿色化。化学实验设计一
般以实验设计方案的形式呈现,通常包括实验课题、实验目的、实验原理、实验仪器与试剂、实验步骤及
注意事项、实验数据及处理、实验结论与讨论等。
③含硫物质的转化实验方案设计:
预期转化 选择试剂 实验操作和现象 实验结论
H 2 S→S 二氧化硫、硫化 将HS和SO 通入水中,生成 SO 与HS反应生
2 2 2 2SO→S 氢、蒸馏水 淡黄色沉淀(或溶液变浑浊) 成单质硫
2
二氧化硫、新制 将SO 通入新制氯水中,溶液 二氧化硫在水中能
2
SO→HSO 氯水、BaCl 溶 浅黄绿色褪去;再向溶液中滴 被强氧化剂氧化为
2 2 4 2
液 入氯化钡溶液,产生白色沉淀 SO
加热铜片和浓硫酸的混合物, 浓硫酸被金属铜还
HSO →SO 浓硫酸、铜片
2 4 2 有刺激性气味气体生成 原为SO
2
【对应训练】1.分别能实现下列从左到右转化的单质是( )
A.Mg和S B.Fe和Cl C.Ca和C D.Cu和Si
【答案】C
【解析】A.Mg与氧气反应生成MgO,MgO是碱性氧化物,MgO与水不反应;S与氧气反应生成
SO ,SO 是酸性氧化物,SO 与水反应生成亚硫酸,亚硫酸与碱或碱性氧化物反应生成亚硫酸盐,故A不
2 2 2
符合题意;B.Fe与氧气反应生成Fe O,Fe O 不是碱性氧化物,且Fe O 与水不反应,故B不符合题
3 4 3 4 3 4
意;C.Ca与氧气反应生成CaO,CaO是碱性氧化物,CaO与水反应生成Ca(OH) ,Ca(OH) 是碱,
2 2
Ca(OH) 与盐酸反应生成盐CaCl ;C与氧气反应生成CO,CO 是酸性氧化物,CO 与水反应生成碳酸,
2 2 2 2 2
碳酸与碱反应生成碳酸盐,故C符合题意;D.Cu与氧气反应生成CuO,CuO是碱性氧化物,但是CuO
与水不反应,故D不符合题意。故选C。
2.含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产
品,该工艺流程如图所示,下列叙述不正确的是( )
A.该工艺流程是用来除去煤燃烧时产生的SO
2
B.该过程中可得到化工产品HSO
2 4
C.图中涉及的反应之一为
Fe (SO )+SO+2H O=2FeSO +2H SO
2 4 3 2 2 4 2 4
D.该过程中化合价发生改变的元素只有Fe和S
【答案】D
【解析】由图可知发生反应为:Fe (SO )+SO+2H O=2FeSO +2H SO ,同时4FeSO +
2 4 3 2 2 4 2 4 4
2HSO +O =2Fe (SO )+2H O,总反应为2SO +O +2H O=2HSO 。A.根据总反应2SO +O +2H O=2HSO
2 4 2 2 4 3 2 2 2 2 2 4 2 2 2 2 4
可知该工艺流程是用来除去煤燃烧时产生的SO ,A正确;B.根据总反应为2SO +O +2H O=2HSO 可知
2 2 2 2 2 4
该过程中可得到化工产品HSO ,B正确;C.Fe (SO ) 与SO 反应生成FeSO 和HSO ,其反应的化学方
2 4 2 4 3 2 4 2 4
程式为Fe (SO )+SO+2H O=2FeSO +2H SO ,C正确;D.该过程中Fe (SO ) 与SO 反应生成FeSO 和
2 4 3 2 2 4 2 4 2 4 3 2 4
HSO ,同时FeSO 、O 和HSO 反应生成Fe (SO ),则反应过程中Fe、O和S的化合价发生改变,D错
2 4 4 2 2 4 2 4 3
误;故合理选项是D。
活动二、实验验证含硫物质的转化任务一、联系教材P8页“探究”栏目,根据下表实验步骤完成实验,并填写表格内容。
【答案要点】
实验操作 实验现象 原理分析
NaS中-2价硫与HSO (或SO )中+4价
2 2 3 2
在一支试管中加入1mL Na 2 S 硫发生归中反应,生成中间价态0价的硫
溶液,边振荡边滴加H 2 SO 3 试管中产生淡黄色 单质。SO 为酸性氧化物与碱反应。2S2-
2
溶液,用浸NaOH溶液的棉 沉淀
+SO+4H+=3S↓+2H O
2 2
团塞住试管口
SO +2OH-=SO+H O
2 2
在一支试管中加入1mL Na S Na 2 S中-2价硫被酸性KMnO 4 溶液氧化成
溶液,边振荡边滴加酸性
2 紫红色褪去,试管 硫单质,本身被还原成Mn2+。
中产生淡黄色沉淀
KMnO 4 溶液 5S2-+2MnO -+16H+=5S↓+2Mn2++8H O
4 2
任务二、问题探究:将SO 气体分别通入BaCl 溶液、Ba(NO ) 溶液能否产生沉淀?如何防止SO 可能
2 2 3 2 2
对环境产生的污染?
【答案要点】①SO 气体通入BaCl 溶液无明显现象,因为酸性HSO