文档内容
第五章 化学生产中的重要非金属元素
第一节 硫及其化合物
第三课时 硫酸根离子的检验 粗盐的提纯
【学习目标】1.通过阅读教材,引导思考,了解几种常见硫酸盐的主要性质及用途,培养科学精神与
社会责任的学可核心素养。
2.通过素养探究、讨论交流,了解硫酸根离子的检验方法,学会排除干扰离子的方法,培养证据推理
和科学态度的核心核心素养。
3.通过实验设计、问题探究(原理分析),掌握粗盐提纯的基本方法,了解化学实验设计的原则。初
步了解自然界中硫元素的存在与转化,探究不同价态含例句物质的转化途径。
【学习重点】硫酸根离子的检验、粗盐的提纯
【学习难点】粗盐精制原理及方案设计
【课前预习】
旧知回顾:1.氯离子的检验方法是什么?检验氯离子时,如何排除碳酸根离子的干扰?
2.浓硫酸吸水性和脱水性有何区别?
新知预习:1.SO的检验方法是什么?应注意哪些问题?
2.粗盐中的SO、Mg2+、Ca2+的除杂试剂及其顺序如何?
【课中探究】情景导入:造纸术、指南针、火药、印刷术是中国古代四大发明,其中火药武器的使用,改变了作战
方式,帮助欧洲资产阶级摧毁了封建堡垒,加速了欧洲的历史进程。黑火药的成分为“一硫二硝三木炭”
(S + 2KNO + 3C = K S + N ↑ + 3CO ↑ )(见PPT图片)。自然界中化合态的硫主要以硫化物或硫酸盐
3 2 2 2
形式存在。
一、硫酸盐及硫酸根离子的检验
活动一、常见硫酸盐及主要用途
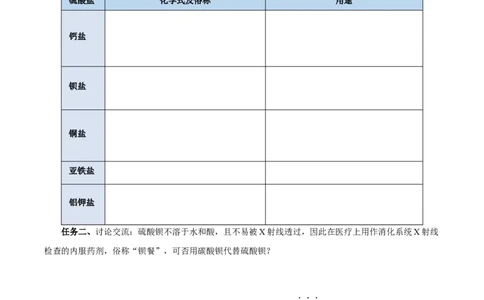
任务一、阅读教材P6页“资料卡片”,回答常见几种硫酸盐组成特点及主要用途是什么?并填写表
格内容。
硫酸盐 化学式及俗称 用途
钙盐
钡盐
铜盐
亚铁盐
铝钾盐
任务二、讨论交流:硫酸钡不溶于水和酸,且不易被X射线透过,因此在医疗上用作消化系统X射线
检查的内服药剂,俗称“钡餐”,可否用碳酸钡代替硫酸钡?
【对应训练】1.硫及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然界中硫化物在地表附近受氧气和水的长期作用会转化为硫酸盐
B.石膏(CaSO•2H O)被加热到150℃时转化为熟石膏(2CaSO•H O)
4 2 4 2
C.工业上以黄铁矿为原料经煅烧、催化氧化、吸收等反应生成HSO
2 4
D.火山口附近的硫单质会被大气中氧气氧化为三氧化硫
2.下列有关硫酸盐的说法中正确的是( )
A.硫酸钡在医学上用作钡餐,Ba2+对人体无毒B.明矾常用于净水,含Al3+的盐作为食品膨化剂时可以过量添加
C.Fe2+对人体有益,FeSO 可用于制补血剂
4
D.Cu2+有毒,CuSO 与生石灰可配成杀菌剂波尔多液
4
活动二、硫酸根离子的检验
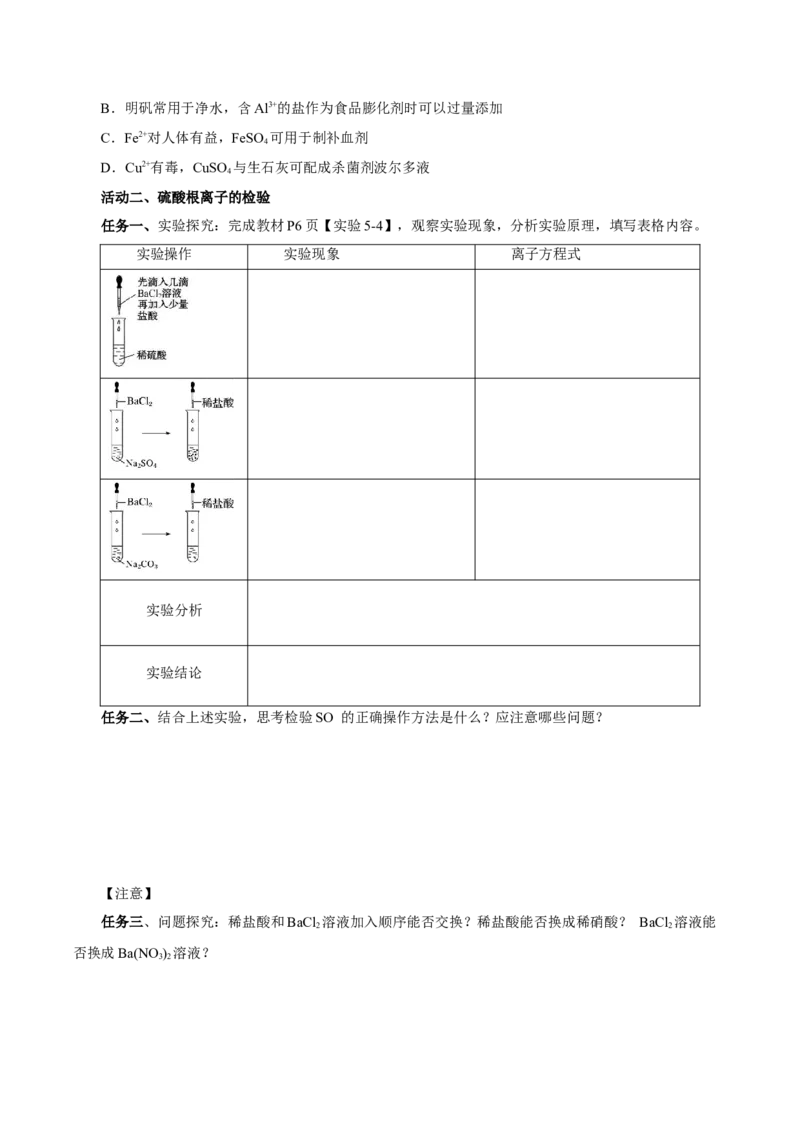
任务一、实验探究:完成教材P6页【实验5-4】,观察实验现象,分析实验原理,填写表格内容。
实验操作 实验现象 离子方程式
实验分析
实验结论
任务二、结合上述实验,思考检验SO 的正确操作方法是什么?应注意哪些问题?
【注意】
任务三、问题探究:稀盐酸和BaCl 溶液加入顺序能否交换?稀盐酸能否换成稀硝酸? BaCl 溶液能
2 2
否换成Ba(NO ) 溶液?
3 2【对应训练】1.下列实验,能证明溶液中一定含有SO的是( )
A.某溶液加入BaCl 溶液,产生白色沉淀
2
B.某溶液加入BaCl 溶液,产生白色沉淀,再加盐酸沉淀不溶解
2
C.某溶液加入硝酸酸化,再加入Ba(NO ) 溶液有白色沉淀产生
3 2
D.某溶液加入盐酸酸化,再加入BaCl 溶液有白色沉淀产生
2
2.有一瓶NaSO 溶液,可能被部分氧化。某同学取少量该溶液,滴加BaCl 溶液,产生白色沉淀,
2 3 2
再加入足量稀硫酸,充分振荡后仍有白色沉淀。下列结论中不正确的是( )
A.NaSO 已部分被空气中的O 氧化
2 3 2
B.加入BaCl 溶液后,生成的沉淀中可能有BaSO
2 4
C.加入稀硫酸后,不溶的沉淀一定是BaSO
4
D.该实验不能确定NaSO 是否部分被氧化
2 3
二、粗盐的提纯
活动一、物质除杂和分离的基本原则
任务一、讨论交流:物质除杂和分离的基本原则是什么?物质除杂和分离应注意哪些问题?
任务二、阅读教材P7“思考与讨论”内容,思考粗盐中含有哪些杂质?如何利用除杂和分离方法将粗
盐制成精盐?
【对应训练】1.下列说法中正确的是( )
A.将CO 通入氯化钙溶液中有白色沉淀生成
2
B.向硝酸酸化的㭉溶液中加入BaCl 溶液生成白色沉淀,说明该溶液中一定含有SO
2
C.常温下可以用铝制容器盛装浓硫酸或浓硝酸,因为铝和这两种酸不发生化学反应
D.可以用饱和食盐水除去Cl 中混有的少量HCl气体
2
2.下列说法中正确的是( )A.某酸性溶液中:Cl-、CHCOO-、Mg2+、SO 能大量共存
3
B.含有大量HCO的溶液中:NH、K+、SO 、OH-能大量共存
C.某透明溶液中:K+、NO、Na+、Cl-可能大量共存
D.取少量某溶液,向其中加入盐酸酸化的BaCl 溶液,观察到有白色沉淀生成,证明该溶液中含有
2
SO
活动二、粗盐的提纯
任务一、讨论交流:经溶解、过滤、蒸发操作得到的粗盐中含有一些可溶性硫酸盐及 CaCl 、MgCl 等
2 2
杂质。参考物质的溶解性表,思考如果按照下表所示顺序除去它们,应加入什么试剂?
杂质 加入的试剂 离子方程式
硫酸盐(SO)
MgCl (Mg2+)
2
CaCl (Ca2+)
2
任务二、归纳小结:上述加入的试剂除去杂质后,有没有引入其他离子?并归纳总结粗盐提纯时加入
试剂的顺序是什么?
【注意】
【对应练习】1.为了除去粗盐中的CaCl 、MgCl 、NaSO 及泥沙,得到纯净的NaCl,可将粗盐溶于
2 2 2 4
水,然后在下列操作中选取必要的步骤和正确的操作顺序( )
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量NaCO 溶液 ⑤加过量BaCl 溶液
2 3 2
A.④②⑤ B.④①②⑤③
C.②⑤④①③ D.①④②⑤③
2.要除去NaCl溶液中混有的MgCl ,应选用的试剂和操作方法是( )
2
A.加入适量NaSO 溶液后过滤 B.加入适量NaOH溶液后过滤
2 4C.加入过量NaOH溶液后蒸发 D.加入过量NaCO 溶液后过滤
2 3
【课后巩固】1.下列叙述正确的是( )
A.“钡餐”是医疗上作消化系统X射线检查的内服药剂,其主要成分是BaSO
3
B.向某溶液中加入BaCl ,产生不溶于稀HNO 的白色沉淀,则溶液中一定含有SO
2 3
C.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体
D.常温下能够用铁、铝等容器盛放浓硫酸,是因为浓硫酸的强氧化性使其钝化
2.在检验SO的过程中,下列操作正确的是( )
(提示:稀硝酸具有强氧化性,可将SO氧化为SO)
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO存在
D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO存在
3.下列实验方案不可行的是( )
选项 实验目的 实验方案
A 检验干燥的氯气是否具有漂白性 将干燥的氯气通过鲜花花瓣
B 鉴别NaCO 和NaHCO 两种溶液 分别逐滴滴加稀盐酸,观察现象
2 3 3
C 鉴别NaCO、BaCl 、NaCl溶液 分别加入稀HSO ,观察现象
2 3 2 2 4
先加稀盐酸无明显现象,再加BaCl 溶液,观察
D 检验溶液中是否有SO 2
是否有沉淀
4.下列有关实验的操作正确的是( )
A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有0刻度:它们使
用时均需水洗后再润洗
B.为观察Mg条在CO 气体中的燃烧,在一个底部铺有少量沙子的集气瓶中收集满CO 气体,取一
2 2
小段除去表面氧化膜的Mg条用坩埚钳夹持伸入集气瓶中燃烧
C.检验某溶液是否含有 时,应取少量该溶液,依次加入 溶液和稀硝酸
D.用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在桌面的 试纸上测 值
5.实验是解决化学问题的基本途径。下列对于某些离子的检验及结论正确的是( )
A.向某溶液中加入BaCl 溶液,有白色沉淀生成,则溶液中一定含SO
2
B.用铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色,则溶液中一定含Na+无K+
C.向溶液中滴加KSCN溶液,溶液无明显变化,溶液中一定不含Fe3+D.向某溶液中加入足量稀盐酸,有能使澄清石灰水变浑独的气体生成,则溶液中一定含CO
6.某工业废水中存在大量的Na+、Cl-、Cu2+、SO ,欲除去其中的Cu2+、SO ,设计工艺流程如图
所示:
下列有关说法错误的是 ( )
A.NaOH的作用是除去Cu2+
B.试剂a为NaCO,试剂b为BaCl
2 3 2
C.操作x为过滤,试剂c为稀盐酸
D.检验SO 是否除尽可取适量待测溶液,先加入盐酸,再加入BaCl 溶液
2
7.食盐是日常生活中的必需品。粗盐中常含有少量泥沙以及Mg2+、Ca2+、SO ,某兴趣小组用稀盐
酸、氢氧化钠、碳酸钠、氧化钡等试剂,设计了如下的精制的方案。下列说法中不正确的是( )
A.试剂①、②、③依次是氢氧化钠、碳酸钠、氧化钡
B.操作Ⅰ是过滤,操作Ⅱ是蒸发结晶
C.除去Mg2+的反应为:Mg2++2OH-=Mg(OH) ↓
2
D.加入盐酸发生的反应只有OH-+H+=H O
2
8.某无色溶液中可能含有Mg2+、Cu2+、Ba2+、CO、Cl-、SO、NO中的几种,现进行如下实验:
Ⅰ.取适量溶液,加入足量NaOH溶液,生成白色沉淀。
Ⅱ.过滤,向实验Ⅰ所得的滤液中加入足量HSO 溶液,有白色沉淀生成。根据上述实验回答下列问
2 4
题。
(1)溶液中一定不存在的离子是_______;
(2)写出Ⅰ和Ⅱ中所发生反应的离子方程式_______、_______;
III.“生活无处不化学”,请你回答下列问题。
(3)小苏打可以治疗胃酸过多,用离子方程式表示其原理___________。
(4)食盐的精制,需要将粗盐中含有的SO、Mg2+、Ca2+离子沉淀除去,进行提纯,下列加入试剂的顺序
不可行的是___________。
A.BaCl 溶液→NaOH溶液→NaCO 溶液→过滤→盐酸Ⅲ
2 2 3B.NaOH溶液→NaCO 溶液→BaCl 溶液→过滤→盐酸
2 3 2
C.NaOH溶液→BaCl 溶液→NaCO 溶液→过滤→盐酸
2 2 3
D.BaCl 溶液→NaCO 溶液→NaOH溶液→过滤→盐酸
2 2 3