文档内容
第五章 化工生产中的重要非金属元素
第一节 硫及其化合物 课时作业
第三课时 硫酸根离子的检验 粗盐的提纯
基础达标
1.下列物质的俗称、化学式、主要用途都正确的是( )
A.生石膏(2CaSO·H O):用于制造各种模型
4 2
B.纯碱(NaHCO ):用于制玻璃、肥皂、造纸、纺织
3
C.硫酸钡(BaSO):作白色颜料、钡餐
4
D.胆矾(CuSO ):用于制造农药
4
【答案】C
【解析】A.生石膏化学式CaSO·2H O,用于制造各种模型,A错误;B.纯碱化学式为NaCO,用
4 2 2 3
于制玻璃、肥皂、造纸、纺织,B错误;C.硫酸钡(BaSO)是白色固体,不溶于水,不溶于酸,可做作白
4
色颜料、钡餐,C正确;D.胆矾化学式为CuSO ·5H O,用于制造农药,D错误;故答案选C。
4 2
2.下列实验,能证明溶液中一定含有SO的是( )
A.某溶液加入BaCl 溶液,产生白色沉淀
2
B.某溶液加入BaCl 溶液,产生白色沉淀,再加盐酸沉淀不溶解
2
C.某溶液加入硝酸酸化,再加入Ba(NO ) 溶液有白色沉淀产生
3 2
D.某溶液加入盐酸酸化,再加入BaCl 溶液有白色沉淀产生
2
【答案】D
【解析】能和氯化钡溶液产生白色沉淀的离子有 Ag+、SO、CO、SO等,A项错误。能和氯化钡溶液
产生不溶于稀盐酸白色沉淀的离子有Ag+、SO等,B项错误。硝酸具有强氧化性,能将亚硫酸根离子氧化
生成硫酸根离子,所以不能确定原溶液中是否含有硫酸根离子,C项错误。先加盐酸酸化,能排除Ag+、
SO、CO的干扰,再加氯化钡溶液产生白色沉淀说明含有硫酸根离子,D项正确。
3.化学与职业息息相关,下列化学职业有关说法不正确的是( )
A.科技考古人员在研究文物和古迹时,可利用 的测定分析古代人类的食物结构
B.测试工程师可运用各类高精度化学检测仪器或化学检测方法,以获得金属材料的组成及含量
C.化学科研工作者可从事特定功能新分子合成、安全高效和节能环保物质转化工艺的研发等
D.水质检测员需要在自来水出厂前,需要对其中的CO、Cl-放射性物质、微生物和有机物等进行检
测
【答案】A【解析】A.科技考古研究人员是根据放射性同位素的半衰期推算文物的年代,放射性同位素被考古
学家称为“碳钟”,它可以用来断定文物的年代, A错误;B.测试工程师可运用各类高精度化学检测仪
器或化学检测方法,测定某些组成元素及其含量,以获得金属材料的组成及含量,B正确;C.特定功能
新分子合成、节能环保物质转化工艺的研发都属于化学前沿科学,化学科研工作者可从事特定功能新分子
合成、节能环保物质转化工艺的研发等,C正确;D.自来水厂水质检验员的工作是在自来水出厂前,利
用化学分析仪器对水中的硫酸根离子、氯离子、微生物、有机物等进行检测和分析,只有达到标准才可以
让自来水出厂,D正确; 故选A。
4.某同学进行了如图所示的实验,由实验现象得到的结论中正确的是( )
A.原溶液中一定只含有SO B.原溶液中一定含有SO和Cl-
C.原溶液中一定只含有Cl- D.原溶液中可能含有SO,也可能含有Cl-
【答案】D
【解析】能够与氯化钡反应生成不溶于稀盐酸的沉淀的离子有 SO或Ag+,由于步骤①中加入氯化钡
溶液,引进了Cl-,步骤③也无法确定是否存在氯离子,所以无法确定原溶液中一定存在的离子。
5.除去下列物质中的杂质(括号内为杂质),选择试剂及操作方法均正确的是( )
A.Cl(HCl气体):通过足量的NaOH溶液
2
B.FeCl 溶液(FeCl ):通入适量Cl
3 2 2
C.Fe O(AlO),HCl溶液,过滤
2 3 2 3
D.CO(HCl):通过盛有饱和NaCO 溶液的洗气瓶
2 2 3
【答案】B
【解析】A.Cl、HCl都能与NaOH溶液反应,不能用氢氧化钠溶液除氯气中的氯化氢,一般用饱和
2
食盐水除氯气中的氯化氢,故A错误;B.FeCl 和Cl 反应生成FeCl ,用氯气除FeCl 溶液中的FeCl ,故
2 2 3 3 2
B正确;C.Fe O、Al O 都能溶液HCl溶液,故C错误;D.CO、HCl都能和饱和NaCO 溶液反应,一
2 3 2 3 2 2 3
般用饱和NaHCO 溶液除CO 中的HCl,故D错误;选B。
3 2
6.下列叙述正确的是( )
A.“钡餐”是医疗上做消化系统X射线检查的内服药剂,其主要成分是BaSO
3
B.向某溶液中加入BaCl ,产生不溶于稀HNO 的白色沉淀,则溶液中一定含有SO
2 3
C.用浓硫酸在纸上书写的字迹变黑,体现浓硫酸的氧化性
D.浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
【答案】D
【解析】“钡餐”的主要成分是BaSO ,故A错误;由于AgCl也是不溶于稀硝酸的白色沉淀,且
4BaSO 能被稀硝酸氧化为BaSO ,故向某溶液中加入BaCl ,产生不溶于稀HNO 的白色沉淀,则溶液中不
3 4 2 3
一定含有SO,也可能含有Ag+或者SO,B错误;用浓硫酸在纸上书写的字迹变黑,体现浓硫酸的脱水
性,C错误;浓硫酸具有吸水性、浓盐酸具有挥发性,两者在空气中敞口放置时浓度均减小,D正确。
7.下列物质的检验中,其结论一定正确的是( )
A.向某溶液中加入BaCl 溶液,产生白色沉淀,加入稀HNO 后,白色沉淀不溶解,也无其他现象,
2 3
说明原溶液中一定含有SO
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清石灰水变浑浊,说明该溶液中一定含有 CO
或SO
C.取少量久置的NaSO 样品于试管中加水溶解,再加足量盐酸酸化,然后加BaCl 溶液,若加盐酸
2 3 2
时有气体产生,加BaCl 溶液时有白色沉淀产生,说明NaSO 样品已部分被氧化
2 2 3
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO
2
【答案】C
【解析】该溶液中还可能含有Ag+或SO,A错误;使澄清石灰水变浑浊的气体可能为CO 、SO ,溶
2 2
液中可能存在CO、HCO、SO或HSO,B错误;加入足量盐酸有气体产生,气体为SO ,排除SO的干
2
扰,再加入BaCl 溶液有白色沉淀产生,沉淀为BaSO,说明一定含有SO,所以说明NaSO 样品已部分被
2 4 2 3
氧化,C正确;氧化性气体如氯气等都能使品红溶液褪色,D错误。
8.仅用下列方法或试剂不能达到鉴别离子目的的是( )
选项 离子 方法或试剂
A Na+、K+ 焰色试验
B SO、SO 稀硝酸、氯化钡溶液
C Fe2+、Fe3+ HO 溶液、KSCN溶液
2 2
D SiO2-、AlO- 稀盐酸
3 2
【答案】B
【解析】A.钠的焰色反应呈现黄色,钾的焰色反应呈现紫色(通过蓝色钴玻璃观察),故通过焰色反应
能够鉴别Na+和K+,A不合题意;B.SO与SO都能与BaCl2溶液反应分别转化为BaSO 、BaSO 白色沉
3 4
淀,且BaSO 能被硝酸氧化为BaSO ,故含有SO、SO的溶液中分别加入稀硝酸、氯化钡溶液现象相同,
3 4
不能鉴别,B符合题意;C.含有Fe3+的溶液中滴加KSCN溶液,可观察到溶液立即变为血红色,而含有
Fe2+的溶液中滴加KSCN溶液,无明显现象,滴加HO 后溶液立即变为血红色,即用HO 溶液、KSCN溶
2 2 2 2
液可以鉴别Fe2+、Fe3+,C不合题意;D.往含有SiO2-的溶液中滴加稀盐酸至过量,可观察到生成白色
3
沉淀,且沉淀不溶解,而向含有AlO-的溶液中滴加稀盐酸至过量,可观察到先生成白色沉淀,至最多,而
2
后沉淀又逐渐减少直至消失,可有稀盐酸来鉴别SiO2-、AlO-,D不合题意;故答案为:B。
3 2
9.某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、
Cu2+、Ag+、Ca2+、CO、SO、Cl-中的若干种离子。该小组同学取部分水样进行实验,向水样中先滴加足量
硝酸钡溶液,产生白色沉淀;再滴加足量稀盐酸,沉淀部分溶解;最后滴加硝酸银溶液,又产生白色沉淀。下列说法正确的是( )
A.观察水样可以确定一定不存在的离子只有Cu2+
B.经过实验可以确定一定存在的离子是K+、CO、SO、Cl-
C.水样中可能存在Cl-
D.水样中可能存在K+
【答案】C
【解析】某无色水样,则不含有Cu2+、Fe3+,向水样中先滴加足量硝酸钡溶液,产生白色沉淀,则含
有CO 、SO中的一种或两种;再滴加足量稀盐酸,沉淀部分溶解,则CO 、SO均存在;故不存在Mg2+、
Ag+、Ca2+,根据溶液电中性,则一定含有一种阳离子K+,最后滴加硝酸银溶液,又产生白色沉淀,该白
色沉淀为氯化银,则氯离子可能来自于前面所加盐酸而不一定是原溶液的,故不能确定原溶液中是否含有
Cl-。A.因水样无色,则观察水样可以确定一定不存在的离子有Cu2+、Fe3+,选项A错误;B.经过实验
可以确定一定存在的离子是K+、CO 、SO,不能确定是否有Cl-,选项B错误;C.滴加硝酸银溶液之前
加了盐酸,引入了Cl-,所以无法确定水样中是否含有Cl-,选项C正确;D.水样中一定存在K+,选项D
错误。答案选C。
10.从海水所得的粗盐中含有杂质Mg2+、SO、Ca2+,除去粗盐中的杂质加入药品顺序正确的是
( )
A. 溶液 溶液 溶液 过滤后加盐酸
B.BaCl 溶液 溶液 溶液 过滤后加盐酸
2
C. 溶液 溶液 溶液 过滤后加硫酸
D. 溶液 溶液 溶液 过滤后加盐酸
【答案】B
【解析】粗盐中含有杂质Mg2+常用NaOH溶液除掉,SO常用BaCl 溶液除掉、Ca2+常用NaCO 溶液
2 2 3
除掉,除杂时要将杂质离子尽量除尽,则加入的试剂要过量,由于过量会引入新的杂质,因此后面加入的
试剂要将前面的过量杂质也要除尽即钡离子要用碳酸根除掉,因此BaCl 溶液要加在NaCO 溶液前面,碳
2 2 3
酸钠不仅除掉钙离子,还除掉多余的钡离子,沉淀完离子后先过滤,多余的碳酸钠、氢氧化钠加入盐酸来
除掉,因此加入顺序为BaCl 溶液→NaOH溶液→NaCO 溶液→过滤后加盐酸,故B正确。综上所述,答案
2 2 3
为B。能 力 提 升
11.某企业利用下列流程综合处理工厂排放的含有SO 的烟气,以减少其对环境造成的污染。下列有
2
关说法正确的是( )
A.二氧化硫吸收塔中发生的反应为SO +SO+H O==2HSO
2 2
B.氨气吸收塔中发生的反应为
C.上述流程利用的是氧化还原反应原理
D.上述流程体现出NH HSO 可循环利用
4 3
【答案】A
【解析】A.由分析可知,二氧化硫吸收塔中发生的反应为(NH )SO +SO+H O=2NH HSO ,离子方
4 2 3 2 2 4 3
程式为SO +SO+H O==2HSO,A正确;B.氨气吸收塔中发生的反应为NH HSO +NH=(NH)SO ,离子方
2 2 4 3 3 4 2 3
程式为HSO+NH==NH ++SO,B不正确;C.上述流程中,没有元素的化合价发生变化,利用的是非氧化
3 4
还原反应原理,C不正确;D.上述流程中,首先进入二氧化硫吸收塔的是(NH )SO ,所以(NH )SO 可循
4 2 3 4 2 3
环利用,D不正确;故选A。
12.关于某溶液中所含离子的检验,下列判断正确的是( )
A.加入BaCl 溶液生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含有SO
2
B.加入AgNO 溶液生成白色沉淀,则原溶液中一定含有Cl﹣
3
C.加入KSCN溶液时,溶液不变红色,再滴入氯水溶液变为红色,则原溶液中一定含有Fe2+
D.加入盐酸,生成的气体能使成清石灰水变浑浊,则原溶液中一定含有CO
【答案】C
【解析】A.SO能被硝酸氧化为SO,亚硫酸根离子存在可能生成不溶于硝酸的白色沉淀,并且不能
排除Ag+的干扰,氯离子和银离子反应生成不溶于硝酸的氯化银白色沉淀,故A错误;B.Ag SO 、
2 4
Ag CO 等都是白色沉淀,加入AgNO 溶液生成白色沉淀,则原溶液中不一定含有Cl﹣,故B错误;C.
2 3 3
向某溶液中加入2滴KSCN溶液,溶液不显红色,一定不含有三价铁离子,再向溶液中滴几滴新制的氯
水,溶液变为红色,该溶液中一定含有Fe2+,故C正确;D.加入盐酸若有能使澄清石灰水变浑浊的气体生成,该气体可能为二氧化硫或二氧化碳,原溶液中可能含有SO 、HCO、HSO等离子,不一定含有
CO,故D错误;故选C。
13.粗食盐水中常含有少量Ca2+、Mg2+、SO杂质离子,实验室提纯粗食盐水制取食盐的流程如下,关
于实验过程中所选用的试剂、目的及所发生反应的离子方程式均正确的是( )
选项 试剂 目的 离子方程式
A KOH溶液 仅除去Mg2+ Mg2++2OH-=Mg(OH) ↓
2
B BaCl 溶液 仅除去 Ba2++Na SO =BaSO ↓+2Na+
2 2 4 4
C NaCO 溶液 仅除去Ca2+ Ca2++CO=CaCO ↓
2 3 3
H++OH-=H O
2
D 盐酸 除去OH-和CO
2H++CO=CO ↑+H O
2 2
【答案】D
【解析】A.除去NaCl溶液中的Mg2+,应该用NaOH,不能用KOH,故A错误;B.加入BaCl 溶液
2
除去SO的离子方程式是Ba2++SO=BaSO ↓,故B错误;C.加入NaCO 溶液的目的是除去Ca2+、Ba2+,故
4 2 3
C错误;D.加入盐酸的目的是除去过量的NaOH、NaCO,反应的离子方程式是H++OH-=H O、2H+
2 3 2
+CO=CO ↑+H O,故D正确;选D。
2 2
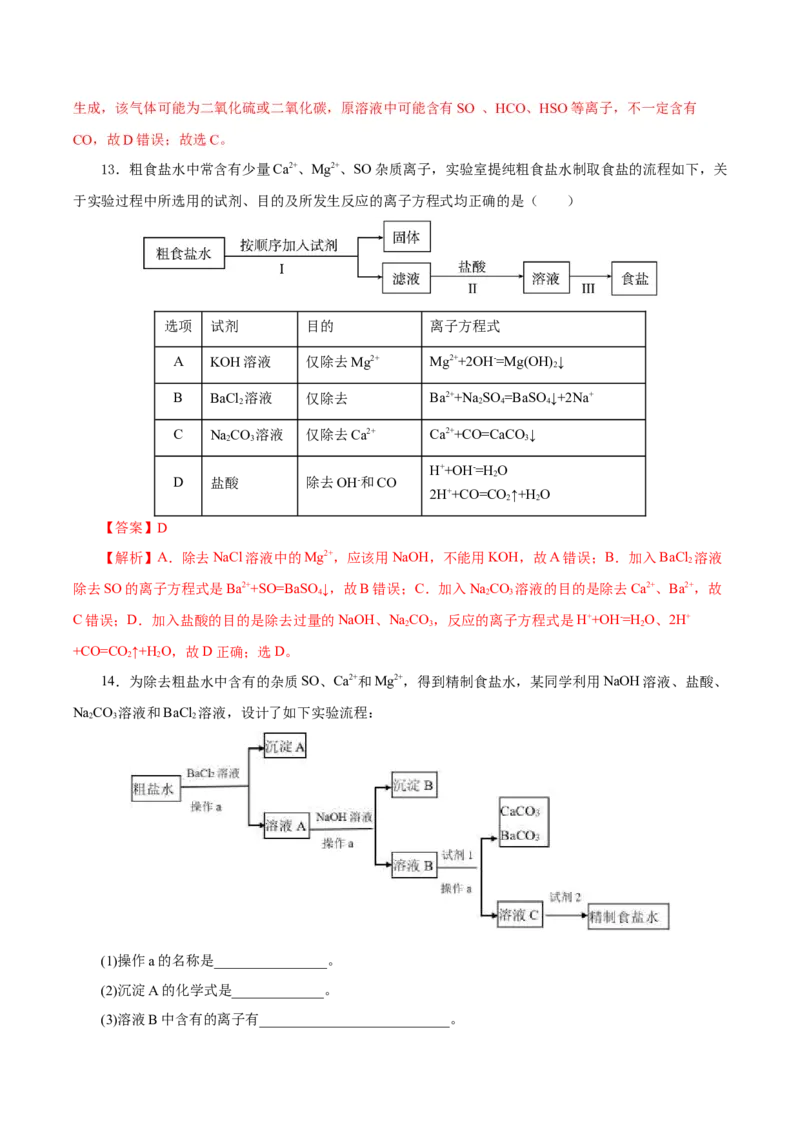
14.为除去粗盐水中含有的杂质SO、Ca2+和Mg2+,得到精制食盐水,某同学利用NaOH溶液、盐酸、
NaCO 溶液和BaCl 溶液,设计了如下实验流程:
2 3 2
(1)操作a的名称是________________。
(2)沉淀A的化学式是_____________。
(3)溶液B中含有的离子有___________________________。(4)写出试剂2参与反应的离子方程式_______________________________________________。
(5)某小组认为也可以选用Ba(OH) 溶液作为除杂试剂,若采用此方案,加入试剂的顺序依次为:
2
_____________________________________。
【答案】 过滤 BaSO Ba2+、Cl-、Ca2+、Na+、OH- CO +2H+=H O+CO↑,OH-
4 2 2
+H+=H O Ba(OH) 、NaCO、盐酸
2 2 2 3
【解析】为除去粗盐水中含有的杂质SO、Ca2+和Mg2+,得到精制食盐水,在粗盐水中加入氯化钡,经
过过滤生成硫酸钡沉淀A和溶液A,在溶液A中加入氢氧化钠,生成氢氧化镁沉淀和溶液B,在溶液B中
加入碳酸钠生成碳酸钡和碳酸钙,经过滤得到溶液C,在溶液C中加入盐酸得到精制食盐,以此分析解
答;
(1)由上述分析可知,操作a为过滤,故答案为:过滤;
(2)由上述分析知,沉淀A为硫酸钡,其化学式为BaSO,故答案为:BaSO;
4 4
(3)粗食盐水中含有杂质SO、Ca2+和Mg2+,加入氯化钡以后除去了SO,溶液A中含有Ba2+、Cl-、
Ca2+、Na+、Mg2+,加入氢氧化钠溶液以后除去了Mg2+得到溶液B,溶液B中含有的离子为Ba2+、Cl-、
Ca2+、Na+、OH-,故答案为:Ba2+、Cl-、Ca2+、Na+、OH-;
(4) 试剂2为盐酸,可以与溶液C中的碳酸根和氢氧根反应,其离子方程式为 CO +2H+=H O+CO↑,
2 2
OH-+H+=H O,故答案为: CO +2H+=H O+CO↑,OH-+H+=H O;
2 2 2 2
(5) 首先在粗盐水中加入氢氧化钡,可以除去硫酸根离子和镁离子,溶液中存在的离子有Ba2+、Cl-、
Ca2+、Na+、OH-,然后加入碳酸钠除去Ba2+和Ca2+,最后加入盐酸除去 CO 和OH-,得到精制食盐,故答
案为:Ba(OH) 、NaCO、盐酸。
2 2 3
直击高考
15.根据下列实验操作和现象所得到的结论不正确的是( )
选项 实验操作和现象 结论
A 向某溶液中滴加BaCl 溶液,产生白色沉淀 该溶液中一定含有SO
2
将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜
B 色相同时,再用铂丝蘸取少量待测溶液进行焰色试验, 该溶液中含有Na+
火焰呈黄色
向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉
C Br 的氧化性比Ⅰ 强
溶液,溶液显蓝色 2 2
D 将新制的Al(OH) 3 沉淀分装在两支试管中,向一支试管中 Al(OH) 3 是两性氢氧化物滴加2mol/L盐酸,另一支试管中滴加2mol/LNaOH溶
液,沉淀均溶解
A.A B.B C.C D.D
【答案】A
【解析】A.由于AgCl、BaCO 、BaSO 均为白色沉淀,故向某溶液中滴加BaCl 溶液,产生白色沉
3 3 2
淀,不能说明该溶液中一定含有SO的结论,A符合题意;B.将铂丝用盐酸洗净后,在外焰上灼烧至与原
来的火焰颜色相同时,再用铂丝蘸取少量待测溶液进行焰色试验,火焰呈黄色,说明该溶液中含有Na+,B
不合题意;C.向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色,说明有I 生
2
成,即发生2KI+Br =2KBr+I ,故能得出Br 的氧化性比Ⅰ 强的结论,C不合题意;D.将新制的Al(OH)
2 2 2 2 3
沉淀分装在两支试管中,向一支试管中滴加2mol/L盐酸,另一支试管中滴加2mol/LNaOH溶液,沉淀均溶
解,说明Al(OH) 既能与强酸反应,也能与强碱反应,故可得出Al(OH) 是两性氢氧化物的结论,D不合题
3 3
意;故答案为:A。
16.某同学为了验证Fe3+是否能将HSO 氧化成SO,用50mL0.1mol∙L-1FeCl 溶液吸收制取SO 气体的
2 3 3 2
尾气后,进行以下实验:
(1)取少量样品溶液于试管中,先滴入足量的稀盐酸,再滴入氯化钡溶液,如果有白色沉淀生成,由此
证据可证明Fe3+能够把HSO 氧化成______________________。
2 3
(2)由此可写出该反应的化学方程式为_______________________________________,反应中的氧化产
物是___________________________(写化学式)。
(3)该同学为了探究吸收液中其他成分(Fe3+、Fe2+、HSO )的可能组合进行了以下探究:
2 3
①提出假设。
假设1:溶液中存在Fe2+。
假设2:溶液中存在Fe3+、Fe2+。
假设3:溶液中存在____________。
②设计方案,进行实险,验证假设。请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂
和仪器:试管、滴管、0.1mol∙L-1KMnO 溶液、0.1mol∙L-1KSCN溶液、品红稀溶液。
4
已知:HSO 可使品红溶液由红色变为无色。
2 3
实验步骤 预期现象和结论
若出现红色,则假设2成立,假设1、3不
步骤1:用试管取样品溶液2~
成立;若未出现红色,则假设2不成立,假设1
3mL,并滴入_________________
或3成立
步骤2:_______________________
______________________________________
__________________________________
_ _____________________________________
_
【答案】(1)SO或HSO
2 4
(2) 2FeCl +SO+2H O=2FeCl +H SO +2HCl HSO
3 2 2 2 2 4 2 4
(3) Fe2+、HSO 1~2滴0.1mol∙L-1KSCN溶液 另取2~3mL样品溶液于试管中,滴入
2 3
1~2mL (或少量)品红稀溶液 若品红稀溶液红色褪去,则假设3成立;若品红稀溶液红色不褪去,
则假设3不成立,假设1或假设2成立
【解析】因为用Fe3+氧化HSO ,则生成Fe2+和SO,溶液中Fe2+一定存在;若存在Fe3+,则不存在
2 3
HSO ;若不存在Fe3+,则可能存在HSO 。
2 3 2 3
(1)判断Fe3+能否将H2SO3氧化成SO,只需检验反应后的溶液中是否含有SO,方法是:取少量样
品溶液于试管中,先滴入足量的稀盐酸,再滴入氯化钡溶液,如果有白色沉淀生成,由此证据可证明
Fe3+能够把HSO 氧化成SO或HSO 。
2 3 2 4
(2)FeCl 溶液将SO2氧化为HSO ,自身被还原为FeCl 等,该反应的化学方程式为
3 2 4 2
2FeCl +SO+2H O=2FeCl +H SO +2HCl,反应中SO 是还原剂,则氧化产物是HSO 。
3 2 2 2 2 4 2 2 4
(3)①三种情况下溶液中都一定存在Fe2+,但由于Fe3+与HSO 不共存,所以有Fe3+就不存在
2 3
HSO ,有HSO 就不存在Fe3+。
2 3 2 3
则假设3:溶液中存在Fe2+、HSO 。
2 3
②
实验步骤 预期现象和结论
步骤1:检验Fe3+时,需使用硫氰化 若出现红色,则假设2成立,假设1、3不成
钾溶液,所以需滴入1~2滴 立;若未出现红色,则假设2不成立,假设1或3
0.1mol∙L-1KSCN溶液 成立
步骤2:检验HSO 时,需使用品 若品红稀溶液红色褪去,则含有HSO ,假
2 3 2 3
红,所以:另取2~3mL样品溶液于试管 设3成立;若品红稀溶液红色不褪去,则不含有
中,滴入1~2mL (或少量)品红稀溶液 HSO ,假设3不成立,假设1或假设2成立
2 3
另取2~3mL样品溶液于试管中,滴入1~2mL (或少量)品红稀溶液;若品红稀溶液红色褪去,则假设3
成立;若品红稀溶液红色不褪去,则假设3不成立,假设1或假设2成立。