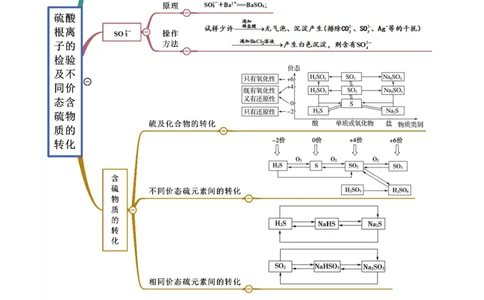
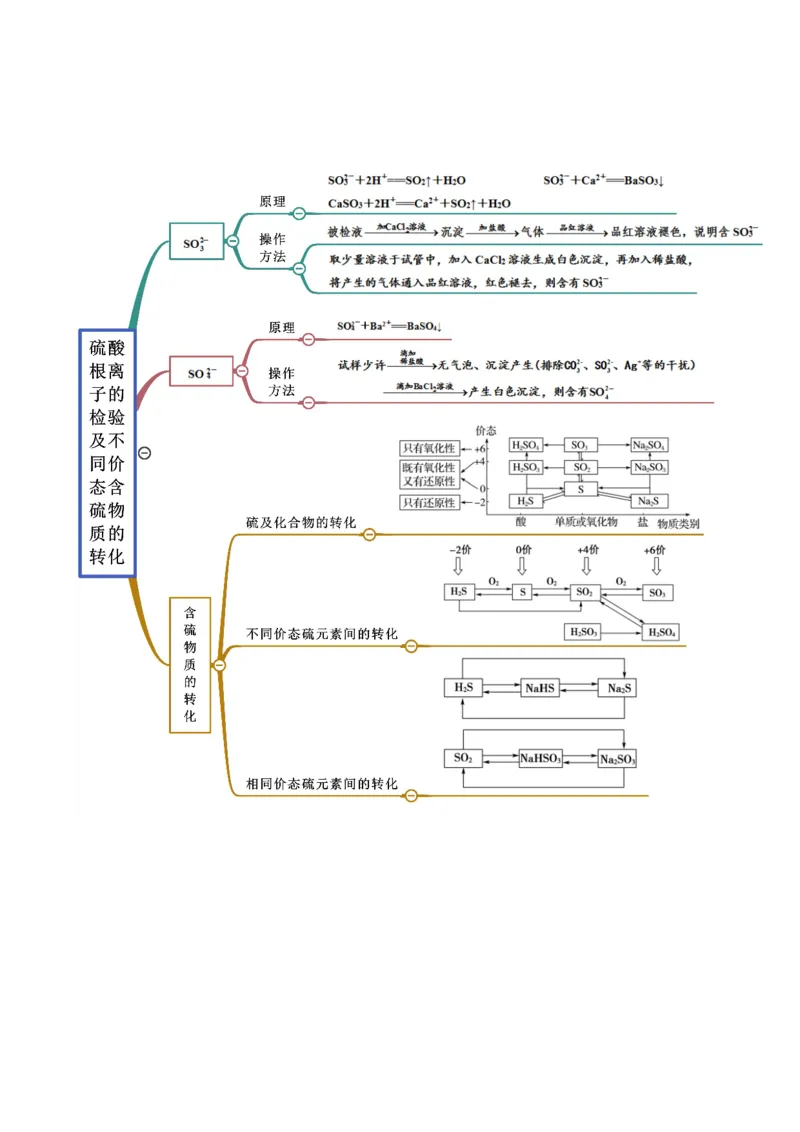
文档内容
5.1.2 硫及其化合物(精讲)
思维导图常见考点
考点一 硫酸
【例1-1】(2021·天津二中高一期中)下列有关浓硫酸的叙述正确的是( )
①浓硫酸在常温下能够使用铁或铝制容器盛装
②浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
③浓硫酸具有吸水性,因而能使蔗糖炭化
④浓硫酸与铜加热反应后,铜片有剩余,向反应后的溶液中再加入铁片,会有氢气生成
⑤浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
⑥浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外只有SO
2
⑦浓硫酸具有强氧化性,常温下能与Cu发生剧烈反应
⑧浓硫酸具有强氧化性,SO 具有还原性,所以浓硫酸不能干燥SO
2 2
⑨向5mL18mol·L-1的浓硫酸中加入足量Cu并加热使其充分反应,被还原的HSO 和生成的SO 气体均小
2 4 2
于0.045mol
A.①④⑨ B.①②⑤ C.⑥⑦⑧ D.③④⑨
【答案】A
【解析】①铁或铝在常温下遇浓硫酸发生钝化,浓硫酸不能进一步与铝或铁反应,因此能够使用铁或铝制
容器盛装浓硫酸,①正确;
②浓硫酸与铜加热反应后发生反应,2HSO (浓)+Cu CuSO +SO↑+2H O,硫酸变稀后不再与Cu反应,
2 4 4 2 2
因此硫酸不能完全反应,②错误;
③浓硫酸具有脱水性,因而能使蔗糖炭化,③错误;
④浓硫酸与铜加热反应后,根据②的分析,铜片有剩余,且还有稀硫酸存在,向反应后的溶液中再加入铁
片,发生反应HSO +Fe=FeSO +H ↑,因此会有氢气生成,④正确;
2 4 4 2⑤浓硫酸与氨气反应,不能干燥氨气,⑤错误;
⑥浓硫酸与铁加热反应生成SO ,6HSO (浓)+2Fe Fe (SO )+3SO↑+6H O,铁片有剩余说明铁过量,硫
2 2 4 2 4 3 2 2
酸变稀后还会与Fe反应生成H,因此生成的气体除水蒸气外还有SO 和H,⑥错误;
2 2 2
⑦浓硫酸具有强氧化性,但常温与Cu反应很慢,加热反应的较快,⑦错误;
⑧HSO 的S为+6价, SO 的S为+4价,S没有中间价+5价,因此二者不会发生氧化还原反应,可以用
2 4 2
浓硫酸干燥SO ,⑧错误;
2
⑨浓硫酸的物质的量为0.005L×18mol·L-1=0.09mol,由于浓硫酸变稀后不能与Cu继续反应,根据物质的量
之比等于化学计量数之比,被还原的HSO 和生成的SO 气体均小于0.045mol,⑨正确;
2 4 2
综上所述,①④⑨正确,故选A。
【例1-2】(2021·北京延庆·高一期中)下列反应中,不属于HSO 类别通性的是( )
2 4
A.C+2H SO (浓) CO↑+SO↑+2H O
2 4 2 2 2
B.HSO +2NaOH=Na SO +2H O
2 4 2 4 2
C.HSO +CuO=CuSO +H O
2 4 4 2
D.HSO +Na CO=Na SO +CO ↑+H O
2 4 2 3 2 4 2 2
【答案】A
【解析】A.C+2H SO (浓) CO↑+SO↑+2H O中S的化合价降低,体现强氧化性,不是酸的通性,A符合
2 4 2 2 2
题意;
B.HSO +2NaOH=Na SO +2H O,属于中和反应,属于酸的通性,B不符题意;
2 4 2 4 2
C.HSO +CuO=CuSO +H O,硫酸和碱性氧化物反应生成盐和水,属于酸的通性,C不符题意;
2 4 4 2
D.HSO +Na CO=Na SO +CO ↑+H O,硫酸与碳酸盐反应生成盐和较弱的酸,属于酸的通性,D不符题
2 4 2 3 2 4 2 2
意;
选A。
【例1-3】(2021·浙江·高一月考)硫酸是重要的化工原料,可用于生产化肥、农药、炸药等,工业上一般
以硫磺或其他含硫矿物如黄铁矿(主要成分 )为原料制备硫酸,其制备原理示意图如下。下列说法不正
确的是A.用黄铁矿燃烧生成 的化学方程式为
B. 氧化成 时,加催化剂能使 全部转化为
C.用98.3%的浓硫酸吸收 ,目的是防止形成酸雾,以使 吸收完全
D.为减少 对大气的污染,可选用CaO做固硫剂把尾气中的 以盐的形式固定
【答案】B
【解析】A.用黄铁矿燃烧生成 的同时,还能生成铁的氧化物,故其燃烧的化学方程式是
,故A说法正确;
B. 氧化成 时,其反应是个可逆反应,加催化剂只是改变反应速率,并不能提高转化率,另外可
逆反应的转化不可能是全部,故B说法不正确;
C.吸收 不能用水,用水会生成酸雾,会阻碍 的吸收,故工业制硫酸用98.3%的浓硫酸吸收 ,
目的是防止形成酸雾,以使 吸收完全,则C说法正确;
D.为减少 对大气的污染,可选用CaO与 反应生成亚硫酸钙,然后亚硫酸钙被氧化成硫酸钙,故
D说法正确;本题答案B。
【一隅三反】
1.(2021·重庆·西南大学附中高一月考)利用如图所示装置进行下列实验,能达到实验目的的是 ()
选项 ① ② ③ 实验结论验证浓硫酸具有强氧化
A 浓硫酸 Cu 溴水
性
酸性高锰酸钾溶
B 浓硫酸 NaSO 验证SO 的漂白性
2 3 液 2
C 稀硫酸 Zn 空气 制取并收集H
2
D 稀硫酸 NaCO 澄清石灰水 验证非金属性:S > C
2 3
A.A B.B C.C D.D
【答案】D
【解析】A.铜与浓硫酸反应需要加热,常温下不发生反应,也就不能产生二氧化硫,故A错误;
B.浓硫酸与亚硫酸钠混合反应生成二氧化硫, 二氧化硫能够把酸性高锰酸钾还原为锰离子,溶液变为无
色,体现了二氧化硫的还原性而非漂白性,故B错误;
C.稀硫酸与锌反应产生氢气,氢气的密度小于空气,采用向下排空气法收集,即③号试管中进气管要短,
出气管要长,故C错误;
D.稀硫酸与碳酸钠反应生成二氧化碳气体,二氧化碳能够使澄清的石灰水变浑浊,体现了强酸制备弱酸
的规律;由于碳酸、硫酸分别是碳、硫元素的最高价含氧酸,所以可以验证非金属性:S > C,故D正确;
故选D。
2.(2021·四川南充·高一期末)下列关于浓硫酸的说法中,正确的是( )
A.浓硫酸使干燥的木条炭化,体现其吸水性
B.浓硫酸与金属反应生成的一般是H
2
C.浓硫酸可以用来干燥HCl、NH 、HS等气体
3 2
D.浓硫酸与铜共热的反应中,浓硫酸既表现出强氧化性,又表现出酸性
【答案】D
【解析】A. 浓硫酸使干燥的木条炭化,体现其脱水性,故A错误;
B. 浓硫酸有强氧化性与金属反应生成的一般是SO ,故B错误;
2
C. 浓硫酸可以用来干燥HCl,不能干燥碱性气体NH 、还原性气体HS等气体,故C错误;
3 2
D. 浓硫酸与铜共热的反应中,浓硫酸既表现出强氧化性,生成二氧化硫,又表现出酸性,生成硫酸铜,
故D正确;
故选D。
3(2021·江苏南通·高一期末)硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类。我国
工业上一般以黄铁矿为原料来制备硫酸。工业制硫酸涉及到下列反应:① ;② ;③ 。
生产中用浓硫酸代替水吸收 ,制得发烟硫酸( ),将发烟硫酸稀释后可制得密度为
、质量分数为 的浓硫酸。下列有关硫及其化合物的性质与用途具有对应关系的是( )
A.硫具有还原性,可用硫黄处理洒落的汞单质
B.二氧化硫具有氧化性,可用作葡萄酒的抗氧化剂
C.稀硫酸具有酸性,可用于去除铁锈
D.浓硫酸具有脱水性,可用于干燥二氧化硫
【答案】C
【解析】A. 可用硫磺处理洒落的汞单质,是利用其氧化性,故A错误;
B. SO 可用作葡萄酒的抗氧化剂,利用了SO 的还原性,故B错误;
2 2
C. 稀硫酸具有酸性,可用于去除铁锈,铁锈主要成分时Fe O,能与酸反应存在因果关系,故C正确;
2 3
D. 浓硫酸具有吸水性,可用于干燥二氧化硫,故D错误;
故选C。
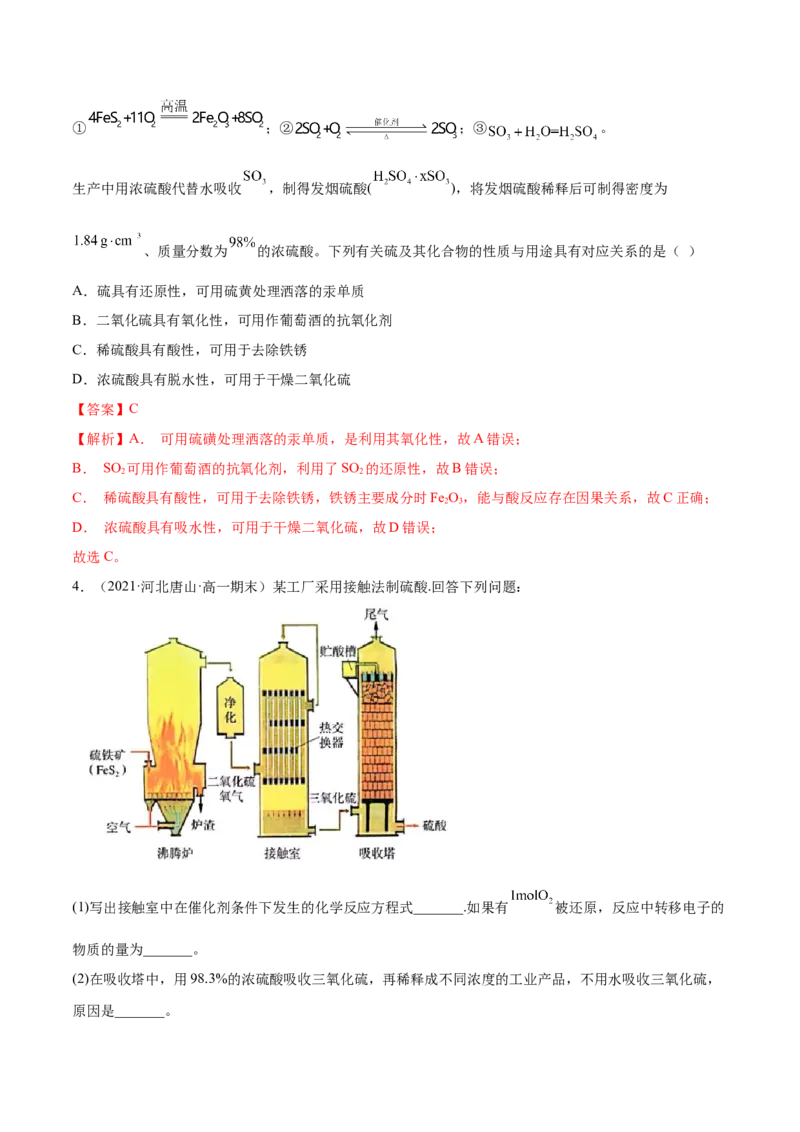
4.(2021·河北唐山·高一期末)某工厂采用接触法制硫酸.回答下列问题:
(1)写出接触室中在催化剂条件下发生的化学反应方程式_______.如果有 被还原,反应中转移电子的
物质的量为_______。
(2)在吸收塔中,用98.3%的浓硫酸吸收三氧化硫,再稀释成不同浓度的工业产品,不用水吸收三氧化硫,
原因是_______。(3)现采购了一批100吨含 的硫铁矿矿石(杂质不参与反应).已知生产过程中沸腾炉中原料损失
10%,接触室和吸收塔中原料损失4%,则该批硫铁矿可生产98%浓硫酸_______吨(计算结果保留小数点后
一位)。
【答案】(1)
(2)防止三氧化硫溶于水时反应放出大量热导致酸雾,降低吸收效率
(3)129.6
【解析】(1)在接触室中二氧化硫与氧气在催化剂加热的条件下反应生成三氧化硫,反应方程式为:
;O 得电子作氧化剂,发生还原反应,有 被还原时转移电子的物质的量为
2
,故答案为: ;4mol;
(2)在吸收塔中,用98.3%的浓硫酸吸收三氧化硫,再稀释成不同浓度的工业产品,不用水吸收三氧化硫,
原因是防止三氧化硫溶于水时反应放出大量热导致酸雾,降低吸收效率,故答案为:防止三氧化硫溶于水
时反应放出大量热导致酸雾,降低吸收效率;
(3)根据硫原子守恒计算得:
(吨),故答案为:129.6。
考点二 硫酸根离子的检验
【例2】(2021·黑龙江·伊春市友好区第三中学高一期中)检验某溶液中是否含有 时,为防止 、
、 等离子的干扰,下列实验方案比较严密的是
A.先加稀 将溶液酸化,再滴加 溶液,看是否生成白色沉淀
B.先加稀 将溶液酸化,再滴加 溶液,看是否生成白色沉淀
C.向溶液中滴加稀盐酸酸化的 溶液,看是否生成白色沉淀
D.向溶液中滴加稀硝酸酸化的 溶液,看是否生成白色沉淀【答案】A
【解析】银离子、碳酸根离子和亚硫酸根等离子会干扰硫酸根离子的检验,则检验硫酸根离子时,应先加
入稀盐酸酸化使溶液呈酸性,排出银离子、碳酸根离子和亚硫酸根等离子的干扰后,再滴加氯化钡溶液,
若有白色沉淀生成,说明溶液中含有硫酸根离子,若没有白色沉淀生成,说明溶液中不含有硫酸根离子,
故选A。
【一隅三反】
1.(2021·四川省蓬安中学校高一月考)检验某未知溶液中是否含有SO ,下列操作最合理的是( )
A.先加稀HSO 酸化,再加BaCl 溶液 B.加入BaCl 溶液
2 4 2 2
C.加入稀HNO 和BaCl 溶液 D.先用盐酸酸化,再加BaCl 溶液
3 2 2
【答案】D
【解析】A.检验SO ,加稀HSO 酸化,引入了SO ,故A不合理;
2 4
B.直接加入BaCl 溶液,溶液中若有CO ,也会产生白色沉淀,故B不合理;
2
C.加入稀HNO,若溶液中有SO ,HNO 会将其氧化为SO ,加入BaCl 溶液,也会产生白色沉淀,
3 3 2
故C不合理;
D.先用盐酸酸化,可以反应掉溶液中可能存在的CO 、SO ,也可检验溶液中是否存在Ag+,若加入
盐酸,无明显现象,再加BaCl 溶液,生成白色沉淀,可证明未知溶液中含有SO ,故D合理;故选D。
2
2.(2021·湖南师大附中高一期中)某溶液中含有大量的Cl-、CO 、SO 。若只取一次该溶液就能够分
别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加HNO 溶液 ②过滤 ③滴加AgNO 溶液 ④滴加Ba(NO ) 溶液
3 3 3 2
A.①②③④ B.①④②③ C.③②①④ D.④②①③
【答案】B
【解析】检验Cl-可以使用Ag+,检验SO 可以使用Ba2+,检验CO 可以使用H+,而Ag+和Ba2+都可以
与CO 结合成沉淀,所以需先检验CO ,此时可以加入稀硝酸,检验Cl-所用的Ag+可以与SO 结合成微溶于水的硫酸银,所以需先检验SO ,此时可以加入Ba(NO ) 溶液,最后检验Cl-,可以加入AgNO
3 2 3
溶液,为不干扰的Cl-检验,在加入AgNO 溶液之前先过滤,则实验操作顺序:①④②③,答案选B。
3
3.(2021·四川·邻水实验学校高一月考)某溶液可能含有 、 、 中的一种或几种,为确定该溶
液的离子组成,现进行如下实验:①取少量溶液滴加硝酸钡溶液,产生白色沉淀;②然后继续加入稀盐酸
至溶液呈酸性,产生无刺激性气味,且能使澄清石灰水变浑浊的无色气体,白色沉淀部分溶解;③取上层
清液继续滴加硝酸钡溶液至无沉淀时,再滴加硝酸银溶液,产生白色沉淀。根据实验,以下推测不正确的
是()
A.一定有 B.一定有
C.不能确定 是否存在 D.一定存在
【答案】D
【解析】A.由分析可知一定有 ,A正确;
B.由分析可知一定有 ,B正确;
C.由分析可知不能确定 是否存在,C正确;
D.由分析可知不能确定 是否存在,D错误;
选D。
4.(2021·安徽·定远县育才学校高一月考)对于溶液中某些离子的检验及结论一定正确的是()
A.加入足量稀盐酸无沉淀,再加入氯化钡溶液后有白色沉淀产生,一定有SO
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C.无色试液加入NaOH溶液,试管口湿润的红色石蕊试纸未变蓝,结论:试液中无NH
D.无色溶液中加入稀盐酸产生无色气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO
【答案】A
【解析】A.加入足量稀盐酸无现象,可排除 的影响,如再加入氯化钡溶液后有白色沉淀产生,说明含有 ,A正确 ;
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,生成的沉淀也可能为AgCl,如检验 ,
应先加入盐酸酸化,如无现象,再加入氯化钡溶液,如生成沉淀则可说明含有 ,B错误;
C.无色试液加入NaOH溶液,试管口湿润的红色石蕊试纸未变蓝,只能说明没有按期放出,并不能证明
试液中无 ,C错误;
D.加入稀盐酸产生无色气体,说明含有 或 ,D错误;故选A。
考点三 不同价态含硫物质的转化
【例3-1】(2021·云南昆明·高一期末)元素的价类二维图是学习元素及其化合物的重要模型和工具。下图
为硫元素的价类二维图,其中的箭头表示部分物质间的转化关系。下列说法正确的是
A.附着有X的试管常用酒精清洗
B.Y使溴水褪色体现了其漂白性
C.加热条件下,Z的浓溶液与铜反应能实现转化②
D.Y与 气体混合能实现转化①
【答案】C
【解析】A.X为硫元素的单质,硫单质易溶于CS 难溶于酒精和水,硫单质附着在试管上常用CS 溶液清
2 2
洗,故A错误;
B.Y为+4价氧化物,所以Y为SO ,SO 具有还原性,使溴水褪色是发生了氧化还原反应,故B错误;
2 2
C.Y为SO ,Z为HSO ,HSO 的浓溶液与铜反应能实现转化SO ,故C正确;
2 2 4 2 4 2D.Y为SO ,与 气体反应生成硫单质,不能生成Z,故D错误;
2
故答案为C。
【例3-2】(2021·重庆市第二十九中学校高一期中)硫元素是动植物生长不可缺少的元素,图1是自然界
中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
(1)图1中与图2中M、N对应的物质分别是_______、_______。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为_______。
(3)NaSO 溶液易变质,实验室检验NaSO 溶液是否变质的基本操作是_______。
2 3 2 3
(4)SO 和氯水都有漂白性,有人为增强漂白效果,将Cl 和SO 混合使用,结果适得其反,几乎没有漂
2 2 2
白效果,用离子方程式表示其原因:_______。
(5)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫
酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO
4
方案乙:由Cu→CuO→CuSO
4
①方案甲,中铜和浓硫酸反应的化学方程式是_______。该反应体现了浓硫酸的_______性。
②这两种方案,你认为哪一种方案更合理?_______。理由是_______
【答案】
(1) CaSO•2H O、NaSO •10H O CuFeS
4 2 2 4 2 2
(2)1:2
(3)取少量溶液于试管中,向其中加入过量稀盐酸,再滴加BaCl 溶液,如果产生白色沉淀,证明混有
2
NaSO
2 4
(4)Cl+SO+2H O=2Cl-+SO +4H+
2 2 2
(5)Cu+2H SO (浓) CuSO +SO↑+2H O 强氧化性、酸性 方案乙 无污染产生,原料利用率高
2 4 4 2 2
【解析】(1)图2中M为+6价的硫元素对应的盐,对应图1中的物质为CaSO•2H O、NaSO •10H O,N
4 2 2 4 2为-2价的硫元素对应的盐,对应图1中的物质为CuFeS;
2
(2)X为HS、Y为SO ,发生归中反应得到S单质,SO 做氧化剂,化合价降低4,HS做还原剂,化合
2 2 2 2
价升高2,由升降相等,则反应中氧化剂与还原剂的物质的量之比为1:2;
(3)NaSO 溶液易被氧气氧化为NaSO 而变质,即检验硫酸根是否存在即可,实验操作为:取少量溶液
2 3 2 4
于试管中,向其中加入过量稀盐酸,再滴加BaCl 溶液,如果产生白色沉淀,证明混有NaSO ;
2 2 4
(4)二氧化硫与氯气和水发生氧化还原反应生成盐酸和硫酸,离子方程式:Cl+SO+2H O=2Cl-+SO
2 2 2
+4H+;
(5)①铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫与水,反应方程式为:Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O,反应中硫元素的化合价部分降低生成二氧化硫,部分不变存在与硫酸铜中,浓硫酸表
4 2 2
现强氧化性与酸性;
②方案①生成二氧化硫,污染空气,硫元素不能完全利用,方案②与方案①相比,没有污染产生且原料的
利用率高,故方案②更合理。
【一隅三反】
1.(2021·山西·陵川县平城中学高一月考)图为含硫物质之间的转化关系,其中属于氧化还原反应的有(
)
A.1 个 B.2 个 C.3 个 D.4 个
【答案】B
【解析】HS转化为S单质,S元素化合价由-2价变为0价;S单质转化为SO ,S元素化合价由0价变为
2 2
+4价;SO 转化为HSO 及NaSO ,S元素化合价始终为+4价;综上,本题选B。
2 2 3 2 3
2.(2021·河北遵化·高一开学考试)含硫元素物质间发生转化:S SO SO HSO Al (SO ),其中
2 3 2 4 2 4 3
硫元素化合价发生变化的是( )
A.①② B.③④ C.①③ D.②④
【答案】A
【解析】①S单质与O 在点燃时反应转化为SO ,S元素化合价由0价变为+4价,反应前后S元素化合价
2 2发生了变化,①符合题意;
②SO 与O 在一定条件下反应产生SO ,S元素化合价由+4价变为+6价,S元素化合价升高,可见在反应
2 2 3
前后S元素化合价发生了变化,②符合题意;
③SO 被水吸收得到HSO ,S元素化合价都是+6价,因此S元素化合价未发生变化,③不符合题意;
3 2 4
④HSO 可以与Al O 发生反应产生Al (SO ) 和水,S元素化合价都是+6价,反应前后S元素化合价未发
2 4 2 3 2 4 3
生变化,④不符合题意;
综上所述可知:在物质转化中硫元素化合价发生变化的序号是①②,故合理选项是A。
3.(2021·河北香河·高一期末)用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略,
下列说法不正确的是( )
途径①:
途径②:
途径③:
A.途径①的反应中体现了浓 的强氧化性
B.途径②、③的第二步反应在实际生产中可以通过增大 的浓度来降低成本
C.由途径①、②、③分别制取 ,理论上各消耗 S,各转移
D.途径②、③比途径①污染相对小且原子利用率高,更能体现“绿色化学”的理念
【答案】C
【解析】A.S与浓硝酸反应生成硫酸、二氧化氮和水,该反应中体现了浓硝酸的强氧化性,故A正确;
B.增大一种反应物的浓度,可以提高另一种反应物的转化率,途径②、③的第二步反应在实际生产中可
以通过增大O 的浓度来降低成本,故B正确;
2
C.途径①和②都是由S来制备HSO ,S的化合价从0价升高到+6价,制取1molH SO ,理论上各消耗
2 4 2 4
1molS,各转移6mole-,途径③中S的化合价从-1价升高到+6价,制取1molH SO ,转移7mole-,故C错
2 4
误;
D.途径①S与浓硝酸反应生成硫酸、二氧化氮和水,有副产物二氧化氮,而且二氧化氮会污染大气,所
以途径②、③与途径①相比更能体现“绿色化学”的理念,故D正确;
故选C。
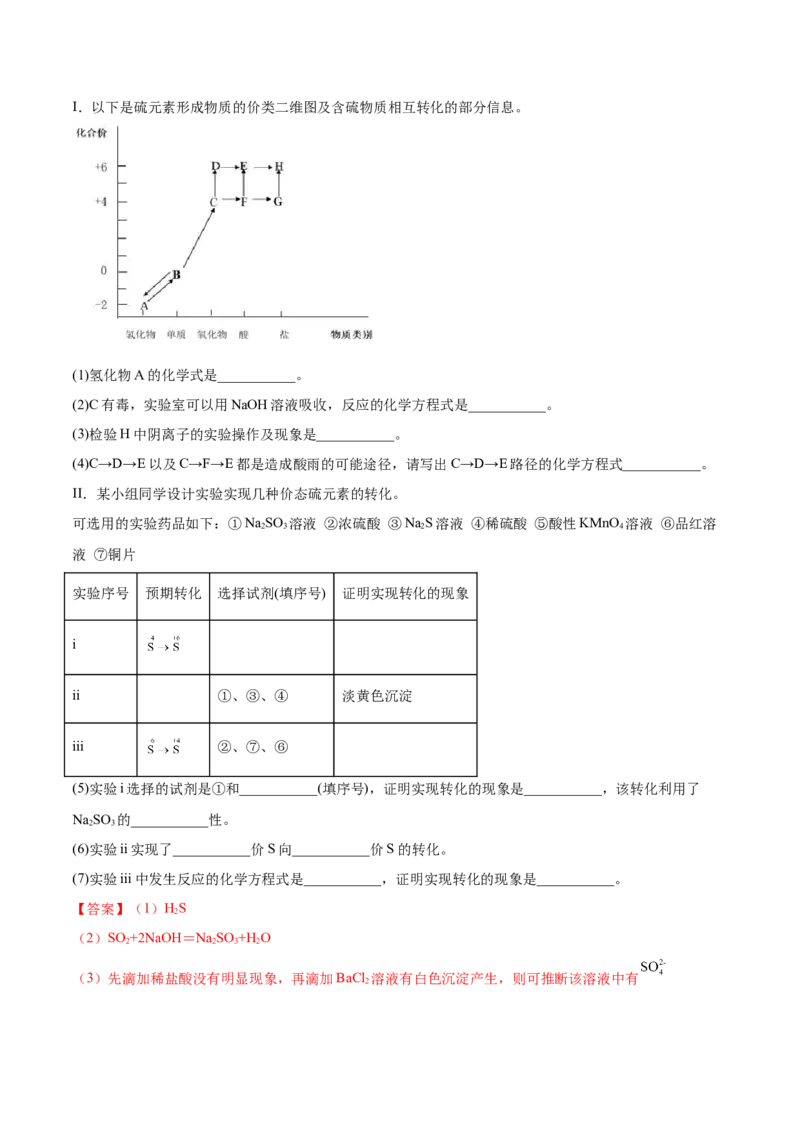
4.(2021·安徽·亳州二中高一期末)研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。I.以下是硫元素形成物质的价类二维图及含硫物质相互转化的部分信息。
(1)氢化物A的化学式是___________。
(2)C有毒,实验室可以用NaOH溶液吸收,反应的化学方程式是___________。
(3)检验H中阴离子的实验操作及现象是___________。
(4)C→D→E以及C→F→E都是造成酸雨的可能途径,请写出C→D→E路径的化学方程式___________。
II.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①NaSO 溶液 ②浓硫酸 ③NaS溶液 ④稀硫酸 ⑤酸性KMnO 溶液 ⑥品红溶
2 3 2 4
液 ⑦铜片
实验序号 预期转化 选择试剂(填序号) 证明实现转化的现象
i
ii ①、③、④ 淡黄色沉淀
iii ②、⑦、⑥
(5)实验i选择的试剂是①和___________(填序号),证明实现转化的现象是___________,该转化利用了
NaSO 的___________性。
2 3
(6)实验ii实现了___________价S向___________价S的转化。
(7)实验iii中发生反应的化学方程式是___________,证明实现转化的现象是___________。
【答案】(1)HS
2
(2)SO +2NaOH=NaSO +H O
2 2 3 2
(3)先滴加稀盐酸没有明显现象,再滴加BaCl 溶液有白色沉淀产生,则可推断该溶液中有
2(4) 2SO +O 2SO 、SO +H O=HSO
2 2 3 3 2 2 4
(5) ⑤ 酸性高锰酸钾溶液褪色 还原性
(6)+4(或者-2) 0
(7) Cu+2H SO (浓) CuSO +SO↑+2H O 将产生气体通入品红溶液,品红褪色
2 4 4 2 2
【解析】Ⅰ.(1)A是S的氢化物,S的最低价是-2价,则A的化学式是HS;
2
(2)C为+4价硫的氧化物,为二氧化硫,有毒,实验室可以用NaOH溶液吸收生成亚硫酸钠和水,反应的化
学方程式SO +2NaOH=NaSO +H O;
2 2 3 2
(3)H是硫元素的最高价含氧酸盐,即硫酸盐,因此检验H中阴离子的实验操作及现象是:先滴加稀盐酸没
有明显现象,再滴加BaCl 溶液有白色沉淀产生,则可推断该溶液中有 ;
2
(4)C→D→E是S 2→SO →HSO ,C→F→E是SO →HSO →HSO ,都是造成酸雨的可能途径,则
O 3 2 4 2 2 3 2 4
C→D→E路径反应的化学方程式为:2SO +O 2SO 、SO +H O=HSO ;
2 2 3 3 2 2 4
Ⅱ.(5)实验ⅰ是+4价硫变化为+6价硫,被氧化,失去电子,选择的试剂是①NaSO 溶液和氧化剂⑤酸性
2 3
KMnO 溶液,发生氧化还原反应,高锰酸钾溶液紫红色褪去,说明亚硫酸钠具有还原性;
4
(6)实验ⅱ选择①NaSO 溶液、③NaS溶液、④稀硫酸试剂,在酸性溶液中,硫离子和亚硫酸根离子发生
2 3 2
氧化还原反应生成单质硫,实现了+4价或-2硫元素转化为0价硫的过程;
(7)实验ⅲ中②浓硫酸⑦铜片加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式:Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O,二氧化硫能使⑥品红溶液褪色,证明实现转化的现象是:将产生气体通入品红溶液,
4 2 2
品红褪色。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育