文档内容
5.1.2 硫及其化合物(精练)
题组一 硫酸
1.(2021·吉林江城中学高一期末)下列关于硫酸的说法中错误的是( )
A.常温下可用铝制罐车运输浓硫酸 B.稀硫酸可以与铁反应产生氢气
C.浓硫酸有脱水性可使白糖变黑 D.浓硫酸可以干燥氨气
2.(2021·云南·大关县第一中学高一月考)下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是
( )
A.在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性)
B.在加热条件下铜与浓硫酸反应(强氧化性、酸性)
C.蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D.浓硫酸可用来干燥某些气体(脱水性)
3.(2021·重庆南开中学高一期中)下列有关浓硫酸的叙述正确的是
①浓硫酸在常温下能够使铁、铝等金属钝化
②浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
③浓硫酸具有吸水性,因而能使蔗糖炭化
④浓硫酸与过量的铜加热反应后,硫酸会有剩余
⑤浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
⑥浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外只有SO
2
⑦浓硫酸具有强氧化性,常温下能与Cu发生剧烈反应
⑧浓硫酸具有强氧化性,SO 具有还原性,所以浓硫酸不能干燥SO
2 2
⑨向5 mL 18 mol•L-1的浓硫酸中加入足量Cu并加热使其充分反应,被还原的HSO 和生成的SO 气体均小
2 4 2
于0.045 mol
A.①②⑤ B.①④⑨ C.⑥⑦⑧ D.③④⑨
4.(2021·辽宁·大连市第一中学高一期中)下列叙述错误的是
A.硫酸钡(BaSO)在医疗上可用作钡餐 B.石膏(CaSO·2H O)可用来制作各种模型
4 4 2
C.常温下可用铁、铝制容器来盛装浓硫酸 D.制取NH 时,可用浓硫酸做干燥剂
3
5.(2021·重庆·西南大学附中高一月考)HSO 具有多种性质,回答下列问题:
2 4
(1)浓HSO 使蔗糖变黑,体现了浓HSO 的什么性质___________。黑色物质为炭粉,炭粉与浓硫酸继
2 4 2 4
续反应的化学方程式为___________。(2)浓HSO 是常见的气体干燥剂,但它不能干燥HS和HI,原因是___________。
2 4 2
(3)过量的锌与一定量浓HSO 反应,随着硫酸浓度变稀得到的两种气体产物为___________。使一定量
2 4
Zn与100 mL 18.4 mol/L浓HSO 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6 L,则Zn
2 4
的质量为___________g。
6.(2021·山西英才学校高一月考)已知铜和浓硫酸可以在加热条件下发生反应(已配平):
。试通过计算和推理完成下面的问题
(1)此反应中,硫酸体现了___________性和___________性。
(2)A物质可以导致酸雨的形成。A应该属于___________。(用字母代号填写)
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO 溶液褪色,此褪色反应中(填写化学式,下同)___________失去电子,氧
4
化剂是___________。
7.(2021·湖南省邵东市第三中学高一月考)下列各过程主要表现了浓硫酸的哪些性质?请将答案的序号
分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体___________。
(2)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体___________。
(3)常温下可以用铁或铝的容器贮存浓硫酸___________。
(4)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体___________。
(5)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑___________。
8.(2021·安徽合肥·高一期末)硫酸是当今世界最重要的化工产品之一。
I.硫酸的各种制法:
(1)早在1000多年前,我国就已采用加热胆矾(CuSO ·5H O)或绿矾(FeSO ·7H O)的方法制取硫酸。FeSO
4 2 4 2 4
受热分解的化学方程式:2FeSO Fe O+SO↑+SO↑。
4 2 3 2 3
①将FeSO 受热产生的气体通入如图1装置中,以检验产生的气体中是否含有SO 和SO 。能说明SO 存在
4 3 2 2
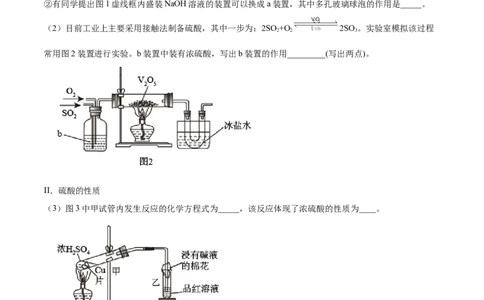
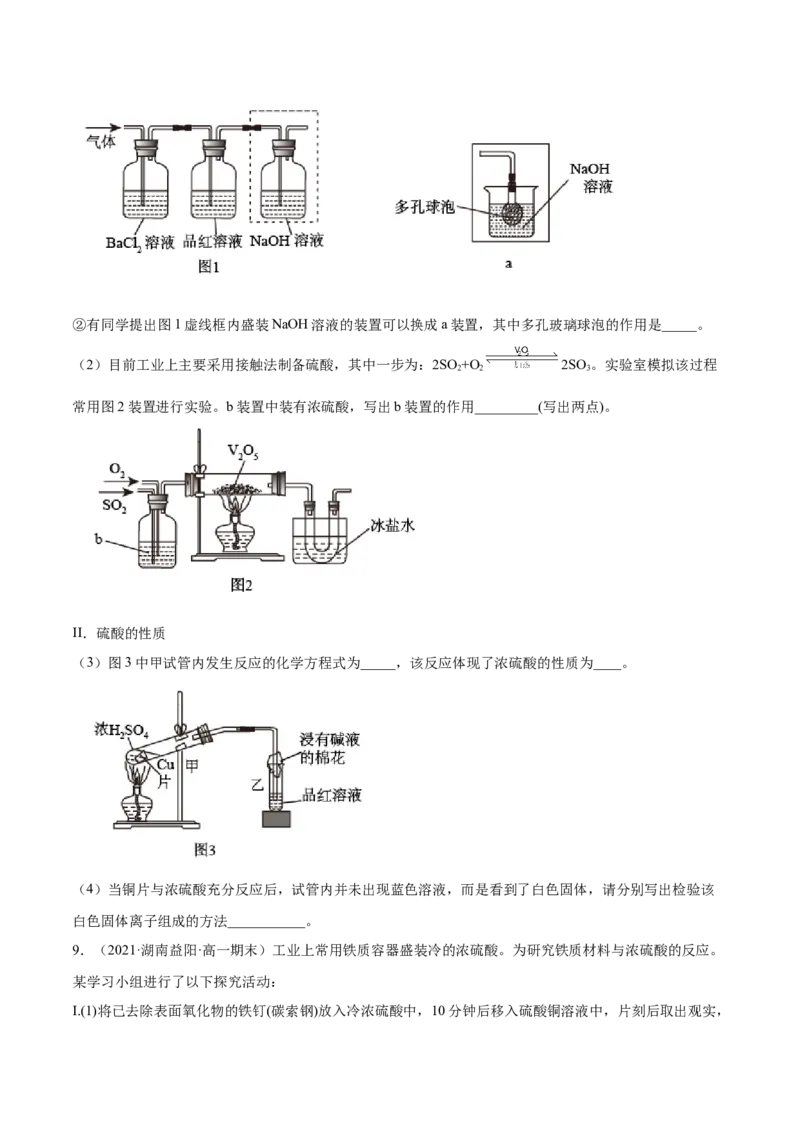
的实验现象是_________。②有同学提出图1虚线框内盛装NaOH溶液的装置可以换成a装置,其中多孔玻璃球泡的作用是_____。
(2)目前工业上主要采用接触法制备硫酸,其中一步为:2SO +O 2SO 。实验室模拟该过程
2 2 3
常用图2装置进行实验。b装置中装有浓硫酸,写出b装置的作用_________(写出两点)。
II.硫酸的性质
(3)图3中甲试管内发生反应的化学方程式为_____,该反应体现了浓硫酸的性质为____。
(4)当铜片与浓硫酸充分反应后,试管内并未出现蓝色溶液,而是看到了白色固体,请分别写出检验该
白色固体离子组成的方法___________。
9.(2021·湖南益阳·高一期末)工业上常用铁质容器盛装冷的浓硫酸。为研究铁质材料与浓硫酸的反应。
某学习小组进行了以下探究活动:
Ⅰ.(1)将已去除表面氧化物的铁钉(碳索钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观实,铁钉表面无明显变化,其原因是___________。
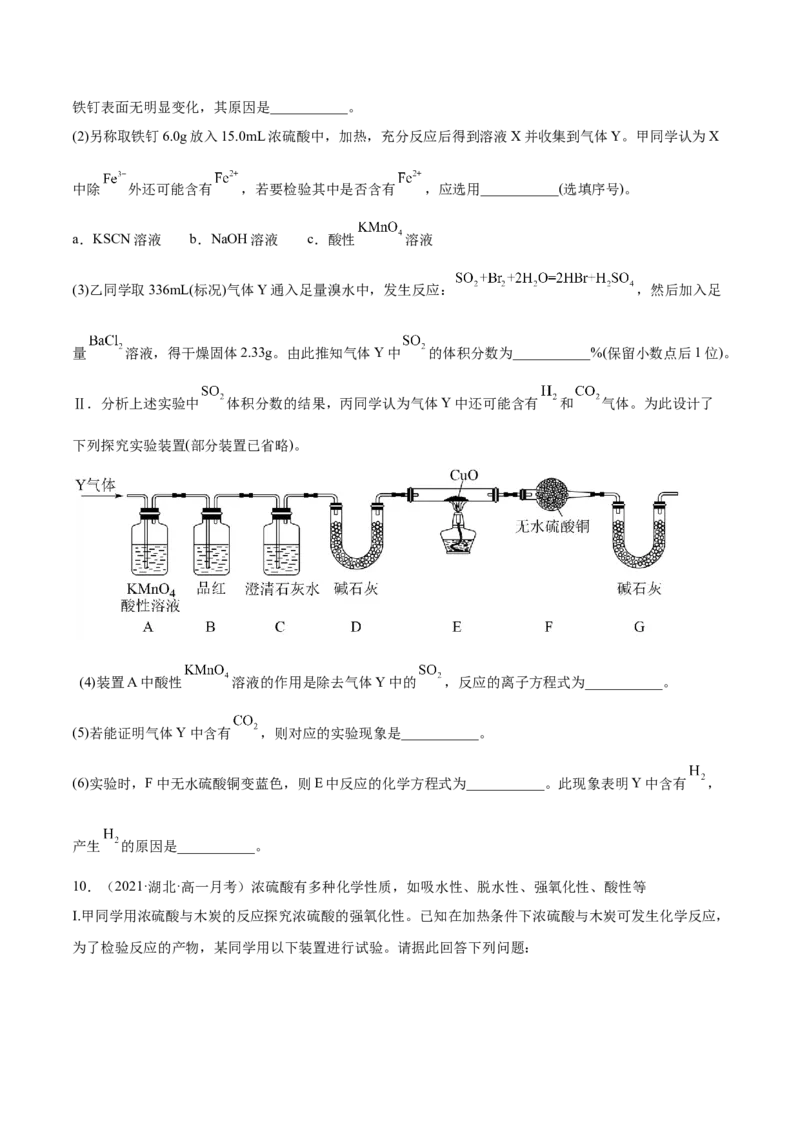
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。甲同学认为X
中除 外还可能含有 ,若要检验其中是否含有 ,应选用___________(选填序号)。
a.KSCN溶液 b.NaOH溶液 c.酸性 溶液
(3)乙同学取336mL(标况)气体Y通入足量溴水中,发生反应: ,然后加入足
量 溶液,得干燥固体2.33g。由此推知气体Y中 的体积分数为___________%(保留小数点后1位)。
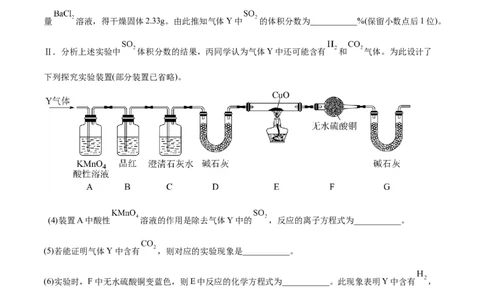
Ⅱ.分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含有 和 气体。为此设计了
下列探究实验装置(部分装置已省略)。
(4)装置A中酸性 溶液的作用是除去气体Y中的 ,反应的离子方程式为___________。
(5)若能证明气体Y中含有 ,则对应的实验现象是___________。
(6)实验时,F中无水硫酸铜变蓝色,则E中反应的化学方程式为___________。此现象表明Y中含有 ,
产生 的原因是___________。
10.(2021·湖北·高一月考)浓硫酸有多种化学性质,如吸水性、脱水性、强氧化性、酸性等
Ⅰ.甲同学用浓硫酸与木炭的反应探究浓硫酸的强氧化性。已知在加热条件下浓硫酸与木炭可发生化学反应,
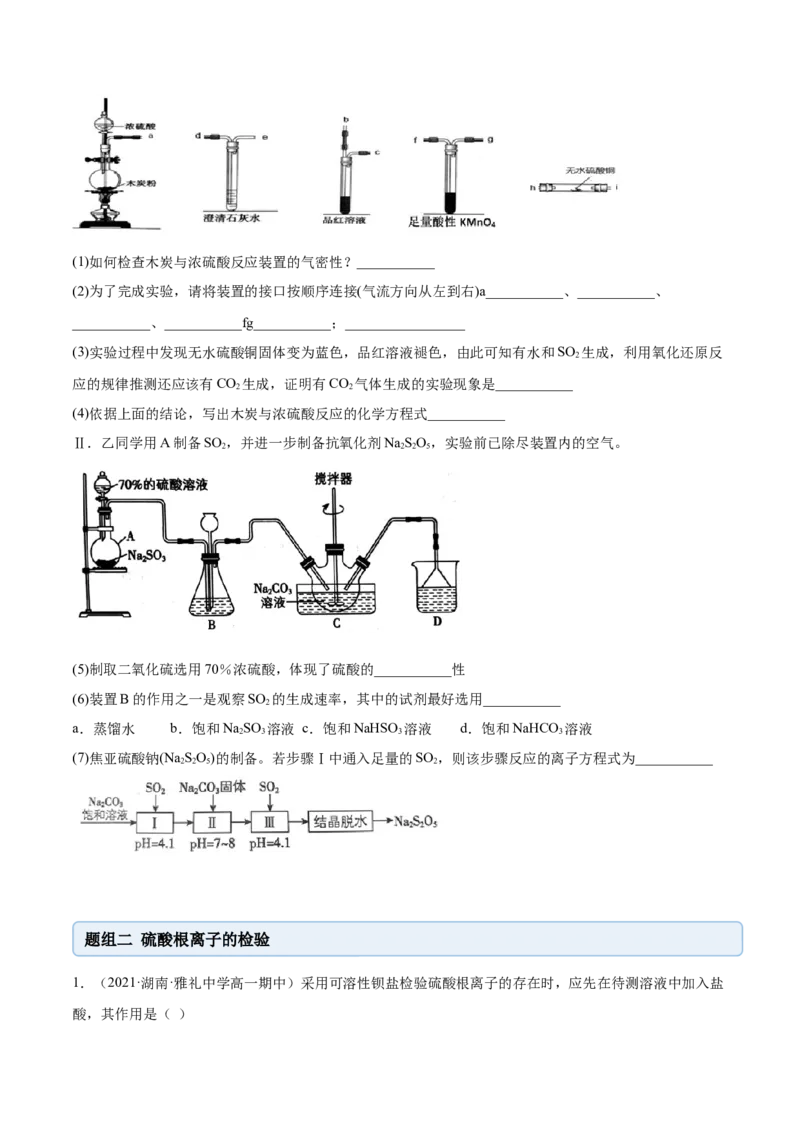
为了检验反应的产物,某同学用以下装置进行试验。请据此回答下列问题:(1)如何检查木炭与浓硫酸反应装置的气密性?___________
(2)为了完成实验,请将装置的接口按顺序连接(气流方向从左到右)a___________、___________、
___________、___________fg___________;_________________
(3)实验过程中发现无水硫酸铜固体变为蓝色,品红溶液褪色,由此可知有水和SO 生成,利用氧化还原反
2
应的规律推测还应该有CO 生成,证明有CO 气体生成的实验现象是___________
2 2
(4)依据上面的结论,写出木炭与浓硫酸反应的化学方程式___________
Ⅱ.乙同学用A制备SO ,并进一步制备抗氧化剂NaSO,实验前已除尽装置内的空气。
2 2 2 5
(5)制取二氧化硫选用70%浓硫酸,体现了硫酸的___________性
(6)装置B的作用之一是观察SO 的生成速率,其中的试剂最好选用___________
2
a.蒸馏水 b.饱和NaSO 溶液 c.饱和NaHSO 溶液 d.饱和NaHCO 溶液
2 3 3 3
(7)焦亚硫酸钠(Na SO)的制备。若步骤Ⅰ中通入足量的SO ,则该步骤反应的离子方程式为___________
2 2 5 2
题组二 硫酸根离子的检验
1.(2021·湖南·雅礼中学高一期中)采用可溶性钡盐检验硫酸根离子的存在时,应先在待测溶液中加入盐
酸,其作用是( )A.形成较多的白色沉淀 B.形成的沉淀纯度更高
C.排除 、 及Ag+等的干扰 D.排除钡离子以外的其它阳离子干扰
2(2021·吉林·汪清县汪清第四中学高一月考)检验某未知溶液中是否含有SO ,下列操作最合理的是
( )
A.加入稀HNO 酸化的Ba(NO ) 溶液 B.先加稀盐酸酸化,再滴加BaCl 溶液
3 3 2 2
C.加入稀HNO 酸化的BaCl 溶液 D.先用稀HNO 酸化,再滴加Ba(NO ) 溶液
3 2 3 3 2
3.(2021·吉林江城中学)检验某未知溶液中是否含有 的下列操作中最合理的是( )
A.加入硝酸酸化的 B.先加 酸化,再加 溶液
C.先加盐酸酸化,再加 溶液 D.加入盐酸酸化了的 溶液
4.(2021·广东·顺德市李兆基中学)下列检验试样中有无SO 的操作及结论正确的是( )
A.先加盐酸无明显现象,再加BaCl 溶液有白色沉淀,一定有SO
2
B.加盐酸酸化的BaCl 溶液有白色沉淀,一定有SO
2
C.滴加硝酸酸化的AgNO 溶液没有白色沉淀,一定没有SO
3
D.滴加BaCl 有白色沉淀,一定有SO
2
5.(2021·上海·华师大二附中高一月考)下列离子检验的方法正确的是( )
A.某溶液 产生白色沉淀,说明原溶液中有
B.某溶液 产生白色沉淀,说明原溶液中有
C.某溶液 产生蓝色沉淀,说明原溶液中有
D.某溶液 生成无色无味气体,说明原溶液中有
题组三 不同价态的含硫物质的转化
1.(2021·吉林·白城一中高一期中)下列转化需加入还原剂才能实现的是( )A.HSO →SO B. →SO C.HS→S D.S→SO
2 4 2 2 2 2
2.(2021·广东肇庆·高一期末)部分含硫物质的分类与相应化合价关系如图所示。下列推断正确的是
( )
A.a可与氧气反应直接生成d
B.b与c反应可以得到a
C.c因其漂白性可以使酸性 溶液褪色
D.e、f均为二元强酸
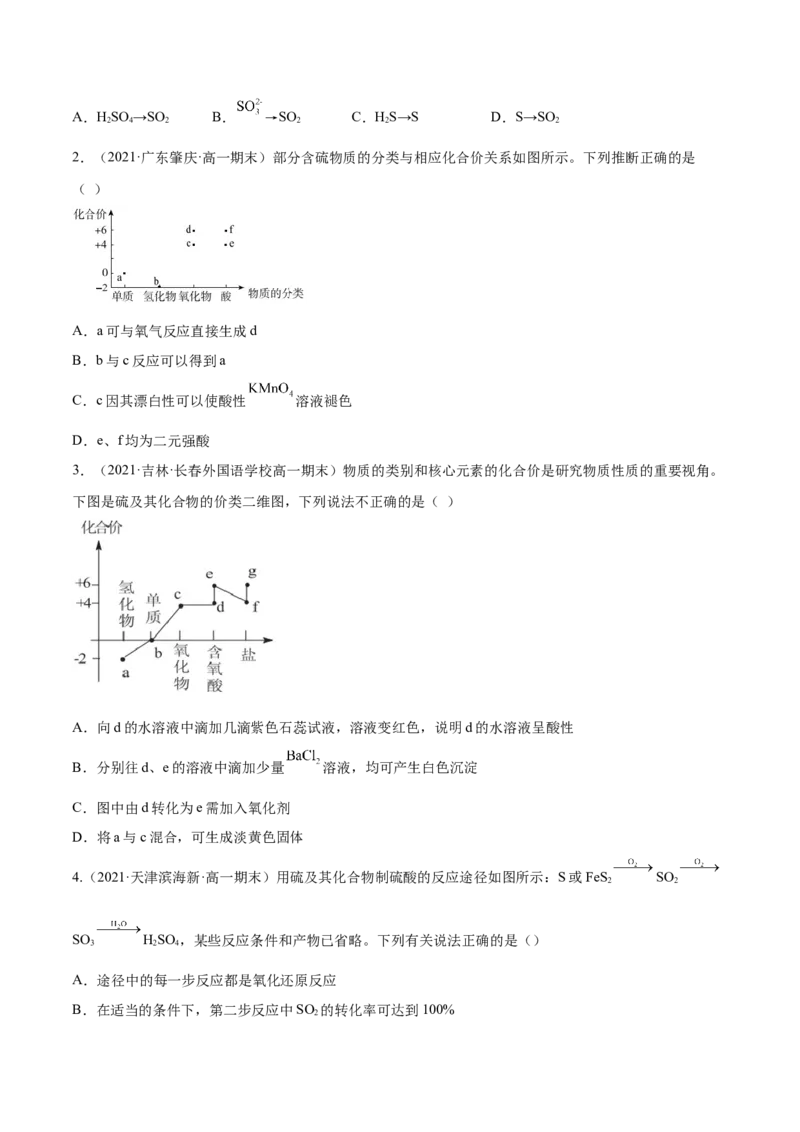
3.(2021·吉林·长春外国语学校高一期末)物质的类别和核心元素的化合价是研究物质性质的重要视角。
下图是硫及其化合物的价类二维图,下列说法不正确的是( )
A.向d的水溶液中滴加几滴紫色石蕊试液,溶液变红色,说明d的水溶液呈酸性
B.分别往d、e的溶液中滴加少量 溶液,均可产生白色沉淀
C.图中由d转化为e需加入氧化剂
D.将a与c混合,可生成淡黄色固体
4.(2021·天津滨海新·高一期末)用硫及其化合物制硫酸的反应途径如图所示:S或FeS SO
2 2
SO HSO ,某些反应条件和产物已省略。下列有关说法正确的是()
3 2 4
A.途径中的每一步反应都是氧化还原反应
B.在适当的条件下,第二步反应中SO 的转化率可达到100%
2C.在实际工业生产中通常用98.3%的浓硫酸吸收SO
3
D.制备硫酸的反应途径可简化为S SO HSO
3 2 4
5.(2021·江苏南通·高一期末)硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类。我
国工业上一般以黄铁矿为原料来制备硫酸。工业制硫酸涉及到下列反应:
① ;② ;③ 。
生产中用浓硫酸代替水吸收 ,制得发烟硫酸( ),将发烟硫酸稀释后可制得密度为
、质量分数为 的浓硫酸。下列有关工业制硫酸的说法正确的是( )
A. 的浓硫酸的物质的量浓度为
B.反应①中 既是氧化剂又是还原剂
C.该条件下反应②中生成的 不能转化为
D.将 发烟硫酸与 混合,可得到 质量分数为 的硫酸溶液
6.(2021·山东聊城·高一期末)图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分
物质类别的对应关系。请回答下列问题:
(1)图2中N所对应图1中物质的化学式为_______,Y与金属铜反应所得产物的化学式为_______。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为_______。
(3)碳和M的浓溶液反应生成Z的化学方程式为_______。
(4)从分类角度分析判断,下列物质不属于酸性氧化物的是_______。
A.SO B.SO C.SiO D.NO
2 3 2 2
(5)NaSO 溶液易变质,实验室检验NaSO 溶液是否变质的基本操作是_______。
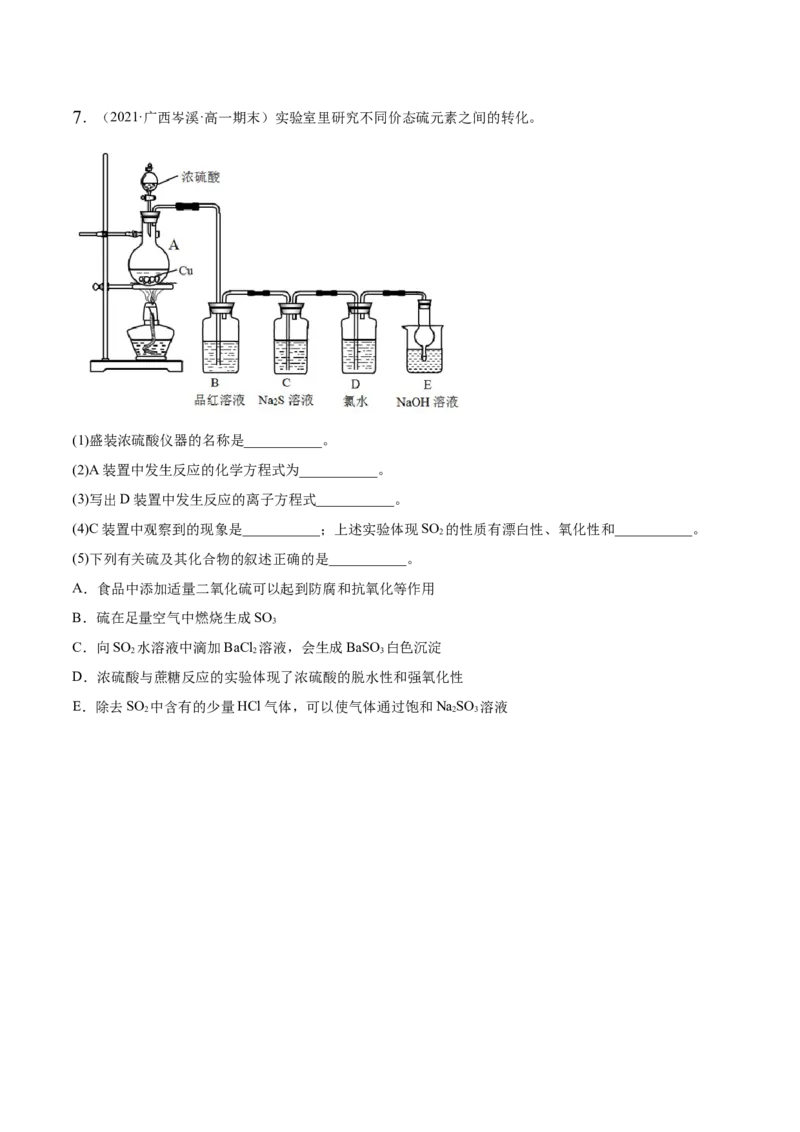
2 3 2 37.(2021·广西岑溪·高一期末)实验室里研究不同价态硫元素之间的转化。
(1)盛装浓硫酸仪器的名称是___________。
(2)A装置中发生反应的化学方程式为___________。
(3)写出D装置中发生反应的离子方程式___________。
(4)C装置中观察到的现象是___________;上述实验体现SO 的性质有漂白性、氧化性和___________。
2
(5)下列有关硫及其化合物的叙述正确的是___________。
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.硫在足量空气中燃烧生成SO
3
C.向SO 水溶液中滴加BaCl 溶液,会生成BaSO 白色沉淀
2 2 3
D.浓硫酸与蔗糖反应的实验体现了浓硫酸的脱水性和强氧化性
E.除去SO 中含有的少量HCl气体,可以使气体通过饱和NaSO 溶液
2 2 3倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育