文档内容
第五章 化学生产中的重要非金属元素
第一节 硫及其化合物
第二课时 硫酸
【学习目标】1.通过实验探究,讨论交流,能正确描述有关事验现象,分析理解反应原理,进一步认
识硫酸的酸性及酸的通性。
2.结合图示或实验视频,通过实验探究不活泼金属Cu与浓硫酸的反应,引导分析非金属C与浓硫酸的
反应原理,认识浓硫酸的强氧化性、吸水性和脱水性等特性,增强对氧化还原反应的认识。
3.通过对比分析浓硫酸与稀硫酸的不同性质,认识浓度、反应条件对化学反应的影响,并能熟练书写
相关反应方程式,培养宏观辨识与微观探析等化学核心素养。
【学习重点】浓硫酸的三大特性(强氧化性、吸水性、脱水性)
【学习难点】浓硫酸与金属单质、非金属单质、还原性物质的氧化还原理论的分析
【课前预习】
旧知回顾:1.酸通常具有哪些通性?请举例说明。
2.酸有哪些分类方法?
新知预习:浓硫酸具有哪些特性?具体有哪些表现?
【课中探究】情景导入:硫酸是重要的化工原料,有广泛的用途。俗话说盛世古董,乱世黄金,古陶瓷的收藏是比
较热门的一类,而有些人在利益的驱使下,就会烧制大量的仿古瓷器,然后用做旧来把这些仿古瓷做旧,
得以获取暴利,而高锰酸钾加浓硫酸(做色)就是很多瓷器造假者最为常用的手段之一(见PPT图片),今
天我们就来学习硫酸的有关知识。
一、硫酸的工业制法及稀硫酸的性质
活动一、硫酸的工业制备—接触法制硫酸
任务一、阅读教材P4页最后自然段,回答硫酸具有哪些重要用途?
任务二、观看视频,回顾二氧化硫的催化氧化反应,观察教材 P4页图5-4,思考工业上如何制备硫
酸?
【对应训练】1.含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时
可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
A.该过程中可得到化工产品HSO
2 4
B.该工艺流程是除去煤燃烧时产生的SO
2
C.该过程中化合价发生改变的元素为Fe和S
D.图中涉及的反应之一为Fe (SO )+SO +2HO===2FeSO+2HSO
2 4 3 2 2 4 2 4
2.在硫酸的工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是( )
A.硫铁矿煅烧前要粉碎,因为大块硫铁矿不能燃烧
B.从沸腾炉出来的气体只有SO
2
C.SO 氧化成SO ,SO 能全部转化为SO
2 3 2 3
D.SO 用98.3%的浓HSO 吸收,目的是防止形成酸雾,以便使SO 吸收更充分
3 2 4 3
活动二、稀硫酸的性质
任务一、回顾酸的通性,请举例说明稀硫酸具有哪些主要化学性质?任务二、问题探究:实验室如何用稀硫酸与金属反应制备氢气?浓盐酸或浓硫酸可否代替稀硫酸呢?
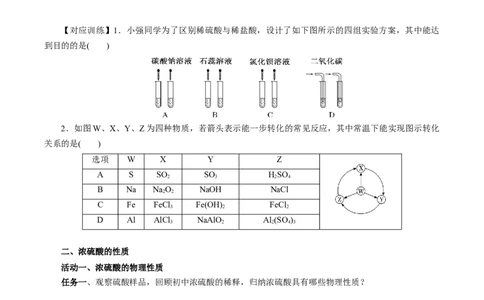
【对应训练】1.小强同学为了区别稀硫酸与稀盐酸,设计了如下图所示的四组实验方案,其中能达
到目的的是( )
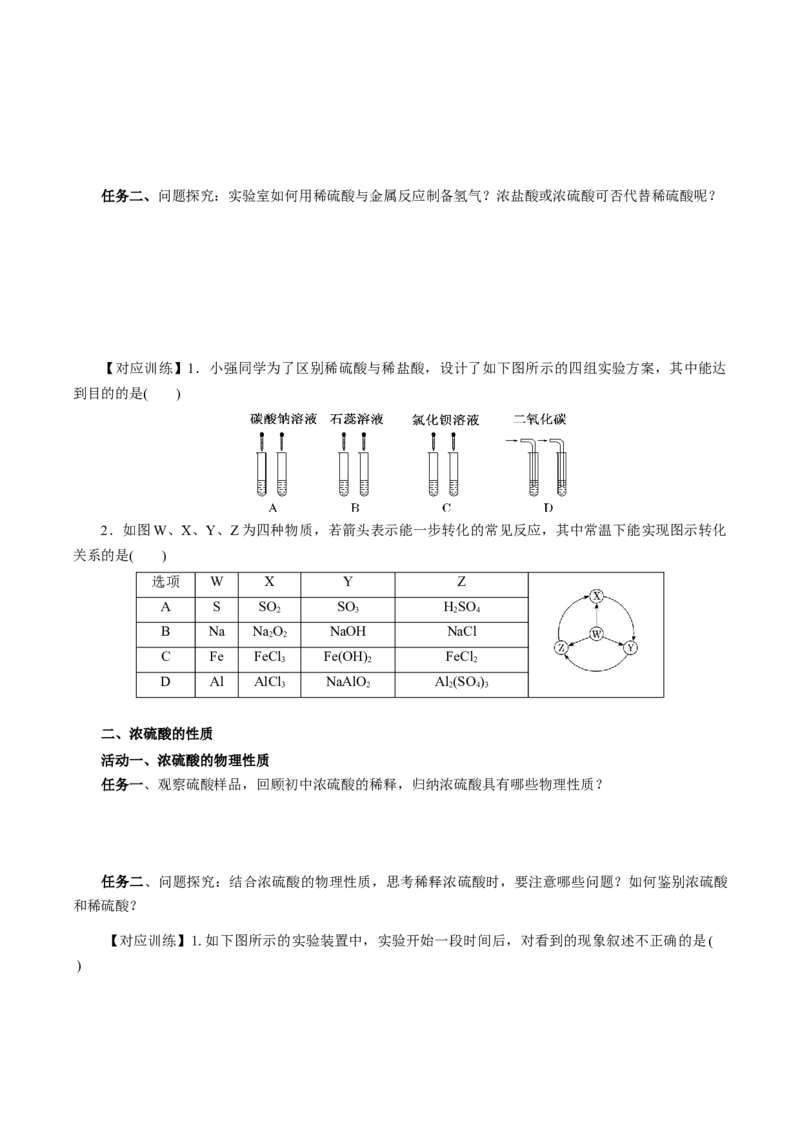
2.如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化
关系的是( )
选项 W X Y Z
A S SO SO HSO
2 3 2 4
B Na NaO NaOH NaCl
2 2
C Fe FeCl Fe(OH) FeCl
3 2 2
D Al AlCl NaAlO Al (SO )
3 2 2 4 3
二、浓硫酸的性质
活动一、浓硫酸的物理性质
任务一、观察硫酸样品,回顾初中浓硫酸的稀释,归纳浓硫酸具有哪些物理性质?
任务二、问题探究:结合浓硫酸的物理性质,思考稀释浓硫酸时,要注意哪些问题?如何鉴别浓硫酸
和稀硫酸?
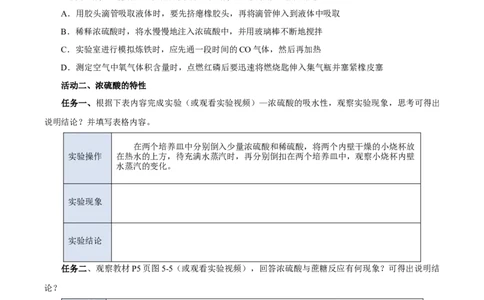
【对应训练】1.如下图所示的实验装置中,实验开始一段时间后,对看到的现象叙述不正确的是(
)A.苹果块会干瘪 B.胆矾晶体表面有“白斑”
C.小试管内有晶体析出 D.pH试纸变红
2.科学的方法是实验成功的前提条件。下列方法或要求存在错误的是( )
A.用胶头滴管吸取液体时,要先挤瘪橡胶头,再将滴管伸入到液体中吸取
B.稀释浓硫酸时,将水慢慢地注入浓硫酸中,并用玻璃棒不断地搅拌
C.实验室进行模拟炼铁时,应先通一段时间的CO气体,然后再加热
D.测定空气中氧气体积含量时,点燃红磷后要迅速将燃烧匙伸入集气瓶并塞紧橡皮塞
活动二、浓硫酸的特性
任务一、根据下表内容完成实验(或观看实验视频)—浓硫酸的吸水性,观察实验现象,思考可得出
说明结论?并填写表格内容。
在两个培养皿中分别倒入少量浓硫酸和稀硫酸,将两个内壁干燥的小烧杯放
实验操作 在热水的上方,待充满水蒸汽时,再分别倒扣在两个培养皿中,观察小烧杯内壁
水蒸汽的变化。
实验现象
实验结论
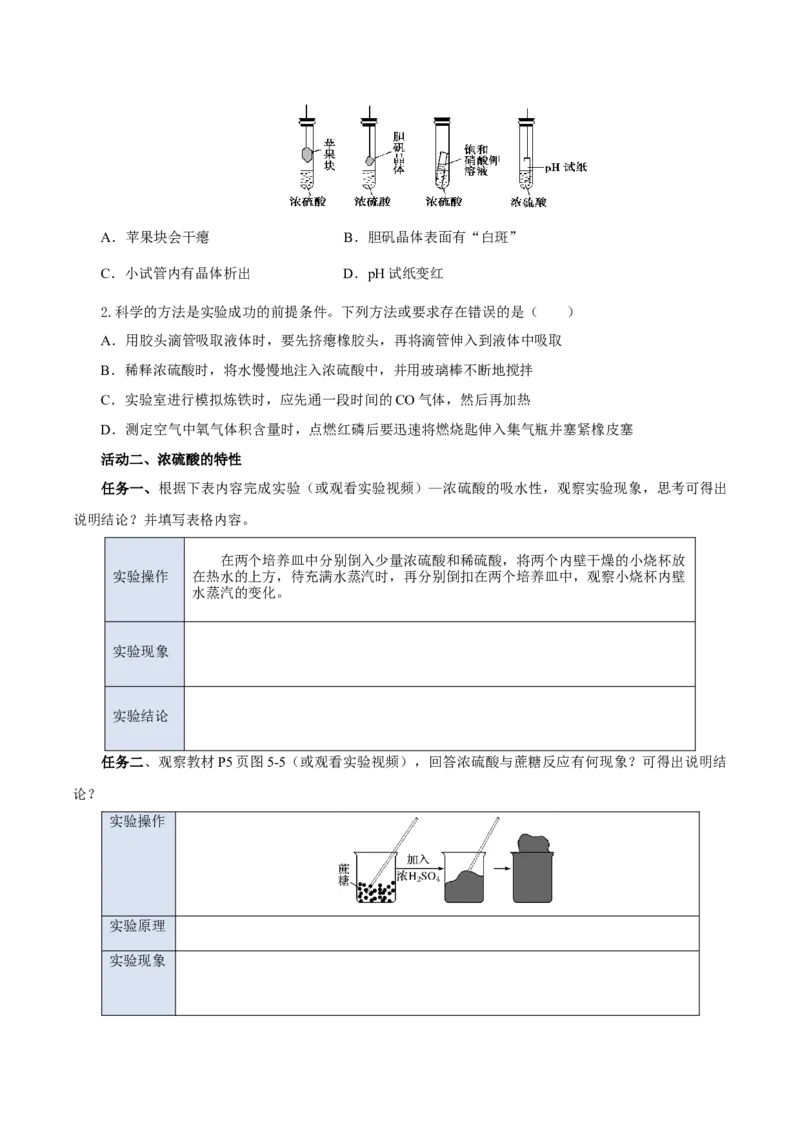
任务二、观察教材P5页图5-5(或观看实验视频),回答浓硫酸与蔗糖反应有何现象?可得出说明结
论?
实验操作
实验原理
实验现象实验结论
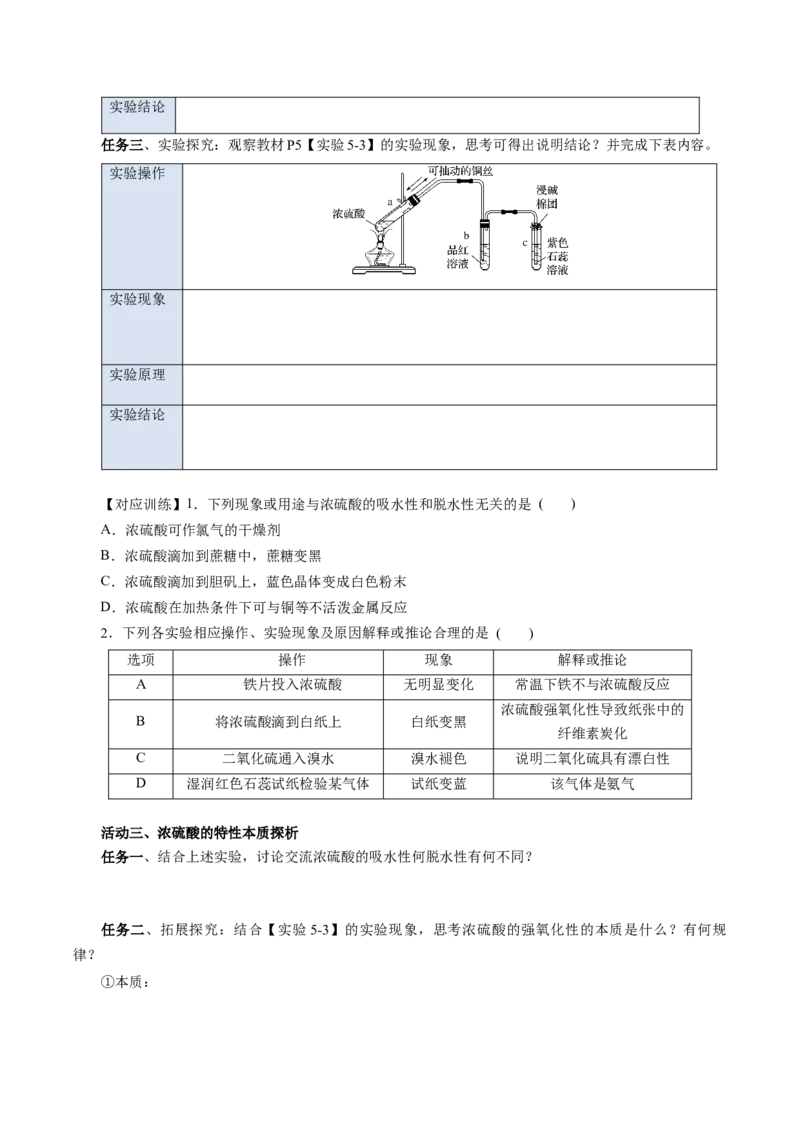
任务三、实验探究:观察教材P5【实验5-3】的实验现象,思考可得出说明结论?并完成下表内容。
实验操作
实验现象
实验原理
实验结论
【对应训练】1.下列现象或用途与浓硫酸的吸水性和脱水性无关的是 ( )
A.浓硫酸可作氯气的干燥剂
B.浓硫酸滴加到蔗糖中,蔗糖变黑
C.浓硫酸滴加到胆矾上,蓝色晶体变成白色粉末
D.浓硫酸在加热条件下可与铜等不活泼金属反应
2.下列各实验相应操作、实验现象及原因解释或推论合理的是 ( )
选项 操作 现象 解释或推论
A 铁片投入浓硫酸 无明显变化 常温下铁不与浓硫酸反应
浓硫酸强氧化性导致纸张中的
B 将浓硫酸滴到白纸上 白纸变黑
纤维素炭化
C 二氧化硫通入溴水 溴水褪色 说明二氧化硫具有漂白性
D 湿润红色石蕊试纸检验某气体 试纸变蓝 该气体是氨气
活动三、浓硫酸的特性本质探析
任务一、结合上述实验,讨论交流浓硫酸的吸水性何脱水性有何不同?
任务二、拓展探究:结合【实验5-3】的实验现象,思考浓硫酸的强氧化性的本质是什么?有何规
律?
①本质:②规律:
任务三、讨论交流:结合浓硫酸的特性,思考鉴别浓硫酸和稀硫酸还有哪些方法?
方法一:
方法二:
方法三:
【对应训练】1.下列事实与原因(括号中)对应关系正确的是( )
A.在空气中敞口久置的浓硫酸,溶液质量增大(浓硫酸具有难挥发性)
B.向某样品溶液中先滴加过量的稀盐酸无现象,再滴加 BaCl 溶液后出现白色沉淀(样品溶液中含有
2
SO)
C.蔗糖与浓硫酸反应中有海绵状的炭生成(浓硫酸具有吸水性)
D.浓硫酸可与铜反应(只显示浓硫酸的强氧化性)
2.下列用来鉴别浓硫酸和稀硫酸的操作错误的是( )
A.分别取10 mL溶液,质量大的是浓硫酸,质量小的是稀硫酸
B.观察液体流动性,流动性好的是稀硫酸,油状黏稠的是浓硫酸
C.把CuSO·5HO晶体投入溶液中,逐渐变为白色粉末的是浓硫酸,晶体溶解的是稀硫酸
4 2
D.将铝片分别投入溶液,快速放出气体的是浓硫酸,放出气体慢的是稀硫酸
【课后巩固】1.下列关于硫酸的工业制备与保存的说法,正确的是( )
A.粉碎后的硫铁矿(FeS )在沸腾炉中燃烧生成SO
2 3
B.在吸收塔中,用质量分数为98.3%的浓硫酸吸收SO
3
C.硫黄制酸法会产生更多的矿渣
D.浓硫酸具有强氧化性,不能保存在铝制容器中
2.关于浓硫酸与Cu反应的叙述正确的是( )A.在反应中,浓硫酸只表现出氧化性
B.该反应中还原剂与氧化剂物质的量之比为1∶2
C.在反应中,浓硫酸既表现出氧化性,又表现出酸性
D.每1 mol 铜参加反应就有2 mol浓硫酸被还原,同时生成2 mol SO
2
3.用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
A.上下移动①中铜丝可控制SO 的量
2
B.②中选用品红溶液验证SO 的生成
2
C.③中选用NaOH溶液吸收多余的SO
2
D.为确认CuSO 生成,向①中加水,观察颜色
4
4.下列实验说明浓硫酸有强腐蚀性的是( )
A.浓硫酸慢慢地注入水中产生大量的热 B.含有水蒸气的氧气通过浓硫酸得到干燥的氧气
C.浓硫酸久置在空气中质量增加 D.用小木棍蘸少量浓硫酸,小木棍变黑
5.下列叙述正确的是( )
A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥有较强还原性的 HI、HS
2
等气体
B.浓硫酸与单质硫反应的方程式为 S+2HSO (浓)=====3SO ↑+2HO,在此反应中,浓硫酸既表现
2 4 2 2
了其强氧化性又表现了其酸性
C.把足量铜粉投入到含2 mol H SO 的浓硫酸中,反应后得到标准状况下气体体积为22.4 L
2 4
D.常温下能够用铁、铝等容器盛放浓HSO ,是因为浓HSO 的强氧化性使其钝化
2 4 2 4
6.如图是检验气体性质的实验装置。向装置中缓慢通入气体X,若关闭活塞K,品红溶液无变化、澄
清石灰水变浑浊;若打开活塞K,品红溶液褪色。据此判断,气体X和液体Y可能是( )
选项
A B C D
物质
X HS SO CO Cl
2 2 2 2
Y 浓硫酸 NaHCO 饱和溶液 NaSO 溶液 NaHSO 溶液
3 2 3 3
7.实验室进行含硫化合物性质探究的装置(夹持装置省略)如图所示,分液漏斗①中盛有浓硫酸,将其
逐滴加入到试管②的固体中。下列说法正确的是( )
A.若②中为NaSO 固体,③中盛石蕊溶液,则③中溶液先变红后褪 色
2 3
B.若②中为蔗糖,③中盛有溴水,能说明浓硫酸具有脱水性和氧化性
C.若②中为NaSO 固体,③中盛有氯化钡溶液,则③中生成白色沉淀
2 3
D.若②中为铜单质,③中盛有硫化氢水溶液,则③中生成黄色沉淀8.浓硫酸能使蔗糖、纸屑、棉花等有机物炭化。在浓硫酸使蔗糖炭化实验中,产生了许多气体使炭
体积膨胀。且闻到有刺激性气味,某同学猜测气体中可能含有SO 和CO 等,为此,该同学设计了如下实
2 2
验装置检验气体的成分。
实验时,在试管中先加入适量的蔗糖(C H O ),再滴入少量的水,混匀,最后加入一定量的浓硫
12 22 11
酸,迅速塞好橡皮塞,振荡试管,将产生的气体通过甲、乙、丙、丁四个洗气瓶。
(1)滴加少量水的目的是为了使反应温度迅速升高,以利于反应进行,写出该试管中产生气体的化学方
程式_______。该实验中体现的浓硫酸的特性是_______。
(2)装置乙中的酸性KMnO 溶液的作用是_______,不能用饱和NaHCO 溶液代替酸性KMnO 溶液的理
4 3 4
由是_______。
(3)产物中含有CO 的实验现象是:_______;对应的离子方程式:
2
_______________________________。