文档内容
第五章 化工生产中的重要非金属元素
第一节 硫及其化合物 课时作业
第二课时 硫酸
基础达标
1.区别浓硫酸和稀硫酸,既简单又可靠的方法是( )
A.常温下与铜片反应 B.与石蕊溶液反应
C.用玻璃棒各蘸少许溶液涂在纸上 D.加入锌片看是否有气体生成
【答案】C
【解析】常温下浓硫酸和稀硫酸都不能与Cu反应;锌与浓硫酸反应产生SO ,与稀硫
2
酸反应产生H ,可以区别,但不是最简单的方法;C项利用浓硫酸有脱水性而稀硫酸没有
2
脱水性来区分两种溶液,较简单。
2.下列叙述或操作中正确的是( )
A.浓硫酸能使硫酸铜晶体失去结晶水,体现了浓硫酸的脱水性
B.浓硫酸对有机物的腐蚀性是浓硫酸脱水性和强氧化性的综合体现
C.浓硫酸具有氧化性,稀硫酸无氧化性
D.浓硫酸不慎沾到皮肤上,应立即用布拭去,再涂上稀NaOH溶液
【答案】B
【解析】浓硫酸使硫酸铜晶体失去结晶水体现浓硫酸的吸水性,A错误;稀硫酸中的
H+具有较弱的氧化性,C错误;NaOH本身具有强腐蚀性,不能涂在皮肤上中和消除浓硫
酸的腐蚀作用,D错误。
3.下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.蓝色胆矾晶体滴加浓硫酸时变为白色固体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.常温下,浓硫酸不与铁、铝反应,所以可以用铁、铝制容器盛装浓硫酸
【答案】B
【解析】浓硫酸具有脱水性,使蔗糖中H、O元素以水的形式脱出,而使蔗糖炭化变
黑,与吸水性无关,A错误;浓硫酸具有吸水性,能吸收胆矾晶体中的结晶水,可以使蓝
色的胆矾晶体失水变为白色晶体,B正确;浓硫酸是一种酸,能和氨气反应,故不能干燥
氨气,C错误;由于浓硫酸的氧化性很强,常温下,铁和铝的表面被氧化为致密的氧化
膜,D错误。
4.下列用来鉴别浓硫酸和稀硫酸的操作错误的是( )
A.分别取10 mL溶液,质量大的是浓硫酸,质量小的是稀硫酸B.观察液体流动性,流动性好的是稀硫酸,油状黏稠的是浓硫酸
C.把CuSO ·5H O晶体投入溶液中,逐渐变为白色粉末的是浓硫酸,晶体溶解的是稀
4 2
硫酸
D.将铝片分别投入溶液,快速放出气体的是浓硫酸,放出气体慢的是稀硫酸
【答案】D
【解析】因浓硫酸的密度大于稀硫酸的密度,则体积相同时质量大的是浓硫酸,则可
以鉴别,故A正确;浓硫酸是油状黏稠的液体,稀硫酸是稀溶液,则可利用液体流动性来
鉴别,故B正确;因浓硫酸具有吸水性,可使CuSO ·5H O晶体失去水而变为白色粉末,
4 2
但稀硫酸不能,则可以鉴别,故C正确;因Al在浓硫酸中发生钝化,与稀硫酸快速反应生
成气体,则放出气体快的是稀硫酸,故D错误。
5.在实验探究课上,同学们积极思考,设计出如图所示四种实验方案用以验证浓硫酸
的吸水性,其中在理论上可行的是( )
A.①②③④ B.仅①②③
C.仅①③④ D.仅②③④
【答案】图①梨失水变干表现出浓硫酸的吸水性;图②可通过胆矾晶体变白说明浓硫
酸具有吸水性;图③通过观察KNO 晶体析出说明浓硫酸具有吸水性;图④浓硫酸的液面
3
上升,水的液面下降,说明浓硫酸具有吸水性。
6.下列关于浓硫酸的说法正确的是( )
A.金属铜在常温下放入浓硫酸中无现象,是因为浓硫酸把铜钝化了
B. 的浓硫酸和足量 在加热条件下反应生成
C.蔗糖和浓硫酸的“黑面包”实验中,浓硫酸主要体现了脱水性和强氧化性
D.浓硫酸和C单质在加热条件下反应,反应中浓硫酸既体现出酸性,又体现出氧化
性
【答案】C
【解析】A.常温下,铜和浓硫酸不反应,所以放入浓硫酸中无现象,铜在浓浓硫酸
中不钝化,故A错误;B.100mL18mol/L的浓硫酸和足量Cu在加热条件下反应,硫酸浓
度不断降低,铜和稀硫酸不反应,参加反应的硫酸小于1.8mol,所以生成的SO 小于
2
0.9mol,故B错误;C.蔗糖和浓硫酸的“黑面包”实验中,蔗糖变黑并有气体生成,浓硫
酸主要体现了脱水性和强氧化性,故C正确;D.浓硫酸和C单质在加热条件下反应生成
二氧化碳、二氧化硫、水,反应中浓硫酸只体现氧化性,故D错误;选C。7.下列反应中,浓硫酸既表现强氧化性,又表现酸性的是( )
①2NaCl(固)+HSO (浓)=====NaSO +2HCl↑
2 4 2 4
②C+2HSO (浓)=====CO↑+2SO ↑+2HO
2 4 2 2 2
③Cu+2HSO (浓)=====CuSO +SO ↑+2HO
2 4 4 2 2
④2FeO+4HSO (浓)===Fe (SO )+SO ↑+4HO
2 4 2 4 3 2 2
A.①② B.③④
C.①③ D.②④
【解析】选B 金属、金属氧化物(具有变价的金属元素处于低价态)与浓HSO 反应
2 4
时,浓HSO 既表现强氧化性又表现酸性;非金属与浓HSO 反应时,浓HSO 只表现强
2 4 2 4 2 4
氧化性。
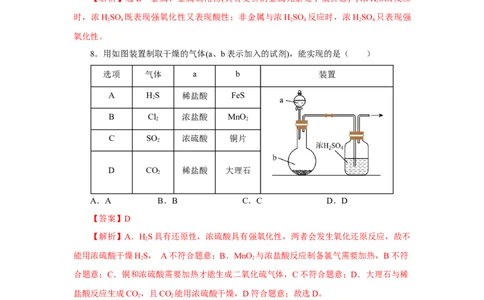
8.用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是( )
选项 气体 a b 装置
A HS 稀盐酸 FeS
2
B Cl 浓盐酸 MnO
2 2
C SO 浓硫酸 铜片
2
D CO 稀盐酸 大理石
2
A.A B.B C.C D.D
【答案】D
【解析】A.HS具有还原性,浓硫酸具有强氧化性,两者会发生氧化还原反应,故不
2
能用浓硫酸干燥HS, A不符合题意;B.MnO 与浓盐酸反应制备氯气需要加热,B不符
2 2
合题意;C.铜和浓硫酸需要加热才能生成二氧化硫气体,C不符合题意;D.大理石与稀
盐酸反应生成CO,且CO 能用浓硫酸干燥,D符合题意;故选D。
2 2
9.下列变化的本质相似的是( )
A.浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
B.SO 和Cl 均能能使品红溶液褪色
2 2
C.浓HSO 和稀HSO 与金属反应时均有气体放出
2 4 2 4
D.HS和HI气体均不能用浓硫酸干燥
2
【答案】D
【解析】A.浓硫酸具有吸水性,敞口放置时浓度减小,浓盐酸易挥发,敞口放置时浓度减小,二者本质不同,A错误;B.SO 和有色物质生成不稳定无色物质而使品红溶液
2
褪色,Cl 与水反应生成的次氯酸具有强氧化性而使品红溶液褪色,二者本质不同,B错
2
误;C.浓HSO 与金属反应放出气体体现酸性和强氧化性,生成二氧化硫气体,稀HSO
2 4 2 4
与金属反应生成氢气,二者本质不同,C错误;D.HS和HI气体均具有还原性,会被浓
2
硫酸氧化而不能用浓硫酸干燥,二者本质相似,D正确;故选D。
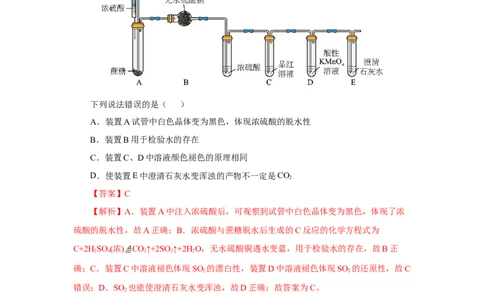
10.某学生设计了一种检验浓硫酸与蔗糖反应产物的实验,装置如图所示:
下列说法错误的是( )
A.装置A试管中白色晶体变为黑色,体现浓硫酸的脱水性
B.装置B用于检验水的存在
C.装置C、D中溶液颜色褪色的原理相同
D.使装置E中澄清石灰水变浑浊的产物不一定是CO
2
【答案】C
【解析】A.装置A中注入浓硫酸后,可观察到试管中白色晶体变为黑色,体现了浓
硫酸的脱水性,故A正确;B.浓硫酸与蔗糖脱水后生成的C反应的化学方程式为
C+2H
2
SO
4
(浓)≜CO
2
↑+2SO
2
↑+2H
2
O,无水硫酸铜遇水变蓝,用于检验水的存在,故B正
确;C.装置C中溶液褪色体现SO 的漂白性,装置D中溶液褪色体现SO 的还原性,故C
2 2
错误;D.SO 也能使澄清石灰水变浑浊,故D正确;故答案为C。
2
能力提升
11.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.100g46%的乙醇溶液中含有氧原子数为4N
A
B.标准状况下,22.4L由O 与O 组成的混合气体含有的氧原子数目为N
2 3 A
C.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
AD.常温常压下,含2molH SO 的浓硫酸与足量铜共热,转移的电子数为2N
2 4 A
【答案】A
【解析】A.100g46%的乙醇溶液中,含有乙醇的质量为:100g×46%=46g,含有氧原
46g 54g
子数为 ×N =N ;含有水的质量为100g-46g=54g,含有氧原子数为
46g/mol A A 18g/mol
×3×N =3N ,所以100g46%的乙醇溶液中含有氧原子数为3N +N =4N ,故A正确;B.标
A A A A A
22.4L
准状况下,22.4LQ 中含有的氧原子数目为 ×2×N =2N ;22.4LO 中含有的氧
2 22.4L/mol A A 3
22.4L
原子数目为 ×3×N =2N ,所以,22.4L由O 与O 组成的混合气体含有的氧原
22.4L/mol A A 2 3
子数目为2N