文档内容
第三章 烃的衍生物
第三节 醛、酮
第一课时 醛 课时作业
基础达标
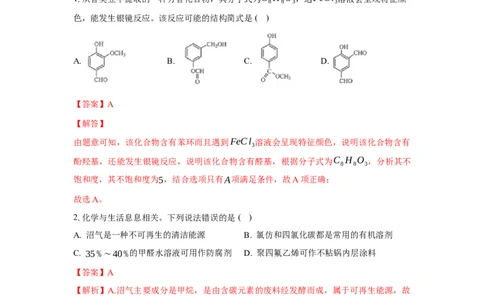
1.从香荚豆中提取的一种芳香化合物,其分子式为C H O ,遇FeCl 溶液会呈现特征颜
8 8 3 3
色,能发生银镜反应。该反应可能的结构简式是( )
A. B. C. D.
【答案】A
【解答】
由题意可知,该化合物含有苯环而且遇到FeCl 溶液会呈现特征颜色,说明该化合物含有
3
酚羟基,还能发生银镜反应,说明该化合物含有醛基,根据分子式为C H O ,分析其不
8 8 3
饱和度,其不饱和度为5,结合选项只有A项满足条件,故A项正确;
故选A。
2.化学与生活息息相关。下列说法错误的是( )
A. 沼气是一种不可再生的清洁能源 B. 氯仿和四氯化碳都是常用的有机溶剂
C. 35%∼40%的甲醛水溶液可用作防腐剂 D. 聚四氟乙烯可作不粘锅内层涂料
【答案】A
【解析】A.沼气主要成分是甲烷,是由含碳元素的废料经发酵而成,属于可再生能源,故
A错误;
B.氯仿、四氯化碳都为液态有机物,都是常用的有机溶剂,故B正确;
C.甲醛能使蛋白质变性,起到防腐的作用,常用35%∼40%的甲醛水溶液(福尔马林)保存
动植物标本,故C正确;
D.化学性质稳定的聚四氟乙烯耐高温,可作耐高温的不粘锅内层涂料,故D正确;
故选A。
3.下列反应的反应类型与“乙烯水化法合成乙醇”的原理相同的是( )A. 苯和液溴反应制溴苯
B. 乙醛与新制Cu(OH) 共热产生砖红色沉淀
2
C. 乙烯和浓硫酸在140℃共热制乙醚
D. 苯和H 反应制环己烷
2
【答案】D
4.下列化学用语表达正确的是( )
A. 氧的基态原子的轨道表示式:
B. 甲烷分子和四氯化碳分子的空间填充模型均为:
C. CH CH(CH )CH COOH的名称:2−甲基丁酸
3 3 2
D. CH OH分子中,碳原子与氧原子之间的共价键:sp3−pσ键
3
【答案】A
【解答】
A.核外电子排布要符合洪特规则,即电子在同一能级的不同轨道上排布时,电子总是各优
先占据一个轨道,且自旋平行,而根据泡利原理,而同一轨道最多容纳两个电子,且自旋
方 向 相 反 , 氧 原 子 核 外 电 子 排 布 式 为 1s22s22p4, 原 子 的 轨 道 表 示 式 为
,正确;
B.四氯化碳分子为正四面体构型,但氯原子半径大于C原子半径,故其空间填充模型为
,错误;
C.CH CH(CH )CH COOH正确命名:3−甲基丁酸,错误;
3 3 2
D.CH OH分子中,碳原子与氧原子之间为共价单键,碳原子的p轨道与氧原子的p轨道
3
重叠形成的p−pσ键,错误。5. 由溴乙烷制 下列流程途径合理的是( )
①加成反应 ②取代反应 ③消去反应 ④氧化反应 ⑤还原反应
A. ②③①④② B. ③①②④② C. ③①②④⑤ D. ②④⑤②②
【答案】B
【解答】
溴乙烷发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2−二溴乙烷,1,2−二溴
乙烷发生取代反应生成乙二醇,乙二醇连续氧化生成乙二酸,乙二酸和乙二醇发生取代反
应(酯化反应)生成乙二酸乙二酯。故B正确。
故选B。
6.两种烃的衍生物A和B,所含碳、氢、氧的质量比均为6:1:4,完全燃烧0.1molA能生
成3.6g水。B只含一个醛基,1.1gB与足量银氨溶液反应,可析出2.7gAg。则下列关于
物质A和B的判断正确的是( )
A. 物质A一定是乙醛
B. 物质B的分子式为C H O
4 8 2
C. 物质B的同分异构体中既含有醛基又含有羟基的有6种
D. 物质A和B互为同分异构体
【答案】B
【解答】
6 1 4
A和B中m(C):m(H):m(O)=6:1:4,则N(C):N(H):N(O)= : : =2:4:1,最简
12 1 16
3.6g
式为C H O。完全燃烧0.1molA能生成3.6g水,n(H O)= =0.2mol,A分
2 4 2 18g/mol
0.2mol×2
子中N(H)= =4,则A的分子式为C H O。B只含有一个醛基,1.1gB与足
0.1mol 2 4
2.7g
量 银 氨 溶 液 反 应 析 出 2.7gAg, n(Ag)= =0.025mol, 由 关 系 式
108g/mol
1
R—CHO∼2Ag可 知 , 1.1gB的 物 质 的 量 为 0.025mol× =0.0125mol,
21.1g
Mr(B)= =88g/mol,令B的分子式为(C H O) ,则44n=88,n=2,B的
0.0125mol 2 4 n
分子式为C H O 。
4 8 2
A错,A的分子式为C H O,可能为乙醛,也可能为环氧乙烷。
2 4
C错,B的分子式为C H O ,若B是C—C—C—CHO型醛,—OH存在时有3种结构;
4 8 2
若B是 型醛,—OH存在时有2种结构,故共有5种。
D错,A和B的分子式不同,不可能互为同分异构体。
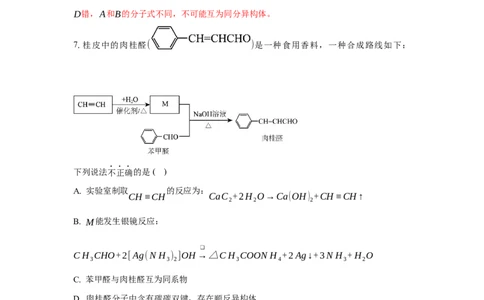
7.桂皮中的肉桂醛( )是一种食用香料,一种合成路线如下:
下列说法不正确的是( )
A. 实验室制取 的反应为:
CH≡CH CaC +2H O→Ca(OH) +CH≡CH↑
2 2 2
B. M能发生银镜反应:
❑
CH CHO+2[Ag(N H ) ]OH→△CH COON H +2Ag↓+3N H +H O
3 3 2 3 4 3 2
C. 苯甲醛与肉桂醛互为同系物
D. 肉桂醛分子中含有碳碳双键,存在顺反异构体
【答案】C
【解答】
乙炔和水发生加成反应生成M为CH CHO,乙醛和苯甲醛发生加成、脱水消去反应生成
3
肉桂醛。
A.实验室用碳化钙和水反应制取乙炔,同时还生成氢氧化钙,反应方程式为
CaC +2H O→Ca(OH) +CH≡CH↑,故A正确;
2 2 2B.M为乙醛,乙醛发生银镜反应生成乙酸铵、氨气、 Ag和水,M能发生银镜反应:
△ ,故 B 正确;
CH CHO+2[Ag(N H ) ]OH→CH COON H +2Ag↓+3N H +H O
3 3 2 3 4 3 2
C.二者结构不相似,所以不互为同系物,故C错误;
D.肉桂醛分子中碳碳双键两端的碳原子连接两个不同的原子或原子团,所以存在顺反异构,
故D正确。
8.两种烃的衍生物A和B,所含碳、氢、氧的质量比均为6:1:4,完全燃烧0.1molA能
生成3.6g水。B只含一个醛基,1.1gB与足量银氨溶液反应,可析出2.7gAg。则下列关
于物质A和B的判断正确的是( )
A. 物质A一定是乙醛
B. 物质B的分子式为C H O
4 8 2
C. 物质B的同分异构体中既含有醛基又含有羟基的有6种
D. 物质A和B互为同分异构体
【答案】B
【解析】两种烃的衍生物A和B,所含碳、氢、氧的质量比均为6:1:4,C、H、O原子
6 1 4
数目之比为 : : =2:4:1,有机物的最简式为C H O。完全燃烧0.1molA能生成
12 1 16 2 4
3.6g 0.2mol×2
3.6g水,n(H O)= =0.2mol,故A分子中H原子数目为 =4,则A
2 18g/mol 0.1mol
的分子式为C H O。B只含有一个醛基,1.1gB与足量银氨溶液反应析出2.7gAg,
2 4
2.7g
n(Ag)=
108g/mol
=0.025mol,由关系式
R−CHO❑
̃(cid:31)
2Ag
可知,1.1gB的物质的量为
1 1.1
0.025mol× =0.0125mol, B的 相 对 分 子 质 量 为 =88, 令 B分 子 式 为
2 0.0125
(C H O)n,则44n=88,n=2,则B的分子式为C H O 。
2 4 4 8 2
A错,物质A的分子式为C H O,可能为乙醛,也可能为乙烯醇。
2 4
C错,B为C H O ,含有一个—CHO,还含有—OH,可以看作丙烷分子中的两个H被
4 8 2
—CHO、—OH取代,CH CH CH 分子中的一个H被—CHO取代有2种,分别为
3 2 3
CH CH CH CHO和(CH ) CHCHO,烃基上的H被—OH取代,前者有3种结构,
3 2 2 3 2后者有2种结构,共5种。
D错,两者分子式不同,不可能互为同分异构体。
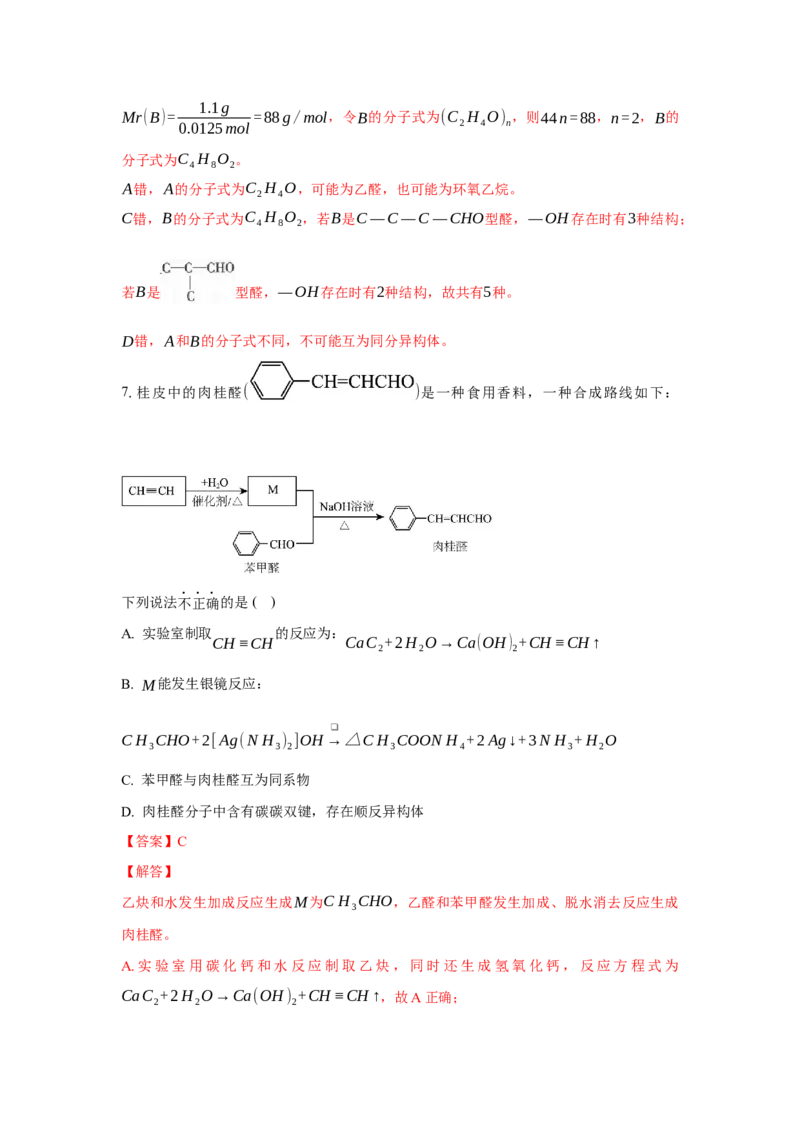
9.有机物R的结构简式如下所示,下列叙述正确的是( )
A. R的所有原子一定在同一平面上
B. 在Ni催化和加热条件下,1molR能与5molH 发生加成反应
2
C. R既能与羧酸、醇反应,还能发生加成、氧化反应
D. 1molR与足量氢氧化钠溶液反应,消耗氢氧化钠的物质的量为2mol
【答案】C
【解答】
A.R含有饱和碳原子,不可能所有的原子共平面,故A错误;
B.R中能与H 反应的有醛基和苯环,则在Ni催化和加热条件下,1molR能与4molH 发
2 2
生加成反应,故B错误;
C.R含有羧基和醇羟基,能与羧酸、醇反应,含有醛基,能发生加成、氧化反应,故 C正
确;
D.能与NaOH溶液反应的只有羧基,则1molR与足量NaOH溶液反应,消耗NaOH的物
质的量为1mol,故D错误。
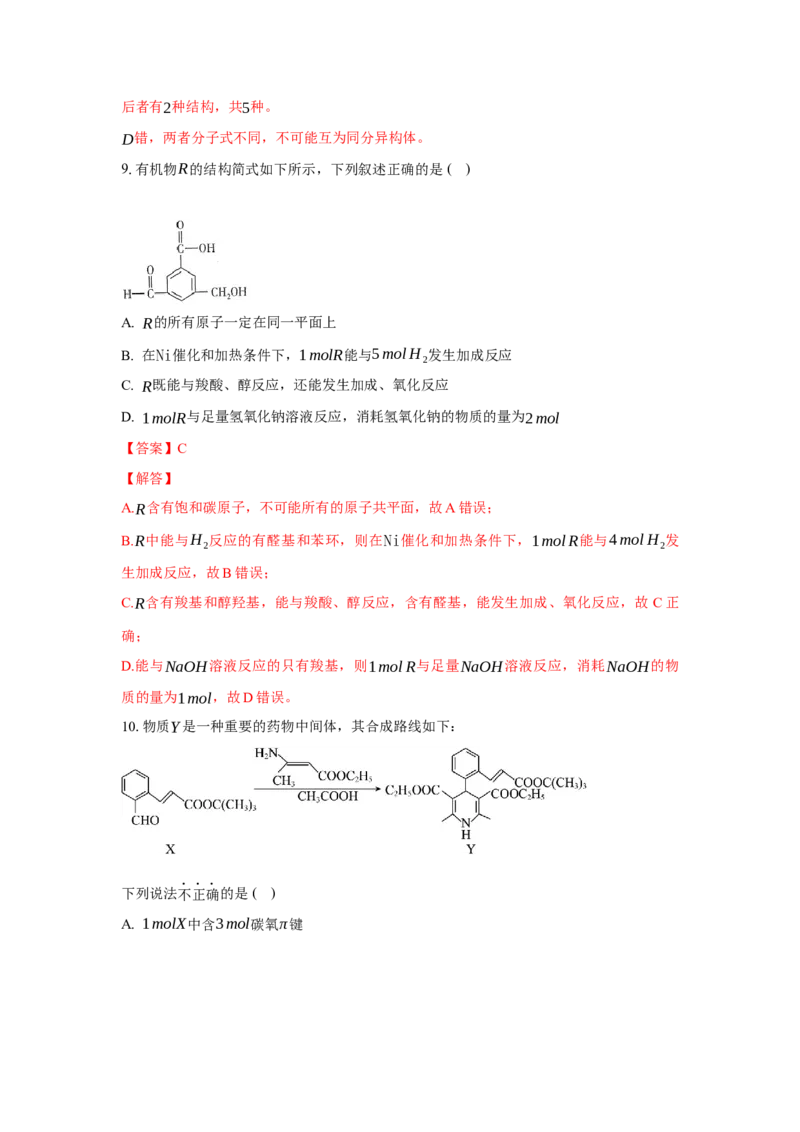
10.物质Y是一种重要的药物中间体,其合成路线如下:
下列说法不正确的是( )
A. 1molX中含3mol碳氧π键B. X与 互为顺反异构体
C. Y分子中不含有手性碳原子
D. 可用新制的Cu(OH) 检验Y中是否有X
2
【答案】A
【解答】
A. 由X的结构简式可知,1molX中含2mol碳氧π键。故错误;
B.由结构简式可知,X与 互为顺反异构体,故正确;
C.一个碳原子连接了四个不同的基团,这个C原子是手性碳原子。Y分子中不含有手性碳原
子,故正确;
D.因为X中的醛基可以与新制的Cu(OH) 反应生成砖红色沉淀,而Y中没有醛基,不会有
2
此反应,可用新制的Cu(OH) 检验Y中是否有X,故正确。
2
11.“宏观辨识与微观探析”是学科核心素养之一,下列离子方程式正确且符合题意的是(
)
A. 在过量银氨溶液中滴加甲醛溶液并加热:
❑
2[Ag(N H ) ] ++2OH−+HCHO→△2Ag↓+HCOO−+N H++H O+3N H
3 2 4 2 3
通电
B. 用铜片作电极,电解饱和食盐水:2H O+2Cl− ̃# H ↑+Cl ↑+2OH−
2 ̃# 2 2
C. 下水道堵塞用铝粉和烧碱溶液疏通:
2Al+2OH−+2H O=2AlO−+3H ↑
2 2 2
D. 向过量的 溶液中滴加少量“ ”消毒液:
NaHSO 84 HSO−+ClO−=SO2−+H++Cl−
3 3 4【答案】C
【解析】A.甲酸铵含醛基,能与银氨溶液反应,A项错误;
B.铜为电极,阳极上Cu发生反应,B项错误;
C.铝与氢氧化钠溶液反应生成氢气,C项正确;
D. 次 氯 酸 钠 与 过 量 亚 硫 酸 氢 钠 反 应 , 离 子 方 程 式 为
2HSO−+ClO− ̃# SO2−+Cl−+SO ↑+H O ,D项错误;
3 ̃# 4 2 2
故选C。
12.下列实验操作、现象及结论均正确的是( )
选项 实验操作 实验现象 结论
将铁锈溶于浓盐酸,滴入酸性KMnO 溶
A 4 紫色褪去 铁锈中含有Fe2+
液
向盛有1mL0.1mol·L−1AgNO
溶液的
3
先 产 生 白 色 沉
试 管 中 滴 加 2mL0.1mol·L−1NaCl溶
B 淀,后产生黄色K (AgCl)>K (AgI)
液 , 再 向 其 中 加 入 4~5滴 sp sp
沉淀
0.1mol·L−1KI溶液
向蔗糖溶液中滴加稀硫酸,水浴加热,无砖红色沉淀生
C 蔗糖未发生水解
加入少量的新制氢氧化铜悬浊液 成
加热盛有少量N H HCO 固体的试管并
D 4 3 试纸变蓝 N H HCO 显碱性
在试管口放置湿润的红色石蕊试纸 4 3
A. A B. B C. C D. D
【答案】B
【解答】
A.浓盐酸中的氯离子可以还原酸性KMnO 溶液,也可以使紫色褪去,不能判断铁锈中是
4
否含有Fe2+,A项错误;
B.该实验中NaCl过量,向AgNO 溶液滴加溶液NaCl溶液,先产生白色沉淀,再滴加KI
3
溶液,有黄色沉淀生成,说明发生了反应 ,从而证
AgCl(s)+I− (aq)=AgI(s)+Cl− (aq)
明K (AgCl)>K (AgI),B项正确;
sp sp
C.葡萄糖与新制氢氧化铜的反应是在碱性条件下进行的,因此需要先中和硫酸再进行反应,
C项错误;D.N H HCO 固体分解产生的氨气能使湿润的红色石试纸变蓝,不能证明N H HCO 显
4 3 4 3
碱性,D项错误.
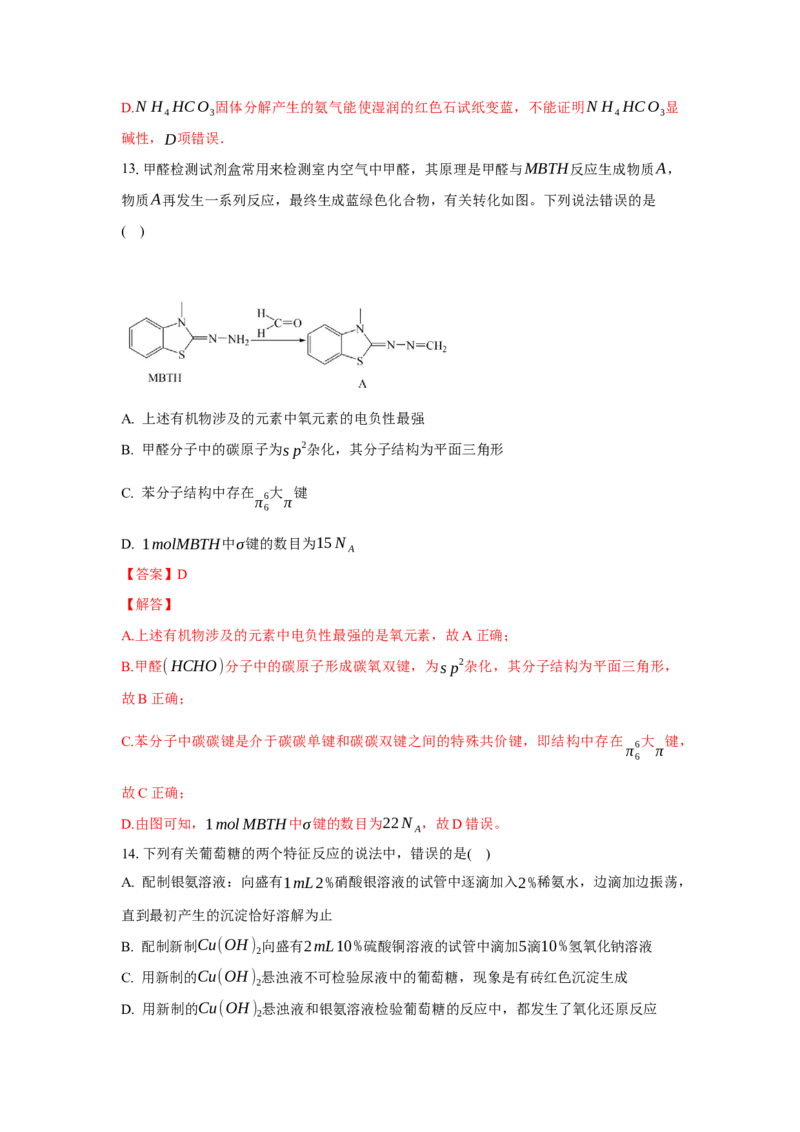
13.甲醛检测试剂盒常用来检测室内空气中甲醛,其原理是甲醛与MBTH反应生成物质A,
物质A再发生一系列反应,最终生成蓝绿色化合物,有关转化如图。下列说法错误的是
( )
A. 上述有机物涉及的元素中氧元素的电负性最强
B. 甲醛分子中的碳原子为sp2杂化,其分子结构为平面三角形
C. 苯分子结构中存在 大 键
π6 π
6
D. 1molMBTH中σ键的数目为15N
A
【答案】D
【解答】
A.上述有机物涉及的元素中电负性最强的是氧元素,故A正确;
B.甲醛(HCHO)分子中的碳原子形成碳氧双键,为sp2杂化,其分子结构为平面三角形,
故B正确;
C.苯分子中碳碳键是介于碳碳单键和碳碳双键之间的特殊共价键,即结构中存在 大 键,
π6 π
6
故C正确;
D.由图可知,1molMBTH中σ键的数目为22N ,故D错误。
A
14.下列有关葡萄糖的两个特征反应的说法中,错误的是( )
A. 配制银氨溶液:向盛有1mL2%硝酸银溶液的试管中逐滴加入2%稀氨水,边滴加边振荡,
直到最初产生的沉淀恰好溶解为止
B. 配制新制Cu(OH) 向盛有2mL10%硫酸铜溶液的试管中滴加5滴10%氢氧化钠溶液
2
C. 用新制的Cu(OH) 悬浊液不可检验尿液中的葡萄糖,现象是有砖红色沉淀生成
2
D. 用新制的Cu(OH) 悬浊液和银氨溶液检验葡萄糖的反应中,都发生了氧化还原反应
2【答案】B
能力提升
15.化合物a和b都是合成抗肝病药莳萝脑的中间体,其相互转化关系如下。下列说法错误
的是( )
A. a和b分子中所有原子均可能处于同一平面上
B. a、b分子中均无手性碳原子
C. 可用FeCl 溶液鉴别a和b
3
D. a、b均能与新制的Cu(OH) 在加热煮沸条件下反应产生砖红色沉淀
2
【答案】A
【解答】
有机物a含有醛基,可发生加成、氧化反应,含有酚羟基,可发生取代、氧化反应,b与a
相比较,含有醛基和碳碳双键,碳碳双键可发生加成、加聚和氧化反应,以此解答该题。
A.a、b均含有甲基,具有甲烷的结构特点,则所有原子不能处于同一平面上,故A错误;
B.手性原子连接4个不同的原子或原子团,则a、b 分子中均无手性碳原子,故B正确;
C.a含有酚羟基,可与氯化铁发生显色反应,b不反应,故C正确;
D.a、b都含有醛基,均能与新制的Cu(OH) 在加热煮沸条件下反应产生砖红色沉淀,故
2
D正确。
16.下列说法不正确的是( )
A. 植物油氢化后所得的硬化油不易被空气氧化变质,可作为制造肥皂的原料
B. 向饱和(N H ) SO 溶液中滴加几滴鸡蛋清溶液,出现沉淀,加蒸馏水后沉淀溶解
4 2 4
C. 酸催化下,nmol苯酚与nmol甲醛反应生成线型酚醛树脂,同时生成(2n−1)molH O
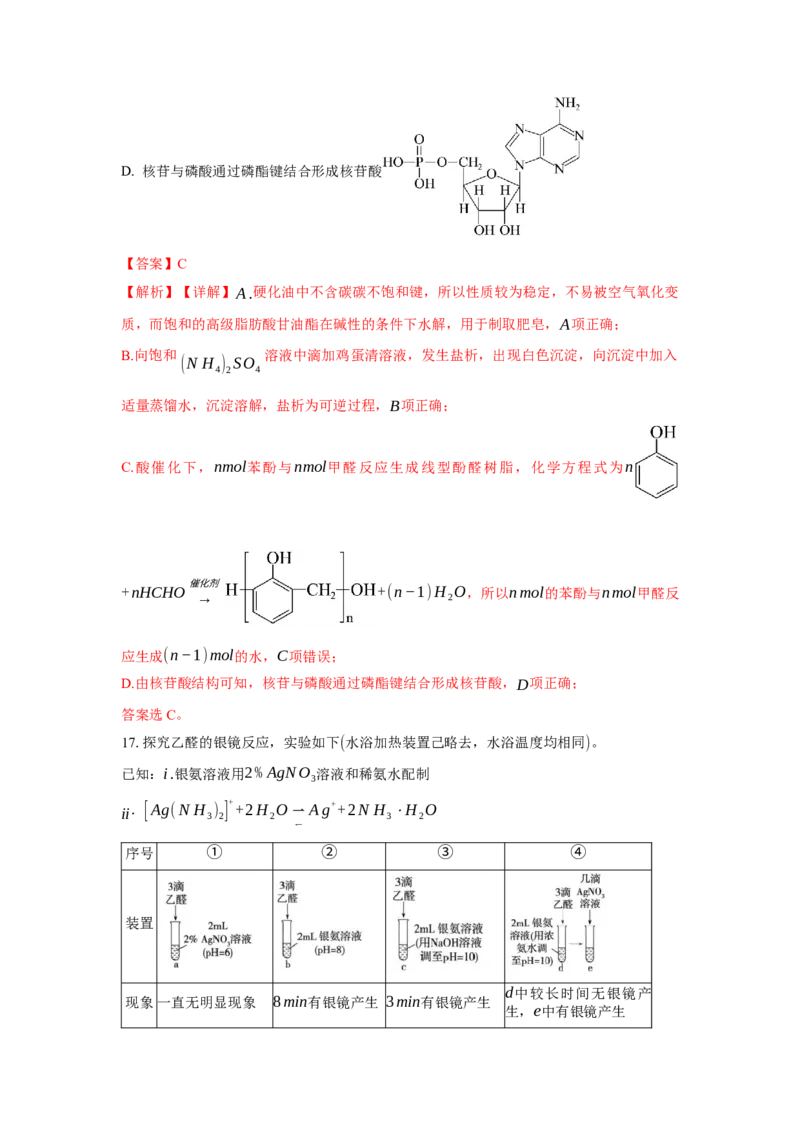
2D. 核苷与磷酸通过磷酯键结合形成核苷酸
【答案】C
【解析】【详解】A.硬化油中不含碳碳不饱和键,所以性质较为稳定,不易被空气氧化变
质,而饱和的高级脂肪酸甘油酯在碱性的条件下水解,用于制取肥皂,A项正确;
B.向饱和 溶液中滴加鸡蛋清溶液,发生盐析,出现白色沉淀,向沉淀中加入
(N H ) SO
4 2 4
适量蒸馏水,沉淀溶解,盐析为可逆过程,B项正确;
C.酸催化下,nmol苯酚与nmol甲醛反应生成线型酚醛树脂,化学方程式为n
+nHCHO 催化剂 +(n−1)H O,所以nmol的苯酚与nmol甲醛反
→ 2
应生成(n−1)mol的水,C项错误;
D.由核苷酸结构可知,核苷与磷酸通过磷酯键结合形成核苷酸,D项正确;
答案选C。
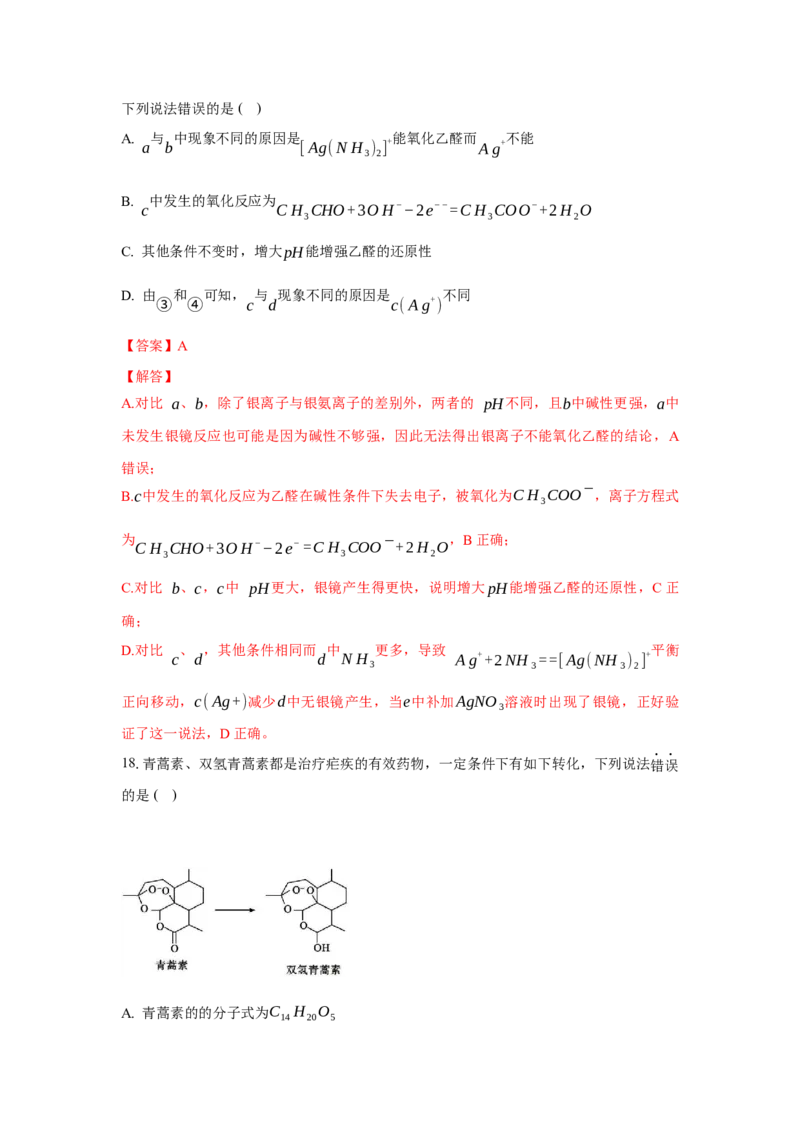
17.探究乙醛的银镜反应,实验如下(水浴加热装置己略去,水浴温度均相同)。
已知:i.银氨溶液用2%AgNO 溶液和稀氨水配制
3
ii.[Ag(N H ) ] + +2H O⇀Ag++2N H ⋅H O
3 2 2 3 2
↽
序号 ① ② ③ ④
装置
d中较长时间无银镜产
现象一直无明显现象 8min有银镜产生 3min有银镜产生
生,e中有银镜产生下列说法错误的是( )
A. 与 中现象不同的原因是 能氧化乙醛而 不能
a b [Ag(N H ) ] + Ag+
3 2
B. 中发生的氧化反应为
c CH CHO+3OH−−2e−−=CH COO−+2H O
3 3 2
C. 其他条件不变时,增大pH能增强乙醛的还原性
D. 由 和 可知, 与 现象不同的原因是 不同
③ ④ c d c(Ag+ )
【答案】A
【解答】
A.对比 a、b,除了银离子与银氨离子的差别外,两者的 pH不同,且b中碱性更强,a中
未发生银镜反应也可能是因为碱性不够强,因此无法得出银离子不能氧化乙醛的结论,A
错误;
B.c中发生的氧化反应为乙醛在碱性条件下失去电子,被氧化为CH COO¯,离子方程式
3
为 ,B正确;
CH CHO+3OH−−2e−=CH COO¯ +2H O
3 3 2
C.对比 b、c,c中 pH更大,银镜产生得更快,说明增大pH能增强乙醛的还原性,C正
确;
D.对比 、 ,其他条件相同而 中 更多,导致 平衡
c d d N H Ag++2NH₃==[Ag(NH₃)₂] +
3
正向移动,c(Ag+)减少d中无银镜产生,当e中补加AgNO₃溶液时出现了银镜,正好验
证了这一说法,D正确。
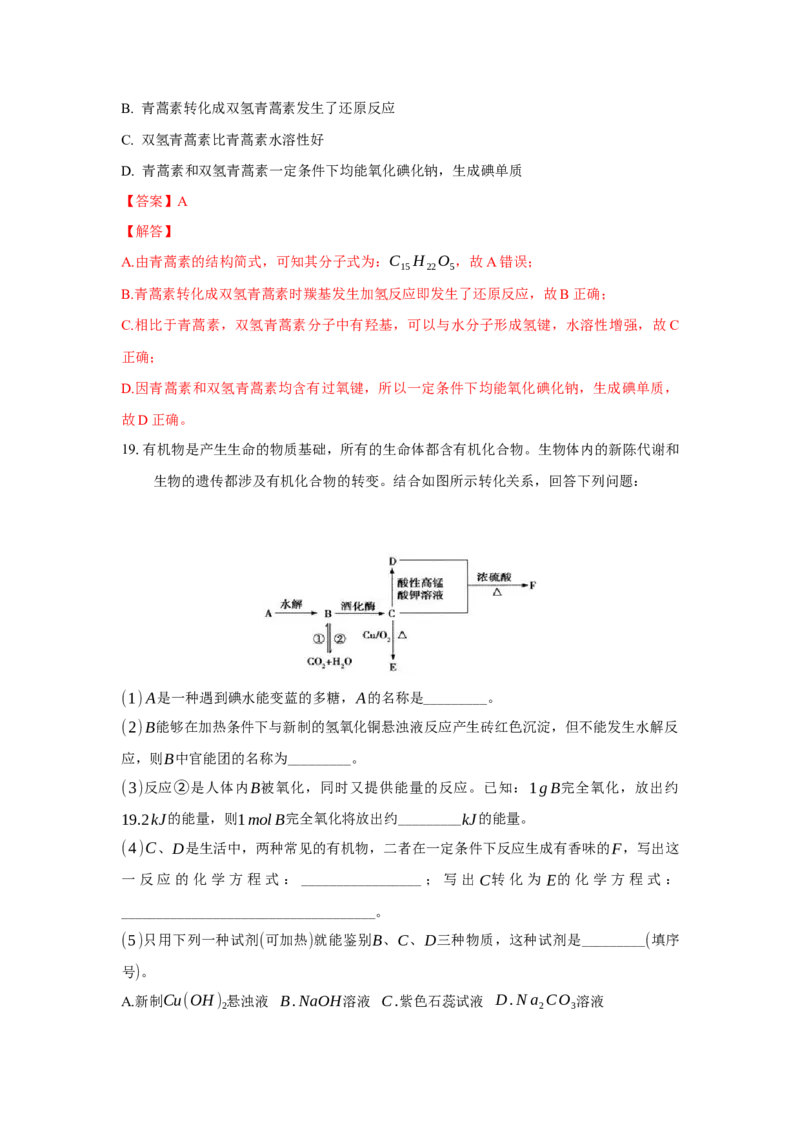
18.青蒿素、双氢青蒿素都是治疗疟疾的有效药物,一定条件下有如下转化,下列说法错误
的是( )
A. 青蒿素的的分子式为C H O
14 20 5B. 青蒿素转化成双氢青蒿素发生了还原反应
C. 双氢青蒿素比青蒿素水溶性好
D. 青蒿素和双氢青蒿素一定条件下均能氧化碘化钠,生成碘单质
【答案】A
【解答】
A.由青蒿素的结构简式,可知其分子式为:C H O ,故A错误;
15 22 5
B.青蒿素转化成双氢青蒿素时羰基发生加氢反应即发生了还原反应,故B正确;
C.相比于青蒿素,双氢青蒿素分子中有羟基,可以与水分子形成氢键,水溶性增强,故C
正确;
D.因青蒿素和双氢青蒿素均含有过氧键,所以一定条件下均能氧化碘化钠,生成碘单质,
故D正确。
19.有机物是产生生命的物质基础,所有的生命体都含有机化合物。生物体内的新陈代谢和
生物的遗传都涉及有机化合物的转变。结合如图所示转化关系,回答下列问题:
(1)A是一种遇到碘水能变蓝的多糖,A的名称是_________。
(2)B能够在加热条件下与新制的氢氧化铜悬浊液反应产生砖红色沉淀,但不能发生水解反
应,则B中官能团的名称为_________。
(3)反应②是人体内B被氧化,同时又提供能量的反应。已知:1gB完全氧化,放出约
19.2kJ的能量,则1molB完全氧化将放出约_________kJ的能量。
(4)C、D是生活中,两种常见的有机物,二者在一定条件下反应生成有香味的F,写出这
一反应的化学方程式: _________________;写出C转化为 E的化学方程式:
____________________________________。
(5)只用下列一种试剂(可加热)就能鉴别B、C、D三种物质,这种试剂是_________(填序
号)。
A.新制Cu(OH) 悬浊液 B.NaOH溶液 C.紫色石蕊试液 D.Na CO 溶液
2 2 3【答案】(1)淀粉
(2)醛基、羟基
(3)3456
(4)CH COOH+C H OH CH COOC H +H O;
3 2 5 3 2 5 2
❑
2CH CH OH+O →2CH CHO+2H O
3 2 2 3 2
❑
(5)A
【解答】
(1)遇碘变蓝色的多糖是淀粉,所以A的名称是淀粉;
故答案为:淀粉;
(2)淀粉水解的最终产物是葡萄糖,能够在加热条件下与新制的氢氧化铜悬浊液反应产生
砖红色沉淀,但本身不能发生水解反应,所以B是葡萄糖,分子中含有的官能团的名称是
醛基、羟基;
故答案为:醛基、羟基;
(3)1mol葡萄糖的质量是180g,所以1molB完全氧化将放出约180×19.2kJ=3456kJ的
能量;
故答案为:3456;
(4)葡萄糖在酒化酶作用下转化为乙醇,所以C是乙醇,乙醇被酸性高锰酸钾溶液氧化得乙
酸,则D是乙酸,乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯和水,化
CH COOH+C H OH CH COOC H +H O Cu
学方程式为 3 2 5 3 2 5 2 ;乙醇在 作催化剂
并加热条件下与氧气发生氧化反应,生成乙醛和水,化学方程式为
❑
2CH CH OH+O →2CH CHO+2H O;
3 2 2 3 2
❑
CH COOH+C H OH CH COOC H +H O
故答案为: 3 2 5 3 2 5 2 ;
❑
2CH CH OH+O →2CH CHO+2H O;
3 2 2 3 2
❑
(5)用新制的氢氧化铜悬浊液即可鉴别乙醇、葡萄糖和乙酸,新制氢氧化铜悬浊液与葡萄糖在加热条件下会产生砖红色沉淀,与乙酸混合变为蓝色溶液,与乙醇混合无明显现象;
故答案为:A。
直击高考
20.现有下列10种与人们生产生活相关的有机物,请回答问题:
①HCHO ②CH CH CHO ③CH CH CH CH
3 2 3 2 2 3
④ ⑤ ⑥ ⑦ ⑧ ⑨CH COOH
3
(1)属于醇的是_________________(填序号)。
(2)互为同系物的是_________________(填序号)。
(3)0.2mol①与足量的新制氢氧化铜溶液反应生成的沉淀的质量是___________g。
(4) 写 出 ②与 银 氨 溶 液 发 生 银 镜 反 应 的 化 学 方 程 式
__________________________________________________________________。
(5) 写 出 ⑤与 ⑨在 浓 硫 酸 加 热 的 条 件 下 , 按 物 质 的 量 1: 2反 应 的 方 程 式
_________________________________________________________________。
(6)⑧与H 在一定条件下完全加成后所得产物的一氯代物共有_______种。
2
(7)完全燃烧0.56g某有机化合物,生成1.76gCO 和0.72gH O。实验测得该有机化合
2 2
物的相对分子质量为56,求该物质的分子式为:___________________
【答案】(1)⑤⑦ (2)①②
(3)57.6
(4)CH CHO+2Ag(N H ) OH→CH COON H +2Ag↓+3N H +H O
3 3 2 3 4 3 2
(5)2C H OH+HOOCCOOH CH CH OOCCOOCH CH +2H O
2 5 3 2 2 3 2
(6)4 (7)C H
4 8