文档内容
2.2.3影响化学平衡的因素(分层作业)
1.对可逆反应 ,在一定条件下达到平衡,下列有关叙述正确的是
A.增大压强,平衡不移动, 的浓度不变
B.当体系的平均相对分子质量不变时,反应达到平衡
C.升高温度,化学平衡常数增大
D.减小 的浓度,v(正)增大,v(逆)减小,平衡正向移动
2.在常温下,下列可逆反应达平衡后,压缩容器容积增大压强,平衡发生移动的是
A.Cl+H O H++Cl-+HClO
2 2
B.2NO (g) 2NO(g)+O (g)
2 2
C.2HI(g) H(g)+I (g)
2 2
D.FeCl +3KSCN Fe(SCN) +3KCl
3 3
3.下列可逆反应达到平衡时,降低温度,平衡向正反应方向移动的是
A.CO+NO CO+NO ΔH<0
2 2
B.3O 2O ΔH>0
2 3
C.PCl (g) PCl (g)+Cl(g) ΔH>0
5 3 2
D.NO NO+O ΔH>0
2 3 2 2
4.10 mL 0.1 mol·L-1KI溶液与5 mL 0.1 mol·L-1FeCl 溶液发生反应:2Fe3+(aq)+2I-(aq) 2Fe2+(aq)+I(aq),
3 2
达到平衡,下列说法不正确的是
A.加入少量氯化钾固体,平衡不移动
B.加适量水稀释,平衡正向移动
C.经过CCl 多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该化学反应存在限度
4
D.该反应的平衡常数K=
5.下列措施或事实不能用勒夏特列原理解释的是
A.将NO 球浸泡在热水中颜色加深
2
B.工业合成氯化氢时使用过量氢气
C.用饱和食盐水除去氯气中的少量HCl气体
D.工业上生产硫酸的过程中,使用过量的空气以提高SO 的利用率
2
6.在一密闭容器中发生反应: ,达到平衡时采取下列措施,可以使正反应速率增大、D的物质的量浓度增大的是
A.移走少量C B.升高温度
C.缩小容积,增大压强 D.容积不变,充入氦气
7.下列事实中,不能用勒夏特列原理解释的是 (填序号)。
①溴水中存在如下平衡:Br +HO HBr+HBrO,当加入NaOH溶液后颜色变浅
2 2
②对2HO 2HO+O↑的反应,使用MnO 可加快制O 的反应速率
2 2 2 2 2 2
③反应:CO+NO CO+NO ΔH<0,升高温度,平衡向逆反应方向移动
2 2
④合成氨反应:N+3H 2NH ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施
2 2 3
⑤H(g)+I(g) 2HI(g),缩小体积加压颜色加深
2 2
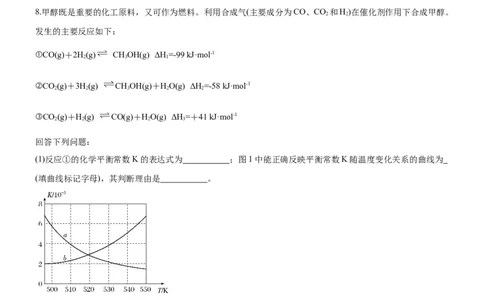
8.甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO 和H)在催化剂作用下合成甲醇。
2 2
发生的主要反应如下:
①CO(g)+2H(g) CHOH(g) ΔH=-99 kJ·mol-1
2 3 1
②CO (g)+3H(g) CHOH(g)+HO(g) ΔH=-58 kJ·mol-1
2 2 3 2 2
③CO (g)+H(g) CO(g)+HO(g) ΔH=+41 kJ·mol-1
2 2 2 3
回答下列问题:
(1)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为
(填曲线标记字母),其判断理由是 。
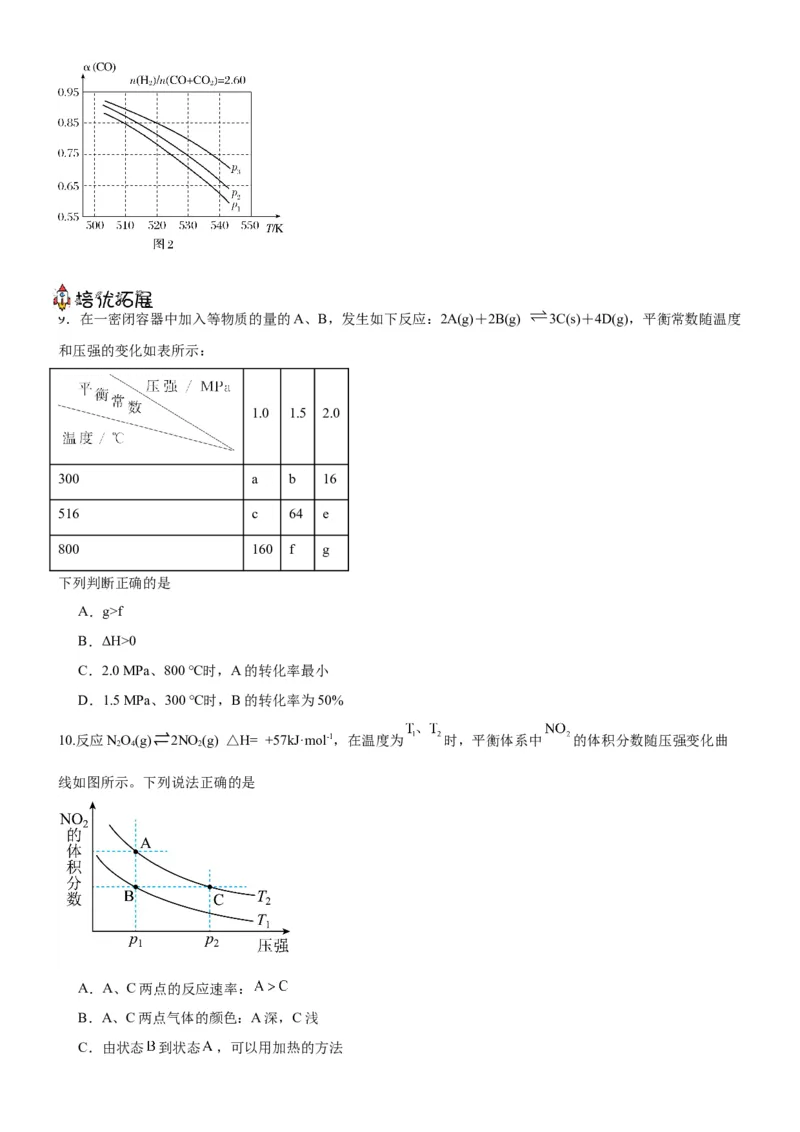
(2)合成气组成 =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随
温度升高而 (填“增大”或“减小”),其原因是 ;图2中的压强由大到小为
,其判断理由是 。9.在一密闭容器中加入等物质的量的A、B,发生如下反应:2A(g)+2B(g) 3C(s)+4D(g),平衡常数随温度
和压强的变化如表所示:
1.0 1.5 2.0
300 a b 16
516 c 64 e
800 160 f g
下列判断正确的是
A.g>f
B.ΔH>0
C.2.0 MPa、800 ℃时,A的转化率最小
D.1.5 MPa、300 ℃时,B的转化率为50%
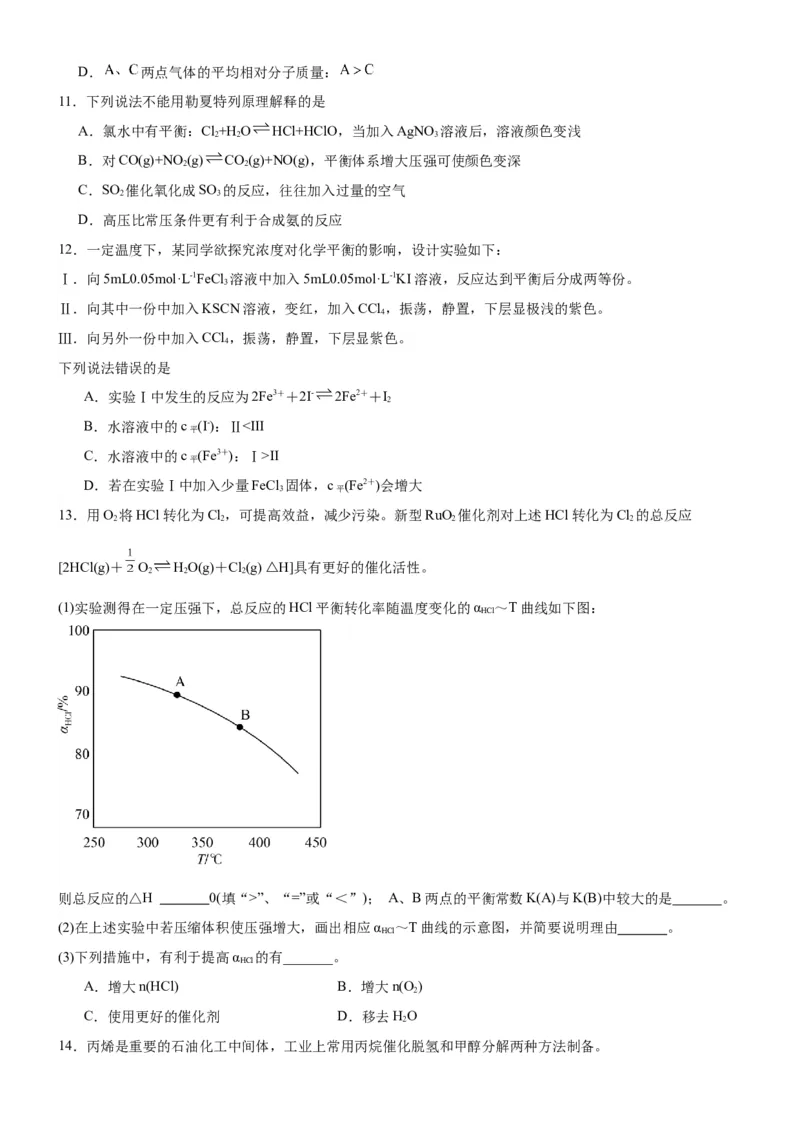
10.反应NO(g)⇌2NO (g) △H= +57kJ·mol-1,在温度为 时,平衡体系中 的体积分数随压强变化曲
2 4 2
线如图所示。下列说法正确的是
A.A、C两点的反应速率:
B.A、C两点气体的颜色:A深,C浅
C.由状态 到状态 ,可以用加热的方法D. 两点气体的平均相对分子质量:
11.下列说法不能用勒夏特列原理解释的是
A.氯水中有平衡:Cl+H O HCl+HClO,当加入AgNO 溶液后,溶液颜色变浅
2 2 3
B.对CO(g)+NO (g) CO(g)+NO(g),平衡体系增大压强可使颜色变深
2 2
C.SO 催化氧化成SO 的反应,往往加入过量的空气
2 3
D.高压比常压条件更有利于合成氨的反应
12.一定温度下,某同学欲探究浓度对化学平衡的影响,设计实验如下:
Ⅰ.向5mL0.05mol·L-1FeCl 溶液中加入5mL0.05mol·L-1KI溶液,反应达到平衡后分成两等份。
3
Ⅱ.向其中一份中加入KSCN溶液,变红,加入CCl ,振荡,静置,下层显极浅的紫色。
4
Ⅲ.向另外一份中加入CCl ,振荡,静置,下层显紫色。
4
下列说法错误的是
A.实验Ⅰ中发生的反应为2Fe3++2I- 2Fe2++I
2
B.水溶液中的c (I-):Ⅱ<Ⅲ
平
C.水溶液中的c (Fe3+):Ⅰ>Ⅱ
平
D.若在实验Ⅰ中加入少量FeCl 固体,c (Fe2+)会增大
3 平
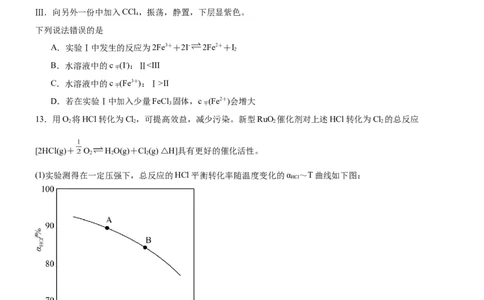
13.用O 将HCl转化为Cl,可提高效益,减少污染。新型RuO 催化剂对上述HCl转化为Cl 的总反应
2 2 2 2
[2HCl(g)+ O HO(g)+Cl(g) △H]具有更好的催化活性。
2 2 2
(1)实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的α ~T曲线如下图:
HCl
则总反应的△H 0(填“>”、“=”或“<”); A、B两点的平衡常数K(A)与K(B)中较大的是 。
(2)在上述实验中若压缩体积使压强增大,画出相应α ~T曲线的示意图,并简要说明理由 。
HCl
(3)下列措施中,有利于提高α 的有_______。
HCl
A.增大n(HCl) B.增大n(O )
2
C.使用更好的催化剂 D.移去HO
2
14.丙烯是重要的石油化工中间体,工业上常用丙烷催化脱氢和甲醇分解两种方法制备。回答下列问题:
I. 丙烷直接脱氢法制丙烯:C H⇌C H(g)+H(g) △H=+123.8kJ·mol-1
3 8 3 6 2 1
(1)该反应在 (填“高温”低温”或“任意温度”)时可自发进行。
(2)570℃、100kPa下,将n(C H):n(H O)=1:9的混合气进行直接脱氢反应,3h后达到平衡,C H 的平衡转化
3 8 2 3 8
率为80%,C H 分压的平均变化率约为 kPa•h-1(保留3位有效数字,下同),脱氢反应的K≈
3 8 p
kPa。(K 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)
p
II.二氧化碳耦合丙烷脱氢制丙烯:CO(g)+H(g)⇌HO(g)+CO(g) ΔH
2 2 2 2
CO(g)+C H(g)⇌C H(g)+HO(g)+CO(g) ΔH =+165kJ•mol-1
2 3 8 3 6 2 3
(3)①ΔH= kJ•mol-1。
2
②与直接脱氢法相比,相同温度下的恒压密闭容器中,二氧化碳耦合丙烷制丙烯能有效提高C H 转化率的原因
3 8
是 、 。
(4)下列能说明该体系在恒温恒压密闭容器中反应达到平衡状态的是 (填序号)。
A.CO 的物质的量分数保持不变
2
B.n(H O):n(CO)保持不变
2
C.气体密度保持不变
D.速率关系:v(C H)=v(C H)
3 8 3 6
III.甲醇催化分解:3CHOH(g)⇌C H(g)+3HO(g)
3 3 6 2
(5)该反应的实验数据遵循Arhenius经验公式:Rlnk=- +C(E 为活化能,假设其受温度影响忽略不计,k为速
a
率常数,R和C为常数),此经验公式说明对于某个基元反应,当升高相同温度时,其活化能越大,反应速率增
大得 (填“越多”或“越少”)。根据如图曲线a计算该反应的活化能E 为 kJ•mol-1。当改变外界
a
条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是 。