文档内容
1.1.1反应热 焓变(分层作业)
【基础检测题】
一、单选题(共0分)
1.下列设备工作时,将化学能转化为热能的是
A B C D
用燃料电池驱动汽
硅太阳能电池 用电烤箱烘焙面包 天然气作为家用燃气蒸煮食物
车
A.A B.B C.C D.D
【答案】D
【详解】A.硅太阳能电池将太阳能转化为电能,不符合题意,故A错误;
B.电烤箱工作时将电能转化为热能,不符合题意,故B错误;
C.燃料电池工作时将化学能转化为电能,不符合题意,故C错误;
D.天然气作为家用燃气蒸煮食物时将化学能转化为热能,符合题意,故D正确;
2.下列装置(或过程)能实现化学能向电能转化的是
A.锌铜原电池 B.燃气燃烧 C.电动车充电 D.风力发电
【答案】A
【详解】A.锌铜原电池为化学能转化为电能的装置,A符合题意;
B.燃气燃烧为化学能转化为热能和光能,B不符合题意;
C.电动车充电为电能转化为化学能,C不符合题意;
D.风力发电为动能转化为电能,D不符合题意;
3.化学反应伴随着能量变化。下列反应的能量变化,符合下图的是A.木炭燃烧 B.氢氧化钡晶体与氯化铵晶体反应
C.镁条与盐酸反应 D.氧化钙溶于水
【答案】B
【详解】A.木炭燃烧为放热反应,不符合题意;
B.氢氧化钡晶体与氯化铵晶体反应为吸热反应,符合题意;
C.镁条与盐酸反应为放热反应,不符合题意;
D.氧化钙溶于水后与水反应过程为放热反应,不符合题意;
4.用如图装置测定盐酸与NaOH溶液反应的中和热。下列说法不正确的是
A.将盐酸、NaOH溶液及发生的反应看成体系
B.盐酸与NaOH溶液反应放热使体系温度升高
C.碎泡沫塑料的作用是保温、隔热
D.反应时将NaOH溶液分多次倒入量热计中
【答案】D
【详解】A.测定盐酸与NaOH溶液反应的中和热,将盐酸、NaOH溶液及发生的反应看成体系(又称系统),与
体系相互影响的其他部分,如盛溶液的烧杯等看做环境,故A正确;
B.酸碱中和反应是放热的,盐酸与NaOH溶液反应放热使体系温度升高,故B正确;
C.测定中和反应的反应热时,要测定温度的变化,需要保证热量不散失,碎泡沫塑料的作用是保温、隔热,
故C正确;
D.为了保证热量不散失,反应时需要将NaOH溶液一次性倒入量热计中,故D错误;
5.下列图示变化为吸热反应的是A. B.
C. D.
【答案】A
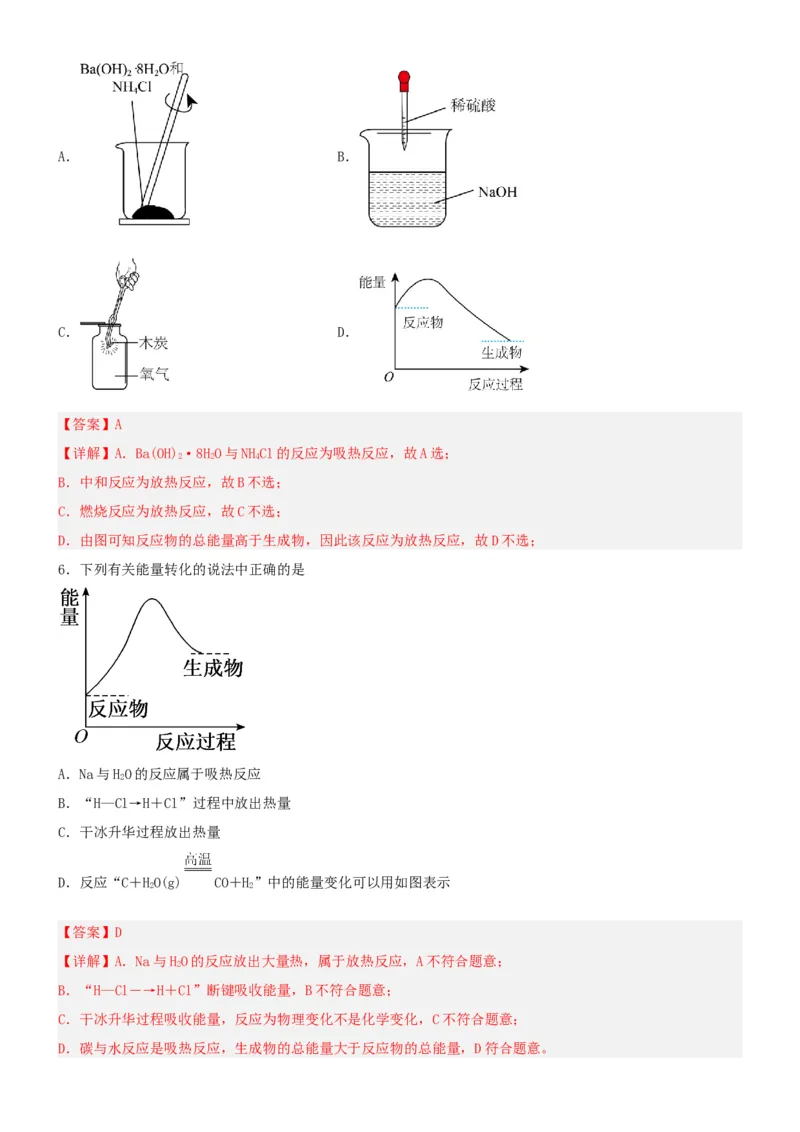
【详解】A.Ba(OH)·8HO与NHCl的反应为吸热反应,故A选;
2 2 4
B.中和反应为放热反应,故B不选;
C.燃烧反应为放热反应,故C不选;
D.由图可知反应物的总能量高于生成物,因此该反应为放热反应,故D不选;
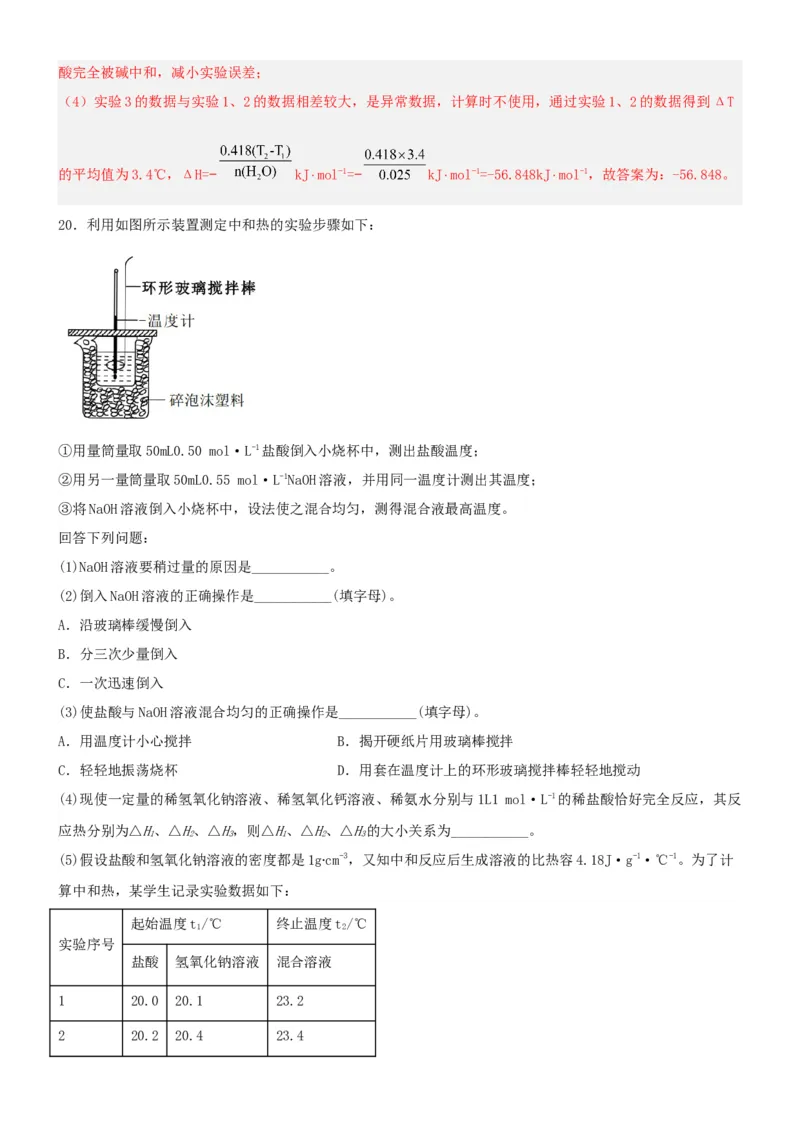
6.下列有关能量转化的说法中正确的是
A.Na与HO的反应属于吸热反应
2
B.“H—Cl→H+Cl”过程中放出热量
C.干冰升华过程放出热量
D.反应“C+HO(g) CO+H”中的能量变化可以用如图表示
2 2
【答案】D
【详解】A.Na与HO的反应放出大量热,属于放热反应,A不符合题意;
2
B.“H—Cl―→H+Cl”断键吸收能量,B不符合题意;
C.干冰升华过程吸收能量,反应为物理变化不是化学变化,C不符合题意;
D.碳与水反应是吸热反应,生成物的总能量大于反应物的总能量,D符合题意。7.下列有关中和反应反应热测定实验的说法正确的是
A.酸碱溶液混合后,应先冷却再测温
B.向内筒中加入稀碱时,应当缓慢而匀速地加入
C.玻璃棒搅拌器若用铜丝代替,则测定出的中和反应反应热偏大
D.任何酸碱之间发生中和反应生成1mol HO (l)时放出的热量都是57.3kJ
2
【答案】C
【详解】A.酸碱溶液混合后,应立即测量温度且取最高温度作为最终温度,A错误;
B.向内筒中加入稀碱时,应当迅速而匀速地加入,B错误;
C.玻璃棒搅拌器若用铜丝代替,会有热量散失,使放出热量偏小所以测定出的中和反应反应热∆H偏大,C正
确;
D.稀的强酸和强碱之间发生中和反应生成1mol HO (l)时放出的热量是57.3kJ,D错误;
2
8.用如图所示的装置进行中和反应反应热的测定。下列说法正确的是
A.如图条件下,实验过程中没有任何热量损失
B.为了使反应充分进行,药品可以分多次加入
C.完成一次中和反应反应热平行样的测定,温度计需要使用2次
D.测量NaOH与不同种类的酸中和反应的反应热,数值可能不同
【答案】D
【详解】A.图示条件下的实验过程中一定有部分热量的损失,故A错误;
B.药品可以分多次加入将导致热量损失过多,应一次性快速加入药品,故B错误;
C.完成一次中和反应反应热测定实验,温度计需要使用3次,分别用于测酸、碱初始温度和反应的最高温度,
故C错误;
D.醋酸是弱酸,电离吸热;NaOH与不同种类的酸中和反应的反应热,数值可能不同,故D错误;
9.实验室测定中和热的步骤如下(如图)第一步:量取40.0mL0.25mol/L 溶液倒入小烧杯中,测量温度;
第二步:量取40.0mL0.55mol/LNaOH溶液,测量温度;
第三步:将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。
请回答:
(1)图中仪器A的名称是_______。
(2)加入NaOH溶液的正确操作是_______(填字母)。
A.沿玻璃棒缓慢加入 B.分三次均匀加入
C.一次迅速加入 D.用滴定管小心滴加
(3)上述实验测得的结果比理论上的57.3kJ/mol偏大,其原因可能是_______。
a.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好。
b.实验装置保温、隔热效果不好
c.用温度计测定NaOH溶液起始温度后又直接测定 溶液的温度
d.量取40ml 溶液后用水清洗量筒,并将洗液倒入量热计
(4)若实验中若改用60mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液进行反应,与上述实验相比,所
放出的热量_______(填“相等”“不相等”),若实验操作均正确,则所求中和热_______(填“相等”“不相
等”)。
【答案】(1)环形玻璃搅拌棒 (2)C
(3)abcd (4) 不相等 相等
【解析】实验室测定中和热要使用稀得强酸强碱溶液且注意保温减少热量损失。
(1)仪器A的名称是:环形玻璃搅拌棒;
(2)为了保证热量不散失,加入NaOH溶液的正确操作是:一次迅速加入,故答案为:C;
(3)中和反应为放热反应,焓变为负值,上述实验测得的结果比理论上的57.3kJ/mol偏大,则测得热量绝对
值偏小;a.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好,热量散失较大,所得中和热的绝对值偏
小,a项正确;b.装置保温、隔热效果差,测得的热量偏小,中和热的绝对值偏小,b项正确;c.温度计测定
NaOH溶液起始温度后直接插入稀HSO 测温度,硫酸的起始温度偏高,温度差偏小,测得的热量偏小,中和热
2 4的绝对值偏小,c项正确, d.量取40ml 溶液后用水清洗量筒,并将洗液倒入量热计,使得温度差偏小,
测得的热量偏小,中和热的绝对值偏小,d项正确,
故选abcd;
(4)反应放出的热量和所用酸以及碱的量的多少有关,改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的
氢氧化钠溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,所放出的热量不相等;但是
中和热均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以改用60 mL 0.50 mol/L的盐酸
与50 mL 0.55 mol/L的氢氧化钠溶液进行实验,测得中和热数值相等,故答案为:不相等;相等。
10.取0.55 的 溶液50 与0.25 的硫酸50 置于如图所示的装置中进行中和热的测定
实验,回答下列问题:
(1)从如图实验装置可知,缺少的一种仪器名称是______________________。
(2)由图可知该装置还有其他不妥之处,改正的操作是________________。
(3)碎纸片与硬纸板的作用是________________。
(4)实验中改用60 0.25 的硫酸与50 0.55 溶液进行反应,与上述实验相比,所测得
的中和热数值___________(填“相等”或“不相等”)
(5)该同学做实验时有些操作不规范,造成测得中和反应反应热的数值偏高,请你分析可能的原因是_________
(填序号)。
A.测量盐酸的温度后,温度计未用水洗净,直接去测 溶液的温度
B.向小烧杯中加入氢氧化钠溶液时,分多次倒入,并且动作迟缓
C.将50 0.25 的硫酸溶液错取成了50 18.4 的浓硫酸
【答案】(1)环形玻璃搅拌棒 (2)在大、小烧杯之间填满碎纸片,使小烧杯口与大烧杯口相平
(3)防止热量散失 (4)相等 (5)C
【解析】测定中和热时,要确保热量不散失、0.25 的硫酸50 反应完全,故要在保温性能好、绝热的
体系中反应、一次性迅速把50 0.55 的 溶液倒入小烧杯中,并用环形玻璃搅拌棒、量取最高温度;测出放出的热量、并计算出中和热,据此回答;
(1)在测定中和热时,为了使酸碱溶液快速混合均匀,要使用环形玻璃搅拌棒进行充分搅拌,从如图实验装
置可知,缺少的一种仪器名称是环形玻璃搅拌棒。
(2)由图可知该装置还有其他不妥之处——图示装置隔热效果差、热量容易散失,改正的操作是:在大、小
烧杯之间填满碎纸片,使小烧杯口与大烧杯口相平。
(3)在大、小烧杯之间填满碎纸片,使小烧杯口与大烧杯口相平时,热量不易散失,故碎纸片与硬纸板的作
用是防止热量散失。
(4)中和热是指在稀溶液中,强酸和强碱反应生成1mol水时所放出的热量,实验中改用60 0.25 的
硫酸与50 0.55 溶液进行反应,虽然实际消耗的反应物的量不同、生成的水量不同、放出的热
量也不同,但实验结果所测得的中和热数值相等。
(5)A.测量盐酸的温度后,温度计未用水洗净,直接去测 溶液的温度,使一部分热量散失、所测得的
中和热数值偏低,A不选;
B.向小烧杯中加入氢氧化钠溶液时,分多次倒入,并且动作迟缓,使一部分热量散失、所测得的中和热数值
偏低,B不选;
C.将50 0.25 的硫酸溶液错取成了50 18.4 的浓硫酸,则硫酸过量,实际消耗的反应物的
量偏大、生成的水量偏大、放出的热量也偏大,且浓硫酸稀释时也会放热,则所测得的中和热数值偏高,C选;
【能力提升题】
11.为了研究化学反应的能量变化情况,某同学设计了如图所示装置。当向盛有试剂甲的试管中加入试剂乙时
(必要时可以搅拌),U形管中液面呈现出左高右低的现象,则试剂甲、乙的组合是
A.甲:镁条、乙:盐酸 B.甲:氢氧化钡晶体、乙:氯化铵
C.甲:氢氧化钡、乙:硫酸 D.甲:二氧化锰、乙:双氧水
【答案】B
【详解】A.镁与盐酸反应放热,瓶内气体膨胀,压强增大,U形管中液面呈现出左低右高的现象,选A不符合;
B.氢氧化钡晶体与氯化铵反应吸热,瓶内气体收缩,压强减小,U形管中液面呈现出左高右低的现象,选项B
符合;C.氢氧化钡与硫酸发生中和反应放热,瓶内气体膨胀,压强增大,U形管中液面呈现出左低右高的现象,选项
C不符合;
D.二氧化锰催化双氧水反应放热,瓶内气压增大,U形管中液面呈现出左低右高的现象,选项D不符合;
12.一定条件下,石墨转化为金刚石要吸收能量。在该条件下,下列结论正确的是
A.1 mol C (金刚石)比1 mol C (石墨)的总能量高
B.金刚石比石墨稳定
C.等质量的金刚石和石墨完全燃烧释放的热量相同
D.金刚石转化为石墨是吸热反应
【答案】A
【详解】A.一定条件下,石墨转化为金刚石要吸收能量,所以1molC(金刚石)比1molC(石墨)的总能量高,选
项A正确;
B.石墨转化为金刚石要吸收能量,说明石墨的能量低,稳定,所以石墨比金刚石稳定,选项B错误;
C.石墨转化为金刚石要吸收能量,说明石墨的能量低,等质量的石墨和金刚石完全燃烧时释放的能量金刚石
比石墨多,选项C错误;
D.金刚石转化为石墨要释放能量,即金刚石转化石墨是放热反应,选项D错误;
13.如图所示装置可用于实验室测定中和热,下列说法正确的是
A.本实验中,读取混合溶液不再变化的温度为终止温度
B.缺少的搅拌器不可以是活泼金属,可用铜质搅拌棒
C.过程中需用同一温度计至少测定三次温度
D.强酸和强碱的稀溶液发生中和反应放出的热量即为中和热
【答案】C
【详解】A.本实验中,读取混合溶液的最高温度为终止温度,故A错误;
B.缺少的搅拌器应该是导热性差的环形玻璃搅拌器,故B错误;
C.中和热测定过程中需用同一温度计测定反应前酸溶液的温度、碱溶液的温度和反应后溶液的最高温度,至
少测定三次温度,故C正确;
D.强酸和强碱的稀溶液发生中和反应生成1mol水放出的热量为中和热,故D错误;14.化学反应 的能量变化如图所示,则下列说法正确的是
A.该反应是吸热反应
B.断裂 键和 键能放出 的能量
C.断裂 键需要吸收ykJ的能量
D. 的总能量高于1molA 和1molB 的总能量
2 2
【答案】C
【详解】A.由图示可知,反应物的总能量高于生成物的总能量,该反应是放热反应,选项A错误;
B.化学键的断裂需要吸收能量,而不是释放能量,选项B错误;
C.化学键的断裂吸收能量,由图可知,断裂2mol A-B键需要吸收y kJ的能量,选项C正确;
D.由图示可知, 的总能量低于 和 的总能量,选项D错误;
15.化学能可与热能、电能等相互转化。下列表述不正确的是
A.化学反应中能量变化的主要原因是化学键的断裂与形成
B.中和反应中,反应物的总能量比生成物的总能量高
C.图I所示的装置能将化学能转变为电能放热
D.图Ⅱ所示的反应为放热反应
【答案】C
【详解】A.化学反应总是伴随着能量变化,断键需要吸收能量,成键放出能量,所以化学反应中能量变化的
主要原因是化学键的断裂与生成,故A正确;
B.中和反应是放热反应,所以反应物总能量大于生成物总能量,故B正确;
C.该装置不能构成闭合回路,所以不能形成原电池,即不能将化学能转变为电能,故C错误;D.根据图像Ⅱ知,反应物总能量大于生成物总能量,则该反应是放热反应,故D正确;
16.下列说法正确的是
A.浓硫酸稀释属于放热反应
B.等质量的硫蒸气和硫固体完全燃烧,后者放出的热量多
C.任何酸与碱发生中和反应生成1 mol HO的过程中,反应热均相同
2
D.已知C(s,石墨)= C(s,金刚石) ΔH= + 1.5 kJ·mol-1 ,则石墨比金刚石稳定
【答案】D
【详解】A.浓硫酸稀释是物理过程,不属于放热反应,故A错误;
B.等质量的硫蒸气能量高于硫固体,则硫蒸气完全燃烧放出的热量多,故B错误;
C.弱酸弱碱没有完全电离,电离时需吸收能量,中和生成1mol水时放出的热量少,强酸强碱稀溶液反应生成
1mol水同时生成沉淀,放出热量会增大,故C错误;
D.由C(s,石墨)= C(s,金刚石) △H=+1.5 kJ/mol,反应吸热,可知金刚石的能量比石墨的能量高,所以石墨
比金刚石稳定,故D正确;
17.氮是粮食作物生长必需的元素,20世纪初德国化学家哈伯在实验室首次利用氮气和氢气合成了氨:N(g)
2
+3H(g) 2NH(g) △H=-92.4kJ•mol-1。从此人类进入了新的农业时代,化肥的使用大大提高了粮食产
2 3
量。下列有关合成氨反应说法不正确的是
A.合成氨反应属于氮的固定
B.NH 既是氧化产物,又是还原产物
3
C.用E 表示物质能量之和,E (反应物)<E (生成物)
总 总 总
D.每生成2molNH(g),反应过程中放出92.4kJ的热量
3
【答案】C
【详解】A.合成氨为游离态的氮变为化合态的氮,属于氮的固定,A正确;
B.N(g)中N元素价态降低,被还原为氨气,H(g)中H元素价态升高,被氧化为氨气,故NH 既是氧化产物,又
2 2 3
是还原产物,B正确;
C.△H=E (生成物)-E (反应物)<0,故E (生成物)E,断开所有反应物化学键所吸收的能量大于形成所有生成物化学键所释放的能量,D
1 2
正确;
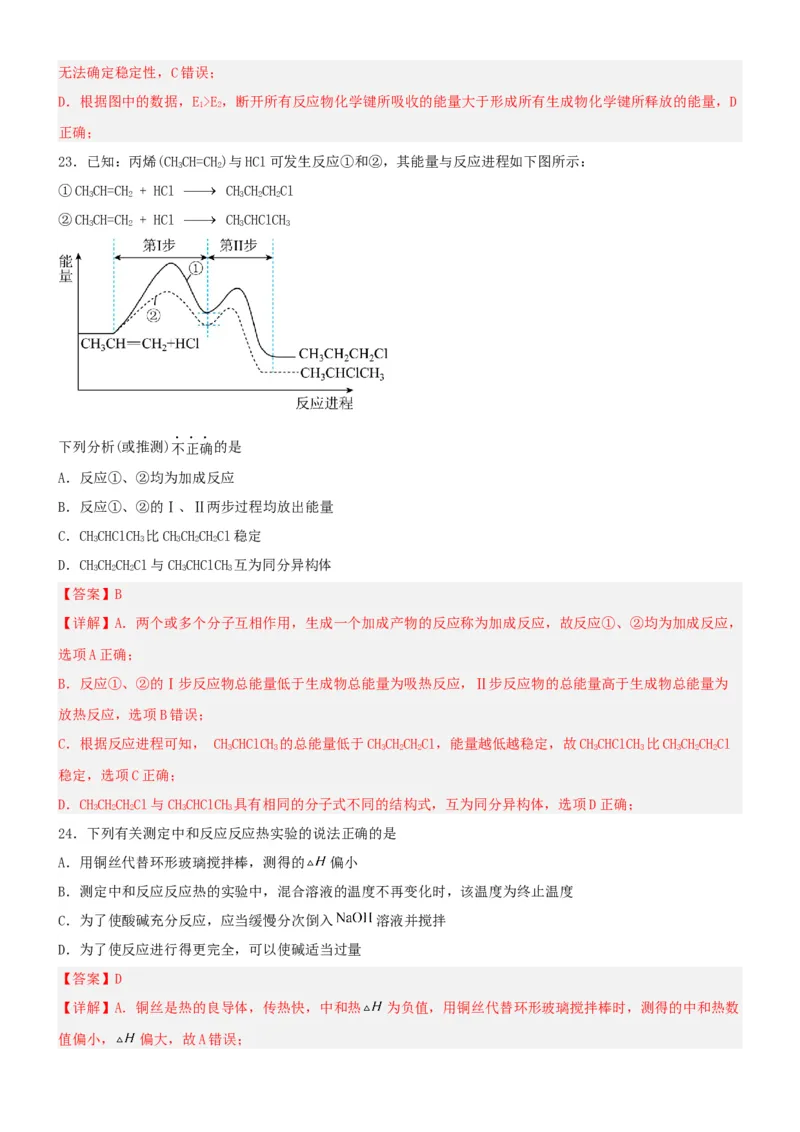
23.已知:丙烯(CHCH=CH)与HCl可发生反应①和②,其能量与反应进程如下图所示:
3 2
①CHCH=CH + HCl CHCHCHCl
3 2 3 2 2
②CHCH=CH + HCl CHCHClCH
3 2 3 3
下列分析(或推测)不正确的是
A.反应①、②均为加成反应
B.反应①、②的Ⅰ、Ⅱ两步过程均放出能量
C.CHCHClCH 比CHCHCHCl稳定
3 3 3 2 2
D.CHCHCHCl与CHCHClCH 互为同分异构体
3 2 2 3 3
【答案】B
【详解】A.两个或多个分子互相作用,生成一个加成产物的反应称为加成反应,故反应①、②均为加成反应,
选项A正确;
B.反应①、②的Ⅰ步反应物总能量低于生成物总能量为吸热反应,Ⅱ步反应物的总能量高于生成物总能量为
放热反应,选项B错误;
C.根据反应进程可知, CHCHClCH 的总能量低于CHCHCHCl,能量越低越稳定,故CHCHClCH 比CHCHCHCl
3 3 3 2 2 3 3 3 2 2
稳定,选项C正确;
D.CHCHCHCl与CHCHClCH 具有相同的分子式不同的结构式,互为同分异构体,选项D正确;
3 2 2 3 3
24.下列有关测定中和反应反应热实验的说法正确的是
A.用铜丝代替环形玻璃搅拌棒,测得的 偏小
B.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度
C.为了使酸碱充分反应,应当缓慢分次倒入 溶液并搅拌
D.为了使反应进行得更完全,可以使碱适当过量
【答案】D
【详解】A.铜丝是热的良导体,传热快,中和热 为负值,用铜丝代替环形玻璃搅拌棒时,测得的中和热数
值偏小, 偏大,故A错误;B.测定中和反应热的实验中,混合溶液的最高温度为终止温度,不是温度不再变化时的温度为终止温度,故B
错误;
C.为了使酸碱充分反应,应当一次性快速倒入 溶液并搅拌,故C错误;
D.为了使反应进行得更完全,可以使碱适当过量,故D正确;
25.如图是金属镁和卤素单质 反应的能量变化示意图。下列说法正确的是
A. 中热稳定性最好的是
B.由 制取 是放热过程
C.金属镁和卤素单质 的反应都是放热反应
D.此温度下四种 中, 所含化学键的键能最大
【答案】C
【详解】A.物质的能量越低越稳定,结合图示可知,热稳定性: MgI