文档内容
2025—2026 学年度上期高 2028届期中考试
化学 试卷
考试时间:75分钟 满分:100分
可能用到的相对原子质量:
H—1 C—12 N—14 O—16 Na—23 Mg—24 Al—27
S—32 Cl—35.5 K—39 Fe—56 Ba—137
一、选择题:本题共15小题,每小题只有一个选项符合题目要求,每题3分,总计45分。
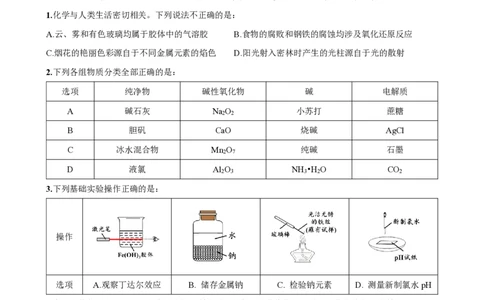
1.化学与人类生活密切相关。下列说法不正确的是:
A.云、雾和有色玻璃均属于胶体中的气溶胶 B.食物的腐败和钢铁的腐蚀均涉及氧化还原反应
C.烟花的艳丽色彩源自于不同金属元素的焰色 D.阳光射入密林时产生的光柱源自于光的散射
2.下列各组物质分类全部正确的是:
选项 纯净物 碱性氧化物 碱 电解质
A 碱石灰 Na O 小苏打 蔗糖
2 2
B 胆矾 CaO 烧碱 AgCl
C 冰水混合物 Mn O 纯碱 石墨
2 7
D 液氯 Al O NH •H O CO
2 3 3 2 2
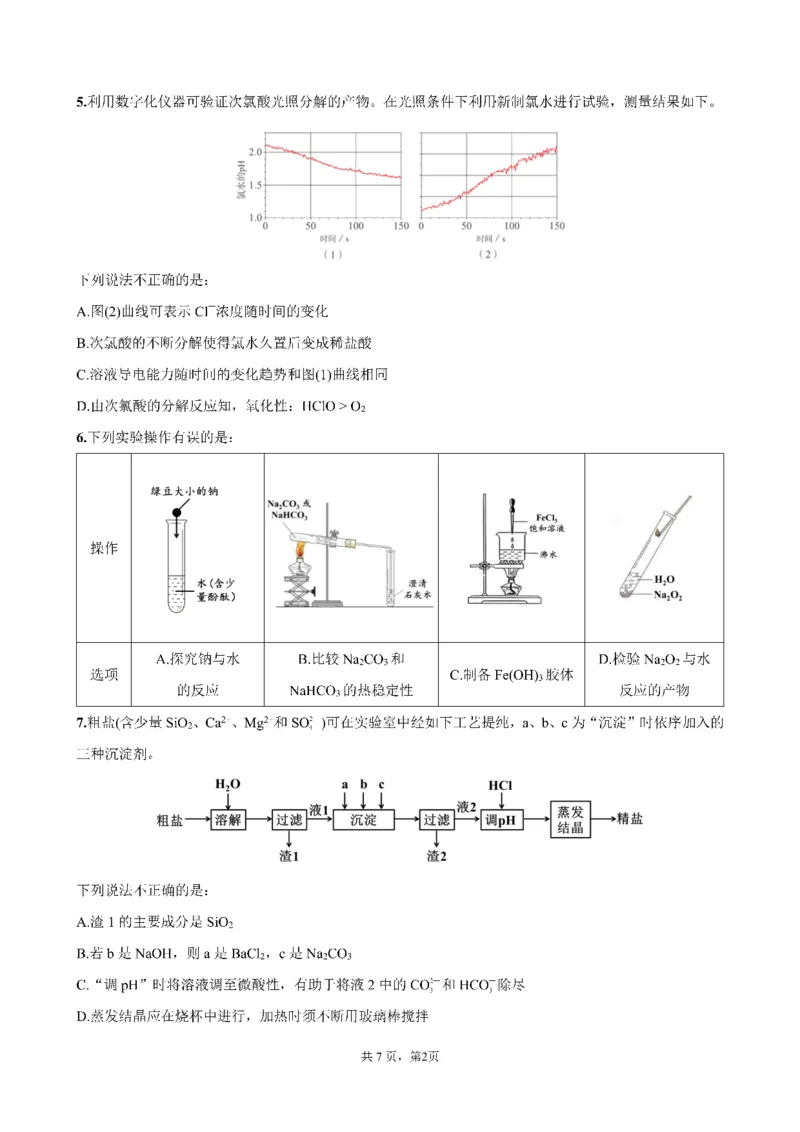
3.下列基础实验操作正确的是:
操作
选项 A.观察丁达尔效应 B. 储存金属钠 C. 检验钠元素 D. 测量新制氯水pH
4.向一定体积的Ba(OH) 溶液中逐滴加入稀硫酸,测得溶液导电能力随时间变化曲线如下图所示。
2
下列说法正确的是:
A. AB段溶液的导电能力不断减弱,说明生成的BaSO 不是电解质
4
B.BC段溶液导电能力不断增大,主要是由于过量的Ba(OH) 导电
2
C.a时刻溶液中OH—与H+恰好完全中和,但Ba2+和SO2— 没有恰好完全沉淀
4
D.向澄清石灰水中不断通入CO ,溶液导电能力随时间变化趋势与右图相同
2
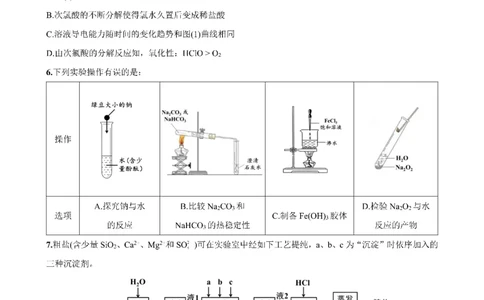
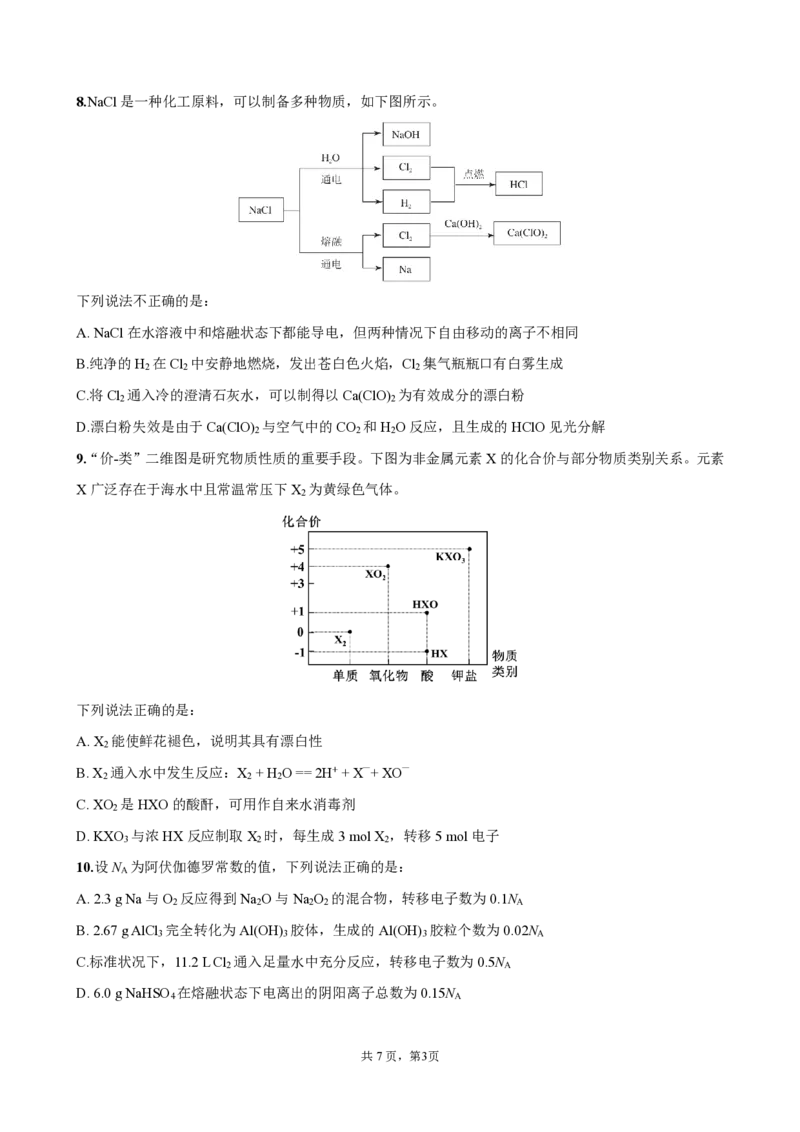
共7页,第1页8.NaCl是一种化工原料,可以制备多种物质,如下图所示。
下列说法不正确的是:
A.NaCl在水溶液中和熔融状态下都能导电,但两种情况下自由移动的离子不相同
B.纯净的H 在Cl 中安静地燃烧,发出苍白色火焰,Cl 集气瓶瓶口有白雾生成
2 2 2
C.将Cl 通入冷的澄清石灰水,可以制得以Ca(ClO) 为有效成分的漂白粉
2 2
D.漂白粉失效是由于Ca(ClO) 与空气中的CO 和H O反应,且生成的HClO见光分解
2 2 2
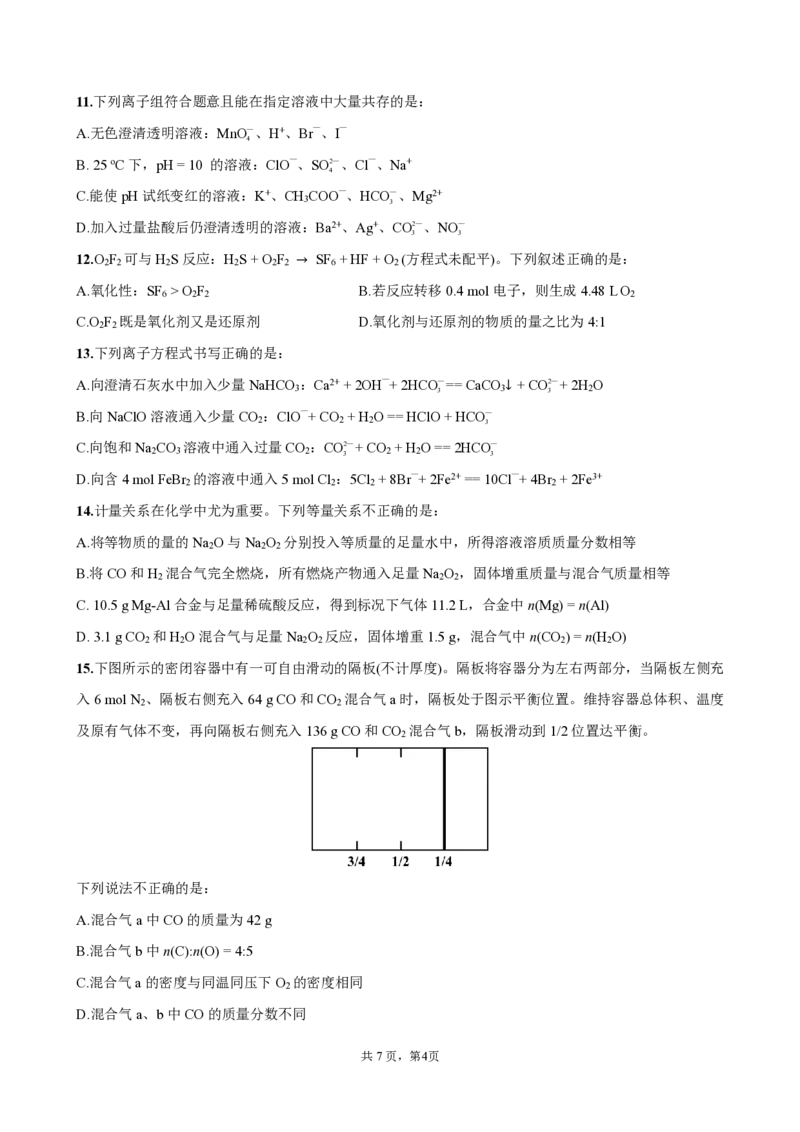
9.““ -类”二维图是研究物质性质的重要手段。下图为非金属元素X的化合 与部分物质类别关系。元素
X广泛存在于海水中且常温常压下X 为黄绿色气体。
2
下列说法正确的是:
A.X 能使鲜花褪色,说明其具有漂白性
2
B.X 通入水中发生反应:X + H O == 2H+ + X—+ XO—
2 2 2
C.XO 是HXO的酸酐,可用作自来水消毒剂
2
D.KXO 与浓HX反应制取X 时,每生成3 mol X ,转移5 mol电子
3 2 2
10.设N 为阿伏伽德罗常数的值,下列说法正确的是:
A
A.2.3 g Na与O 反应得到Na O与Na O 的混合物,转移电子数为0.1N
2 2 2 2 A
B.2.67 g AlCl 完全转化为Al(OH) 胶体,生成的Al(OH) 胶粒个数为0.02N
3 3 3 A
C.标准状况下,11.2 L Cl 通入足量水中充分反应,转移电子数为0.5N
2 A
D.6.0 g NaHSO 在熔融状态下电离出的阴阳离子总数为0.15N
4 A
共7页,第3页11.下列离子组符合题意且能在指定溶液中大量共存的是:
A.无色澄清透明溶液:MnO— 、H+、Br—、I—
4
B.25 oC下,pH = 10 的溶液:ClO—、SO2— 、Cl—、Na+
4
C.能使pH试纸变红的溶液:K+、CH COO—、HCO— 、Mg2+
3 3
D.加入过量盐酸后仍澄清透明的溶液:Ba2+、Ag+、CO2— 、NO—
3 3
12.O F 可与H S反应:H S + O F → SF + HF + O (方程式未配平)。下列叙述正确的是:
2 2 2 2 2 2 6 2
A.氧化性:SF > O F B.若反应转移0.4 mol电子,则生成4.48 L O
6 2 2 2
C.O F 既是氧化剂又是还原剂 D.氧化剂与还原剂的物质的量之比为4:1
2 2
13.下列离子方程式书写正确的是:
A.向澄清石灰水中加入少量NaHCO :Ca2+ + 2OH—+ 2HCO— == CaCO ↓ + CO2— +2H O
3 3 3 3 2
B.向NaClO溶液通入少量CO :ClO—+ CO + H O == HClO + HCO—
2 2 2 3
C.向饱和Na CO 溶液中通入过量CO :CO2— +CO + H O == 2HCO—
2 3 2 3 2 2 3
D.向含4 mol FeBr 的溶液中通入5 mol Cl :5Cl + 8Br—+ 2Fe2+ == 10Cl—+ 4Br + 2Fe3+
2 2 2 2
14.计量关系在化学中尤为重要。下列等量关系不正确的是:
A.将等物质的量的Na O与Na O 分别投入等质量的足量水中,所得溶液溶质质量分数相等
2 2 2
B.将CO和H 混合气完全燃烧,所有燃烧产物通入足量Na O ,固体增重质量与混合气质量相等
2 2 2
C.10.5 g Mg-Al合金与足量稀硫酸反应,得到标况下气体11.2 L,合金中n(Mg) = n(Al)
D.3.1 g CO 和H O混合气与足量Na O 反应,固体增重1.5 g,混合气中n(CO ) = n(H O)
2 2 2 2 2 2
15.下图所示的密闭容器中有一可自由滑动的隔板(不计厚度)。隔板将容器分为左右两部分,当隔板左侧充
入6 mol N 、隔板右侧充入64 g CO和CO 混合气a时,隔板处于图示平衡位置。维持容器总体积、温度
2 2
及原有气体不变,再向隔板右侧充入136 g CO和CO 混合气b,隔板滑动到1/2位置达平衡。
2
下列说法不正确的是:
A.混合气a中CO的质量为42 g
B.混合气b中n(C):n(O) = 4:5
C.混合气a的密度与同温同压下O 的密度相同
2
D.混合气a、b中CO的质量分数不同
共7页,第4页二、非选择题:本题共4小题,总计55分。
16.(14分)物质A~F均含有某一海水中大量存在的金属元素,它们之间的转化关系如下。
回答下列问题:
(1)用小刀切开单质A,可以看到其光亮的表面 (填现象),这是因为发生了反应①。
(2)在实验室中进行反应②,单质A须放置在干燥的 (填仪器名称)中进行加热。加热时可观察到A先
(填现象),然后与氧气剧烈反应。
(3)写出反应③的化学方程式,并用单线桥表示反应转移电子的方向与数目 。
(4)写出反应⑤的化学方程式 。3.9 g化合物C与足量CO 和H O混合气完全反应,转移电子数为 (设
2 2
N 为阿伏伽德罗常数的值)。
A
(5)E的粉末置于空气中易结块,这是由于E吸水形成了 (填物质名称),该过程属于 (选填 物理 或
化学)变化。
(6)取E和F的固体混合物4.7 g,加足量稀硫酸充分反应,得到1.12 L(标况下)气体。则混合物中E与F的
物质的量之比为 。
17.(14分)我国化学家侯德榜改革国外的制碱工艺,发明了如下联合制碱法。
回答下列问题:
(1)“吸氨”与“碳酸化”两步的次序 (选填 能 或 不能)相互调换。
(2)通入气体A使溶液“碳酸化”时析出大量沉淀,该过程的离子方程式为 。
(3)“煅烧”反应的化学方程式为 ,其中产生的气体可返回 (填步骤名称)循环利用。
共7页,第5页(4)D的化学式为 。“冷析”利用了D的溶解度随温度降低而 (选填 增大 或 减小)的特点。
(5)假设产品C中只含有杂质B,下列方法中不能准确测定产品中C的含量的是 。
a.取a g产品充分加热,质量减少b g
b.取a g产品与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体
c.取a g产品与足量NaOH溶液充分反应,得到b g溶液
d.取a g产品与足量稀硫酸充分反应,逸出气体经浓硫酸干燥后用碱石灰吸收,质量增加b g
(6)将2.52 g纯净的B与1.56 g Na O 充分混合后置于真空密闭容器内共热,充分反应后将体系完全干燥。
2 2
最终容器内剩余固体由 2 种组分构成,其中主要成分是 (填化学式),主要成分与次要成分的物质的量
之比为 。
18.(14分)某无色澄清溶液仅可能由下列离子中的几种组成:
阳离子 NH+ 、K+、Na+、Ag+、Cu2+
4
阴离子 OH—、CO2— 、Cl—、HSO— 、SO2—
3 3 4
现将该溶液平均分成三等份,进行如下实验:
① 取第一份试样滴入紫色石蕊试液,溶液呈深蓝色。
② 取第二份试样加入足量Ba(NO ) 溶液,产生白色沉淀,过滤。
3 2
③ 向②的滤渣中加入过量稀盐酸,沉淀部分溶解,再次过滤。
④ 将③的滤渣洗涤、干燥并称重,得2.33 g白色固体。
⑤ 取②中滤液, ,未见白色沉淀生成。
回答下列问题:
(1)实验⑤的目的是检验Cl—。试补充空白处遗漏的操作: 。
(2)根据上述实验,该溶液中一定不存在的离子有 ,一定存在的离子有 。
(3)蘸取少量试样进行焰色试验,观察到火焰呈 色,说明溶液中有Na+存在;为确定K+是否存在,透过
(填仪器名称)再次观察火焰,未见紫色。
(4)向第三份试样中逐滴加入稀盐酸,最终有无色气体产生。生成气体的标况下体积 V(气体)(mL)与加入盐
酸的物质的量n(HCl)(mol)关系如下图。
(i)ab段发生反应的离子方程式为 。
(ii)a点的横坐标值为 。
(iii)原溶液中n(Na+) = mol。
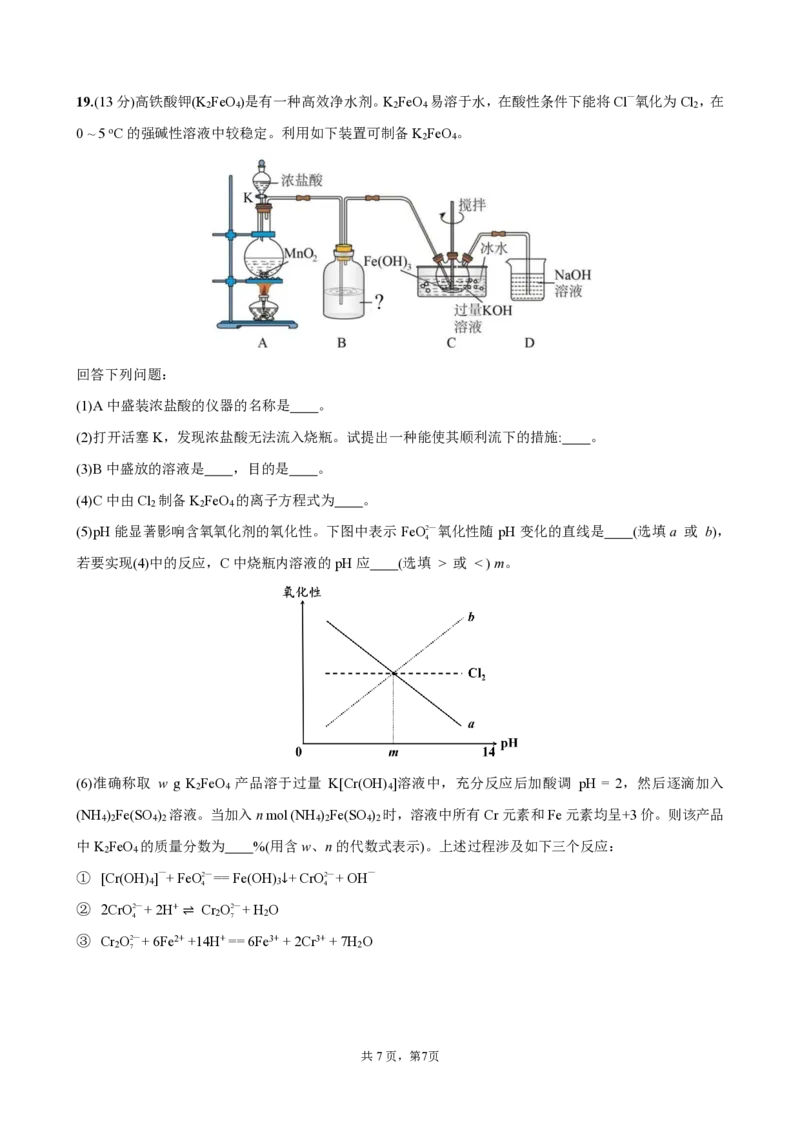
共7页,第6页19.(13分)高铁酸钾(K FeO )是有一种高效净水剂。K FeO 易溶于水,在酸性条件下能将Cl—氧化为Cl ,在
2 4 2 4 2
0 ~ 5 oC的强碱性溶液中较稳定。利用如下装置可制备K FeO 。
2 4
回答下列问题:
(1)A中盛装浓盐酸的仪器的名称是 。
(2)打开活塞K,发现浓盐酸无法流入烧瓶。试提出一种能使其顺利流下的措施: 。
(3)B中盛放的溶液是 ,目的是 。
(4)C中由Cl 制备K FeO 的离子方程式为 。
2 2 4
(5)pH 能显著影响含氧氧化剂的氧化性。下图中表示 FeO2— 氧化性随 pH 变化的直线是 (选填 a 或 b),
4
若要实现(4)中的反应,C中烧瓶内溶液的pH应 (选填 > 或 < ) m。
(6)准确称取 w g K FeO 产品溶于过量 K[Cr(OH) ]溶液中,充分反应后加酸调 pH = 2,然后逐滴加入
2 4 4
(NH ) Fe(SO ) 溶液。当加入n mol (NH ) Fe(SO ) 时,溶液中所有Cr元素和Fe元素均呈+3 。则该产品
4 2 4 2 4 2 4 2
中K FeO 的质量分数为 %(用含w、n的代数式表示)。上述过程涉及如下三个反应:
2 4
① [Cr(OH) ]—+ FeO2— == Fe(OH) ↓+ CrO2— +OH—
4 4 3 4
② 2CrO2— +2H+ ⇌ Cr O2— +H O
4 2 7 2
③ Cr O2— +6Fe2+ +14H+ == 6Fe3+ + 2Cr3+ + 7H O
2 7 2
共7页,第7页