文档内容
第七章 有机化合物
第三节 乙醇与乙酸 课时作业
第二课时 乙酸
基础达标
1.乙酸是生活中常见的一种有机物,下列关于乙酸的说法中正确的是( )
A.乙酸的官能团为—OH B.乙酸的酸性比碳酸弱
C.乙酸能够与金属钠反应产生氢气 D.乙酸能使紫色的石蕊溶液变蓝
【答案】C
【解析】乙酸的官能团为—COOH,A错误;乙酸的酸性比碳酸强,B错误;乙酸具有酸
的通性,与钠反应产生氢气,C正确;乙酸能使紫色石蕊溶液变红,D错误。
2.如图所示是某常见有机物分子的空间填充模型,该物质不具有的性质是( )
A.与大理石反应 B.与稀盐酸反应
C.发生酯化反应 D.使紫色石蕊溶液变红
答案:B
解析:由有机物分子的空间填充模型可知,该物质为乙酸,乙酸为一元弱酸,但比 HCO
2 3
的酸性强,故可与大理石反应,也可使紫色石蕊溶液变红,故 A、D正确;乙酸和乙醇在
浓HSO 加热条件下发生酯化反应,故C正确;乙酸与稀盐酸不反应,故B错误。
2 4
3.乙醇和乙酸是生活中常见的两种有机物,下列说法不正确的是( )
A. 乙醇可经过一步反应直接氧化为乙酸
B. 可通过蒸馏的方法分离乙醇和乙酸
C. 可用NaHCO 溶液检验乙醇中是否混有乙酸
3
D. 乙醇能与钠反应放出氢气,说明乙醇能电离出H+而表现酸性
【答案】D
【解析】A.乙醇能被酸性重铬酸钾氧化生成乙酸,所以乙醇能经过一步反应直接氧化为乙
酸,故A正确;B.互溶的液体可以采用蒸馏的方法分离,乙醇和乙酸互溶并且沸点相差较
大,可以采用蒸馏的方法分离,故B正确;C.乙醇和碳酸氢钠不反应,乙酸和碳酸氢钠反
应生成二氧化碳,所以可以用碳酸氢钠溶液检验乙醇中是否含有乙酸,故C正确;D.乙醇
含有羟基,可与钠发生反应生成氢气,但乙醇为非电解质,不能电离产生氢离子,故D错
误;故选:D。
4.关于酯化反应的叙述不正确的是( )A.浓硫酸在酯化反应中只起催化剂作用
B.酯化反应是有限度的
C.酯化反应的机理是酸去羟基,醇去羟基上的氢原子
D.酯化反应属于取代反应
【答案】A
【解析】A项,浓硫酸在酯化反应中起催化剂和吸水剂作用,错误;B项,酯化反应属于
可逆反应,是有限度的,正确;C项,酯化反应的机理是酸脱去羟基,醇脱去羟基上的氢
原子,正确;D项,酯化反应属于取代反应,正确。
5.将1 乙醇(其中的氧用 标记)在浓硫酸存在的条件下与足量乙酸充分反应。下列
叙述错误的是( )
A.生成的乙酸乙酯中含有 B.生成的水分子中不含有
C.可能生成40g乙酸乙酯 D.可能生成90g乙酸乙酯
【答案】D
【解析】A.酯化反应及断键情况:
,故 只存在于生成物乙酸乙酯中,故A 正确;B.由A
分析可知 只存在于生成物乙酸乙酯中,不存在水中,故B正确;C.若1mol乙醇完全
反应,则可生成1mol ,其质量为90g,但酯化反应为可逆反应,1mol
乙醇不可能完全转化为乙酸乙酯,故生成乙酸乙酯的质量应小于90g,故C项正确,D.由
C分析可知生成乙酸乙酯的质量应小于90g,故D项错误;故答案为:D
6. 实验室用乙酸、乙醇、浓硫酸制取乙酸乙酯,加热蒸馏后,在饱和NaCO 溶液的液面
2 3
上得到无色油状液体,当振荡混合物时,有气泡产生,主要原因可能是( )
A.有部分HSO 被蒸馏出来 B.有部分未反应的乙醇被蒸馏出来
2 4
C.有部分未反应的乙酸被蒸馏出来 D.有部分乙酸乙酯与碳酸钠反应
【答案】C
【解析】制取乙酸乙酯时,加热挥发的乙酸会随蒸气进入碳酸钠溶液中,而乙酸的酸性比
碳酸强,所以会有二氧化碳生成。
7.在下列物质中,不能与 发生化学反应的是( )
①CHCHOH(酸催化) ②CHCHCHCH ③Na ④CHCOOH(酸催化)
3 2 3 2 2 3 3A.①② B.①④ C.只有② D.③④
【答案】C
【解析】根据有机物的结构简式可知,含有的官能团为醇羟基、羧基,含有苯环;①含有
羧基,可与CHCHOH(酸催化)发生酯化反应,不符合题意;②有机物不与CHCHCHCH
3 2 3 2 2 3
发生化学反应,符合题意;③含有的羟基与羧基均可与Na发生化学反应,不符合题意;
④含有羟基可与CHCOOH(酸催化)发生酯化反应,不符合题意;答案选C。
3
8.下列结论正确的是( )
A.乙醇能与金属钠反应,说明在反应中乙醇分子断裂C—O键而失去羟基
B.0.1 mol乙醇与足量的钠反应生成0.05 mol H,说明乙醇分子中有一个羟基
2
C.在制备乙酸乙酯后剩余的反应液中加入碳酸钠溶液,产生气泡,说明还有乙酸剩余
D.将乙醇和浓硫酸共热后得到的气体通入溴水中,溴水褪色,说明生成了乙烯
【答案】B
【解析】乙醇与金属钠反应时,乙醇分子断裂的是H—O键,A项错;0.1 mol乙醇与足量
的钠反应生成0.05 mol H ,说明乙醇分子中有一个羟基,B项正确;酯化反应需要加入浓
2
硫酸作催化剂,硫酸也可以与NaCO 溶液反应生成CO ,C项错误;乙醇与浓硫酸共热,
2 3 2
温度不同,发生的反应也不同,其中浓硫酸有强氧化性,可以将乙醇氧化,而浓硫酸被还
原生成SO ,通入溴水中,也能使溴水褪色,D项错误。
2
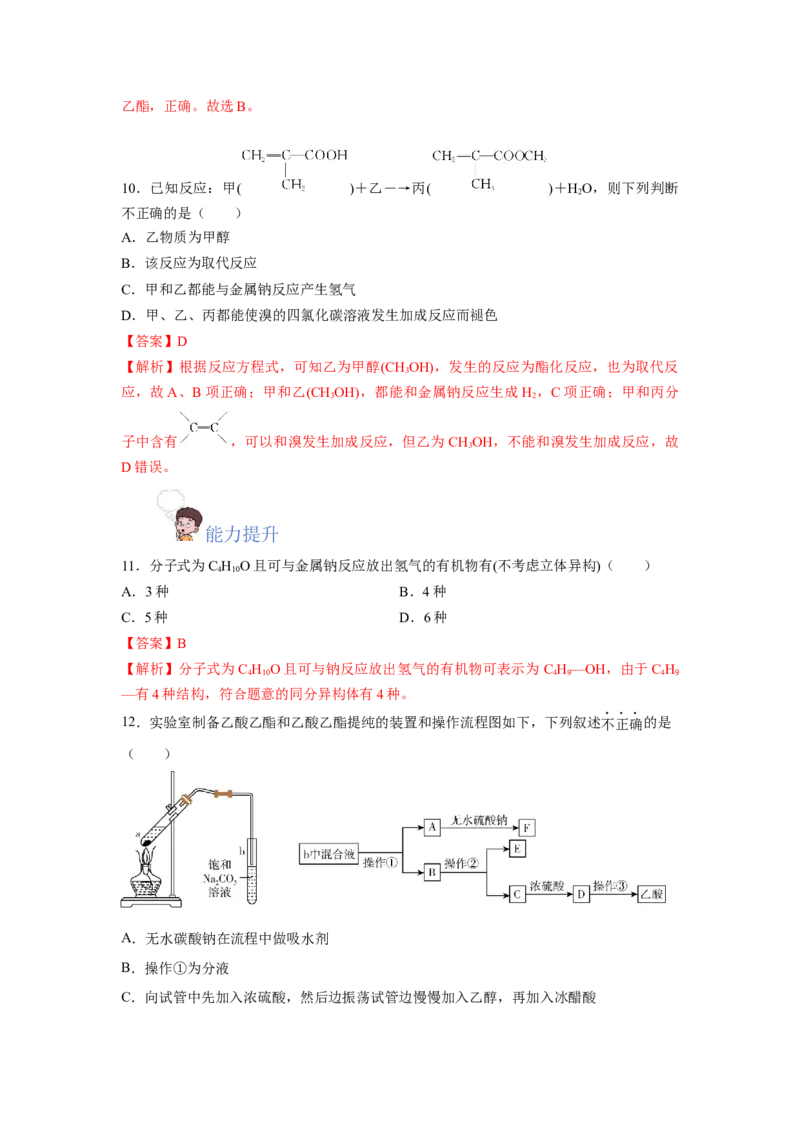
9.乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计了如图所示的两套装置,
用乙醇、乙酸和浓硫酸作原料分别制备乙酸乙酯(沸点77.2 ℃)。下列有关说法不正确的是
( )
A.浓硫酸能提高酯化反应的速率
B.温度越高反应速率越大,装置a更佳
C.装置b比装置a原料损失得少
D.用饱和NaCO 溶液收集乙酸乙酯有利于酯的纯化
2 3
【答案】B
【解析】A选项,乙酸与乙醇生成乙酸乙酯的反应是可逆反应,浓硫酸是该反应的催化
剂,能起到增大反应速率的作用,正确;B选项,乙酸、乙醇都易挥发,温度高会加速反
应物的挥发,降低酯的产率,因此装置 b更佳,错误;C选项,装置b是通过水浴加热,
相对于装置a,温度较低,减少了反应物的挥发,正确;D选项,乙酸乙酯在饱和NaCO
2 3
溶液中的溶解度很小,且能将混在乙酸乙酯中的乙酸和部分乙醇除去,得到较纯净的乙酸乙酯,正确。故选B。
10.已知反应:甲( )+乙―→丙( )+HO,则下列判断
2
不正确的是( )
A.乙物质为甲醇
B.该反应为取代反应
C.甲和乙都能与金属钠反应产生氢气
D.甲、乙、丙都能使溴的四氯化碳溶液发生加成反应而褪色
【答案】D
【解析】根据反应方程式,可知乙为甲醇(CHOH),发生的反应为酯化反应,也为取代反
3
应,故A、B项正确;甲和乙(CHOH),都能和金属钠反应生成H ,C项正确;甲和丙分
3 2
子中含有 ,可以和溴发生加成反应,但乙为CHOH,不能和溴发生加成反应,故
3
D错误。
能力提升
11.分子式为C H O且可与金属钠反应放出氢气的有机物有(不考虑立体异构)( )
4 10
A.3种 B.4种
C.5种 D.6种
【答案】B
【解析】分子式为C H O且可与钠反应放出氢气的有机物可表示为 C H—OH,由于C H
4 10 4 9 4 9
—有4种结构,符合题意的同分异构体有4种。
12.实验室制备乙酸乙酯和乙酸乙酯提纯的装置和操作流程图如下,下列叙述不正确的是
( )
A.无水碳酸钠在流程中做吸水剂
B.操作①为分液
C.向试管中先加入浓硫酸,然后边振荡试管边慢慢加入乙醇,再加入冰醋酸D.试管b中饱和 溶液的作用是吸收蒸出的少量乙酸和乙醇,减小乙酸乙酯的溶解
【答案】C
【解析】实验室制备乙酸乙酯时,向试管中先加无水乙醇,再缓慢加入浓硫酸,冷却后再
加入无水乙酸,加热,用饱和碳酸钠溶液接受,将b中混合液分液得到乙酸乙酯和乙酸钠
和乙醇混合溶液,用无水硫酸钠干燥乙酸乙酯,将乙酸钠和乙醇混合溶液蒸馏得到乙醇和
乙酸钠,向乙酸钠溶液中加入硫酸得到乙酸和硫酸钠,再蒸馏得到乙酸。A.A是乙酸乙
酯,乙酸乙酯中有水分,因此无水碳酸钠在流程中做吸水剂,起干燥作用,故A正确;
B.b中是不相溶的两种液体分离,因此操作①为分液,故B正确;C.向试管中先加入乙
醇,然后边振荡试管边慢慢加入浓硫酸,冷却后再加入冰醋酸,故C错误;D.试管b中
饱和NaCO 溶液的作用是吸收蒸出的少量乙酸,溶解乙醇,降低乙酸乙酯溶解度,减小乙
2 3
酸乙酯的溶解,故D正确。综上所述,答案为C。
13.苹果酸有特殊的酸味,主要用于食品和医药行业。苹果酸的结构简式为:
,下列说法正确的是( )
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.1 mol苹果酸与足量Na反应生成1 mol H
2
D.HOOC—CH —CH(OH)—COOH与苹果酸互为同分异构体
2
【答案】 A
【解析】A项,苹果酸中含—OH和—COOH 2种能发生酯化反应的官能团;B项,1 mol
苹果酸可与2 mol NaOH发生中和反应;C项,1 mol苹果酸与足量Na反应生成1.5 mol
H;D项,二者为同一物质。
2
14.分子式为C HO 的有机化合物A具有如下性质:
2 4 2
①A+Na→迅速产生气泡;②A+CHCHOH――→有香味的物质。
3 2
(1)根据上述信息,对该化合物可作出的判断是__________________(填字母)。
A.一定含有—OH B.一定含有—COOH
C.有机化合物A为乙醇 D.有机化合物A为乙酸
(2)A 与 钠 反 应 的 化 学 方 程 式 为
___________________________________________________。
(3) 化 合 物 A 和 CHCHOH 反 应 生 成 的 有 香 味 的 物 质 的 结 构 简 式 为
3 2
_____________________。
(4)有机化合物B分子式为C HO,与Na反应迅速产生H,且1 mol B与足量Na反应放出
2 4 3 2
1 mol H ,B的结构简式为___________________________。
2答案:(1)BD (2)2CH COOH+2Na―→2CHCOONa+H↑
3 3 2
(3)CH COOCH CH (4)HOCH COOH
3 2 3 2
解析:(1)根据A的分子式及A的化学性质推知A为乙酸。(3)乙醇和CHCOOH发生酯化
3
反应生成乙酸乙酯。(4)与Na反应迅速,则含有—COOH,且产生H 与消耗B的物质的量
2
之比为1∶1,根据分子式,则必含—OH,B的结构简式为HOCH COOH。
2
直击高考
15.某有机物的结构简式如图所示,下列关于这种有机物的说法不正确的是( )
①分子中含有苯环,属于芳香烃
②既能使溴水褪色,又能使酸性KMnO 溶液褪色
4
③既能和乙酸发生酯化反应,又能和乙醇发生酯化反应
④1mol该有机物分别与足量的Na、NaHCO 反应,产生气体的物质的量之比是2∶1
3
A.1种 B.2种
C.3种 D.4种
【答案】B
【解析】①分子中含有苯环,还含有羧基和羟基,则该物质不属于芳香烃,①项错误;②
该分子含有碳碳双键,则既能使溴水褪色,又能使酸性KMnO 溶液褪色,②项正确;③该
4
分子含有羧基和羟基,则既能和乙酸发生酯化反应,又能和乙醇发生酯化反应,③项正
确;④1mol该有机物分别与足量的Na、NaHCO 反应,分别产生1mol氢气和1mol二氧化
3
碳,则产生气体的物质的量之比是1∶1,④项错误;答案选B。
16.已知A是一种气态烃,其密度在标准状况下是H 的14倍。下列关系图中部分产物可
2
能略去,试回答下列问题:已知反应:R—X+NaOH R—OH+NaX(R代表烃基,X代表卤素原子)
(1)C分子的官能团的名称为__________________________。
(2)反应①~⑦中属于取代反应的是____________________。
(3)C与F以物质的量之比2:1反应生成G,反应④的化学方程式为
_______________________。
(4)B物质可在催化剂作用下被空气中的氧气氧化为具有刺激性气味的物质,写出反应的化
学方程式_____________________________________________________。
(5)聚苯乙烯的结构简式为________________________________。
(6)下列说法正确的是_______________________。
a.D在一定条件下可能会和水反应生成B和C b.B和F属于同系物
c.A、B、F和I都能使酸性高锰酸钾溶液褪色 d.与E互为同分异构体的有机物只有1种
【答案】(1)羧基 (2)③④⑤
(3)HOCHCHOH+2CHCOOH CHCOOCH CHOOCCH + 2H O
2 2 3 3 2 2 3 2
(4)2CH CHOH + O ――→2CHCHO + 2H O
3 2 2 3 2
(5) (6)acd
【解析】A是一种气态烃,其密度在标准状况下是H 的14倍,A的相对分子质量是28,
2
因此A是乙烯;A和水发生加成反应生成B是乙醇,乙醇被酸性高锰酸钾溶液氧化生成C
是乙酸,乙酸和乙醇发生酯化反应生成D是乙酸乙酯,乙烯和溴单质发生加成反应生成E
是BrCHCHBr,根据已知信息E发生水解反应生成F是乙二醇,乙二醇和乙酸发生酯化反
2 2应生成G为CHCOOCH CHOOCCH ,E和苯发生取代反应生成H,H发生消去反应生成
3 2 2 3
I,I分子中含有碳碳双键,可发生加聚反应生成聚苯乙烯,据此解答。
(1)C是乙酸,分子的官能团的名称为羧基。
(2)酯化反应和水解反应均属于取代反应,根据以上分析可知反应①~⑦中属于取代反应的
是③④⑤。
(3)C与F以物质的量之比2:1发生酯化反应生成G,反应④的化学方程式为
HOCH CHOH+2CHCOOH CHCOOCH CHOOCCH + 2H O。
2 2 3 3 2 2 3 2
(4)乙醇可在催化剂作用下被空气中的氧气氧化为具有刺激性气味的物质乙醛,反应的化学
方程式为2CHCHOH + O ――→2CHCHO + 2H O。
3 2 2 3 2
(5)聚苯乙烯的结构简式为 。