文档内容
2.2.1化学平衡(分层作业)
1.乙酸和乙醇发生酯化反应: 。起始时向某圆底烧瓶
中加入 浓硫酸和 ,反应达到平衡后,下列有关说法正确的是
A.反应需要加热,则说明该酯化反应为吸热反应
B.反应达到平衡后 的物质的量不可能为0.008mol
C.加入 反应一段时间后,反应混合物分子中均含
D. 和 分子中均含 时,说明该反应已达平衡状态
2.可逆反应N+3H 2NH 在密闭容器中进行一段时间后,达到平衡状态。则下列说法中正确的是
2 2 3
A.N
2
、H
2
不再化⇌合
B.N、H、NH 浓度不再变化
2 2 3
C.N、H、NH 的速率之比为1:3:2
2 2 3
D.改变条件,N、H、NH 的浓度也不再变化
2 2 3
3.在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g) pC(g)+qD(g)(m、n、p、q为任意整
数)。下列不能作为达到平衡状态的标志的是 ⇌
A.单位时间内有m mol A消耗,同时有p mol C生成
B.体系的温度不再改变
C.各组分的浓度不再改变
D.各组分的质量分数不再改变
4.在恒温恒容的条件下,可作为反应 达到平衡状态的标志的是
A.容器内气体的密度不随时间而变化
B.容器内的总压强不随时间而变化
C.容器内气体的颜色不随时间而变化
D.H、I、HI气体的浓度之比为1:1:2的状态
2 2
5.在一定温度下的恒容密闭容器中,当下列物理量不在发生变化时,①混合气体的压强;②混合气体的密度;
③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤混合气体的颜色;⑥各反应物或生成物的浓度
之比等于化学计量数之比;⑦某种气体的百分含量。其中能说明反应NH COONH(s) 2NH (g)+CO (g)达到
2 4 3 2平衡状态的是
A.①②③ B.②④⑦ C.①⑥⑦ D.①②⑦
6.在某恒压密闭容器中充入1molCO和2molH ,发生反应:CO(g)+2H(g) CHOH(g),下列说法中能够判断
2 2 3
该反应一定处于平衡状态的是
A.单位时间内生成1molCH OH的同时消耗2molH
3 2
B.容器中CO与H 的体积之比恒定不变
2
C.容器中CO与CHOH物质的之比为1:1
3
D.容器中混合气体的密度不随时间变化
7.在一密闭容器中进行反应:2SO (g)+O(g) 2SO (g),已知反应过程中某一时刻SO 、O、SO 的浓度分别为
2 2 3 2 2 3
0.1 mol/L、0.05 mol/L、0.3 mol/L。当反应达到⇌平衡时,可能存在的数据是
A.SO 为0.4 mol/L,O 为0.2 mol/L
2 2
B.SO 、SO 均为0.8 mol/L
2 3
C.SO 为0.4 mol/L
3
D.SO 为0.35 mol/L
2
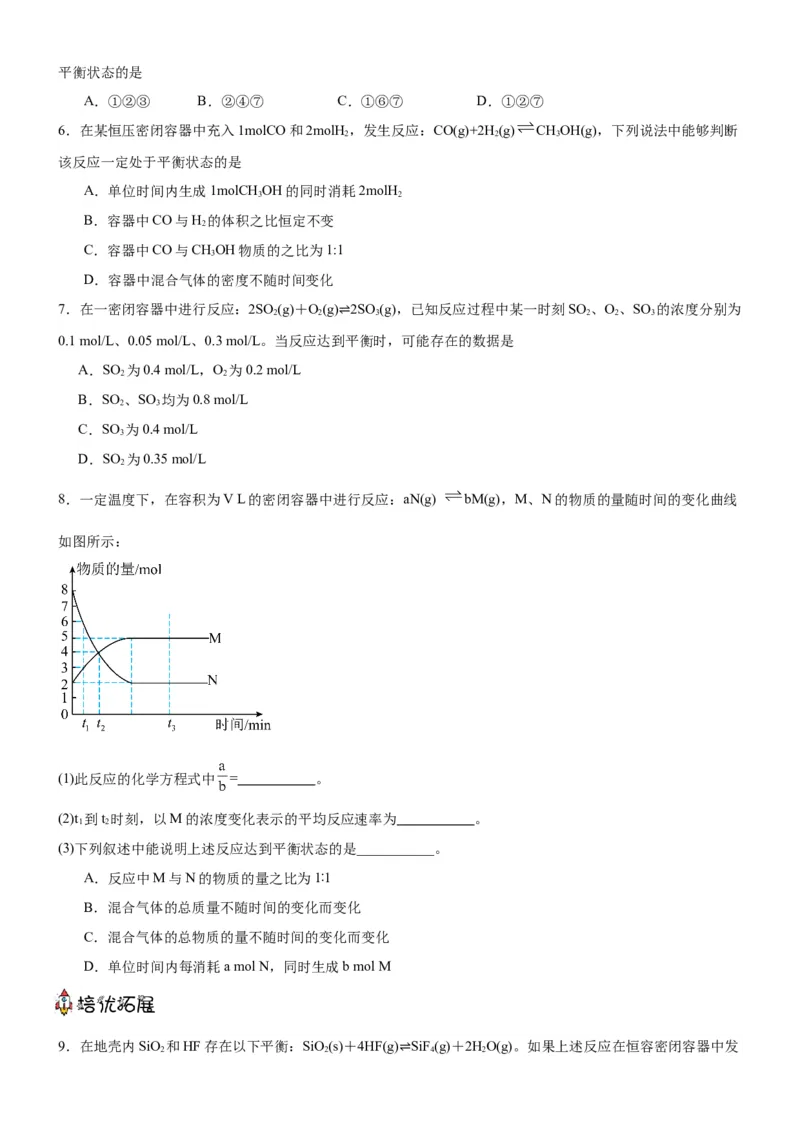
8.一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线
如图所示:
(1)此反应的化学方程式中 = 。
(2)t 到t 时刻,以M的浓度变化表示的平均反应速率为 。
1 2
(3)下列叙述中能说明上述反应达到平衡状态的是___________。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
9.在地壳内SiO 和HF存在以下平衡:SiO(s)+4HF(g) SiF(g)+2HO(g)。如果上述反应在恒容密闭容器中发
2 2 4 2
⇌生,下列不能说明该反应达到平衡状态的是
A. v (HF)=v (H O)
正 逆 2
B.SiF 与HO的浓度之比保持不变
4 2
C.SiO 的质量保持不变
2
D.混合气体的总物质的量保持不变
10.一定温度下,在恒容密闭容器中充入 和 ,发生反应:
(甲基环氧乙烷)。下列不能说明反应达到平衡状态的是
A.混合气体的总压强不再变化
B.混合气体的平均摩尔质量不再变化
C.丙烯与氧气的浓度之比保持不变
D. 不再变化
11.已知: 溶液是检验 的试剂,若溶液中存在 ,将产生蓝色沉淀。将 的KI溶
液和 的 溶液等体积混合后,取混合液分别完成下列实验,其中能说明溶液中存在化学平
衡“ ”的是
实验编
实验操作 实验现象
号
① 滴入KSCN溶液 溶液变红色
② 滴入 溶液 有黄色沉淀生成
③ 滴入 溶液 有蓝色沉淀生成
④ 滴入淀粉溶液 溶液变蓝色
A.① B.②和④ C.③和④ D.①和②
12.已知5 mL 0.01 mol/L KI溶液与1 mL0.01mol/LCuCl 溶液发生反应:2CuCl (aq)+4KI(aq) 2CuI(s)+I (aq)
2 2 2
+4KCl(aq),下列说法错误的是
A.Cu2+的氧化性强于I
2
B.该反应的氧化剂和还原剂的物质的量之比为1∶1
C.该反应的还原产物有两种
D.充分反应后静置,取上层清液并向其中加入NaOH溶液,出现蓝色沉淀,表明该化学反应存在限度13.一定温度下,关于可逆反应 ,下列说法正确的是
A.改变外界条件,可逆反应的限度一定会发生变化
B.若单位时间内生成 的同时消耗 ,则反应达到平衡状态
C.恒容条件下,反应体系中总压强不再发生变化时反应达到了平衡状态
D.恒容条件下,反应体系中混合气体密度不再发生变化时反应到达了平衡状态
14.将2.0mol 、1.0mol 和0.5mol 充入体积不变的密闭容器中,在一定条件下发生反应:
,反应达到平衡时,下列数据合理的是
A. B.
C. D.
15.硫代硫酸钠 是重要的化工原料,易溶于水。实验室中探究 与某些金属阳离子的氧化还原
反应情况。
资料:i. (紫黑色) ;
ii. 为白色沉淀, ;
。
回答下列问题:
探究一
编
装置 试剂X 实验现象
号
① 溶液 混合后溶液先变成紫黑色, 后溶液几乎变为无色
② 溶液 一段时间后,生成白色沉淀,振荡后,沉淀溶解,得到无色溶液
(1)根据实验①的现象,初步判断最终 被 还原为 ,通过 (填操作、试剂和现象),进一步证实
生成了 。进一步实验证明 最终被氧化为 ,该过程总反应的化学方程式为 。(2)氧化性: (同浓度)。但实验②中 未发生氧化还原反应的原因是 。
探究二
编
装置 试剂X 实验现象
号
③ 溶液 立即生成白色絮状沉淀,沉淀很快变为黑色沉淀。
(3)实验③中黑色沉淀可能为 或 。通过 (填操作、试剂和现象),进一步证实生成了 。白色
絮状沉淀变为黑色沉淀的化学方程式为 。