文档内容
第三章 有机化合物
第三节 乙醇与乙酸
第二课时 乙酸
【学习目标】1.通过模型观察,讨论交流、知道乙酸的分子结构特点及物理性质和化学性质,知道
乙酸具有酸的通性且酸性比碳酸强,会写乙酸与Na、NaOH、NaCO 、NaHCO 等物质反应的化学方程
2 3 3
式。
2.通过设计实验探究、动画模拟演示,提高基本化学实验技能,了解酯化反应的概念,知道乙酸的酯
化反应原理和断键部位,能正确书写酯化反应方程式。
3.结合生活经验和化学实验,初步体会有机物制备方法和特点,进一步认识乙酸对于人类日常生活、
身体健康的重要性。
【学习重点】乙酸的结构及化学性质(酸性、酯化反应)
【学习难点】乙酸的酯化反应原理及实验设计
【课前预习】
旧知回顾:1.什么叫烃的含氧衍生物,请举例说明。
2.酸具有哪些通性?请举例说明。
新知预习:1. 乙酸的分子组成、结构有和特点?
2.乙酸具有哪些主要化学性质?
【课中探究】
情景导入:传说古代山西省有个酿酒高手叫杜康,他儿子黑塔跟父亲也学会了酿酒技术后,黑塔觉得
酿酒后把酒糟扔掉可惜,于是他把酒糟浸泡在水缸里,到了第二十一日的酉时,一开缸,却发现一股浓郁
的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”,这“调味酱”就是今天的醋。
一、乙酸的结构与性质
活动一、乙酸的物理性质与结构特征
任务一、联系生活中的食醋,观察乙酸样品,闻其气味,阅读教材P79页内容,思考乙酸具有哪些物
理性质?填写表格内容。
①食醋与乙醇:
②乙酸的物理性质:
俗名 颜色 状态 气味 溶解性 熔点 沸点 挥发性
16.6℃ 117.9℃
③冰醋酸:
注意:
任务二、阅读教材P79页内容,结合图7-21,搭建并观察乙酸分子的球棍模型,思考乙醇分子的组成
和结构有何特点?填写表格内容。
分子式 结构式 结构简式 球棍模型 空间填充模型
结构特
点
注意:
【对应练习】1.下列关于乙酸的说法中不正确的是( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有强烈刺激性气味的液体
D.乙酸分子中有四个氢原子,所以不是一元酸
2.下列说法正确的是( )
A.羧酸的官能团是羟基
B.羟基和氢氧根中含有的电子数不同C.在氧气中燃烧只生成二氧化碳和水的有机物一定是烃
D.乙醇与钠反应生成氢气,此现象说明乙醇具有酸性
活动二、探究乙酸的化学性质
任务一、结合教材P80页”思考与讨论”,根据下列药品,设计实验证明乙酸的酸性,填写表格内
容。
药品:镁条、NaOH溶液、NaCO 粉末、乙酸溶液、酚酞、石蕊 、氧化铜粉末
2 3
实验 实验内容 实验现象 实验结论、反应方程式
向一支盛有少量乙酸的
实验一
试管里加入一小段镁条
乙酸滴加到滴有酚酞的
实验二
NaOH溶液中
向一盛有少量碳酸钠粉
实验三 末的试管里,加入约
3mL乙酸溶液
将石蕊试液滴加到乙酸
实验四
中
将以酸加入到氧化铜粉
实验五
末中
结论
注意:
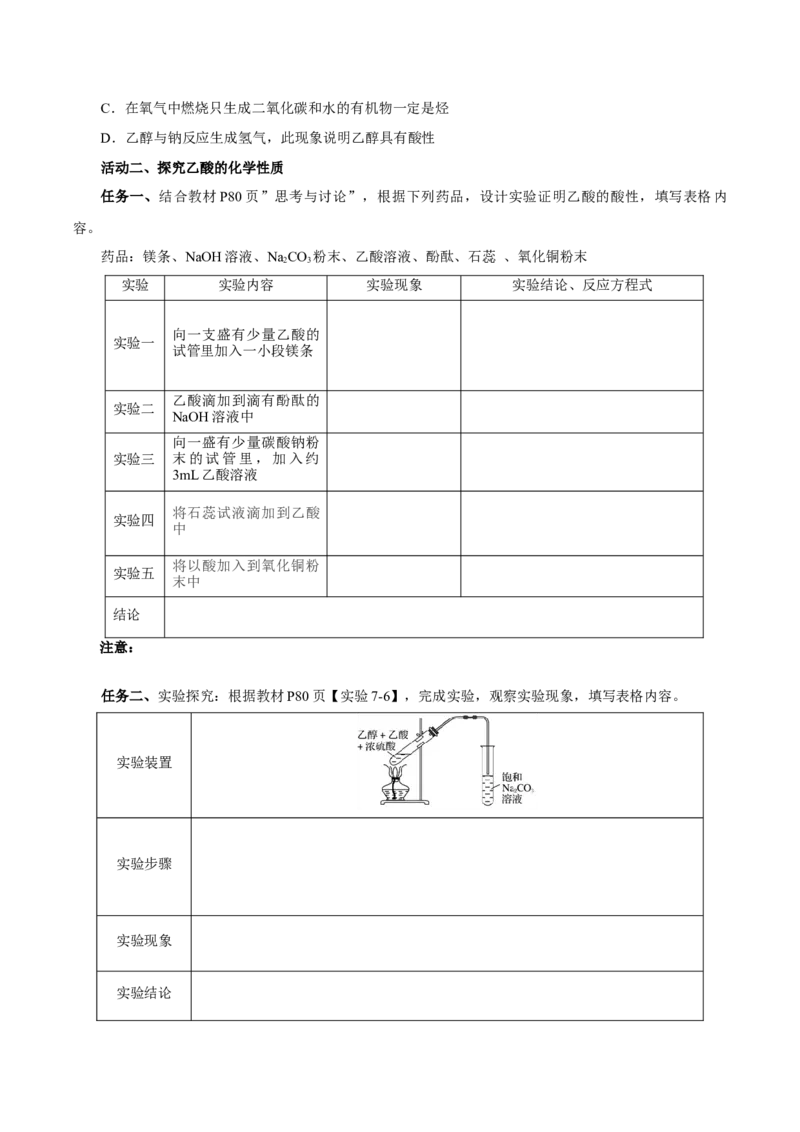
任务二、实验探究:根据教材P80页【实验7-6】,完成实验,观察实验现象,填写表格内容。
实验装置
实验步骤
实验现象
实验结论化学方程式
【对应练习】1.下列说法不正确的是( )
A.乙酸的沸点比乙醇的高
B.乙酸能和碳酸钠反应生成二氧化碳气体,说明乙酸的酸性强于碳酸
C.乙酸和乙醇生成乙酸乙酯的反应属于酸碱中和反应
D.乙酸分子中虽然有4个氢原子,但乙酸是一元酸
2.某同学利用图所示装置制备乙酸乙酯。实验如下:
①向浓H SO 乙醇混合液中滴入乙酸后,加热试管A
2 4
②一段时间后,试管B中红色溶液上方出现油状液体
③停止加热,振荡试管B,油状液体层变薄,下层红色溶液褪色
④取下层褪色后的溶液,滴入酚酞后又出现红色
结合上述实验,下列说法正确的是( )
A. ①中加热利于加快酯化反应速率,故温度越高越好
B. ③中油状液体层变薄主要是乙酸乙酯溶于Na CO 溶液所 致
2 3
C. ③中红色褪去的原因可能是酚酞溶于乙酸乙酯中
D. 取②中上层油状液体测其核磁共振氢谱,共有3组峰
二、酯化反应与酯
活动一、探究酯化反应的原理
任务一、阅读教材P80页内容,结合【实验7-6】,思考酯化反应的概念及特点是什么?如何证明酯
化反应的断键方式?
①概念:
②特点:
③原理:
注意:
任务二、问题探究:(1)酯化反应实验中,从试剂加入顺序、长导管和浓硫酸的作用、酯的分离等
方面分析,酯化反应实验过程中要注意哪些问题?(2)在制备乙酸乙酯的实验中,大试管中加入碎瓷片的目的是什么?该实验中饱和碳酸钠溶液的作
用是什么?
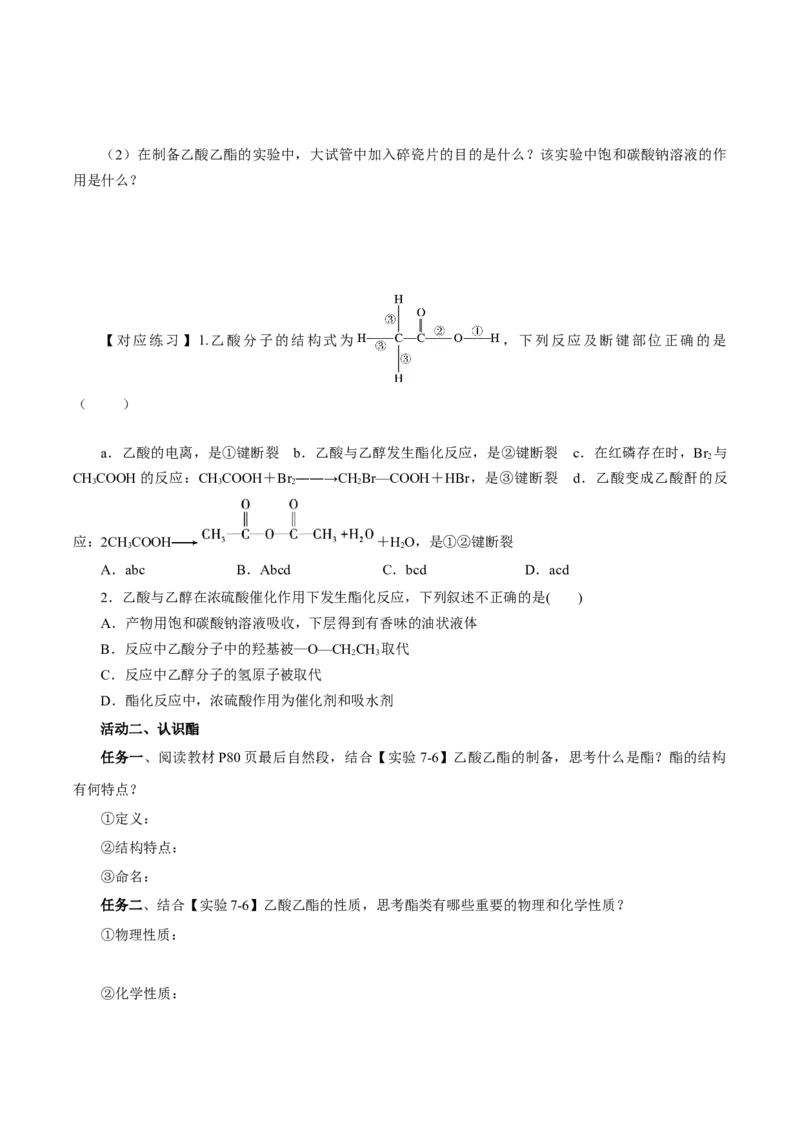
【对应练习】1.乙酸分子的结构式为 ,下列反应及断键部位正确的是
( )
a.乙酸的电离,是①键断裂 b.乙酸与乙醇发生酯化反应,是②键断裂 c.在红磷存在时,Br 与
2
CHCOOH的反应:CHCOOH+Br ――→CHBr—COOH+HBr,是③键断裂 d.乙酸变成乙酸酐的反
3 3 2 2
应:2CHCOOH +HO,是①②键断裂
3 2
A.abc B.Abcd C.bcd D.acd
2.乙酸与乙醇在浓硫酸催化作用下发生酯化反应,下列叙述不正确的是( )
A.产物用饱和碳酸钠溶液吸收,下层得到有香味的油状液体
B.反应中乙酸分子中的羟基被—O—CH CH 取代
2 3
C.反应中乙醇分子的氢原子被取代
D.酯化反应中,浓硫酸作用为催化剂和吸水剂
活动二、认识酯
任务一、阅读教材P80页最后自然段,结合【实验7-6】乙酸乙酯的制备,思考什么是酯?酯的结构
有何特点?
①定义:
②结构特点:
③命名:
任务二、结合【实验7-6】乙酸乙酯的性质,思考酯类有哪些重要的物理和化学性质?
①物理性质:
②化学性质:③用途:
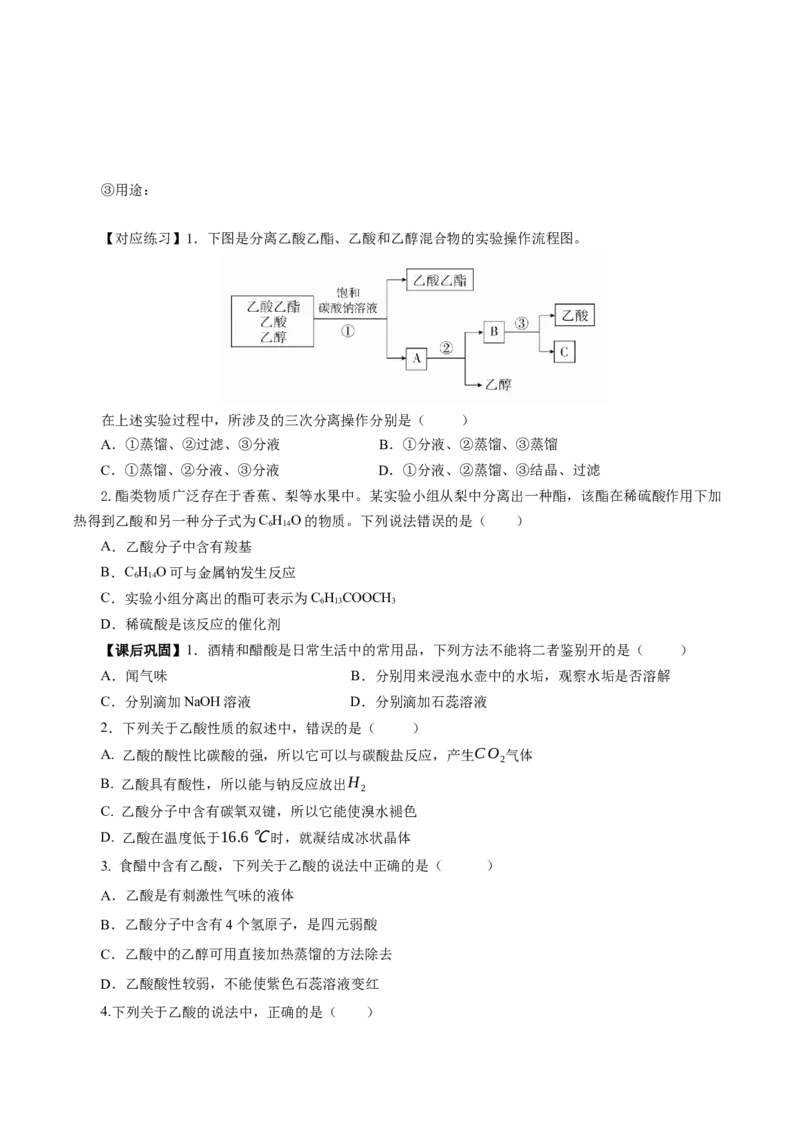
【对应练习】1.下图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图。
在上述实验过程中,所涉及的三次分离操作分别是( )
A.①蒸馏、②过滤、③分液 B.①分液、②蒸馏、③蒸馏
C.①蒸馏、②分液、③分液 D.①分液、②蒸馏、③结晶、过滤
2.酯类物质广泛存在于香蕉、梨等水果中。某实验小组从梨中分离出一种酯,该酯在稀硫酸作用下加
热得到乙酸和另一种分子式为C H O的物质。下列说法错误的是( )
6 14
A.乙酸分子中含有羧基
B.C H O可与金属钠发生反应
6 14
C.实验小组分离出的酯可表示为C H COOCH
6 13 3
D.稀硫酸是该反应的催化剂
【课后巩固】1.酒精和醋酸是日常生活中的常用品,下列方法不能将二者鉴别开的是( )
A.闻气味 B.分别用来浸泡水壶中的水垢,观察水垢是否溶解
C.分别滴加NaOH溶液 D.分别滴加石蕊溶液
2.下列关于乙酸性质的叙述中,错误的是( )
A. 乙酸的酸性比碳酸的强,所以它可以与碳酸盐反应,产生CO 气体
2
B. 乙酸具有酸性,所以能与钠反应放出H
2
C. 乙酸分子中含有碳氧双键,所以它能使溴水褪色
D. 乙酸在温度低于16.6℃时,就凝结成冰状晶体
3. 食醋中含有乙酸,下列关于乙酸的说法中正确的是( )
A.乙酸是有刺激性气味的液体
B.乙酸分子中含有4个氢原子,是四元弱酸
C.乙酸中的乙醇可用直接加热蒸馏的方法除去
D.乙酸酸性较弱,不能使紫色石蕊溶液变红
4.下列关于乙酸的说法中,正确的是( )①乙酸易溶于水和乙醇,其水溶液能导电
②无水乙酸又称为冰醋酸,它是纯净物
③乙酸分子里有四个氢原子,所以它不是一元酸
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤1mol乙酸与足量乙醇在浓硫酸作用下可生成88g乙酸乙酯
⑥食醋中含有乙酸,乙酸可由乙醇氧化得到.
A.②④⑤⑥ B. ①②③⑥
C.①②④⑥ D.①②③④
5.下列物质中,能与醋酸发生反应的是( )
①石蕊 ②乙醇 ③乙醛 ④金属铝 ⑤氧化镁 ⑥碳酸钠 ⑦氢氧化铜
A.①③④⑤⑥⑦ B.②③④⑤
C.①②④⑤⑥⑦ D.全部
6.实验室用下图装置制取乙酸乙酯(使用的乙醇的结构简式为 ),下列有关说法正确的是
( )
A.在甲试管中加入药品的顺序:3mL 、2mL浓硫酸和2mLCHCOOH
3
B.乙试管中的饱和碳酸钠溶液可以换成氢氧化钠溶液
C.从乙试管中分离得到纯净干燥的乙酸乙酯的操作是:振荡、静置、分液
D.生成的乙酸乙酯的结构简式为
7.二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简
式:HO—CH CH—O—CH CH—OH,下列有关二甘醇的叙述中不正确的是( )
2 2 2 2
A.符合通式C H O B.和乙醇中化学键类型相同
n 2n 3
C.能和金属钠反应 D.能使酸性KMnO 溶液褪色
4
8.某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按如图连接好装置并加入混合液,用小火均匀加热3~5 min。③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
回答问题:
(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是________________。
(2)步骤②安装好实验装置,加入药品前还应检查_______________________________。
(3)反应中浓硫酸的作用是________________。
(4)上述实验中饱和碳酸钠溶液的作用是______(填字母)。
a.中和乙酸并吸收乙醇 b.中和乙酸和乙醇
c.减少乙酸乙酯的溶解 d.加速酯的生成,提高其产率
(5)步骤③所观察到的现象是__________________________________________;
从试管乙中分离出乙酸乙酯的实验操作名称是_______________________________。