文档内容
第三章 有机化合物
第三节 乙醇与乙酸
第一课时 乙醇
【学习目标】1.通过模型制作与观察、讨论交流,认识乙醇的物理性质及分子结构特点,了解烃的
衍生物和官能团的概念,初步建立分析有机物官能团与性质关系的思维方法。
2.通过引导分析、实验探究,理解乙醇与钠的反应、乙醇的氧化反应原理,能正确描述实验现象及
书写有关化学反应方程式,培养实验、观察和分析能力。
3.通过对乙醇结构和性质的学习,认识官能团对有机物性质的重要影响,建立“组成—性质—用
途”的有机物学习模式,了解乙醇与人类日常生活和健康的关系。
【学习重点】乙醇的分子组成、结构和化学性质
【学习难点】乙醇与钠及催化氧化反应原理的理解
【课前预习】
旧知回顾:1.将一小块金属钠放入水中,请描述实验现象,并写出有关化学反应方程式。
2.你知道饮用酒和工业酒精有什么区别吗?
新知预习:1.乙醇分子的组成、结构及主要性质有何特点?
2.什么是烃的衍生物?官能团的定义是什么?请举例说明。
【课中探究】
情景导入:播放视频“乙醇的发现史”。“无酒不成席”,当今社会酒已经成为人们餐桌上常见的饮
品之一。中国是最早酿酒的国家,中国的酒文化源远流长,有许多关于酒的脍炙人口的诗句,如:明月几
时有,把酒问青天……这些咏叹酒的诗句证明酒是一种奇特而富有魅力的饮料,其主要成分是什么呢?下
面让我们来细品它那“令人陶醉的醇香”吧!(视频见PPT)一、乙醇的物理性质与结构特点
活动一、认识乙醇的物理性质
任务一、思考与交流:联系生活实际,回答下列应用体现了乙醇的哪些性质和用途?
①用乙醇汽油替代普通汽油-“中国汽车要喝酒” ;②高烧病人擦拭酒精或白酒降温;③碘酒、医用酒
精(含乙醇75%);④酒精灯和固体酒精;⑤洗发时,在水中加入适量的啤酒,洗起来清新爽头,油污一
洗即净。
任务二、阅读教材P77页第二自然段,结合“数据”栏目信息,思考乙醇具有哪些物理性质?
【对应练习】1.有关乙醇的说法不正确的是( )
A.乙醇溶于水 B.乙醇易挥发
C.医用酒精含乙醇体积分数95% D.用工业酒精与生石灰通过加热蒸馏的方法制无水酒
精
2.下列有关乙醇的物理性质的应用中,不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C.由于乙醇能够以任意比溶于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有“酒香不怕巷子深”的说法
活动二、探究乙醇的结构
任务一、阅读教材P77页内容,结合图7-18,搭建乙醇分子的球棍模型,思考乙醇分子的组成和结构
有何特点?填写表格内容。
分子式 结构式 结构简式 球棍模型 空间填充模型
结构特点任务二、讨论交流:结合原子的成键规律,思考分子式为C HO的有机物有哪些可能的结构?并对比
2 6
乙烷的结构,回答什么是烃的衍生物?
①可能结构:
②烃的衍生物定义:
注意:
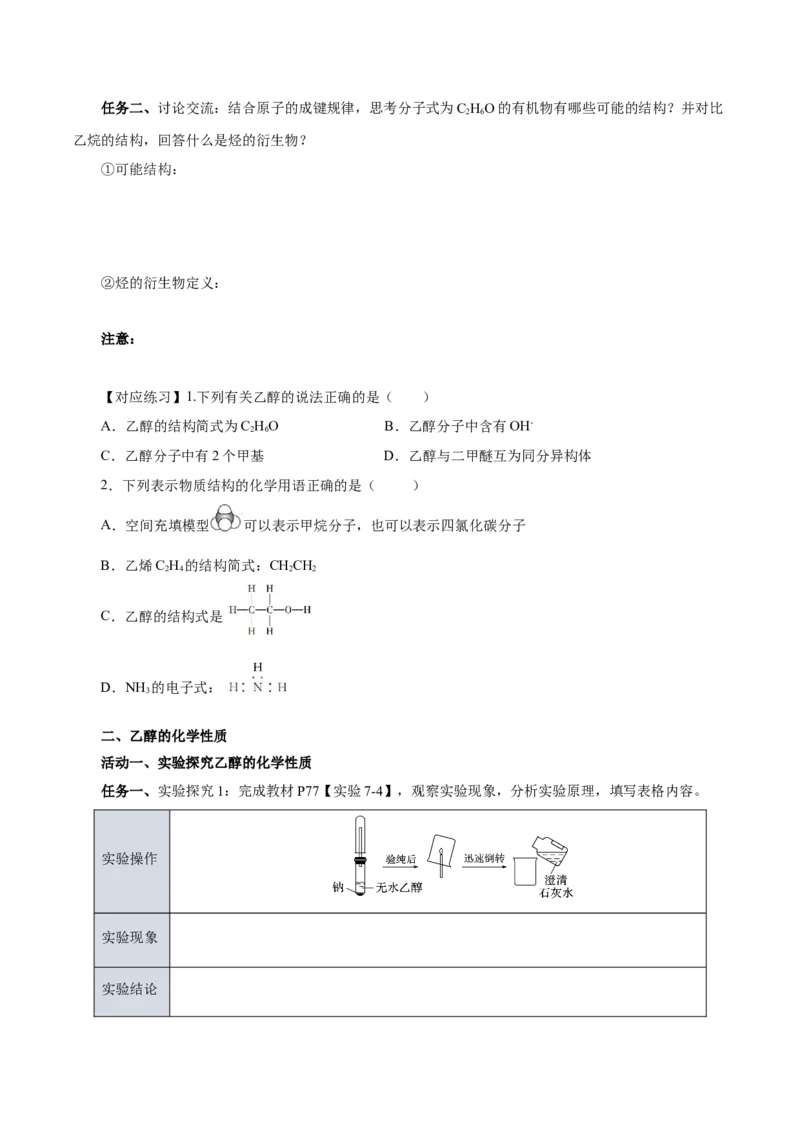
【对应练习】1.下列有关乙醇的说法正确的是( )
A.乙醇的结构简式为C HO B.乙醇分子中含有OH-
2 6
C.乙醇分子中有2个甲基 D.乙醇与二甲醚互为同分异构体
2.下列表示物质结构的化学用语正确的是( )
A.空间充填模型 可以表示甲烷分子,也可以表示四氯化碳分子
B.乙烯C H 的结构简式:CHCH
2 4 2 2
C.乙醇的结构式是
D.NH 的电子式:
3
二、乙醇的化学性质
活动一、实验探究乙醇的化学性质
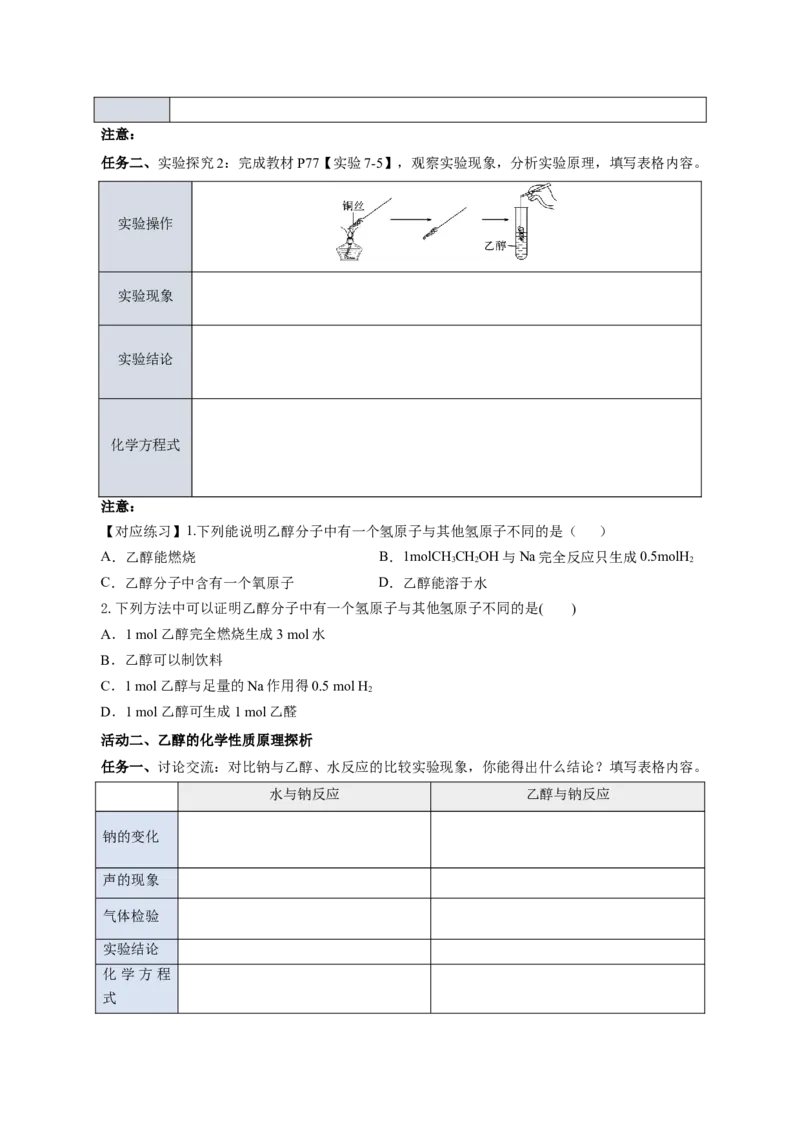
任务一、实验探究1:完成教材P77【实验7-4】,观察实验现象,分析实验原理,填写表格内容。
实验操作
实验现象
实验结论注意:
任务二、实验探究2:完成教材P77【实验7-5】,观察实验现象,分析实验原理,填写表格内容。
实验操作
实验现象
实验结论
化学方程式
注意:
【对应练习】1.下列能说明乙醇分子中有一个氢原子与其他氢原子不同的是( )
A.乙醇能燃烧 B.1molCH CHOH与Na完全反应只生成0.5molH
3 2 2
C.乙醇分子中含有一个氧原子 D.乙醇能溶于水
2.下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子不同的是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇与足量的Na作用得0.5 mol H
2
D.1 mol乙醇可生成1 mol乙醛
活动二、乙醇的化学性质原理探析
任务一、讨论交流:对比钠与乙醇、水反应的比较实验现象,你能得出什么结论?填写表格内容。
水与钠反应 乙醇与钠反应
钠的变化
声的现象
气体检验
实验结论
化学方程
式反应实质
注意:
任务二、阅读教材P78-79页内容,结合【实验7-5】思考乙醇的催化氧化实质及规律是什么?醇的氧
化有何特点?
(1)乙醇催化氧化反应的原理:
(2)乙醇催化氧化反应的断键方式:
(3)醇的催化氧化反应规律:
(4)乙醇与强氧化剂:
(5)乙醇在空气中燃烧 :
注意:
任务三、阅读教材P79页内容,结合“资料卡片”,思考乙醇有哪些用途,生活中过量饮酒对人体有
哪些危害?
【对应练习】1.乙醇能发生如下反应:
①CHCHOH+3O 2CO+3HO;
3 2 2 2 2
②2Cu+O=====2CuO,CHCHOH+CuO CHCHO+HO+Cu。
2 3 2 3 2
由以上反应不能得出的结论是( )
A.由反应①②可知,条件不同,乙醇与O 反应的产物不同
2B.由反应②可知,Cu是乙醇氧化生成乙醛的催化剂
C.由反应①可知,乙醇燃烧时,碳碳键、碳氢键均断裂
D.由反应②可知,乙醇氧化为乙醛时,只断开氢氧键
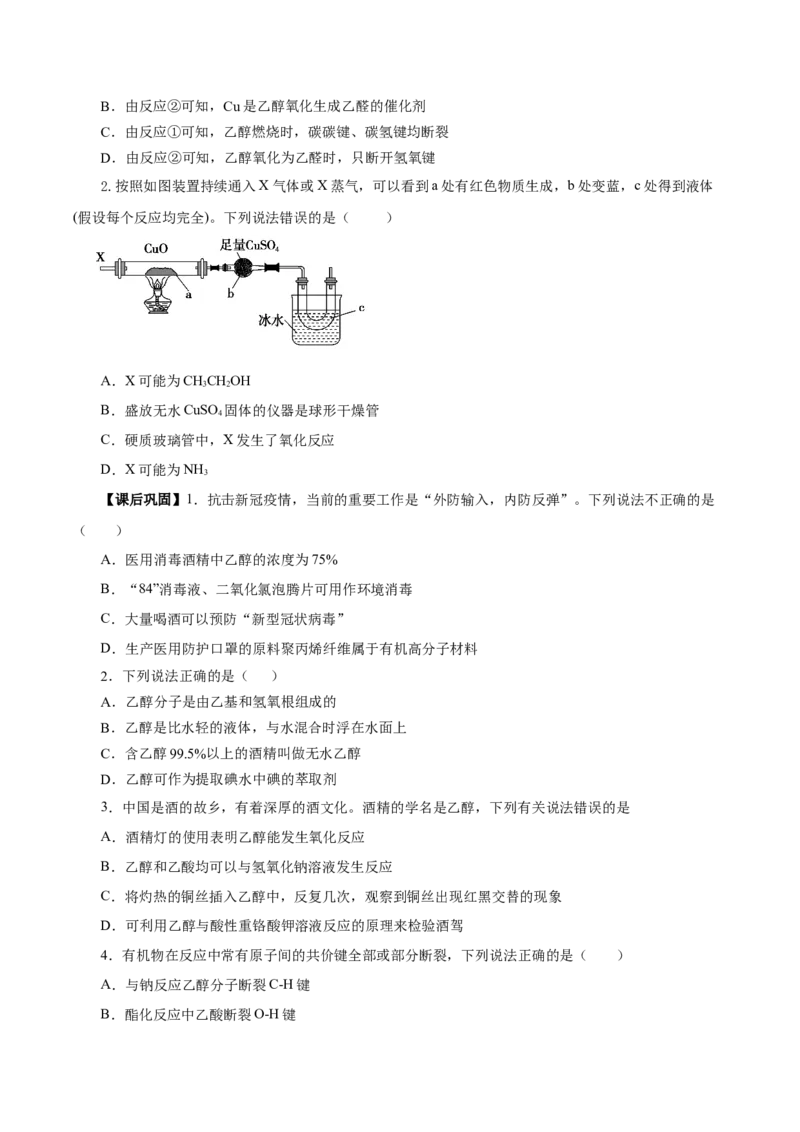
2.按照如图装置持续通入X气体或X蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体
(假设每个反应均完全)。下列说法错误的是( )
A.X可能为CHCHOH
3 2
B.盛放无水CuSO 固体的仪器是球形干燥管
4
C.硬质玻璃管中,X发生了氧化反应
D.X可能为NH
3
【课后巩固】1.抗击新冠疫情,当前的重要工作是“外防输入,内防反弹”。下列说法不正确的是
( )
A.医用消毒酒精中乙醇的浓度为75%
B.“84”消毒液、二氧化氯泡腾片可用作环境消毒
C.大量喝酒可以预防“新型冠状病毒”
D.生产医用防护口罩的原料聚丙烯纤维属于有机高分子材料
2.下列说法正确的是( )
A.乙醇分子是由乙基和氢氧根组成的
B.乙醇是比水轻的液体,与水混合时浮在水面上
C.含乙醇99.5%以上的酒精叫做无水乙醇
D.乙醇可作为提取碘水中碘的萃取剂
3.中国是酒的故乡,有着深厚的酒文化。酒精的学名是乙醇,下列有关说法错误的是
A.酒精灯的使用表明乙醇能发生氧化反应
B.乙醇和乙酸均可以与氢氧化钠溶液发生反应
C.将灼热的铜丝插入乙醇中,反复几次,观察到铜丝出现红黑交替的现象
D.可利用乙醇与酸性重铬酸钾溶液反应的原理来检验酒驾
4.有机物在反应中常有原子间的共价键全部或部分断裂,下列说法正确的是( )
A.与钠反应乙醇分子断裂C-H键
B.酯化反应中乙酸断裂O-H键C.与氢气加成乙烯断裂C=C键中的一条键
D.催化氧化反应中乙醇断裂C-O键
5.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol C HOH 燃烧生成3 mol H O
2 5 2
B.乙醇可以制饮料
C.1 mol C HOH 跟足量的Na反应得0.5 mol H
2 5 2
D.1 mol C HOH燃烧生成2 mol CO
2 5 2
6.乙醇 的结构可能有两种 ,关于确定是 Ⅱ 而不
是 Ⅰ ,下列说法正确的是( )
A.乙醇可以用来制饮料
B.1mol乙醇完全燃烧时生成3mol水
C.1mol乙醇与足量的钠作用生成
D.物质的量相同的乙醇和乙烯气体完全燃烧,耗氧量相同
7.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )
A.和金属钠反应时键①断裂
B.在铜催化共热下与 反应时断裂①和③键
B.与KMnO (H+)反应时只断裂①和⑤键
4
D.在空气中完全燃烧时断裂①②③④⑤键
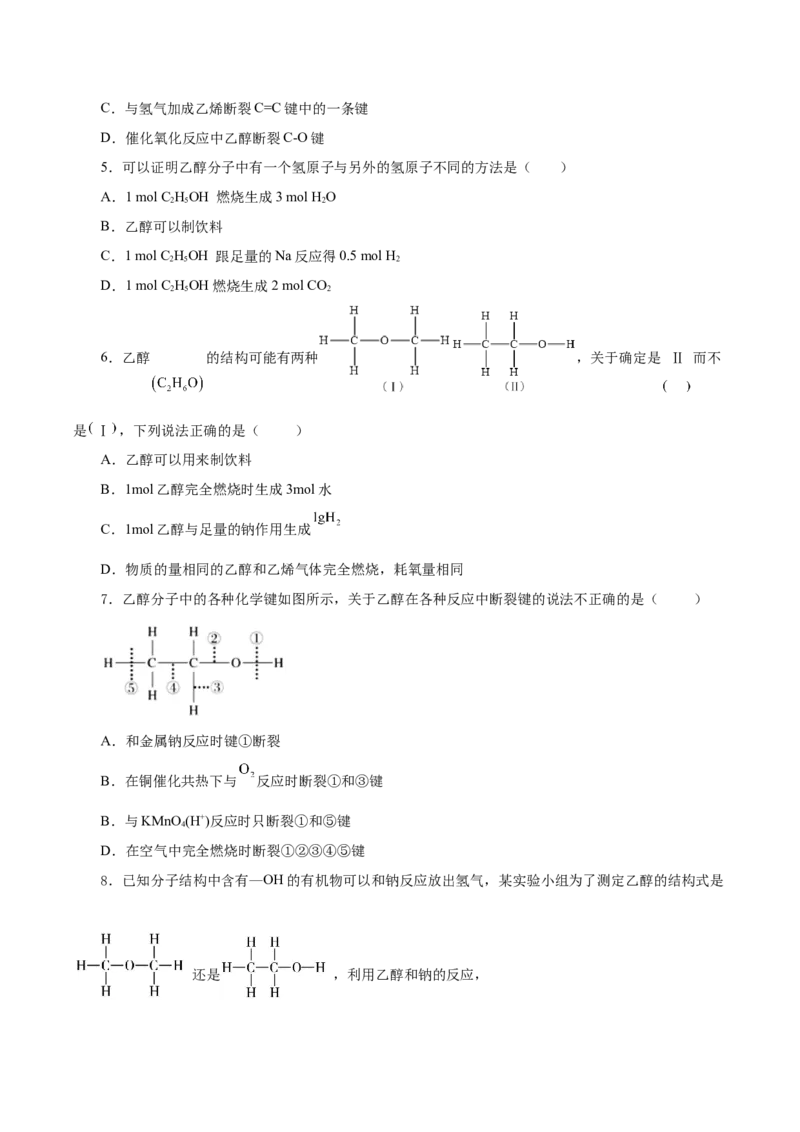
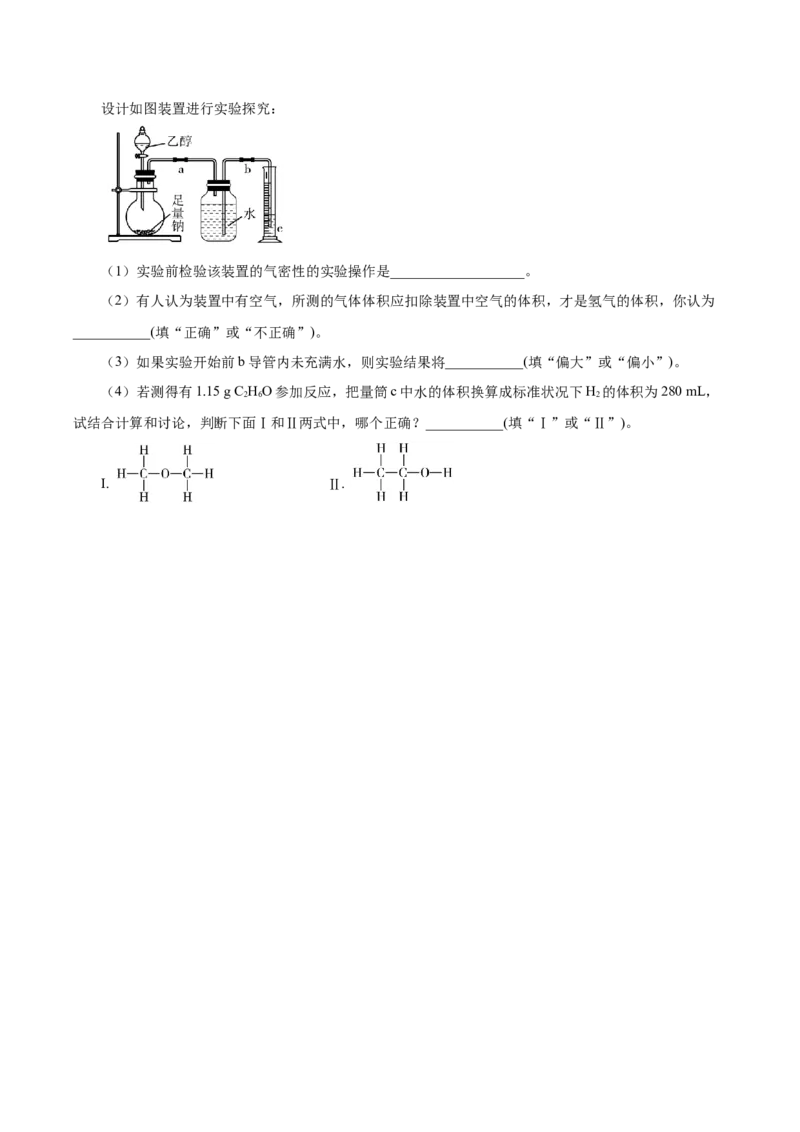
8.已知分子结构中含有—OH的有机物可以和钠反应放出氢气,某实验小组为了测定乙醇的结构式是
还是 ,利用乙醇和钠的反应,设计如图装置进行实验探究:
(1)实验前检验该装置的气密性的实验操作是___________________。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为
___________(填“正确”或“不正确”)。
(3)如果实验开始前b导管内未充满水,则实验结果将___________(填“偏大”或“偏小”)。
(4)若测得有1.15 g C HO参加反应,把量筒c中水的体积换算成标准状况下H 的体积为280 mL,
2 6 2
试结合计算和讨论,判断下面Ⅰ和Ⅱ两式中,哪个正确?___________(填“Ⅰ”或“Ⅱ”)。
Ⅰ. Ⅱ.