文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第二课时 杂化轨道理论简介
基础达标
1.下列关于杂化轨道的说法错误的是( )
A.杂化前后的轨道数不变,但轨道的形状发生了改变
B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
C.部分四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释
D.杂化轨道全部参与形成化学键
2.(多选)关于原子轨道的说法正确的是( )
A.中心原子采取sp3杂化轨道成键的分子,其几何构型可能是正四面体也可能是三角锥形
B.CH 分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合形成
4
C.sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组新轨道
D.AB 型的共价化合物中,中心原子A均采用sp3杂化轨道成键
3
3.下列描述正确的是( )
A.CS 为V形分子
2
B.SiF 与SO 2-的中心原子均为sp3杂化
4 3
C.C H 中σ键与π键的数目比为1:1
2 2
D.水加热到很高温度都难分解是因水分子间存在氢键
4.下列中心原子的杂化轨道类型和分子的空间结构不正确的是( )
A.CCl 中C原子为sp3杂化,为正四面体形 B. HS分子中S原子为sp2杂化,为直线形
4 2
C.CS 中C原子为sp杂化,为直线形 D. BF 中B原子为sp2杂化,为平面三角形
2 3
5.下列有关杂化轨道的说法不正确的是( )
A.轨道杂化前后数目相等,形状、能量不同
B.杂化轨道既可能形成σ键,也可能形成π键
C.杂化轨道成键时,要满足原子轨道最大重叠原理、最小排斥原理
D.原子中能量相近的某些轨道,在成键时能重新组合成能量相等的新轨道6.(多选)下列描述中正确的是( )
A.ClO —的空间结构为V形
2
B.CF 和SO 2-的中心原子均为sp3杂化
4 3
C.在所有的元素中,氟的第一电离能最大
D.C HOH分子中共含有8个极性键,1个π键
2 5
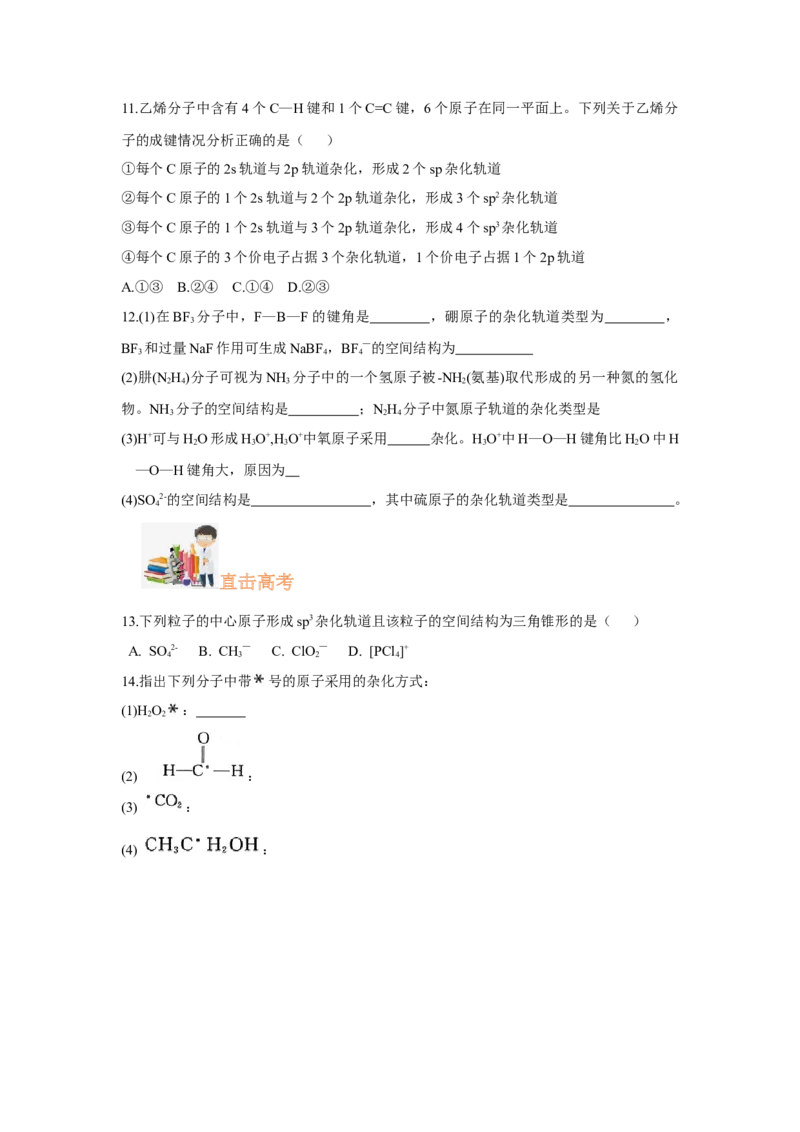
7.甲醛分子的结构式为 ,下列描述正确的是( )
A.甲醛分子中有4个σ键
B.甲醛分子中的C原子为sp3杂化
C.甲醛分子中的O原子为sp杂化
D.甲醛分子为平面三角形,有一个π键垂直于三角形平面
8.下列一组粒子的中心原子杂化轨道类型相同,分子(或离子)的键角不相同的是( )
A.CCl 、SiCl 、SiH B.H Se、NF 、CH C.BCl 、NH 、CO D.TeO 、BF、HO+
4 4 4 2 3 4 3 3 2 3 3 3
9.(1)丙酮( )分子中碳原子轨道的杂化类型是 和 。
(2)I +的空间结构为 形,中心原子的杂化形式为
3
(3)CO 和CHOH分子中C原子的杂化形式分别为 和 。
2 3
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 。
(5)CS 分子中,C原子的杂化轨道类型是
2
(6)[Ni(NH )]SO 中阴离子的空间结构是 。
3 6 4
(7)AsCl 分子的空间结构为 ,其中 As 的杂化轨道类型为
3
。
(8)化合物ClO的空间结构为 形,中心原子的价层电子对数为 。
2
能力提升
10.下列分子的中心原子采用sp2杂化的是( )
①CH ②CH=CH ③ ④HC≡CH ⑤NH ⑥BBr
4 2 2 3 3
A.①②③ B.①②④ C.③④⑤ D.②③⑥11.乙烯分子中含有4个C—H键和1个C=C键,6个原子在同一平面上。下列关于乙烯分
子的成键情况分析正确的是( )
①每个C原子的2s轨道与2p轨道杂化,形成2个sp杂化轨道
②每个C原子的1个2s轨道与2个2p轨道杂化,形成3个sp2杂化轨道
③每个C原子的1个2s轨道与3个2p轨道杂化,形成4个sp3杂化轨道
④每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道
A.①③ B.②④ C.①④ D.②③
12.(1)在BF 分子中,F—B—F的键角是 ,硼原子的杂化轨道类型为 ,
3
BF 和过量NaF作用可生成NaBF ,BF—的空间结构为
3 4 4
(2)肼(N H)分子可视为NH 分子中的一个氢原子被-NH (氨基)取代形成的另一种氮的氢化
2 4 3 2
物。NH 分子的空间结构是 ;NH 分子中氮原子轨道的杂化类型是
3 2 4
(3)H+可与HO形成HO+,H O+中氧原子采用 杂化。HO+中H—O—H键角比HO中H
2 3 3 3 2
—O—H键角大,原因为
(4)SO 2-的空间结构是 ,其中硫原子的杂化轨道类型是 。
4
直击高考
13.下列粒子的中心原子形成sp3杂化轨道且该粒子的空间结构为三角锥形的是( )
A. SO 2- B. CH— C. ClO — D. [PCl ]+
4 3 2 4
14.指出下列分子中带 号的原子采用的杂化方式:
(1)H O :
2 2
(2) :
(3) :
(4) :