文档内容
第 01 章 化学反应的热效应
【一、反应热、焓变】
】
考点过关
一、化学反应与能量变化
1.在化学反应过程中,不仅有物质的变化,还伴随着能量的变化,并遵循_______守恒和_______守恒。
2.化学反应中的能量转化形式:化学能转化为热能、光能、电能等,但主要表现为热能的变化。
3、常见的放热反应与吸热反应
放热反应 吸热反应
①所有燃烧反应;
②大多数化合反应;
①大多数分解反应;
③酸碱中和反应;
②Ba(OH) ·8H O与NH Cl反应;
2 2 4
④金属与酸或水的置换反
③高温条件下C、H 、CO作还原剂的反
应; 2
应。
⑤物质的缓慢氧化;
⑥铝热反应。
思考与交流:①所有分解反应都是吸热反应吗?②需要加热才能发生的反应一定是吸热反应吗?
二、焓变 反应热
1.反应热:一定温度下,化学反应体系向环境_______或从环境_______的_______,称为化学反应的热
效应,简称反应热。
2.焓:焓是与内能有关的物理量,用来描述物质所具有的______,符号为______。
3.焓变:生成物的焓值与反应物的焓值之差,用______表示。
(1)反应热与焓变的关系:反应热在等压条件下等于焓变,用ΔH表示,单位为__________。
(2)意义:当反应体系放热时其焓减小,ΔH为________,即ΔH_______。
当反应体系吸热时其焓减小,ΔH为________,即ΔH_______。
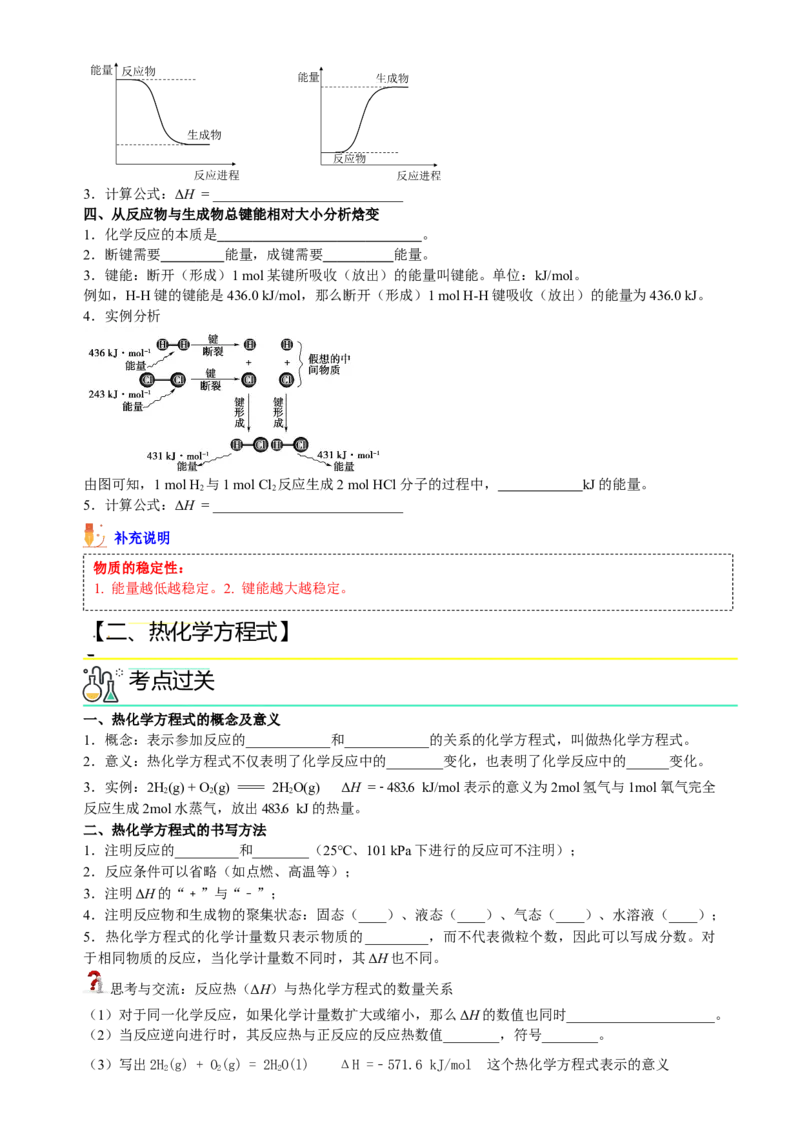
(4)图示:化学反应过程中形成化学键、断裂化学键能量变化可用如图表示:
其中,E 表示反应物断裂化学键_________的总热量,E 表示_________形成化学键_________的总热量,
1 2
E 与E 的差值表示_________。上述反应过程表示该反应为_________反应。
1 2
三、从反应物与生成物总能量相对大小分析焓变
1.放热反应(ΔH<0):反应物的总能量大于生成物的总能量。
2.吸热反应(ΔH>0):反应物的总能量小于生成物的总能量。3.计算公式:ΔH = ___________________________
四、从反应物与生成物总键能相对大小分析焓变
1.化学反应的本质是 。
2.断键需要 能量,成键需要 能量。
3.键能:断开(形成)1 mol某键所吸收(放出)的能量叫键能。单位:kJ/mol。
例如,H-H键的键能是436.0 kJ/mol,那么断开(形成)1 mol H-H键吸收(放出)的能量为436.0 kJ。
4.实例分析
由图可知,1 mol H 与1 mol Cl 反应生成2 mol HCl分子的过程中, kJ的能量。
2 2
5.计算公式:ΔH = ___________________________
补充说明
物质的稳定性:
1. 能量越低越稳定。2. 键能越大越稳定。
【二、热化学方程式】
】
考点过关
一、热化学方程式的概念及意义
1.概念:表示参加反应的____________和____________的关系的化学方程式,叫做热化学方程式。
2.意义:热化学方程式不仅表明了化学反应中的________变化,也表明了化学反应中的______变化。
3.实例:2H(g) + O (g) ==== 2HO(g) ΔH =﹣483.6 kJ/mol表示的意义为2mol氢气与1mol氧气完全
2 2 2
反应生成2mol水蒸气,放出483.6 kJ的热量。
二、热化学方程式的书写方法
1.注明反应的_________和________(25℃、101 kPa下进行的反应可不注明);
2.反应条件可以省略(如点燃、高温等);
3.注明ΔH的“﹢”与“﹣”;
4.注明反应物和生成物的聚集状态:固态(____)、液态(____)、气态(____)、水溶液(____);
5.热化学方程式的化学计量数只表示物质的_________,而不代表微粒个数,因此可以写成分数。对
于相同物质的反应,当化学计量数不同时,其ΔH也不同。
思考与交流:反应热(ΔH)与热化学方程式的数量关系
(1)对于同一化学反应,如果化学计量数扩大或缩小,那么ΔH的数值也同时_____________________。
(2)当反应逆向进行时,其反应热与正反应的反应热数值________,符号________。
(3)写出2H(g) + O(g) = 2HO(l) ΔH =﹣571.6 kJ/mol 这个热化学方程式表示的意义
2 2 2注意事项
物质的聚集状态不同时,它们所具有的内能、焓也均不同。例如,冰熔化为水时、需要吸收热量;水
蒸发为水蒸气时,也需要吸收热量。
因此,H 与O 反应生成1 mol HO(l)与生成1 mol HO(g)时所放出的热量是不同的。
2 2 2 2
【三、中和热、燃烧热】
】
考点过关
一、中和热
1.概念:酸与碱发生中和反应生成________HO时所放出的热量称为中和热。
2
2.单位:______________。
3.大量实验测得,在25℃和101kPa下,强酸的稀溶液与强碱的稀溶液在稀溶液发生中和反应生成 1
mol HO时,放出_________的热量。
2
二、燃烧热
1.概念:在101 kPa 时, 纯物质完全燃烧生成指定产物时所放出的热量,叫做该物质的燃烧
热,2.单位: 。
指定产物:C → ;H → ;S → ;N → 。
思考与交流:燃烧热和中和热有什么异同?
燃烧热 中和热
反应类型
相同点
ΔH及其单位
反应物的量
不同点 生成物的量
数值
三、实验探究——中和反应反应热的测定
【实验用品】(以盐酸和NaOH溶液的反应为例)
(1)仪器:量筒(50 mL两个)、大烧杯(500 mL)、小烧杯(100 mL)、泡沫塑料或纸条、泡沫塑料板或
硬纸 板 (中心有两个孔)、环形玻璃搅拌棒。
(2)药品:0.50 mol/L盐酸、0.55 mol/L NaOH溶液。
【实验步骤】
(1)设计装置如图。
②各部分仪器的作用
a.玻璃搅拌器的作用是使 混合均匀充分接触。
b.隔热层的作用是 热量的散失。c.温度计的作用是测定反应前后 的温度。
(2)操作步骤
①反应物温度测量(t):测量混合前 50 mL 0.50 mol·L-1 、50 mL 0.55 mol·L-1
1
溶液的温度,取两温度 ,记录为起始温度t。
1
②反应后体系温度测量(t):将 溶液迅速混合,用 轻轻搅动溶液,并准确读取
2
混合溶液的 ,记录为终止温度t。
2
③重复实验操作两次,记录每次的实验数据,取其平均值作为计算依据。
思考与交流:
①测量哪些数据?
②如何利用数据计算反应热?
③如何提高实验的准确度?
酸碱中和反应测定实验的注意事项
(1)为了保证0.50mol· L-1的盐酸完全被NaOH中和,采用0.55mol·L-1NaOH溶液,使碱稍稍过量,
因为过量的碱并不参加中和反应。
(2)先后测量酸、碱及混合液的温度时,测定一种溶液后必须用水冲洗干净并用滤纸擦干。温度计的
水银球部分要完全浸入溶液中,且要稳定一段时间再记下读数。
(3)实验中所用的盐酸和氢氧化钠溶液配好后要充分冷却至室温,才能使用。
(4)操作时动作要快,尽量减少热量的散失。
(5)实验时亦可选用浓度体积都不相同的酸碱溶液进行中和热的测定,但在计算时,应取二者中量少
的一种,因为过量的酸/碱并不参加中和反应。
(6)多次试验求平均值时,若有某一组的实验数据有明显偏差,应直接舍去。
(7)隔热层的作用是保温隔热,减少热量损失。
【做一做】中和热与57.3 kJ·mol-1的关系
已知:H+(aq) + OH-(aq) === H O(l) ΔH =﹣57.3 kJ·mol-1
2
试比较下列反应中放出的热量与 57.3 kJ 的大小:
(1)浓酸与浓碱反应生成 1 mol 水,Q _____57.3 kJ, ΔH _____ ΔH;
1 1
(2)弱酸与弱碱反应生成 1 mol 水,Q _____57.3 kJ, ΔH _____ ΔH;
2 2
(3)强酸与强碱反应生成 1 mol 水和难溶性盐,Q _____57.3 kJ, ΔH _____ ΔH。
3 3
【四、盖斯定律】
】考点过关
一、盖斯定律的内容
1. 俄国化学家盖斯从大量的实验事实中总结出一条规律:一个化学反应,不管是一步完成的还是分几
步完成,其___________是相同的,这就是盖斯定律。
2. 也就是说,化学反应的_______只与反应体系的_______和________有关,而与反应的______无关。
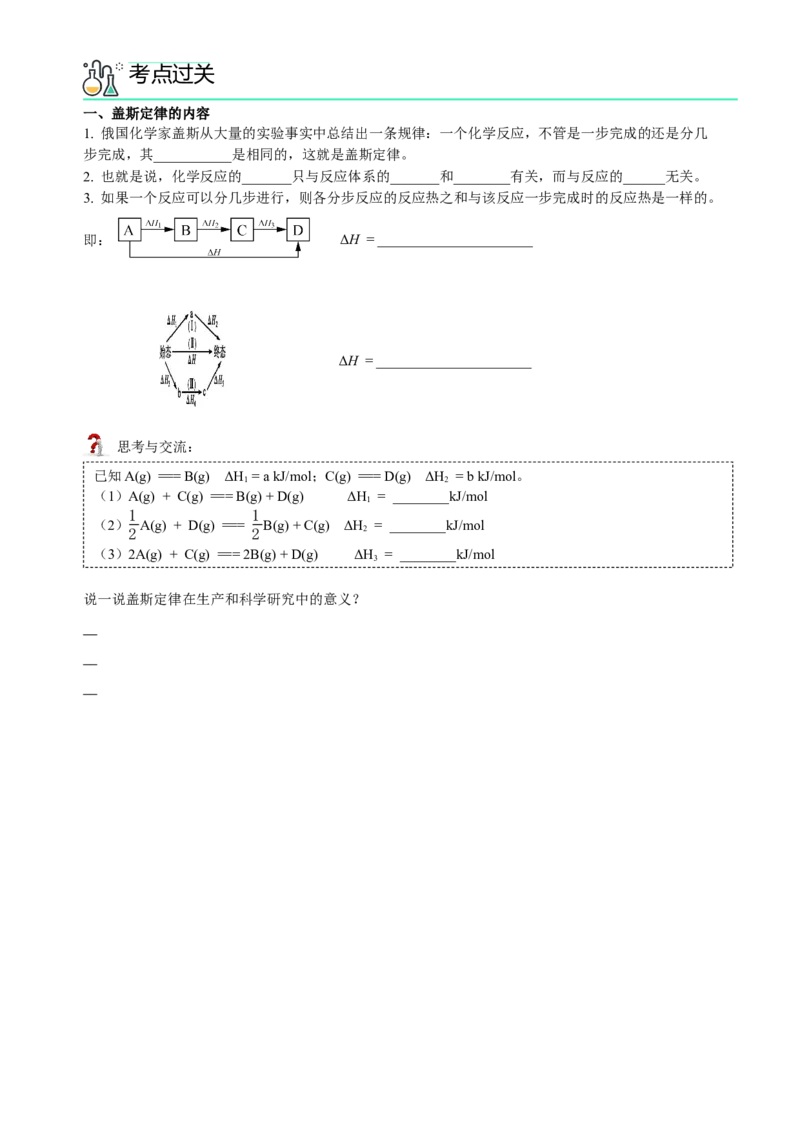
3. 如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是一样的。
即: ΔH = ______________________
ΔH = ______________________
思考与交流:
已知A(g) === B(g) ΔH = a kJ/mol;C(g) === D(g) ΔH = b kJ/mol。
1 2
(1)A(g) + C(g) === B(g) + D(g) ΔH = ________kJ/mol
1
1 1
(2) A(g) + D(g) === B(g) + C(g) ΔH = ________kJ/mol
2 2 2
(3)2A(g) + C(g) === 2B(g) + D(g) ΔH = ________kJ/mol
3
说一说盖斯定律在生产和科学研究中的意义?