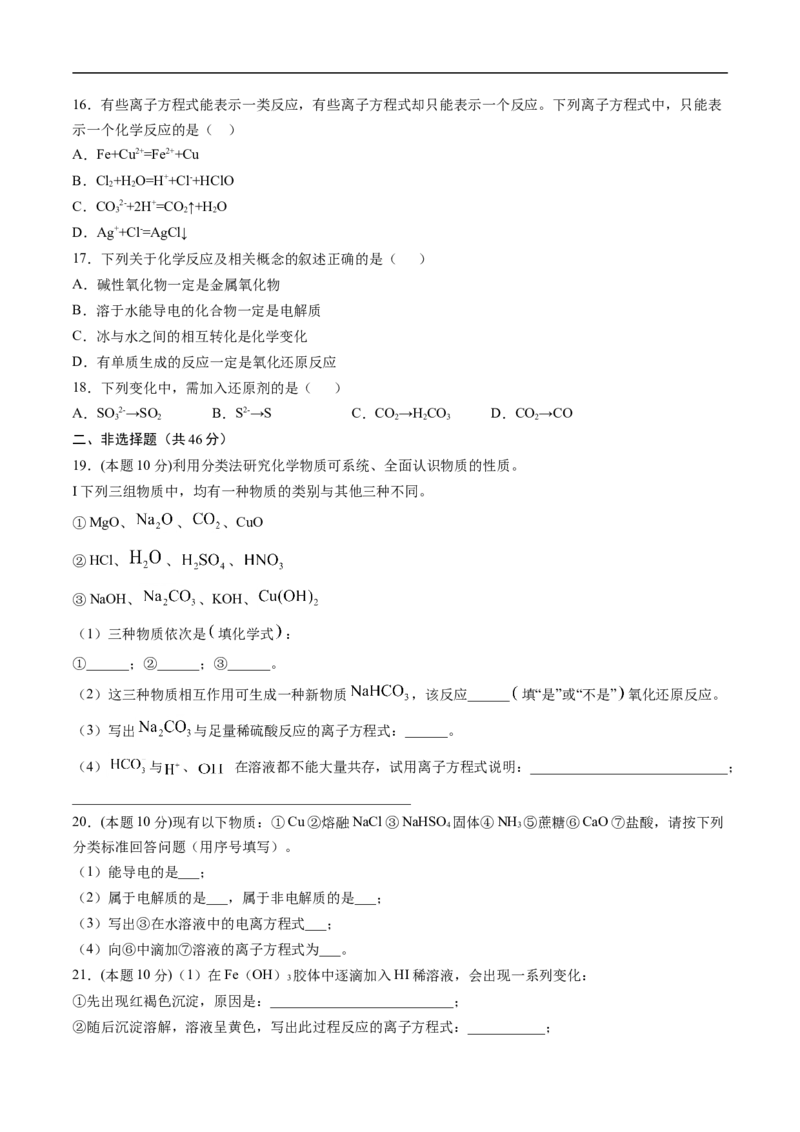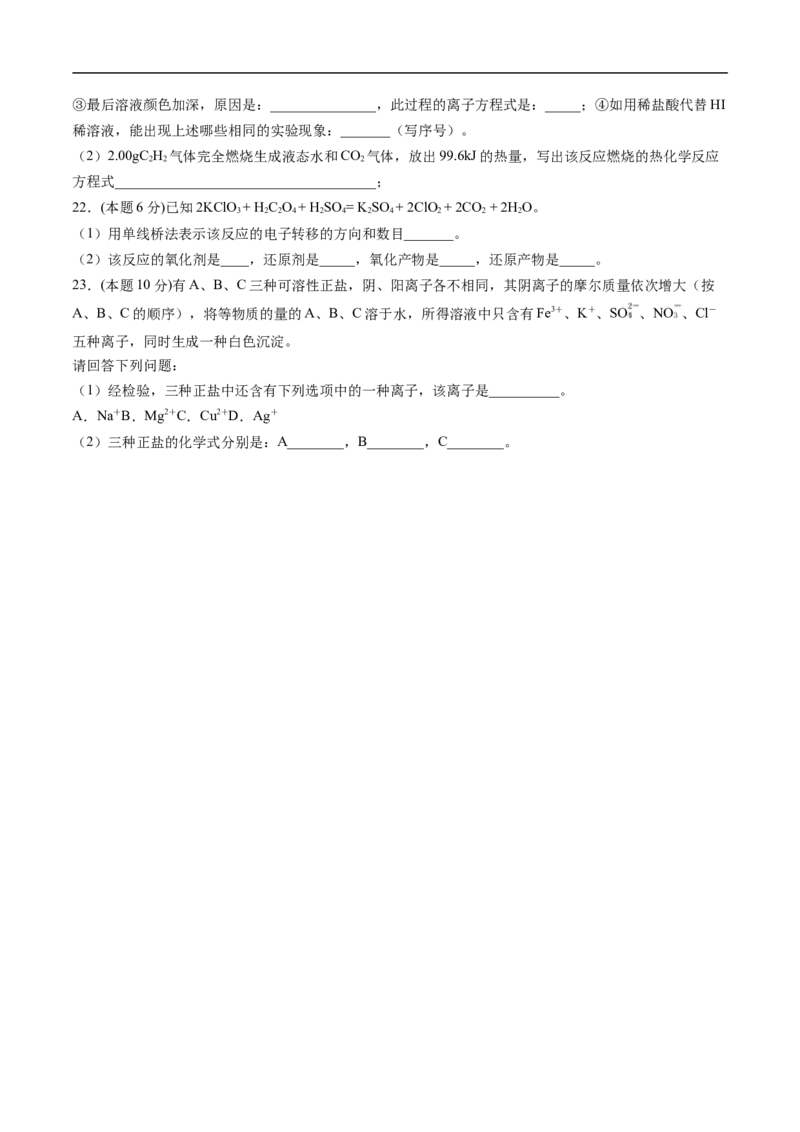文档内容
第一章 物质及其变化
过关测试 基础卷
(时间:90分钟)
一、选择题(每小题3分,共54分)
1.下列过程只涉及物理变化的是( )
A.干冰升华 B.酿酒成醋 C.高炉炼铁 D.伐薪烧炭
2.下列有关胶体的说法不正确的是( )
A.Fe(OH) 胶体制好后可以用渗析的方法进一步净化
3
B.电泳现象可以证明胶体都带电
C.利用丁达尔效应可以区分溶液和胶体
D.由于胶粒之间有排斥作用,胶粒不易聚集成大的颗粒,这是胶体具有介稳性的主要原因
3.下列事实与胶体的说法不正确的是( )
A.由肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
B.在实验中手不慎被玻璃划破,可用FeCl 溶液应急止血
3
C.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
D.氯化钠易溶于水,所以氯化钠一定不能制成胶体
4.下列各组物质,按化合物、单质、混合物顺序排列的是( )
A.氯水、氮气、胆矾 B.碱石灰、液氯、碘酒
C.干冰、铁、水煤气 D.生石灰、白磷、熟石灰
5.下列属于强电解质的是( )
A.Al B.CHOH C.CHCOOH D.BaSO
3 3 4
6.下列说法正确的是( )
A.熔融NaCl能导电,是因为通电时NaCl发生了电离
B.NaCl固体不导电,因为NaCl固体中无带电微粒
C.NH NO 电离时产生了NH +、NO -,无金属离子,所以NH NO 不是盐
4 3 4 3 4 3
D.NaHSO 在水溶液中电离生成了Na+、H+、SO 2-三种离子
4 4
7.下列离子方程式不正确的是( )
A.在一定量硫酸和双氧水的混合液中加少量的铜粉:Cu+2H++HO=2HO+Cu2+
2 2 2
B.碳酸钠溶液和醋酸反应:CO2-+2 H+=CO↑+ HO
3 2 2
C.碳酸氢钠溶液加过量氢氧化钡:HCO -+Ba2++OH-= BaCO ↓+ HO
3 3 2
D.向次氯酸钠溶液中通入少量的SO :HO +3ClO-+ SO = SO 2-+ Cl-+2HClO
2 2 2 4
8.向含有下列离子的溶液中分别加入SO 固体后,溶液中下列离子个数不变的是( )
3
A.Mg2+ B.CO2﹣ C.Ba2+ D.SO 2﹣
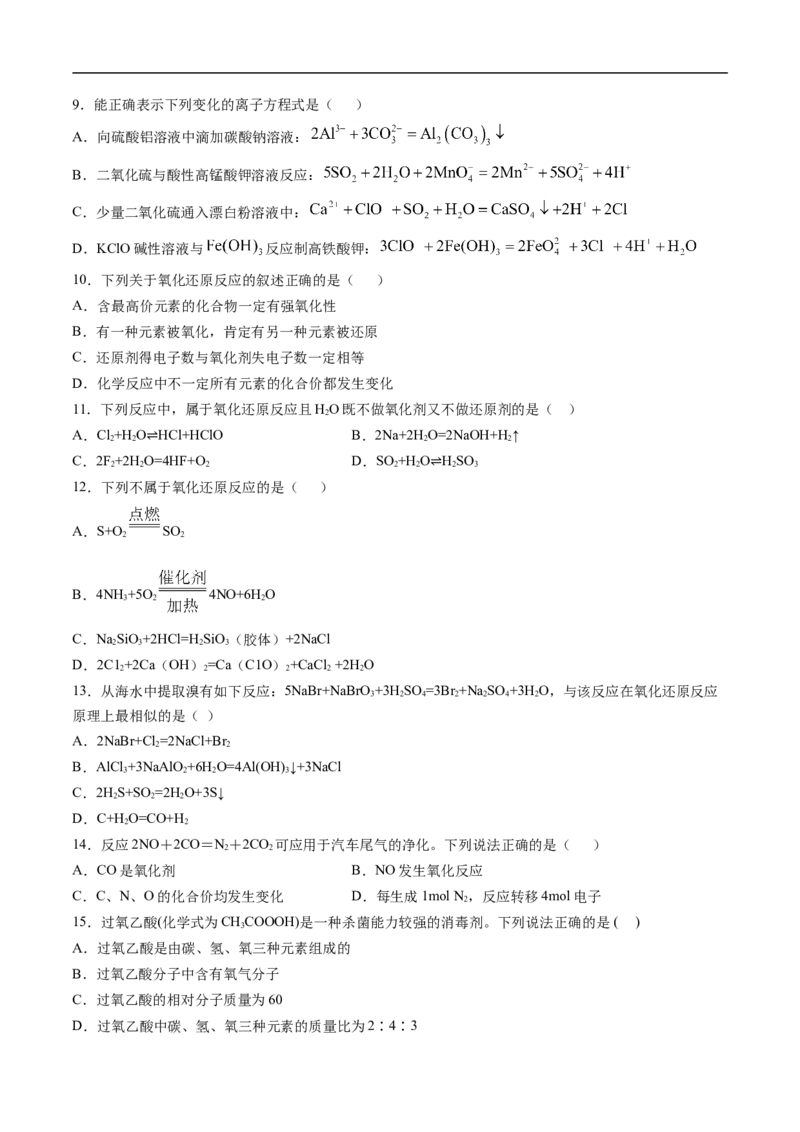
3 39.能正确表示下列变化的离子方程式是( )
A.向硫酸铝溶液中滴加碳酸钠溶液:
B.二氧化硫与酸性高锰酸钾溶液反应:
C.少量二氧化硫通入漂白粉溶液中:
D.KClO碱性溶液与 反应制高铁酸钾:
10.下列关于氧化还原反应的叙述正确的是( )
A.含最高价元素的化合物一定有强氧化性
B.有一种元素被氧化,肯定有另一种元素被还原
C.还原剂得电子数与氧化剂失电子数一定相等
D.化学反应中不一定所有元素的化合价都发生变化
11.下列反应中,属于氧化还原反应且HO既不做氧化剂又不做还原剂的是( )
2
A.Cl+H O HCl+HClO B.2Na+2HO=2NaOH+H ↑
2 2 2 2
C.2F+2H O=4HF+O D.SO +H O HSO
2 2⇌ 2 2 2 2 3
12.下列不属于氧化还原反应的是( )
⇌
A.S+O SO
2 2
B.4NH +5O 4NO+6H O
3 2 2
C.NaSiO+2HCl=H SiO(胶体)+2NaCl
2 3 2 3
D.2C1 +2Ca(OH)=Ca(C1O)+CaCl +2H O
2 2 2 2 2
13.从海水中提取溴有如下反应:5NaBr+NaBrO +3H SO =3Br +Na SO +3H O,与该反应在氧化还原反应
3 2 4 2 2 4 2
原理上最相似的是( )
A.2NaBr+Cl =2NaCl+Br
2 2
B.AlCl +3NaAlO+6H O=4Al(OH)↓+3NaCl
3 2 2 3
C.2HS+SO=2H O+3S↓
2 2 2
D.C+H O=CO+H
2 2
14.反应2NO+2CO=N+2CO 可应用于汽车尾气的净化。下列说法正确的是( )
2 2
A.CO是氧化剂 B.NO发生氧化反应
C.C、N、O的化合价均发生变化 D.每生成1mol N,反应转移4mol电子
2
15.过氧乙酸(化学式为CHCOOOH)是一种杀菌能力较强的消毒剂。下列说法正确的是 ( )
3
A.过氧乙酸是由碳、氢、氧三种元素组成的
B.过氧乙酸分子中含有氧气分子
C.过氧乙酸的相对分子质量为60
D.过氧乙酸中碳、氢、氧三种元素的质量比为2∶4∶316.有些离子方程式能表示一类反应,有些离子方程式却只能表示一个反应。下列离子方程式中,只能表
示一个化学反应的是( )
A.Fe+Cu2+=Fe2++Cu
B.Cl+HO=H++Cl-+HClO
2 2
C.CO2-+2H+=CO ↑+HO
3 2 2
D.Ag++Cl-=AgCl↓
17.下列关于化学反应及相关概念的叙述正确的是( )
A.碱性氧化物一定是金属氧化物
B.溶于水能导电的化合物一定是电解质
C.冰与水之间的相互转化是化学变化
D.有单质生成的反应一定是氧化还原反应
18.下列变化中,需加入还原剂的是( )
A.SO 2-→SO B.S2-→S C.CO→HCO D.CO→CO
3 2 2 2 3 2
二、非选择题(共46分)
19.(本题10分)利用分类法研究化学物质可系统、全面认识物质的性质。
I下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、 、 、CuO
②HCl、 、 、
③NaOH、 、KOH、
(1)三种物质依次是 填化学式 :
①______;②______;③______。
(2)这三种物质相互作用可生成一种新物质 ,该反应______ 填“是”或“不是” 氧化还原反应。
(3)写出 与足量稀硫酸反应的离子方程式:______。
(4) 与 、 在溶液都不能大量共存,试用离子方程式说明:____________________________;
________________________________________________
20.(本题10分)现有以下物质:①Cu②熔融NaCl③NaHSO 固体④NH ⑤蔗糖⑥CaO⑦盐酸,请按下列
4 3
分类标准回答问题(用序号填写)。
(1)能导电的是___;
(2)属于电解质的是___,属于非电解质的是___;
(3)写出③在水溶液中的电离方程式___;
(4)向⑥中滴加⑦溶液的离子方程式为___。
21.(本题10分)(1)在Fe(OH) 胶体中逐滴加入HI稀溶液,会出现一系列变化:
3
①先出现红褐色沉淀,原因是:__________________________;
②随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式:___________;③最后溶液颜色加深,原因是:_______________,此过程的离子方程式是:_____;④如用稀盐酸代替HI
稀溶液,能出现上述哪些相同的实验现象:_______(写序号)。
(2)2.00gC H 气体完全燃烧生成液态水和CO 气体,放出99.6kJ的热量,写出该反应燃烧的热化学反应
2 2 2
方程式_____________________________________;
22.(本题6分)已知2KClO + H C O + H SO = K SO + 2ClO + 2CO + 2H O。
3 2 2 4 2 4 2 4 2 2 2
(1)用单线桥法表示该反应的电子转移的方向和数目_______。
(2)该反应的氧化剂是____,还原剂是_____,氧化产物是_____,还原产物是_____。
23.(本题10分)有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按
A、B、C的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO 、NO 、Cl-
五种离子,同时生成一种白色沉淀。
请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是__________。
A.Na+B.Mg2+C.Cu2+D.Ag+
(2)三种正盐的化学式分别是:A________,B________,C________。