文档内容
优秀领先 飞翔梦
想
2017年苏州市初中毕业暨升学考试试卷
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 K-39
单项选择题(包括25题,每题2分,共50分,每题只有一个选项符合题意)
1.2017年“世界环境日”中国确定的主题是“绿水青山就是金山银山”,下列做法与之相
违背的是
A.利用风力发电 B.增加绿化面积 C.节约用水用电 D.直接排放废气
2.下列元素名称与元素符号书写都正确的是
A.锌 Zn B.硅 SI C.氯 cl D.贡Hg
3.下列化学仪器对应的名称书写正确的是
A.长劲漏斗子 B.量桶 C.坩埚钳 D.椎形瓶
4.下列变化属于化学变化的是
A.滴水成冰 B.蜡烛燃烧 C.汽油挥发 D.铜丝折弯
5.下列物质属于纯净物的是
A.盐水B.石油C.生铁D.氢气
6.下列反应发球置换反应的是
点燃 △
A.2CO+O=====2CO B.HCO=====HO+CO↑
2 2 2 3 2 2
C.NaOH+HCl===NaCl+H O D.2Al+6HCl====2AlCl +3H ↑
2 3 2
7.下列关于空气的说法中,不正确的是
A.工业上采用分离液态空气法获得氧气
B.二氧化硫是空气的污染物之一
C.空气中的氧气质量占空气质量的21%
D.空气中的氧气来源于绿色植物的光合作用
8.下列实验操作图示不正确的是
A.过滤悬浊液 B.加热液体 C.蒸发溶液 D.倾倒液体
9.下列有关水的说法中,不正确的是
A.水是一种常用的溶剂
B.保护水资源是全人类的责任
www.youyi100.com
第 1 页 共 8 页优秀领先 飞翔梦
想
C.常用肥皂水来鉴别硬水和软水
D.电解水得到的氧气和氢气的体积比为2:1
10.下列物质由离子构成的是
A.二氧化碳 B.氯化钠 C.铁 D.水
11.下列关于氧气的说法中,不正确的是
A.氧气能支持燃烧,所以氧气可作燃料
B.氧气能使带火星的木条复燃
C.红磷在氧气中燃烧,产生浓厚的白烟
D.实验室加热高锰酸钾制取氧气时,试管内靠近导管处放一团蓬松的棉花
12.下列有关分子的说法中,不正确的是
A.分子的质量和体积都很小 B.温度升高,分子的体积变大
C.分子在不停地运动 D.温度越高,分子运动的速率越快
13.下列有关化学用语表示不正确的是
A.2个铝离子:2Al3+ B.钠原子的结构示意图:
+2
C.氧分子:O D。氧化镁中镁元素显+2价:MgO
14.下列关于金属的说法中,不正确的是
A.铜有良好的导电性,常用于制作导线
B.所有的金属都能与稀盐酸反应
C.铁制品在干燥的空气中不易生锈
D.不锈钢具有较强的耐腐蚀性,可用于制作医疗器械
15.下列材料属于有机合成材料的是
A.陶瓷 B.硬铝 C.塑料 D.钢筋混凝土
16.下列关于溶液的说法中,正确的是
A.泥土加入水中,振荡后可以形成溶液
B.蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度
C.氢氧化钠溶液能导电,是因为溶液中有较多自由移动的离子
D.氯化钠饱和溶液中不能再溶解少量的硝酸钾晶体
17.下列叙述正确的是
A.用小苏打治疗胃酸过多 B.用氢氧化钠改良酸性土壤
C.用铁桶长时间存放硫酸铜溶液 D.用食盐水除去热水瓶中的水垢
18.苏州盛产杨梅,杨梅中含有丰富的叶酸,对防癌抗癌有积极的作用。其化学式为
C H NO。下列有关叶酸的说法中正确的是
19 19 7 4
A.叶酸的相对分子质量为441g
B.叶酸中氮元素的质量分数大于氧元素的质量分数
C.叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
D.叶酸由19个碳原子、19个氢原子、7个氮原子、6氧原子构成
19.下列说法中不正确的是
A.大米主要成分是淀粉,淀粉遇碘化钾溶液变蓝色
B.鸡蛋清加入饱和硫酸铵溶液,有白色沉淀
C.油脂不溶于水,易溶于汽油等有机溶剂
D.新鲜蔬菜、水果中含有丰富的维生素C
www.youyi100.com
第 2 页 共 8 页优秀领先 飞翔梦
想
20.下列各组离子在水溶液中能大量共存的是
A.Cu2+、Na+、NO -、OH- B.H+、K+、CO2-、Cl-
3 3
C.Mg2+、NH +、OH-、SO 2- D.Na+、Ca2+、NO -、Cl-
4 4 3
21.氯化钠和硝酸钾两种固体的溶解度曲线如右图所示。下列说法正确的是
A.硝酸钾的溶解度大于氯化钠的溶解度
B.常用冷却结晶的方法从氯化钠溶液中获得其晶体
C.40℃时,将35g硝酸钾晶体放入50g水中,充分搅拌
后,所得溶液的溶质质量分数为39.0%
D.将20℃的硝酸钾饱和溶液升温至60℃,溶液的溶质
质量分数增大(忽略水分蒸发)
22.鉴别下列各组物质,不能达到目的的是
A.黄铜片和纯铜片:相互刻划比较硬度
B.棉线和羊毛线:灼烧后闻气味
C.硫酸铵固体和氯化铵固体:加熟石灰混合研磨后闻气味
D.向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝
24.除去下列物质中的少量杂质(括号内为杂质),所选试剂正确的是
A.CaCO 粉末(CaCl 粉末)------水
3 2
B.CaO粉末[Ca(OH) 粉末]-------水
2
C.KC l溶液(KOH)---------稀硝酸
D.NaOH溶液(NaCO)--------稀盐酸
2 3
25.甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应一步实现,部分物质和反应
条件已略去)。下列选项不能实现图示转化的是
甲 乙 丙
A HO HO H
2 2 2 2
B NaCO CO CaCO
2 3 2 3
C C CO CO
2
D NaCO NaCl NaNO
2 3 3
非选择题(共50分)
26.(5分)请用线段连接有对应关系的相邻两行间的点(每个点只能连接1次)
27.(5分)化学与人类生活、生产息息相关,请回答下列问题:
⑴可燃冰的主要成分是甲烷水合物,燃烧时化学能转化为________能。
⑵用灯帽盖灭酒精灯火焰的原理是______________。
⑶用洗涤精除去餐具上的油污是因为洗涤精在水中对油污具有________作用。
⑷家庭用净水器利用活性炭的_________作用,除去有色有味的杂质。
⑸人体缺钙易患疾病是__________(用序号填写)
www.youyi100.com
第 3 页 共 8 页优秀领先 飞翔梦
想
①骨质疏松 ②贫血
28.(10分)根据下列反应事实写出相应的化学方程式。
⑴双氧水在二氧化锰的催化作用下生成水和氧气:
____________________________________。
⑵在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO ):
3
_____________________________________。
⑶Cu和AgNO 溶液反应,生成Cu(NO ) 溶液和Ag:
3 3 2
__________________________________________。
⑷少量CuSO 溶液滴入NaOH稀溶液中生成Cu(OH) 沉淀和NaSO 溶液:
4 2 2 4
____________________________________________。
⑸一氧化碳和四氧化三铁(Fe O)在高温下反应,生成铁和二氧化碳:
3 4
______________________________________________。
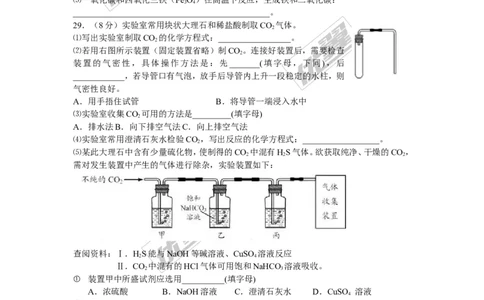
29.(8分)实验室常用块状大理石和稀盐酸制取CO 气体。
2
⑴写出实验室制取CO 的化学方程式:_________________。
2
⑵若用右图所示装置(固定装置省略)制CO。连接好装置后,需要检查
2
装置的气密性,具体操作方法是:先_______(填字母,下同),后
____________,若导管口有气泡,放手后导管内上升一段稳定的水柱,则
气密性良好。
A.用手捂住试管 B.将导管一端浸入水中
⑶实验室收集CO 可用的方法是_________(填字母)
2
A.排水法B.向下排空气法C.向上排空气法
⑷实验室常用澄清石灰水检验CO,写出反应的化学方程式:__________________。
2
⑸某此大理石中含有少量硫化物,使制得的CO 中混有HS气体。欲获取纯净、干燥的CO,
2 2 2
需对发生装置中产生的气体进行除杂,实验装置如下:
查阅资料:Ⅰ.HS能与NaOH等碱溶液、CuSO 溶液反应
2 4
Ⅱ.CO 中混有的HCl气体可用饱和NaHCO 溶液吸收。
2 3
① 装置甲中所盛试剂应选用__________(填字母)
A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO 溶液
4
②装置丙的作用是___________________________________________。
30.(6分)某工厂产生的烧渣(主要含FeO、Fe O,还有一定量的SiO)可用于制七水合硫酸
2 3 2
亚铁晶体(FeSO ·7HO),其工艺流程如下:
4 2
↓
查阅资料:SiO 不
2
www.youyi100.com
第 4 页 共 8 页优秀领先 飞翔梦
想
溶于水,也不与稀硫酸反应。
⑴“浸取”步骤中,FeO、Fe O 和稀硫酸发生反应的化学方程式分别为
2 3
FeO+HSO ===FeSO+H O 、_________________________________。
2 4 4 2
⑵为提高“浸取”步骤的反应速率,可采取的具体措施有__________(写2条,不考虑“搅
拌”和“使用催化剂”)。
⑶“还原”步骤的目的是将Fe3+转化为Fe2+,试剂X可用SO 或Fe。
2
①若试剂X是SO,转化原理为SO+Fe(SO)+2Y===2FeSO+2HSO,则Y的化学式是______。
2 2 2 4 3 4 2 4
②若试剂X是Fe,转化原理为Fe+ Fe(SO)===3FeSO。测得“还原”后溶液的pH明显增大,
2 4 3 4
其原因是______________________。
31.(8分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下
两组实验。(提示:本实验所用汽油与KMnO ,碘均不发生化学反应)
4
【实验1】KMnO 晶体在不同溶剂中的溶解实验
4
根据实验步骤、实验操作图示填写相关实验现象。
实验步骤 实验操作图示 实验操作及现象
步骤1
振荡后静置:
⑴A试管中晶体全部溶解,溶液呈_______
色;B试管中晶体不溶解,汽油不变色。
步骤2
将步骤1中A试管内溶液倒入B试管中,
振荡后静置:
⑵B试管中观察到的现象为__________
_______________。
【实验2】碘在不同溶剂中的溶解实验
根据实验操作图示回答相关问题。
实验操作图示 实验结论或解释
⑶由图2所示现象可知:碘________(选
“不”、“微”或“易”)溶于水。
⑷图3所示试管中液体分层。上层紫红色
溶液的名称___________。说明碘在汽油
中的溶解性比在水中________(选填
“强”或“弱”)
【反思与应用】
⑸①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体________
(选填“分层”或“不分层”)。
www.youyi100.com
第 5 页 共 8 页优秀领先 飞翔梦
想
②“从稀碘水中提取碘”是“海带提碘”工艺中一个重要步骤,其原理类似【实验2】中第二
步骤操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件
是_________________________________________
32.(8分)实验室常会产生含硫酸的废水,需经处理至中性。某兴趣小组同学配制一定质量
分数的氢氧化钾溶液来处理酸性废水。
⑴定性检测废水
检测废水呈酸性的方法是________________________________________。
⑵配制200g质量分数为5.6%的氢氧化钾溶液
① 计算
m(KOH)=___________g,V(HO)=__________mL(水的密度近似为1.0g·mL-1)
2
② 称取氢氧化钾
调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量。然后________(按操作
先后顺序,填字母),直至天平平衡。
③量取水;④溶解;⑤转移。
⑶定量测定废水
取酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如右下
图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
①P点对应溶液中一定存在的阳离子有________________(填离子符号)
②酸性废水中硫酸的质量分数为_______________(用百分数表示,保留到0.1%)
③计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示,
保留到0.1%)
www.youyi100.com
第 6 页 共 8 页优秀领先 飞翔梦
想
2017年苏州市初中毕业暨升学考试试卷
化学试题参考答案
选择题(共50分)
1.D 2.A 3.C 4.B 5.D 6.D 7.C 8.B 9.D 10.B
11.A 12.B 13.C 14.B 15.C16.C 17.A 18.B 19.A 20.D
21.C 22.C 23.A 24.A 25.D
非选择题(共50分)
26.(5分)
27.(5分)⑴热 ⑵隔绝氧气 ⑶乳化 ⑷吸附 ⑸①
28.(10分)
MnO 尘埃
2
⑴2HO======2H O+O↑ ⑵2SO +O ====2SO
2 2 2 2 2 2 3
⑶Cu+2AgNO ====Cu(NO )+2Ag ⑷2NaOH+CuSO ====Cu(OH)↓+Na SO
3 3 2 4 2 2 4
高温
⑸Fe O+4CO=====3Fe+4CO
3 4 2
29.(8分)
⑴CaCO +2HCl==CaCl +H O+CO↑ ⑵B A ⑶AC
3 2 2 2
⑷CO+Ca(OH) ===CaCO ↓+H O
2 2 3 2
⑸①D ②除去CO 中的水蒸气(或干燥CO)
2 2
30.(6分)⑴Fe O+3H SO ==Fe (SO )+3H O
2 3 2 4 2 4 3 2
⑵增大硫酸的浓度 升高温度 将烧渣粉碎(3点中任意2点)
⑶①HO ②铁消耗过量的硫酸,溶液酸性减弱
2
31.(8分)
⑴紫(紫红、红) ⑵液体分层,上层为无色,下层为紫红色,试管底部无固体残留
⑶微 ⑷碘的汽油溶液 强
⑸①不分层 ②与水不互溶,碘在这种液体中的溶解度远远大于在水中的溶解度
32.(8分)
⑴取样,滴入紫色石蕊试液,若变红则呈酸性(或其他合理答案)
⑵①11.2 188.8 ②BA
www.youyi100.com
第 7 页 共 8 页优秀领先 飞翔梦
想
⑶①K+、H+ ②4.9%
③ 解:设生成硫酸钾的质量为x
2KOH+H SO ===KSO +2H O
2 4 2 4 2
112 174
100g×5.6% x
112:174=100g×5.6%:x x=8.7g
硫酸钾的溶质质量分数为4.4%(或其他合理解法)
www.youyi100.com
第 8 页 共 8 页