文档内容
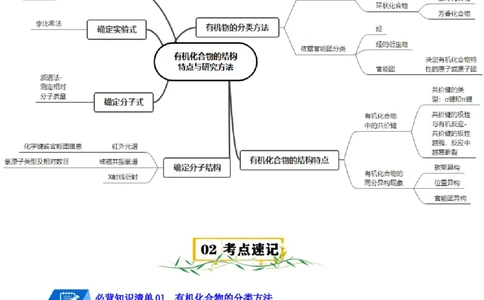
第一章 有机化合物的结构特点与研究方法
必背知识清单01 有机化合物的分类方法
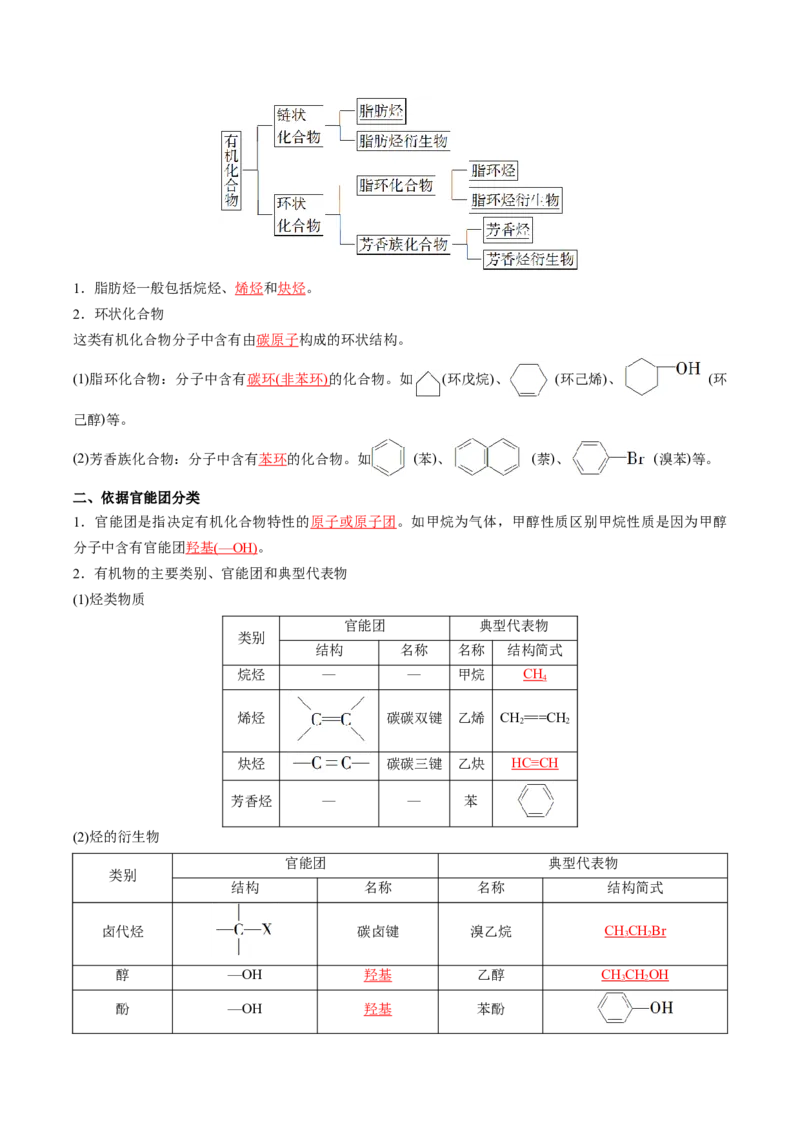
一、依据碳骨架分类1.脂肪烃一般包括烷烃、烯烃和炔烃。
2.环状化合物
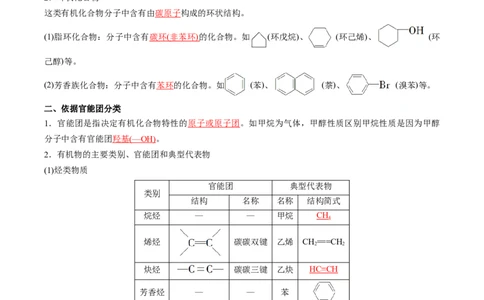
这类有机化合物分子中含有由碳原子构成的环状结构。
(1)脂环化合物:分子中含有 碳环 ( 非苯环 )的化合物。如 (环戊烷)、 (环己烯)、 (环
己醇)等。
(2)芳香族化合物:分子中含有苯环的化合物。如 (苯)、 (萘)、 (溴苯)等。
二、依据官能团分类
1.官能团是指决定有机化合物特性的原子或原子团。如甲烷为气体,甲醇性质区别甲烷性质是因为甲醇
分子中含有官能团 羟基 (—OH )。
2.有机物的主要类别、官能团和典型代表物
(1)烃类物质
官能团 典型代表物
类别
结构 名称 名称 结构简式
烷烃 — — 甲烷 CH
4
烯烃 碳碳双键 乙烯 CH===CH
2 2
炔烃 碳碳三键 乙炔 HC≡CH
芳香烃 — — 苯
(2)烃的衍生物
官能团 典型代表物
类别
结构 名称 名称 结构简式
卤代烃 碳卤键 溴乙烷 CHCHBr
3 2
醇 —OH 羟基 乙醇 CHCHOH
3 2
酚 —OH 羟基 苯酚醚 醚键 乙醚 CHCHOCH CH
3 2 2 3
醛 醛基 乙醛
酮 酮羰基 丙酮
羧酸 羧基 乙酸
酯 酯基 乙酸乙酯
胺 —NH 氨基 甲胺 CHNH
2 3 2
酰胺 酰胺基 乙酰胺
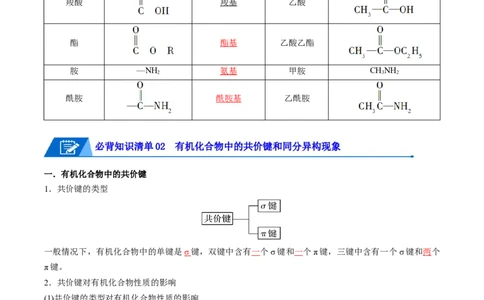
必背知识清单02 有机化合物中的共价键和同分异构现象
一.有机化合物中的共价键
1.共价键的类型
一般情况下,有机化合物中的单键是σ 键,双键中含有一个σ键和一个π键,三键中含有一个σ键和两个
π键。
2.共价键对有机化合物性质的影响
(1)共价键的类型对有机化合物性质的影响
π 键的轨道重叠程度比σ 键的小,比较容易断裂而发生化学反应。例如乙烯和乙炔分子的双键和三键中含
有π 键,都可以发生加成反应,而甲烷分子中含有C—H σ 键,可发生取代反应。
(2)共价键的极性对有机化合物性质的影响
共价键的极性越强,在反应中越容易发生断裂,因此有机化合物的官能团及其邻近的化学键往往是发生化
学反应的活性部位。
二.有机化合物的同分异构现象
1.同分异构现象和同分异构体
同分异构现象:化合物具有相同的分子式,但具有不同结构的现象同分异构体:具有同分异构现象的化合物的互称
2.同分异构体的类型
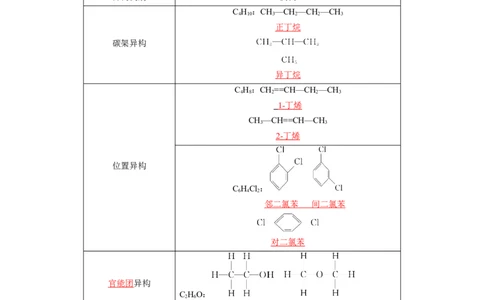
3.构造异构现象举例
异构类别 实例
C H :CH—CH—CH—CH
4 10 3 2 2 3
正丁烷
碳架异构
异丁烷
C H:CH==CH—CH—CH
4 8 2 2 3
1- 丁烯
CH—CH==CH—CH
3 3
2- 丁烯
位置异构
C HCl:
6 4 2
邻二氯苯 间二氯苯
对二氯苯
官能团异构
C HO:
2 6
乙醇 二甲醚
4.键线式
在表示有机化合物的组成和结构时,将碳、氢元素符号省略,只表示分子中键的连接情况和官能团,每个
拐点或终点均表示有一个碳原子,这样得到的式子称为键线式。例如:丙烯可表示为 ,乙醇可表
示为 。
必背知识清单03 有机化合物的分离、提纯一.研究有机化合物的一般步骤
分离、提纯―→确定实验式―→确定分子式―→确定分子结构
二.有机物的分离、提纯方法
1.蒸馏
(1)适用条件
①液态有机化合物含有少量杂质且该有机化合物热稳定性较高;
②有机化合物的沸点与杂质的沸点相差较大。
(2)蒸馏装置及注意事项
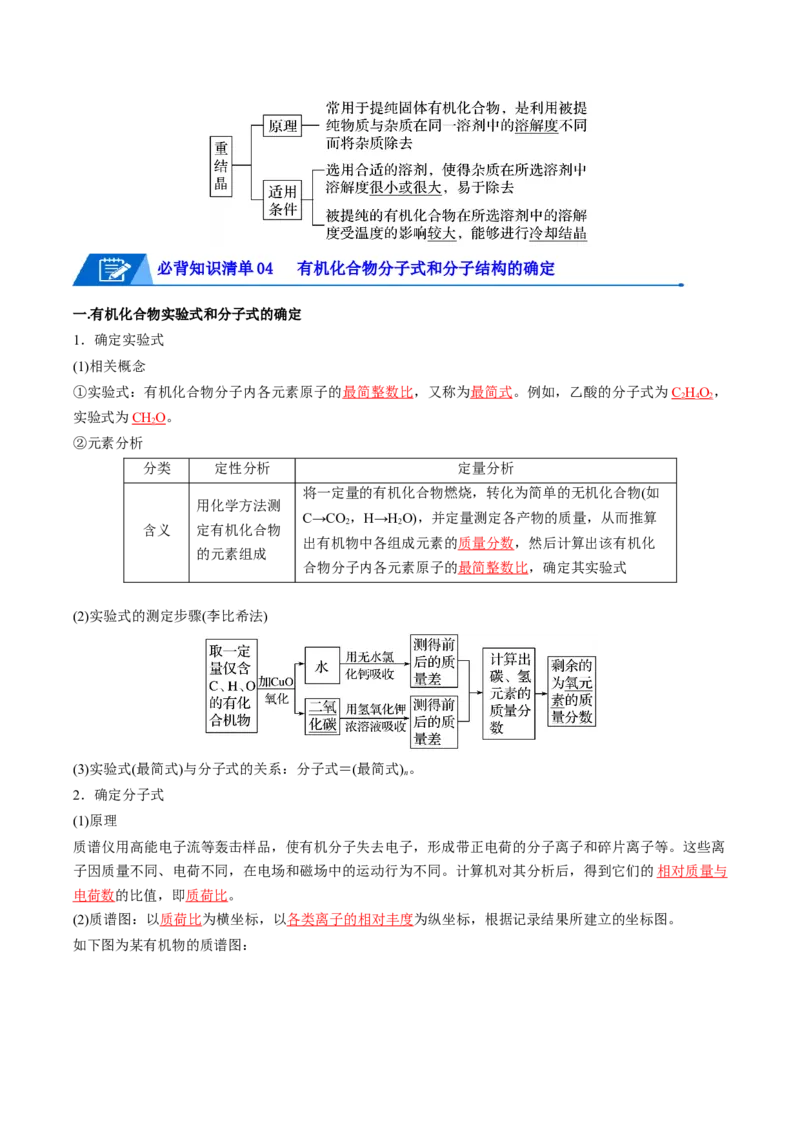
①实验装置——写出相应仪器的名称
②注意事项
a.温度计水银球位置:蒸馏烧瓶的支管口处;b.加碎瓷片的目的:防止液体暴沸;c.冷凝管中水的流向:
下口流入,上口流出。
2.萃取
液-液萃取:利用待分离组分在两种不互溶的溶剂中的溶解性不
类型 同,将其从一种溶剂转移到另一种溶剂的过程
固-液萃取:用溶剂从固体物质中溶解出待分离组分的过程
装置和仪器
对萃取剂的要求:
①萃取剂与原溶剂互不相溶;
萃取剂 ②溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应
常用萃取剂:乙醚、乙酸乙酯、二氯甲烷等
定义 将萃取后的两层液体分开的操作
加入萃取剂后充分振荡,静置分层,然后打开分液漏斗上方的玻
分液
操作 璃塞和下方的活塞将两层液体分离,下层液体从下口流出,并及
时关闭活塞,上层液体从上口倒出
3.重结晶必背知识清单04 有机化合物分子式和分子结构的确定
一.有机化合物实验式和分子式的确定
1.确定实验式
(1)相关概念
①实验式:有机化合物分子内各元素原子的最简整数比,又称为最简式。例如,乙酸的分子式为C HO ,
2 4 2
实验式为CHO。
2
②元素分析
分类 定性分析 定量分析
将一定量的有机化合物燃烧,转化为简单的无机化合物(如
用化学方法测
C→CO,H→H O),并定量测定各产物的质量,从而推算
2 2
含义 定有机化合物
出有机物中各组成元素的质量分数,然后计算出该有机化
的元素组成
合物分子内各元素原子的最简整数比,确定其实验式
(2)实验式的测定步骤(李比希法)
(3)实验式(最简式)与分子式的关系:分子式=(最简式)。
n
2.确定分子式
(1)原理
质谱仪用高能电子流等轰击样品,使有机分子失去电子,形成带正电荷的分子离子和碎片离子等。这些离
子因质量不同、电荷不同,在电场和磁场中的运动行为不同。计算机对其分析后,得到它们的相对质量与
电荷数的比值,即质荷比。
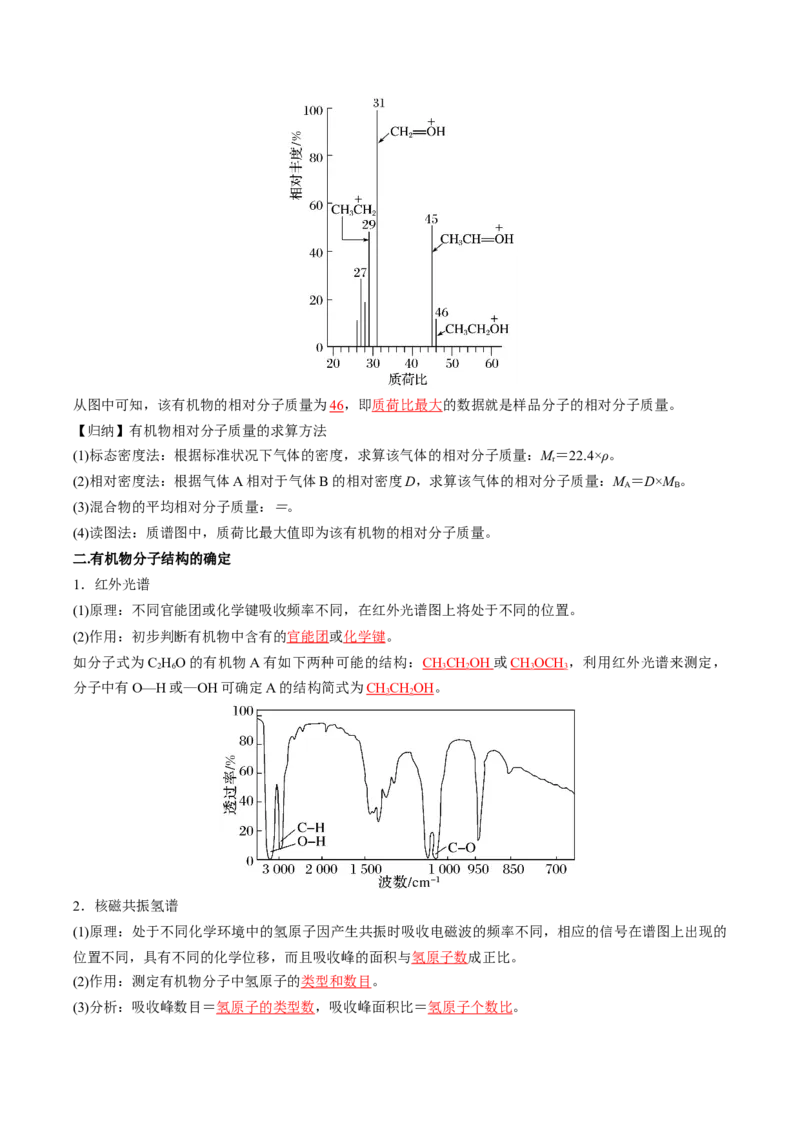
(2)质谱图:以质荷比为横坐标,以各类离子的相对丰度为纵坐标,根据记录结果所建立的坐标图。
如下图为某有机物的质谱图:从图中可知,该有机物的相对分子质量为46,即质荷比最大的数据就是样品分子的相对分子质量。
【归纳】有机物相对分子质量的求算方法
(1)标态密度法:根据标准状况下气体的密度,求算该气体的相对分子质量:M=22.4×ρ。
r
(2)相对密度法:根据气体A相对于气体B的相对密度D,求算该气体的相对分子质量:M =D×M 。
A B
(3)混合物的平均相对分子质量:=。
(4)读图法:质谱图中,质荷比最大值即为该有机物的相对分子质量。
二.有机物分子结构的确定
1.红外光谱
(1)原理:不同官能团或化学键吸收频率不同,在红外光谱图上将处于不同的位置。
(2)作用:初步判断有机物中含有的官能团或化学键。
如分子式为C HO的有机物A有如下两种可能的结构:CHCHOH 或CHOCH ,利用红外光谱来测定,
2 6 3 2 3 3
分子中有O—H或—OH可确定A的结构简式为CHCHOH。
3 2
2.核磁共振氢谱
(1)原理:处于不同化学环境中的氢原子因产生共振时吸收电磁波的频率不同,相应的信号在谱图上出现的
位置不同,具有不同的化学位移,而且吸收峰的面积与氢原子数成正比。
(2)作用:测定有机物分子中氢原子的类型和数目。
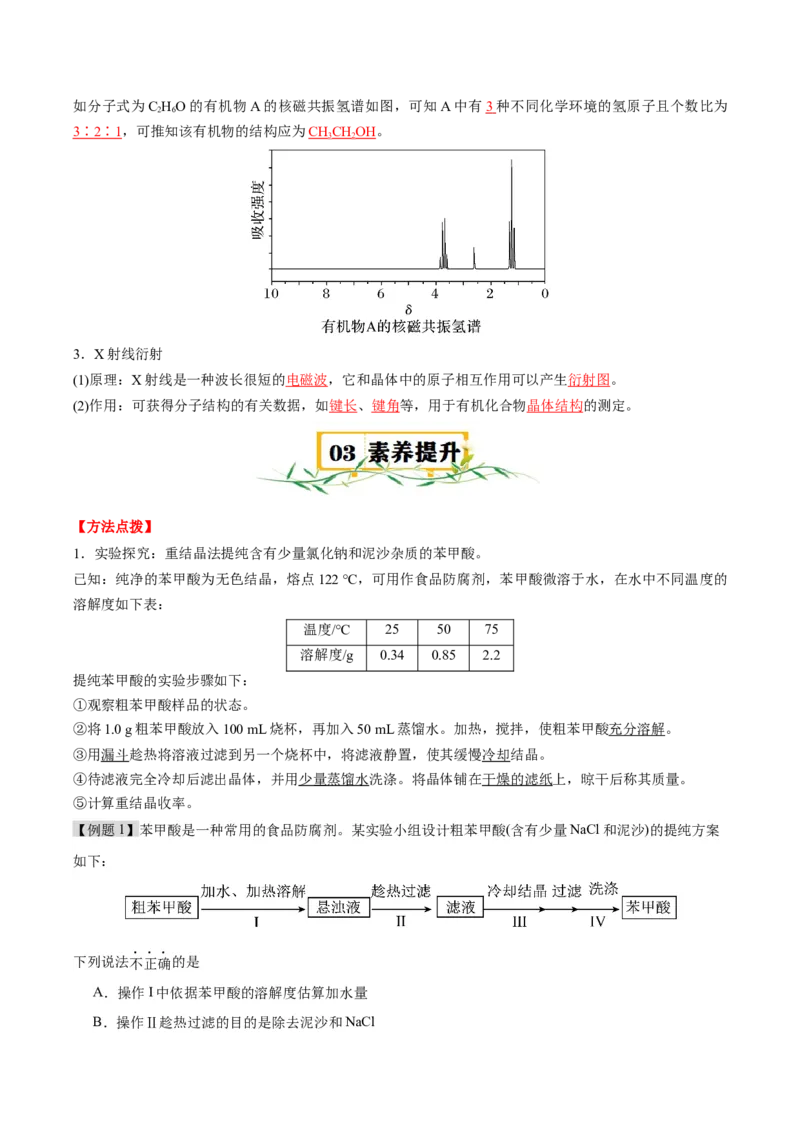
(3)分析:吸收峰数目=氢原子的类型数,吸收峰面积比=氢原子个数比。如分子式为C HO的有机物A的核磁共振氢谱如图,可知A中有3 种不同化学环境的氢原子且个数比为
2 6
3 ∶ 2 ∶ 1 ,可推知该有机物的结构应为CHCHOH。
3 2
3.X射线衍射
(1)原理:X射线是一种波长很短的电磁波,它和晶体中的原子相互作用可以产生衍射图。
(2)作用:可获得分子结构的有关数据,如键长、键角等,用于有机化合物晶体结构的测定。
【方法点拨】
1.实验探究:重结晶法提纯含有少量氯化钠和泥沙杂质的苯甲酸。
已知:纯净的苯甲酸为无色结晶,熔点122 ℃,可用作食品防腐剂,苯甲酸微溶于水,在水中不同温度的
溶解度如下表:
温度/℃ 25 50 75
溶解度/g 0.34 0.85 2.2
提纯苯甲酸的实验步骤如下:
①观察粗苯甲酸样品的状态。
②将1.0 g粗苯甲酸放入100 mL烧杯,再加入50 mL蒸馏水。加热,搅拌,使粗苯甲酸充分溶解。
③用漏斗趁热将溶液过滤到另一个烧杯中,将滤液静置,使其缓慢冷却结晶。
④待滤液完全冷却后滤出晶体,并用少量蒸馏水洗涤。将晶体铺在干燥的滤纸上,晾干后称其质量。
⑤计算重结晶收率。
【例题1】苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案
如下:
下列说法不正确的是
A.操作I中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaClC.操作Ⅲ缓慢冷却结晶可减少杂质被包裹
D.操作Ⅳ可用冷水洗涤晶体
【答案】B
【分析】苯甲酸微溶于冷水,易溶于热水。粗苯甲酸中混有泥沙和氯化钠,加水、加热溶解,苯甲酸、
NaCl溶解在水中,泥沙不溶,从而形成悬浊液;趁热过滤出泥沙,同时防止苯甲酸结晶析出;将滤液冷却
结晶,大部分苯甲酸结晶析出,氯化钠仍留在母液中;过滤、用冷水洗涤,便可得到纯净的苯甲酸。
【详解】A.操作I中,为减少能耗、减少苯甲酸的溶解损失,溶解所用水的量需加以控制,可依据苯甲
酸的大致含量、溶解度等估算加水量,A正确;
B.操作Ⅱ趁热过滤的目的,是除去泥沙,同时防止苯甲酸结晶析出,NaCl含量少,通常不结晶析出,B
不正确;
C.操作Ⅲ缓慢冷却结晶,可形成较大的苯甲酸晶体颗粒,同时可减少杂质被包裹在晶体颗粒内部,C正
确;
D.苯甲酸微溶于冷水,易溶于热水,所以操作Ⅳ可用冷水洗涤晶体,既可去除晶体表面吸附的杂质离子,
又能减少溶解损失,D正确;
故选B。
2.谱图法在确定有机物分子结构中的应用
(1)核磁共振氢谱图中,峰的个数即氢原子的种类数,而峰面积之比为各类氢原子个数之比。
(2)可根据红外光谱图推知有机物分子中含有哪些化学键、官能团,从而确定有机物的结构。
(3)将X射线衍射技术用于有机化合物(特别是复杂的生物大分子)晶体结构的测定。
3.确定有机物分子式(结构式)的一般思路【例题2】有机物M可从酸牛奶中提取。已知纯净的M为无色黏液体,易溶于水。研究M的组成与结构,
进行了如下实验,请根据实验步骤解释或得出实验结论:
(1)称取M 4.5g,升温使其汽化,测其密度是相同条件下H 的45倍。则M的摩尔质量为: 。
2
(2)将此4.5g M在足量纯O 中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重
2
2.7g和6.6g,则M的分子式为: 。
(3)通过M的红外光谱图发现该分子中既有羟基,还有羧基,则羟基电子式 。
(4)M的核磁共振氢谱如下图,M中含有 种氢原子。
(5)综上所述,M的结构简式为 。
(6)M易溶于水的原因 。
【答案】(1)90g/mol
(2)C HO
3 6 3
(3)
(4)4(5)
(6)M中含有羟基,可以和水形成分子间氢键,增大其溶解度
【分析】根据相同条件下密度比等于摩尔质量之比计算;产物依次缓缓通过浓硫酸、碱石灰,发现两者分
别增重2.7g和6.6g,可知燃烧生成水、二氧化碳分别是2.7g和6.6g,根据元素守恒计算;羟基有1个没成
对电子;根据M的核磁共振氢谱图,可知M有4组峰,比值为1:1:1:3,以此解题。
【详解】(1)相同条件下,气体的密度比等于摩尔质量之比,所以摩尔质量是氢气的45倍,M的摩尔质
量是 =90g/mol;
(2)4.5gM在足量纯O 中充分燃烧生成水、二氧化碳分别是2.7g和6.6g,则n(HO)=
2 2
,n(CO)= ,则4.5gM 中含C、H、O的物质的量分别为
2
0.15mol、 、 ,C、H、O的物质的量之
比为1:2:1,摩尔质量是90g/mol,所以分子式为C HO;
3 6 3
(3)羟基的电子式 ;
(4)根据M的核磁共振氢谱图,可知M有4组峰,即有4种等效氢;
(5)根据M的核磁共振氢谱图,可知M有4组峰,即有4种等效氢,比值为1:1:1:3,通过M的红外光谱
图发现该分子中既有羟基,还有羧基,结合分子式可知含有1个羟基,1个羧基;综上所述,M的结构简
式为 ;
(6)根据M的结构可知,其中含有羟基,则M易溶于水的原因是:M中含有羟基,可以和水形成分子间
氢键,增大其溶解度。
【例题3】我国科学家屠呦呦因成功提取青蒿素获得诺贝尔奖,某实验小组拟提取青蒿素并测定其化学式。
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,分子中含有过氧键(―O―O―)具有热不稳定性。
易溶于乙醚,在水中几乎不溶。I.实验室用乙醚提取青蒿素的工艺流程如图:
(1)欲测定青蒿素的分子结构,应选用以下哪种化学分析仪器:___________。
A.质谱仪 B.红外光谱仪 C.核磁共振氢谱 D.X射线衍射
(2)在操作I前要对青蒿进行粉碎,其目的是 。为操作Ⅱ应选择以下 。
A.过滤 B.蒸馏 C.柱色谱分离 D.分液
(3)操作Ⅲ进行的是重结晶,其操作步骤为微热溶解→ → →过滤、洗涤、干燥。
Ⅱ.已知青蒿素是一种烃的含氧衍生物,为确定其化学式,又进行了如下实验:
实验步骤:
①连接装置,检查装置的气密性。
②称量E、F中仪器及药品的质量
③取14.10g青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧
④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量
(4)装置E装入的药品为 ,为减小实验误差可在F后加装盛 的装置。
(5)实验测得:
装置 实验前 实验后
E 24.00g 33.90g
F 100.00g 133.00g
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式为 。
【答案】(1)D
(2)增大青蒿与乙醚的接触面积,提高浸出效率 B
(3)趁热过滤 冷却结晶
(4)无水氯化钙(五氧化二磷、硅胶) 碱石灰(5)C H O
15 22 5
【详解】(1)测定分子的空间结构最普遍的方法是X射线衍射法可以看到微观结构,可以测定晶体的晶
胞参数,从而确定分子的结构,故选D;
(2)根据乙醚浸取法的流程可知,操作I前对青蒿进行干燥破碎,可以增大青蒿与乙醚的接触面积,提高
青蒿素的浸取率;提取液经过蒸馏后可得青蒿素的粗品,故选B;
(3)重结晶的步骤为加热溶解、趁热过滤、冷却结晶、过滤、洗涤、干燥;
(4)E和F一个吸收生成的HO,一个吸收生成的CO,应先吸水后再吸收CO,所以E内装的无水
2 2 2
CaCl 或硅胶或PO,需准确测量青蒿素燃烧生成的CO 和HO,实验前应排除装置内的空气,防止干扰实
2 2 5 2 2
验,故应在左侧增加除去空气中二氧化碳、水蒸气的除杂装,同时在右侧增加防止空气中二氧化碳、水蒸
气进入装置F的装置,可在F后加装盛碱石灰的装置;