文档内容
第一章 总结与检测 练习(解析版)
一.选择题(共25小题,每题3分,共75分)
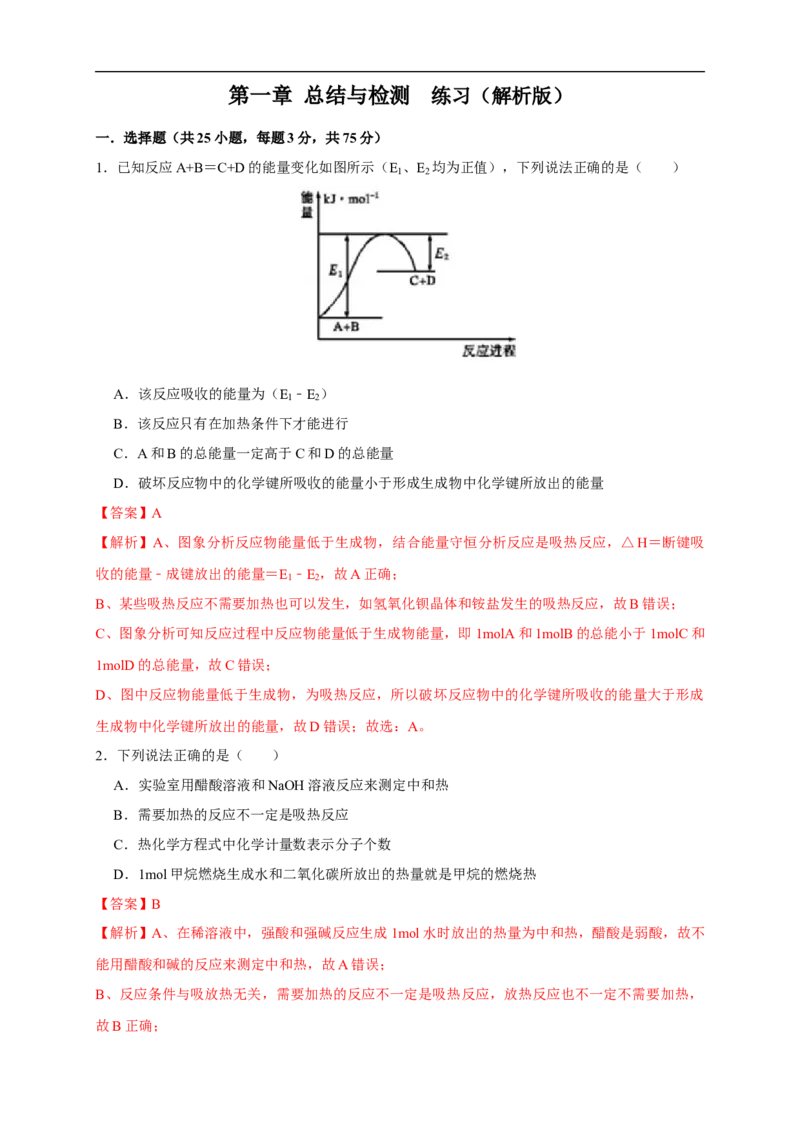
1.已知反应A+B=C+D的能量变化如图所示(E 、E 均为正值),下列说法正确的是( )
1 2
A.该反应吸收的能量为(E ﹣E )
1 2
B.该反应只有在加热条件下才能进行
C.A和B的总能量一定高于C和D的总能量
D.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
【答案】A
【解析】A、图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,△H=断键吸
收的能量﹣成键放出的能量=E ﹣E ,故A正确;
1 2
B、某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故B错误;
C、图象分析可知反应过程中反应物能量低于生成物能量,即1molA和1molB的总能小于1molC和
1molD的总能量,故C错误;
D、图中反应物能量低于生成物,为吸热反应,所以破坏反应物中的化学键所吸收的能量大于形成
生成物中化学键所放出的能量,故D错误;故选:A。
2.下列说法正确的是( )
A.实验室用醋酸溶液和NaOH溶液反应来测定中和热
B.需要加热的反应不一定是吸热反应
C.热化学方程式中化学计量数表示分子个数
D.1mol甲烷燃烧生成水和二氧化碳所放出的热量就是甲烷的燃烧热
【答案】B
【解析】A、在稀溶液中,强酸和强碱反应生成1mol水时放出的热量为中和热,醋酸是弱酸,故不
能用醋酸和碱的反应来测定中和热,故A错误;
B、反应条件与吸放热无关,需要加热的反应不一定是吸热反应,放热反应也不一定不需要加热,
故B正确;C、热化学方程式中的计量数只能表示物质的量,不能表示分子个数,故C错误;
D、在101kp时,1mol可燃物完全燃烧生成指定的产物时放出的热量为该物质的燃烧热,生成的水
必须是液态水,故D错误。故选:B。
3.已知:燃烧热指101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量。101kPa
时,下列过程放出的热量属于碳的燃烧热的是( )
A.1mol C燃烧完全转化为CO气体
B.24g C燃烧完全转化为CO 气体
2
C.12g C燃烧完全转化为CO 气体
2
D.1mol C与CO 反应完全转化为CO气体
2
【答案】C
【解析】A、C完全燃烧应生成二氧化碳,故A错误;
B、24gC的物质的量为2mol,故B错误;
C、12gC的物质的量为1mol,燃烧完全转化为CO 气体放出的热量就是C的燃烧热,故C正确;
2
D、C与CO 反应吸热,而燃烧放热,故D错误;故选:C。
2
4.强酸与强碱的稀溶液发生中和反应:H+(aq)+OH﹣(aq)═H O(l)△H=﹣57.3kJ/mol。向
2
1L 0.5mol/L的NaOH溶液中加入下列物质: 稀醋酸, 稀盐酸, 浓硫酸,恰好完全反应时
对应的热效应△H 、△H 、△H 的关系正确的①是( )② ③
1 2 3
A.△H <△H <△H B.△H >△H >△H
1 3 2 1 2 3
C.△H <△H <△H D.△H >△H >△H
1 2 3 1 3 2
【答案】B
【解析】强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH﹣(aq)═H O(l)△H=﹣
2
57.3kJ/mol,
分别向1L 0.5mol/L的NaOH溶液中加入: 稀醋酸; 稀盐酸; 浓硫酸,
醋酸的电离吸热,浓硫酸溶于水放热,则恰①好完全反应②时的放出的③热量为 > > ,所以△H
1
>△H >△H ,故选:B。 ③ ② ①
2 3
5.下列叙述正确的是( )
A.乙醇的燃烧热为△H=﹣1366.8kJ/mol,则乙醇燃烧的热化学方程式可表示为C H OH
2 5
(1)+3O (g)═2CO (g)+3H O(g)△H=﹣1366.8kJ/mol
2 2 2
B.已知H+(aq)+OH﹣(aq)═H O(1)△H=﹣573 kJ/mol,则H SO 溶液和稀Ba(OH)
2 2 4 2
溶液反应生成18gH O(1)时放出的热量为57.3kJ
2
C.已知2H S(g)+O (g)═2s(s)+2H O(D)△H ,2H S(g)+3O (g)═2SO (g)
2 2 2 1 2 2 2
+2H O(l)△H ,则△H >△H
2 2 1 2D.常温下,反应A(s)+B(g)=2C(g)不能自发进行,则该反应的△H<0
【答案】C
【解析】A.已知C H OH(l) 的燃烧热是 1366.8KJ/mol,则C H OH(l)+3O (g)═2CO
2 5 2 5 2 2
(g)+3H O(l)反应的△H=﹣1366.8kJ/mol,故A错误;
2
B.HCl和NaOH反应的中和热△H=﹣57.3 kJ•mol﹣1,但生成沉淀也要放热,则 H SO 和Ba
2 4
(OH) 的中和热大于57.3kJ/mol,故B错误;
2
C.硫单质进一步燃烧生成二氧化硫的反应是放热反应,所以硫化氢燃烧生成二氧化硫的过程放热
热多,则△H >△H ,故C正确;
1 2
D.反应不能自发进行,说明:△H﹣T△S>0,该反应是一个气体体积增大的反应,所以熵增大,
要使△H﹣T△S>0,则△H一定大于0,故D错误;故选:C。
6.下列热化学方程式中的△H表示可燃物的燃烧热的是( )
A.C(s)+ O (g)═CO(g)△H=﹣110.5kJ/mol
2
B.2H (g)+O (g)═2H O(1)△H=﹣571.6kJ/mol
2 2 2
C.CO(g)+ O (g)═CO (g)△H=﹣283kJ/mol
2 2
D.CH (g)+2O (g)═CO (g)+2H O(g)△H=﹣802.3kJ/mol
4 2 2 2
【答案】C
【解析】A、CO不是碳元素的稳定的氧化物,应该是产生二氧化碳,故A错误;
B、燃烧热是指1mol纯净物完全燃烧,方程式中为2mol,不是燃烧热,故B错误;
C、1molCO完全燃烧生成稳定的CO ,符合燃烧热的概念要求,放出的热量为燃烧热,故C正确;
2
D、气态水不是稳定的氧化产物,应该是液态水,故D错误。故选:C。
7.已知25°C、101 kPa时,强酸与强碱的稀溶液发生中和反应生成1 mol水放出的热量为57.3kJ,
则下列描述正确的是( )
A.酸碱中和反应的中和热为57.3kJ
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l)△H=+57.3 kJ•mol﹣1
2
C.1 mol强酸和1 mol强碱完全反应,放出的热量一定为57.3 kJ
D.稀盐酸与稀氨水反应生成1 mol水,放出的热量小于57.3 kJ
【答案】D
【解析】A.中和热的单位为 kJ•mol﹣1,故A错误;
B.酸碱中和反应为放热反应,则NaOH(aq)+HCl(aq)═NaCl(aq)+H O(l);△H=﹣57.3
2
kJ•mol﹣1,故B错误;
C.在稀溶液中,稀的强酸跟强碱发生中和反应而生成 1mo水,这时的反应热叫做中和热,放出的热量为57.3 kJ,但1 mol强酸和1 mol强碱完全反应所放出的热量不一定等于中和热,如 1mol硫
酸与1mol氢氧化钡反应生成2mol水,反应热不是中和热,故C错误;
D.弱碱电离时吸热,则稀盐酸与稀氨水反应生成1 mol水,放出的热量小于57.3 kJ,故D正确。
故选:D。
8.50mL0.50mol•L﹣1盐酸与50mL0.55 mol•L ﹣1NaOH 溶液进行中和反应,通过测定反应过程中
所放出的热量可计算中和热,下列说法正确的是( )
A.在测定中和热的实验中,至少需要测定并纪录的温度是3次
B.大烧杯上如不盖硬纸板,测得的中和热数值会偏小
C.用相同浓度和体积的氨水代替NaOH 溶液进行上述实验,测得中和热的数值会偏大
D.从实验装置上看,除了缺少环形玻璃搅拌棒外没有其他问题
【答案】B
【解析】A.中和反应之前,分别记录盐酸和氢氧化钠的温度,中和反应开始后,记录下混合溶液
的最高温度,即最终温度,所以每一组要记录 3次温度,而我们实验时至少要做2组,所以至少要
记录6次温度,故A错误;
B.大烧杯上如不盖硬纸板,会有部分能量损失,这样测得的中和热数值会偏小,故B正确;
C.一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热
量偏小,测得中和热的数值会偏小,故C错误;
D.根据量热计的构造可知该装置的缺少仪器是:环形玻璃搅拌器以及大小烧杯口不平,故 D错误;
故选:B。
9.将V mL 1.0mol/L HCl溶液和V mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,
1 2
实验结果如图所示(实验中始终保持V +V =50mL).下列叙述正确的是( )
1 2A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为电能
C.NaOH溶液的浓度约是1.5mol/L
D.该实验表明有水生成的反应都是放热反应
【答案】C
【解析】A.温度为22℃是指5mL盐酸的温度,则不是环境温度,故A错误;
B.由图示可以看出该反应过程放出热量,表明化学能可能转化为热能,故B错误;
C.恰好反应时参加反应的盐酸溶液的体积是 30mL,由V +V =50ml可知,消耗的氢氧化钠溶液
1 2
的质量为20mL。
设恰好反应时氢氧化钠溶液中溶质的物质的量是n。
HCl+NaOH=NaCl+H O
2
1 1
1.0mol•L﹣1×0.03L n
则n=1.0mol•L﹣1×0.03L=0.03mol,所以浓度是 =1.5mol/L,故C正确;
D.只是该反应放热,其他有水生成的反应不一定,故D错误;故选:C。
10.下列中和反应中放出热量最多的是( )
A.100mL0.3mol/L的HCl和50mL0.3mol/L的NaOH相混合
B.80mL0.3mol/L的HCl和80mL0.3mol/L的NaOH溶液相混合
C.80mL0.3mol/L的H SO 和80mL0.3mol/L的NaOH溶液相混合
2 4
D.50mL0.3mol/L的H SO 和50mL0.6mol/L的NaOH溶液相混合
2 4
【答案】D
【解析】A.n(HCl)=0.03mol,n(NaOH)=0.015mol,则生成水0.015mol;
B.n(HCl)=0.024mol,n(NaOH)=0.024mol,则生成水0.024mol;
C.n(H SO )=0.024mol,n(NaOH)=0.024mol,则生成水0.024mol;
2 4
D.n(H SO )=0.015mol,n(NaOH)=0.03mol,则生成水0.03mol;
2 4
则D生成的水最多,放出的热量最多,故选:D。
11.已知H+(aq)+OH﹣(aq)═H O(l)△H=﹣57.3kJ•mol﹣1.下列酸和碱反应测得的中和热
2
(△H)偏高的是( )
A.稀HClO 溶液和稀KOH溶液
4
B.稀氨水和稀醋酸
C.浓硫酸与稀NaOH溶液
D.稀硫酸和Ba(OH) 稀溶液
2【答案】B
【解析】A.稀HClO 溶液和稀KOH溶液生成盐和水,对测定中和热无影响,故A不选;
4
B.一水合氨、醋酸电离吸热,导致测定热量偏小,测得的中和热(△H)偏高,故B选;
C.浓硫酸稀释放热,测定热量偏大,测得的中和热(△H)偏低,故C不选;
D.生成硫酸钡放热,测定热量偏大,测得的中和热(△H)偏低,故D不选;故选:B。
12.下列热化学方程式中,△H能正确表示物质的燃烧热的是( )
A.2C H (l)+25O (g)═16CO (g)+18H O(l)△H═﹣11003 kJ/mol
8 18 2 2 2
B.H (g)+ O (g)═H O(g)△H═﹣241.8 kJ/mol
2 2 2
C.2C(s)+O (g)═2CO(g)△H═﹣221 kJ/mol
2
D.CO(g)+ O (g)═CO (g)△H═﹣283.0 kJ/mol
2 2
【答案】D
【解析】A、C H 的化学计量数为2,产物是稳定氧化物,△H不代表燃烧热,故A错误;
8 18
B、H 的化学计量数为1,但产物不是稳定氧化物,△H不代表燃烧热,故B错误;
2
C、C的化学计量数为2,产物不是稳定氧化物,△H不代表燃烧热,故C错误;
D、CO的化学计量数为1,产物为稳定氧化物,△H代表燃烧热,故D正确;故选:D。
13.一些烷烃的标准燃烧热如表:
化合物 标准燃烧热 化合物 标准燃烧热
(H/kJ•mol﹣1) (H/kJ•mol﹣1)
甲烷 ﹣891.0 正丁烷 ﹣2878.0
乙烷 ﹣1560.8 异丁烷 ﹣2869.6
丙烷 ﹣2221.5 异戊烷 ﹣3531.3
下列说法正确的是( )
A.热稳定性:正丁烷>异丁烷
B.正戊烷的标准燃烧热△H大约为﹣3540kJ•mol﹣1
C.乙烷燃烧的热化学方程式为2C H (g)+7O (g)=4CO (g)+6H O(l) H=﹣1560.8
2 6 2 2 2
kJ•mol﹣1
D.甲烷的热值是表格中6 种物质里最小的
【答案】B
【解析】A.由表格中的数据可知,异丁烷的燃烧热比正丁烷的燃烧热小,则异丁烷的能量低,即
热稳定性为正丁烷<异丁烷,故A错误;
B.正戊烷和异戊烷互为同分异构体,由表格中正丁烷、异丁烷的燃烧热比较可知,则互为同分异构体的化合物,支链多的燃烧热小,则正丁烷的燃烧热大于异戊烷,即正戊烷的燃烧热大约在
3540kJ/mol左右,故B正确;
C.根据乙烷燃烧热的含义:完全燃烧1mol乙烷生成二氧化碳和液态水时会放出1560.8kJ的热量,
所以热化学方程式为2C H (g)+7O (g)=4CO (g)+6H O(l)△H=﹣3121.6kJ/mol,故C错
2 6 2 2 2
误;
D.根据表格数据,甲烷的热值是 kJ•g﹣1>乙烷的热值是 kJ•g﹣1,故D错误。故选:
B。
14.下列热化学方程式中△H能表示可燃物燃烧热的是( )
A.2H (g)+O (g)=2H O(g)△H=﹣483.6kJ•mol﹣1
2 2 2
B.CO(g)+ O (g)=CO (g)△H=﹣283kJ•mol﹣1
2 2
C.CH (g)+2O (g)=CO (g)+2H O(g)△H=﹣802kJ•mol﹣1
4 2 2 2
D.C(s)+ O (g)=CO(g)△H=﹣108kJ•mol﹣1
2
【答案】B
【解析】A.燃烧热是指1mol纯净物完全燃烧,方程式中为2mol,气态水不是稳定氧化物的状态,
生成稳定的氧化物,水应为液态,故A错误;
B.1molCO完全燃烧生成稳定的CO ,符合燃烧热的概念要求,放出的热量为燃烧热,故B正确;
2
C.气态水不是稳定氧化物的状态,生成稳定的氧化物,水应为液态,故C错误;
D.CO不是稳定氧化物,不符合燃烧热的概念要求,故D错误;故选:B。
15.下列说法正确的是( )
A.1 mol盐酸与1 mol Mg(OH) 完全中和所放出的热量为57.3kJ.mol﹣1
2
B.25℃、101 kPa时,1 mol H 和2 mol H 燃烧生成液态水,求出的燃烧热相等
2 2
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO ,所以C燃烧生成CO反应一
2
定是吸热反应
D.25℃时,1 mol甲烷燃烧所放出的热量为甲烷的燃烧热
【答案】B
【解析】A.1 mol盐酸与1 mol Mg(OH) 完全中和生成氯化镁和1molH O,同时Mg(OH)
2 2 2
反应要溶解,需要吸收热量,所以放出的热量不是57.3kJ.mol﹣1,故A错误;
B.燃烧热指1mol可燃物完全燃烧生成稳定的化合物时所放出的热量,与反应物的量无关,所以
25℃、101 kPa时,1 mol H 和2 mol H 燃烧生成液态水,求出的燃烧热相等,故B正确;
2 2
C.燃烧反应是放热反应,则C燃烧生成CO反应一定是放热反应,故C错误;D.1 mol甲烷燃烧生成稳定的化合物即二氧化碳和液态水时所放出的热量为甲烷的燃烧热,故D
错误。故选:B。
17.下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa ):
C H (g)+ O (g)═4CO (g)+5H O(l)△H=﹣2 878kJ•mol﹣1
4 10 2 2 2
①
C H (g)+ O (g)═4CO (g)+5H O(g)△H=﹣2 658kJ•mol﹣1
4 10 2 2 2
②
C H (g)+ O (g)═4CO(g)+5H O(l)△H=﹣1 746kJ•mol﹣1
4 10 2 2
③
C H (g)+ O (g)═4CO(g)+5H O(g)△H=﹣1 526kJ•mol﹣1
4 10 2 2
④由此判断,正丁烷的燃烧热是( )
A.△H=﹣2 878 kJ•mol﹣1 B.△H=﹣2 658 kJ•mol﹣1
C.△H=﹣1 746 kJ•mol﹣1 D.△H=﹣1 526 kJ•mol﹣1
【答案】A
【解析】正丁烷的燃烧热是1mol正丁烷完全燃烧生成CO (气),H O(液)放出的热量,故热化
2 2
学方程式(1)C H (g)+O (g)═4CO (g)+5H O(l)△H=﹣2878kJ/mol,符合燃烧热的概
4 10 2 2 2
念,所以正丁烷的燃烧热为﹣2878 kJ/mol。故选:A。
18.下列热化学方程式中△H的数值表示可燃物燃烧热的是( )
A.CO(g)+ O (g)═CO (g)△H=﹣283kJ•mol﹣1
2 2
B.CH (g)+2O (g)═CO (g)+2H O(g)△H=﹣802.3kJ•mol﹣1
4 2 2 2
C.2H (g)+O (g)═2H O(l)△H=﹣571.6kJ•mol﹣1
2 2 2
D.H (g)+Cl (g)═2HCl(g)△H=﹣184.6kJ•mol﹣1
2 2
【答案】A
【解析】A、符合燃烧热的概念,故A正确;
B、生成产物中的水是气体,属于不稳定氧化物,故B错误;
C、热化学方程式中是2mol可燃物氢气燃烧放热,不符合燃烧热的概念,故C错误;
D、HCl不是氧化物,不符合燃烧热的概念要求,故D错误;故选:A。
19.机动车尾气中含NO,在催化剂作用下,利用CO可将其转化为无毒的物质。已知下列热化学
方程式:
N (g)+O (g)═2NO(g)△H =+180kJ•mol﹣1;
2 2 1
①2CO(g)+O (g)═2CO (g)△H =﹣564kJ•mol﹣1;
2 2 2
②则NO(g)+CO(g)═﹣CO (g)+ N (g)△H=xkJ•mol﹣1,x为( )
2 2
A.﹣744 B.+744 C.﹣372 D.+372
【答案】C
【解析】由 N (g)+O (g)═2NO(g)△H =+180kJ•mol﹣1;
2 2 1
2CO(g)①+O (g)═2CO (g)△H =﹣564kJ•mol﹣1;
2 2 2
②
结合盖斯定律可知, ×( ﹣ )得到 NO(g)+CO(g)═﹣CO (g)+ N (g),则
2 2
② ①
,故选:C。
20.在1200℃时,天然气脱硫工艺中会发生下列反应
H S(g)+ O (g)═SO (g)+H O(g)△H
2 2 2 2 1
①
2H S(g)+SO (g)═ S (g)+2H O(g)△H
2 2 2 2 2
②
H S(g)+ O (g)═S(g)+H O(g)△H
2 2 2 3
③2S(g)═S (g)△H 则△H 的正确表达式为( )
2 4 4
A.△H = (△H +△H ﹣3△H ) B.△H = (3△H ﹣△H ﹣△H )
4 1 2 3 4 3 1 2
C.△H = (△H +△H ﹣2△H ) D.△H = (△H ﹣△H ﹣3△H )
4 1 2 3 4 1 2 3
【答案】A
【解析】H S(g)+ O (g)=SO (g)+H O(g)△H
2 2 2 2 1
①
2H S(g)+SO (g)= S (g)+2H O(g)△H
2 2 2 2 2
②
H S(g)+ O (g)=S(g)+H O(g)△H
2 2 2 3
将2× +2× ﹣6× 得到6S(g)=3S (g)③的焓变3△H =2△H +2△H ﹣6△H ;所以2S(g)
2 4 1 2 3
② ① ③
=S (g)的焓变△H = (2△H +2△H ﹣6△H )= (H +△H ﹣3△H );故选:A。
2 4 1 2 3 1 2 3
21.以下反应可表示获得乙醇并用作汽车燃料的过程,下列有关说法正确的是( )
6CO (g)+6H O(1)═C H O (s)+6O (g)△H
2 2 6 12 6 2 1
①C
6
H
12
O
6
(s)═2C
2
H
5
OH(1)+2CO
2
(g)△H
2
②C H OH(1)+3O (g)═2CO (g)+3H O(1)△H
2 5 2 2 2 3
③A.2△H
3
=﹣△H
1
﹣△H
2
B.△H 、△H 、△H 均为△H<0
3 1 2
C.在不同油耗汽车中发生反应 ,△H 会不同
3
D.植物的光合作用通过反应 ③将热能转化为化学能
【答案】A ①
【解析】A、由盖斯定律可知:﹣ ﹣ = ×2,则2△H =﹣△H ﹣△H ,故A正确;
3 1 2
B、假设反应热均小于0,根据2△①H
3
=②﹣△③H
1
﹣△H
2
可知△H
2
=﹣△H
1
﹣2△H
3
,则若△H
1
<0,
△H <0,则△H >0,与假设矛盾,故B错误;
3 2
C、焓变与反应的始态和终态有关,则在不同油耗汽车中发生反应 ,△H 相同,故C错误;
3
D、植物的光合作用利用太阳能,将太阳能转化成化学能,故D错③误。故选:A。
22.已知: 2H (g)+O (g)═2H O(l)△H=akJ•mol﹣1
2 2 2
①
H (g)+ O (g)═H O(g)△H=bkJ•mol﹣1( )
2 2 2
②A.a=2b>0 B.a<2b C.a>2b D.a=2b<0
【答案】B
【解析】已知: H (g)+ O (g)═H O(g)△H=bkJ•mol﹣1所以2H (g)+O (g)═2H O
2 2 2 2 2 2
(g)△H=2bkJ②•mol﹣1, 2H (g)+O (g)═2H O(l)△H=akJ•mol﹣1
2 2 2
燃烧为放热反应,△H<0①,相同物质的量的氢气燃烧,生成液态水比生成水蒸气释放的热量多,
所以a<2b,故B符合;故选:B。
23.已知下列热化学方程式:2Zn(s)+O (g)═2ZnO(s);△H =﹣702.2kJ/mol
2 1
Hg(l)+ O (g)═HgO(s)△H =﹣90.7kJ/mol
2 2
由此可知Zn(s)+HgO(s)═ZnO(s)+Hg(l)的△H ,其中△H 的值是( )
3 3
A.﹣260.4kJ/mol B.﹣254.6kJ/mol
C.﹣438.9kJ/mol D.﹣441.8kJ/mol
【答案】A
【解析】已知 2Zn(s)+O (g)═2ZnO(s)△H =﹣702.2kJ/mol
2 1
①
Hg(l)+ O (g)═HgO(s)△H =﹣90.7kJ/mol
2 2
②根据盖斯定律: ×0.5﹣ 即可得:Zn(s)+HgO(s)=ZnO(s)+Hg(l)△H =(﹣
3
702.2×0.5+90.7)k①J•mol﹣1=②﹣260.4kJ•mol﹣1,故选:A。24.已知下列热化学方程式:
C(s,石墨)+O (g)═CO (g)△H=﹣393.5 kJ•mol﹣1
2 2
①2H (g)+O (g)═2H O(1)△H=﹣571.6 kJ•mol﹣1
2 2 2
②CH (g)+2O (g)═CO (g)+2H O(1)△H=﹣890.3 kJ•mol﹣1
4 2 2 2
③则C(s,石墨)+2H
2
(g)═CH
4
(g)的△H是( )
A.+74.8 kJ•mol﹣1 B.﹣149.6 kJ•mol﹣1
C.﹣74.8 kJ•mol﹣1 D.﹣149.6 kJ•mol﹣1
【答案】C
【解析】已知反应 C(s,石墨)+O (g)═CO (g)△H=﹣393.5 kJ•mol﹣1
2 2
2H (g)+O (g①)═2H O(1)△H=﹣571.6 kJ•mol﹣1
2 2 2
②CH (g)+2O (g)═CO (g)+2H O(1)△H=﹣890.3 kJ•mol﹣1
4 2 2 2
③结合盖斯定律反应 + ﹣ 即可得:C(,石墨)+2H2(g)=CH4(g)△H=(﹣393.5﹣
571.6+890.3)kJ•mo①l﹣1=②﹣74③.8kJ•mol﹣1,故选:C。
25.已知溴跟氢气反应的热化学方程式如下(Q 、Q 、Q 均为正值):H (g)+Br (g)→2HBr
1 2 3 2 2
(l)+Q ,H (g)+Br (g)→2HBr(g)+Q ,H (g)+Br (l)→2HBr(g)+Q ,下列判断
1 2 2 2 2 2 3
正确的是( )
A.Q >Q >Q
1 2 3
B.Q 与 Q 的大小无法判断
1 3
C.溴蒸气转化为液态溴需要放出(Q ﹣Q )kJ 的热量
2 3
D.1LH 和 1LBr 蒸气反应生成 2LHBr 气体时放出 Q kJ 热量
2 2 2
【答案】A
【解析】A.同种物质气态比液体能量高,则2molHBr(g)具有的能量大于2molHBr(l)具有的
能量,则Q >Q ,1molBr (g)具有的能量大于1molBr (l)具有的能量,则Q >Q ,所以Q >
1 2 2 2 2 3 1
Q >Q ,故A正确;
2 3
B.由A可知Q >Q >Q ,则Q 与 Q 的大小可以判断,故B错误;
1 2 3 1 3
C. H (g)+Br (g)→2HBr(g)+Q , H (g)+Br (l)→2HBr(g)+Q ,根据盖斯定律
2 2 2 2 2 3
﹣② 得Br (g)→Br (l)+(Q ﹣Q ),③所以1mol溴蒸气转化为1mol液态溴需要放出(Q ﹣
2 2 2 3 2
②Q )k③J 的热量,题干没有说明溴蒸气的物质的量,故C错误;
3
D.由H (g)+Br (g)→2HBr(g)+Q 可知,1molH 和 1molBr 蒸气反应生成 2molHBr 气体
2 2 2 2 2
时放出 Q kJ 热量,所以1LH 和 1LBr 蒸气反应生成 2LHBr 气体时放出热量不是Q kJ,故D错
2 2 2 2
误;故选:A。
二.解答题(共2小题)26.(15分)中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L
的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从图实验装置看,其中尚缺少的一种玻璃用品是______________。
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于____________。
(3)若改用60mL 0.25mol•L﹣1 H SO 和50mL 0.55mol•L﹣1 NaOH溶液进行反应与上述实验相
2 4
比,所放出的热量______________(填“相等”、“不相等”),若实验操作均正确,则所求
中和热______________(填“相等”、“不相等”)。
(4)50mL 0.55mol/L NaOH溶液和50mL 0.25mol/L硫酸溶液的实验数据如表,请填写表中的
空白。
温度 起始温度t ℃ 终止温度 温度差平均值
1
t /℃
实验次数 2 (t ﹣t )/℃
H SO NaOH 平均值 2 1
2 4
1 26.2 26.0 26.1 29.5 ______
2 27.0 27.4 27.2 32.3 ①
3 25.9 25.9 25.9 29.2
4 26.4 26.2 26.3 29.8
近似认为50mL 0.55mol/L NaOH溶液和50mL 0.25mol/L硫酸溶液的密度都是1g/cm3,中和
②后生成溶液的比热容c=4.18J/(g•℃)。则中和热△H=_____________kJ/mol(取小数点后一
位)。
上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是_______________(填字母)。
③a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H SO 溶液的温度
2 4
【答案】(1)环形玻璃搅拌棒;
(2)隔热,减少热量的损失;
(3)不相等;相等;
(4) 3.4; ﹣56.8; acd。
【解析①】(1)②由量热计的③构造可知该装置的缺少仪器是环形玻璃搅拌器,故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中
的热量损失,
故答案为:隔热,减少热量的损失;
(3)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol•L﹣1H SO 溶液跟
2 4
50mL0.55mol•L﹣1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,
但是中和热的均是强酸和强碱反应生成1mol水时放出的热,中和热相等;
故答案为:不相等;相等;
(4) 第一次测定温度差为:(29.5﹣26.1)℃=3.4℃,
第二次①测定的温度差为:(32.3﹣27.2)℃=5.1℃,
第三次测定的温度差为:(29.2﹣25.9)℃=3.3℃,
第三次测定的温度差为:(29.8﹣26.3)℃=3.5℃,
其中第二次的温度差误差较大,应该舍弃,其它三次温度差的平均值为 (3.4+3.3+3.5)℃=
3.4℃,
故答案为:3.4;
50mL0.55mol/L氢氧化钠溶液与50mL0.25mol/L硫酸溶液进行中和反应,生成水的物质的量为
②0.05L×0.50mol/L=0.025mol,溶液的质量为:100mL×1g/cm3=100g,温度差为△T=3.4℃,则生成
0.025mol水放出的热量Q=m•c•△T=100g×4.18J/(g•℃)×3.4℃=1421.2J=1.4212KJ,所以实验
测得的中和热△H=﹣ =﹣56.8 kJ/mol,
故答案为:﹣56.8;
a.实验装置保温、隔热效果差,使热量散失多,测定结果偏小,故a正确;
③b.量取NaOH溶液的体积时仰视读数,使量取的NaOH溶液体积偏大,反应放热增多,测定结果
偏大,故b错误;
c.尽量一次快速将NaOH溶液倒入盛有硫酸的小烧杯中,分多次把NaOH溶液倒入盛有硫酸的小
烧杯中,会导致较多热量散失,测定结果偏小,故c正确;
d.用温度计测定NaOH溶液起始温度后后直接测定H SO 溶液的温度,使温度差偏小,测定结果
2 4
偏小,故d正确;故答案为:acd。
27.(10分)研究化学反应时,既要关注物质变化,又要关注能量变化。请回答以下问题。
(1)氢气在氧气中燃烧,破坏1mol H﹣H键吸收Q kJ的热量,破坏1mol O=O键吸收Q kJ的
1 2
热量,形成1mol H﹣O键释放Q kJ的热量,则下列关系式正确的是_____。(填字母序号)
3
A.2Q +Q >4Q B.Q +Q <Q
1 2 3 1 2 3C.Q +Q <4Q D.2Q +Q =4Q
1 2 3 1 2 3
(2)用CH 催化还原氮氧化物可以消除氮氧化物的污染。
4
已知: 2N (g)+CO (g)+2H O(g)═CH (g)+4NO(g)△H =akJ/mol
2 2 2 4 1
CH
4
(①g)+4NO
2
(g)═4NO(g)+CO
2
(g)+2H
2
O(g)△H
2
=bkJ/mol
②H
2
O(1)═H
2
O(g)△H
3
=ckJ/mol
③则CH
4
(g)+2NO
2
(g)═N
2
(g)+CO
2
(g)+2H
2
O(1)△H=kJ/mol_____。(用含a、b、c
的代数式表示)
(3)红磷P(s)和Cl (g)发生反应生成PCl (g)和PCl (g),反应过程中的热量关系如图
2 3 5
所示(图中的△H表示生成1mol产物的数据)。根据如图回答下列问题:
写出P(s)和Cl (g)反应生成PCl (g)的热化学方程式_____。
2 5
①已知:常温时红磷比白磷稳定,比较下列反应中△H的大小:△H
1
_____△H
2
.(填“>”、
②“<”或“=”)
ⅰ.P (白磷,s)+5O (g)=2P O (s)△H <0
4 2 2 5 1
ⅱ.4P(红磷,s)+5O (g)=2P O (s)△H <0
2 2 5 2
【答案】(1)C;
(2) (b﹣a)﹣2c;
(3) P(s)+ Cl (g)=PCl (g)△H=﹣399kJ/mol; <。
2 5
【解析①】(1)氢气燃烧的反应为2H (g)+O (g)=2H O②(1),其焓变△H=反应物的总键能
2 2 2
﹣生成物的总键能=(2Q +Q ﹣4Q )kJ/mol,由于氢气在氧气中燃烧是放热反应,则2Q +Q ﹣
1 2 3 1 2
4Q <0,即Q +Q <2Q +Q <4Q ,故C正确,
3 1 2 1 2 3
故答案为:C;
(2) 2N (g)+CO (g)+2H O(g)═CH (g)+4NO(g)△H =akJ/mol
2 2 2 4 1
CH①4 (g)+4NO
2
(g)═4NO(g)+CO
2
(g)+2H
2
O(g)△H
2
=bkJ/mol
②H
2
O(1)═H
2
O(g)△H
3
=ckJ/mol
③据盖斯定律( ﹣ )× ﹣ ×2计算CH (g)+2NO (g)═N (g)+CO (g)+2H O(1)的
4 2 2 2 2
② ① ③
△H=[ (b﹣a)﹣2c]kJ/mol,
故答案为: (b﹣a)﹣2c;
(3) P(s)和Cl (g)反应生成PCl (g)的化学方程式为P(s)+ Cl (g)=PCl (g),由
2 5 2 5
①
图可知,该反应分两步完成,焓变△H=△H +△H =﹣399kJ/mol,即热化学方程式为P(s)+
1 2
Cl (g)=PCl (g)△H=﹣399kJ/mol,
2 5
故答案为:P(s)+ Cl (g)=PCl (g)△H=﹣399kJ/mol;
2 5
常温时红磷比白磷稳定,则白磷的具有的能量高,即4P(s)=P (s)△H>0,
4
②ⅰ.P
4
(白磷,s)+5O
2
(g)=2P
2
O
5
(s)△H
1
<0
ⅱ.4P(红磷,s)+5O (g)=2P O (s)△H <0
2 2 5 2
根据盖斯定律:反应ii﹣i得到△H=△H ﹣△H >0,所以△H <△H ,
2 1 1 2
故答案为:<。