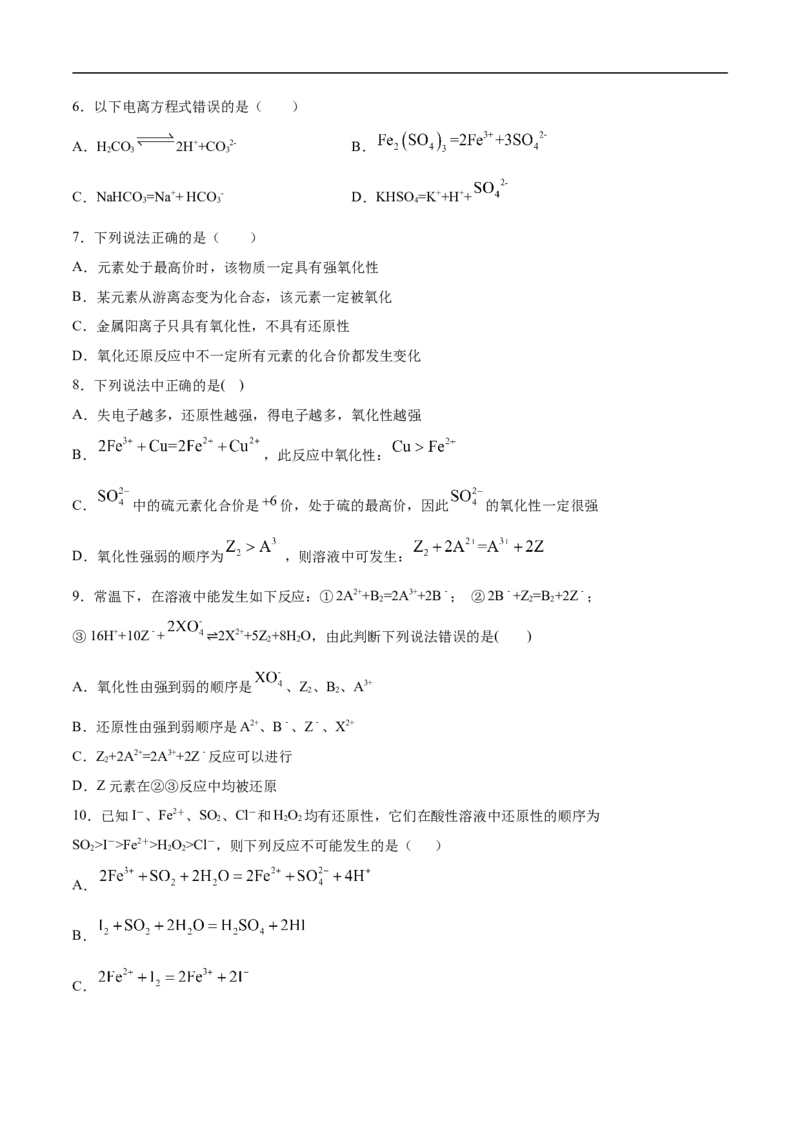文档内容
第一章 物质及其变化
过关测试 提高卷
(时间:90分钟)
一、选择题(每小题3分,共54分)
1.纳米是长度单位,1纳米等于1×10-9m,物质的颗粒达到纳米级时,具有特殊的性质。例如将单质铜制
成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧。下列对“纳米铜"的有关叙述正确的是(
)
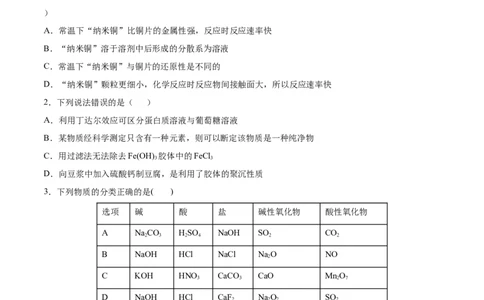
A.常温下“纳米铜”比铜片的金属性强,反应时反应速率快
B.“纳米铜”溶于溶剂中后形成的分散系为溶液
C.常温下“纳米铜”与铜片的还原性是不同的
D.“纳米铜”颗粒更细小,化学反应时反应物间接触面大,所以反应速率快
2.下列说法错误的是( )
A.利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液
B.某物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物
C.用过滤法无法除去Fe(OH) 胶体中的FeCl
3 3
D.向豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质
3.下列物质的分类正确的是( )
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A NaCO HSO NaOH SO CO
2 3 2 4 2 2
B NaOH HCl NaCl NaO NO
2
C KOH HNO CaCO CaO MnO
3 3 2 7
D NaOH HCl CaF NaO SO
2 2 2 2
4.下列变化,只有加入酸才能一步实现的是( )
A.Zn→ZnSO B.CaCO →CO C.MgO→MgCl D.BaCl →BaSO
4 3 2 2 2 4
5.下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为( )
A.纯盐酸、氨气、硫酸、干冰
B.蒸馏水、氨水、碳酸氢钠、二氧化硫
C.胆矾、盐酸、铁、碳酸钙
D.生石灰、漂白粉、氯化铜、碳酸钠6.以下电离方程式错误的是( )
A.HCO 2H++CO 2- B.
2 3 3
C.NaHCO =Na++ HCO - D.KHSO=K++H++
3 3 4
7.下列说法正确的是( )
A.元素处于最高价时,该物质一定具有强氧化性
B.某元素从游离态变为化合态,该元素一定被氧化
C.金属阳离子只具有氧化性,不具有还原性
D.氧化还原反应中不一定所有元素的化合价都发生变化
8.下列说法中正确的是( )
A.失电子越多,还原性越强,得电子越多,氧化性越强
B. ,此反应中氧化性:
C. 中的硫元素化合价是 价,处于硫的最高价,因此 的氧化性一定很强
D.氧化性强弱的顺序为 ,则溶液中可发生:
9.常温下,在溶液中能发生如下反应:①2A2++B =2A3++2B﹣; ②2B﹣+Z=B +2Z﹣;
2 2 2
③16H++10Z﹣+ 2X2++5Z+8H O,由此判断下列说法错误的是( )
2 2
⇌
A.氧化性由强到弱的顺序是 、Z、B 、A3+
2 2
B.还原性由强到弱顺序是A2+、B﹣、Z﹣、X2+
C.Z+2A2+=2A3++2Z﹣反应可以进行
2
D.Z元素在②③反应中均被还原
10.已知I-、Fe2+、SO 、Cl-和HO 均有还原性,它们在酸性溶液中还原性的顺序为
2 2 2
SO >I->Fe2+>H O>Cl-,则下列反应不可能发生的是( )
2 2 2
A.
B.
C.D.
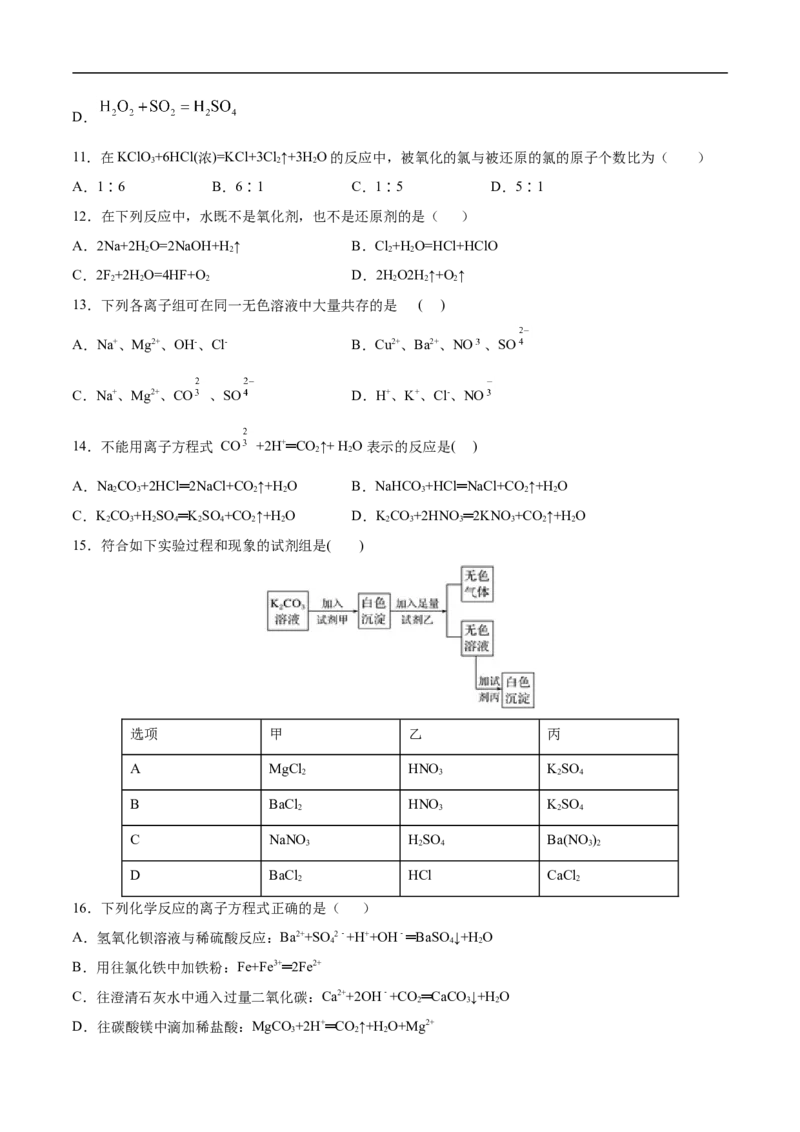
11.在KClO+6HCl(浓)=KCl+3Cl ↑+3H O的反应中,被氧化的氯与被还原的氯的原子个数比为( )
3 2 2
A.1∶6 B.6∶1 C.1∶5 D.5∶1
12.在下列反应中,水既不是氧化剂,也不是还原剂的是( )
A.2Na+2HO=2NaOH+H ↑ B.Cl+H O=HCl+HClO
2 2 2 2
C.2F+2H O=4HF+O D.2HO2H ↑+O ↑
2 2 2 2 2 2
13.下列各离子组可在同一无色溶液中大量共存的是 ( )
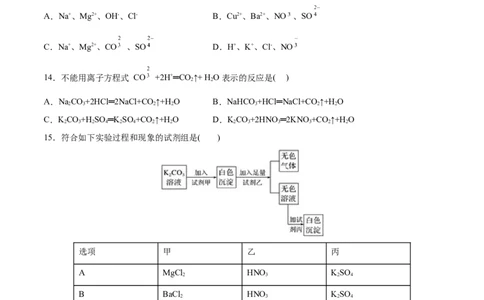
A.Na+、Mg2+、OH-、Cl- B.Cu2+、Ba2+、NO 、SO
C.Na+、Mg2+、CO 、SO D.H+、K+、Cl-、NO
14.不能用离子方程式 CO +2H+═CO ↑+ H O 表示的反应是( )
2 2
A.NaCO+2HCl═2NaCl+CO ↑+H O B.NaHCO +HCl═NaCl+CO ↑+H O
2 3 2 2 3 2 2
C.KCO+H SO ═K SO +CO ↑+H O D.KCO+2HNO ═2KNO+CO ↑+H O
2 3 2 4 2 4 2 2 2 3 3 3 2 2
15.符合如下实验过程和现象的试剂组是( )
选项 甲 乙 丙
A MgCl HNO KSO
2 3 2 4
B BaCl HNO KSO
2 3 2 4
C NaNO HSO Ba(NO )
3 2 4 3 2
D BaCl HCl CaCl
2 2
16.下列化学反应的离子方程式正确的是( )
A.氢氧化钡溶液与稀硫酸反应:Ba2++SO2﹣+H++OH﹣═BaSO ↓+H O
4 4 2
B.用往氯化铁中加铁粉:Fe+Fe3+═2Fe2+
C.往澄清石灰水中通入过量二氧化碳:Ca2++2OH﹣+CO ═CaCO↓+H O
2 3 2
D.往碳酸镁中滴加稀盐酸:MgCO +2H+═CO ↑+H O+Mg2+
3 2 217.下列反应的离子方程式正确的是( )
A.大理石溶于醋酸溶液中:CaCO +2H+===Ca2++CO ↑+H O
3 2 2
B.往硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO2-===BaSO ↓+Cu(OH) ↓
4 4 2
C.用FeCl 溶液腐蚀印刷电路板:Fe3++Cu===Fe2++Cu2+
3
D.铁与稀盐酸反应:2Fe+6H+===2Fe3++3H ↑
2
18.溶液中只存在五种离子,各离子个数比为:Cl-∶SO 2-∶Fe3+∶K+∶M=2∶3∶1∶3∶1,(不考虑水的
4
电离),则M为( )
A.CO2- B.Mg2+ C.Na+ D.Ba2+
3
二、非选择题(共46分)
19.(10分)现有下列10种物质:①铝,②纯醋酸,③CO,④HSO ,⑤Ba(OH) ,⑥红褐色的氢氧化
2 2 4 2
铁胶体,⑦稀盐酸,⑧NaHSO,⑨碳酸钙,⑩乙醇
4
(1)上述物质中属于电解质的有_______,属于非电解质的有_____(填序号)。
(2)向⑥中逐渐滴加④的溶液,看到的现象是_______。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=HO,则该反应的化学方程
2
式为____。
(4)⑧在水中的电离方程式为________。
(5)⑨和⑦混合,反应的离子方程式为_____。
20.(8分)取少量 Fe O 粉末( 红棕色) 加入适量盐酸, 得到黄色溶液, 用此溶液进行以下实验:
2 3
(1)在小烧杯中加入 20mL 蒸馏水, 加热至沸腾后, 向沸水中加入制取的黄色溶液 2mL, 继续煮沸至液
体呈______色, 停止加热, 用激光笔照射烧杯中的液体, 可以观察到液体中______, 用这个实验可以区
别_______和_______。
(2)氢氧化铁胶体制备的原理_______________________________
(3)向烧杯中逐滴加入过量的盐酸, 会出现一系列变化:现象____________________原因
( 用离子方程式表示)__________________________
(4)氢氧化铁胶体稳定存在的主要原因是______________________________________。
21.(8分)在工业上次磷酸(H PO )常用于化学镀银,发生的反应如下:____Ag+
3 2
+___H PO +___H O→____Ag↓+____H PO +___H+
3 2 2 3 4
请回答下列问题:
(1)HPO 中,P元素的化合价为___;该反应中,HPO 被___(填“氧化”或“还原”)。
3 2 3 2
(2)配平该离子方程式:__Ag++__HPO +__HO→__Ag↓+__HPO +__H+。
3 2 2 3 4
(3)若反应中生成1.08gAg,则转移的电子数为___。(4)HPO 是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:__。
3 2
22.(12分)氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:
①Ⅰ中发生反应的离子方程式为__________________________________;
②Ⅱ中铜丝上观察到的现象是___________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:
2KNO+3C+S===KS+N↑+3CO↑。其中氧化产物是________
3 2 2 2
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成
Fe2+,有利于人体吸收,说明维生素C具有_______(填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化
成亚铁盐。此反应的化学方程式为________________________________________________
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。
________________________________________________
23.(8分)有一包白色固体粉末,其中可能含有NaCl、Ba(NO )、CuSO 、NaCO 中的一种或几种,现
3 2 4 2 3
做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的滤液加入足量AgNO 溶液,产生白色沉淀。
3
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是________,一定不含有的物质是________,可能含有的物质是________。
(写化学式)
(2)过滤时需要用的玻璃仪器有________、________、________。
(3)写出对应各步反应的离子方程式:
②________________________________________________________________________;
③________________________________________________________________________。