文档内容
第一章 化学反应的热效应知识清单
考点1 反应热 焓变
一、反应热及其测定
1.体系(系统)及环境--以研究盐酸与NaOH溶液的反应为例
2.反应热
(1)含义:在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反
应热。
(2)测定方法:利用量热计直接测定。
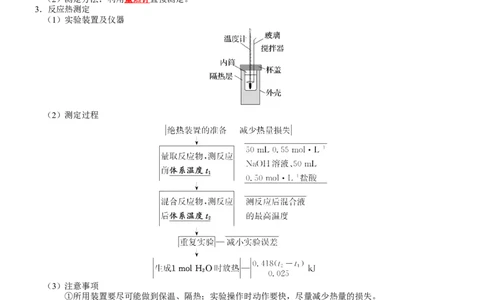
3.反应热测定
(1)实验装置及仪器
(2)测定过程
(3)注意事项
①所用装置要尽可能做到保温、隔热;实验操作时动作要快,尽量减少热量的损失。
②用溶液的配制必须准确,且浓度要小;为了保证酸完全中和,常采用碱稍过量的方法。
③实验中所用的盐酸和氢氧化钠溶液配好后要充分冷却至室温,才能使用。
④要使用同一支温度计,温度计读数要尽可能准确;水银球部位一定要完全浸没在溶液中,且要稳定一
段时间后再读数,以提高测量的精度;两次读数的时间间隔要短,这样才能读到最高温度,即最终温度。
⑤实验中若用弱酸(碱)代替强酸(碱),因中和过程中弱酸或弱碱的电离吸热,会使测得的反应热数
值的绝对值偏小。
⑥可采用多次测量取平均值的方法,减小实验误差。
(4)结论
25℃和101kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1mol HO时,放出57.3kJ 的热量。
2
二、反应热与焓变
1.产生反应热的原因:化学反应前后体系的内能发生了变化。
2.内能、焓、焓变
(1)内能(符号为U):体系内物质的各种能量的总和,受温度、压强和物质的聚集状态等影响。
(2)焓(符号为H):与内能有关的物理量。
(3)焓变:在等压条件下进行的化学反应,其反应热等于反应的焓变。①符号:ΔH。
②单位:kJ/mol(或 kJ · mol - 1 )。
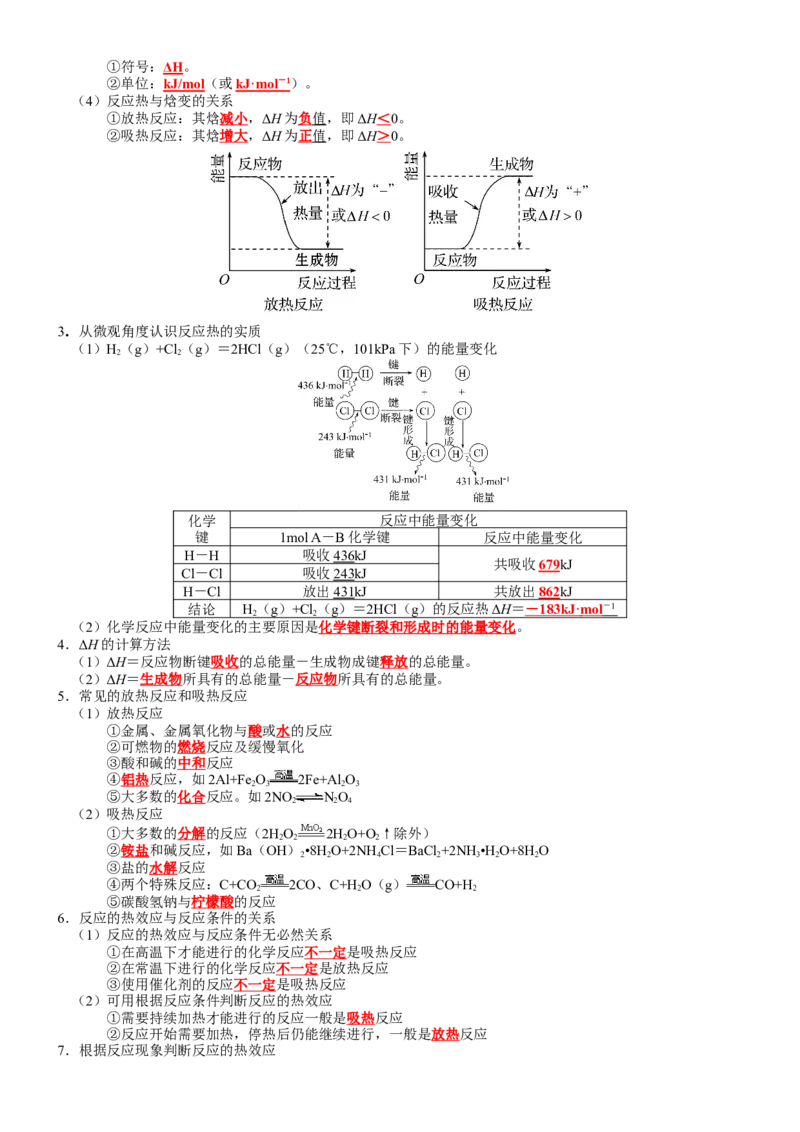
(4)反应热与焓变的关系
①放热反应:其焓减小,ΔH为 负 值 ,即ΔH<0。
②吸热反应:其焓增大,ΔH为 正 值 ,即ΔH>0。
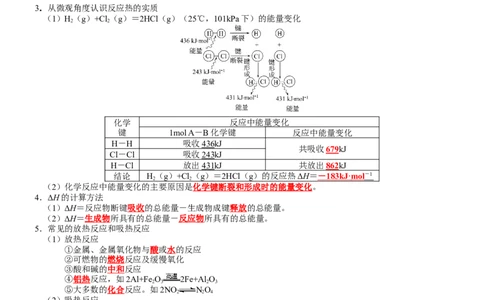
3.从微观角度认识反应热的实质
(1)H(g)+Cl(g)=2HCl(g)(25℃,101kPa下)的能量变化
2 2
化学 反应中能量变化
键 1mol A-B化学键 反应中能量变化
H-H 吸收436kJ
共吸收679kJ
Cl-Cl 吸收243kJ
H-Cl 放出431kJ 共放出862kJ
结论 H(g)+Cl(g)=2HCl(g)的反应热ΔH= - 183k J · mo l - 1
2 2
(2)化学反应中能量变化的主要原因是化学键断裂和形成时的能量变化。
4.ΔH的计算方法
(1)ΔH=反应物断键吸收的总能量-生成物成键释放的总能量。
(2)ΔH=生成物所具有的总能量-反应物所具有的总能量。
5.常见的放热反应和吸热反应
(1)放热反应
①金属、金属氧化物与酸或水的反应
②可燃物的燃烧反应及缓慢氧化
③酸和碱的中和反应
④铝热反应,如2Al+Fe O 2Fe+Al O
2 3 2 3
⑤大多数的化合反应。如2NO NO
2 2 4
(2)吸热反应
①大多数的分解的反应(2HO 2HO+O↑除外)
2 2 2 2
②铵盐和碱反应,如Ba(OH)•8H O+2NH Cl=BaCl +2NH•H O+8HO
2 2 4 2 3 2 2
③盐的水解反应
④两个特殊反应:C+CO 2CO、C+HO(g) CO+H
2 2 2
⑤碳酸氢钠与柠檬酸的反应
6.反应的热效应与反应条件的关系
(1)反应的热效应与反应条件无必然关系
①在高温下才能进行的化学反应不一定是吸热反应
②在常温下进行的化学反应不一定是放热反应
③使用催化剂的反应不一定是吸热反应
(2)可用根据反应条件判断反应的热效应
①需要持续加热才能进行的反应一般是吸热反应
②反应开始需要加热,停热后仍能继续进行,一般是放热反应
7.根据反应现象判断反应的热效应(1)反应体系的温度变化
①体系的温度升高:放热反应
②体系的温度降低:吸热反应
(2)密闭体系的压强变化
①体系的压强增大:放热反应
②体系的压强减小:吸热反应
(3)液体的挥发程度
①液体的挥发程度增大:放热反应
②液体的挥发程度减小:吸热反应
(4)催化剂的红热程度
①停热后催化剂继续红热:放热反应
②停热后催化剂不再红热:吸热反应
考点2 热化学方程式
一、热化学方程式
1.概念:表明反应所释放或吸收的热量的化学方程式。
2.热化学方程式中各量的含义
(1)化学计量数
①含义:只表示物质的量,不表示分子个数
②特点:可以是整数也可以是分数
(2)热化学方程式的意义:
① 2 mol A ( g )和 1 mol B ( g ) 完全反应 生成 3 mol C ( g ) 时释放 a kJ 的热量 。
2A(g)+B(g) 3C(g) △H=-akJ·mol-1
② 25℃ 、 101kPa 下, 1mol 气态 H 与 0.5mo l 气态 O 反应生成 1mo l 液态 H O 时,放出的热量是
2 2 2
285.8kJ 。
1
H(g)+2O(g)=HO(l)ΔH=-285.8kJ·mol-1
2 2 2
(3)热化学方程式中的△H
①△H=-akJ·mol-1中mol-1的含义:每摩尔反应
②单位: kJ · mol - 1 ,与化学计量数无关
③正负:正逆反应的数值相等,符号相反
3.热化学方程式的正误判断
(1)注意标明物质的聚集状态:方程式中每种物质的化学式后面用括号注明物质的聚集状态(g、l、s),
不用标“↑”或“↓”,水溶液用aq表示。
(2)注意注明必要的反应条件:焓变与温度等测定条件有关,所以书写时必须在ΔH后指明反应的温度
(298K时可不注明)。
(3)注意明确化学计量数的含义:化学计量数只表示该物质的物质的量,不表示分子个数或原子个数,因此
热化学方程式中化学计量数也可以是分数。
(4)注意ΔH的单位及符号:ΔH的单位是J·mol-1或kJ·mol-1,ΔH只能写在化学方程式的右边,表示正向
反应的焓变。ΔH<0表示为放热反应;ΔH>0表示为吸热反应。
(5)注意同一反应中化学计量数与ΔH数值的对应关系:化学方程式中各物质的化学计量数加倍,则 ΔH数
值的绝对值也加倍;若反应逆向进行,则ΔH的数值改变符号,但绝对值不变。
4.热化学方程式的书写方法
5.根据已知信息书写热化学方程式的方法思路
(1)根据题目给出的信息,确定反应物和生成物,写出化学方程式,并标明各物质的状态。
(2)根据题中一定量反应物(或生成物)反应(或生成)时对应的热量变化,求出 1mol反应物(或生成
物)反应(或生成)时对应的热量变化,标明该反应的ΔH。
(3)注意特殊要求。如表示中和热的热化学方程式中生成物HO(l)的化学计量数必须是1。
2
二、燃烧热
1.概念:在25℃、101kPa时,1mol 纯物质完全燃烧生成指定产物时所放出的热量。
(1)反应条件:25℃和101kPa(2)可燃物用量:1mol
(3)完全燃烧生成指定产物:指单质或化合物燃烧后变为最稳定的物质。
元素 C H S N
产物 CO ( g ) H O ( l ) SO ( g ) N ( g )
2 2 2 2
(4)ΔH:放热反应,ΔH均为负值
(5)单位: kJ · mol - 1
2.意义:甲烷的燃烧热为ΔH=-890.3kJ·mol-1,它表 示 2 5 ℃ 、 101kPa 时, 1molCH 完全燃烧生成 CO ( g )
4 2
和液态 H O 时放出 890.3kJ 的热量 。
2
3.表示燃烧热的热化学方程式的书写
(1)要求:以燃烧1mol 物质为标准来配平其余物质的化学计量数。
(2)实例:表示C H 的燃烧热的热化学方程式
8 18
25
①正确:CH ( l ) + 2 O ( g ) = 8CO ( g ) +9H O ( l ) Δ H =- 5 518kJ · mol - 1
8 18 2 2 2
②错误:2C H (l)+25O (g)=16CO(g)+18H O(l)ΔH=-11 036kJ·mol-1。
8 18 2 2 2
考点3 盖斯定律及其应用
一、盖斯定律
1.内容:一个化学反应,不管是一步完成还是分几步完成,其反应热是相同的。
2.特点
(1)在一定条件下,化学反应的反应热只与反应体系的 始态 和 终态 有关,而与反应的途径无关。
(2)反应热总值一定,如图表示始态到终态的反应热。
则ΔH= Δ H +Δ H = Δ H +Δ H +Δ H 。
1 2 3 4 5
3.应用:可以间接计算以下情况的反应热
(1)反应进行得很慢的反应;
(2)不容易直接发生的反应;
(3)伴有副反应发生的反应。
二、反应热的计算
1.根据热化学方程式计算
(1)化学计量数∶│⊿H│=反应的物质的量∶热量(Q)
(2)n(A) ∶n(B) ∶n(C) ∶n(D) ∶Q=a∶b∶c∶d∶ │ ⊿ H │
反应 反应 生成 生成
2.根据反应物和生成物的总能量计算
(1)△H=生成物的能量和-反应物的能量和
(2)△H=生成物的相对能量和-反应物的相对能量和
3.根据键能计算焓变
(1)△H=反应物的键能和-生成物的键能和
(2)计算关键:弄清物质中化学键的数目
①常见分子:根据成键原则画出结构式即可判断
分子
Cl O N HO
式 2 2 2 2
结构
Cl-Cl O=O N≡N H-O-H
式
分子
HO CO HCN NH
式 2 2 2 3
结构
H-O-O-H O=C=O H-C≡N
式
分子
CH C H C H NH
式 4 2 4 2 6 2 4结构
式
②信息分子:根据分子结构示意图数共价键个数
物质 硫化磷 雄黄(As S) PO
4 4 4 10
结构
12 个P-S键 2 个As-As键 4 个P=O键
键数
2 个P=S键 8 个S-As键 12 个P-O键
物质 S 单质 N 分子 PO
8 4 4 6
结构
键数 8 个S-S键 8 个N-N键 12 个P-O键
③特殊物质:选修物质结构内容
物质/mol 白磷 金刚石 晶体硅 SiO 石墨
2
结构
键数/mol 6 2 2 4 1.5
4.根据燃烧热和热值计算
(1)根据燃烧热计算:Q(放)= n (可燃物) × | 燃烧热 |
(2)根据热值计算:Q(放)= m (可燃物) × | 热值 |
4.计算燃烧热、热值、中和热
(1)计算燃烧热:H =- kJ/mol
燃烧热
(2)计算热值:H =- kJ/g
热值
(3)计算中和热:H =- kJ/mol
中和热
5.根据比热公式进行计算:Q= cm ΔT 。
(1)水的比热容:c=4.18×10-3kJ/(g·℃)
(2)m代表液体或混合液的总质量
(3)ΔT表示反应前后温度的变化值,ΔT=T - T
2 1
6.虚拟路径法:若反应物A变为生成物D,可以有两个途径:
(1)由A直接变成D,反应热为ΔH;
(2)由A经过B变成C,再由C变成D,每步的反应热分别为ΔH、ΔH、ΔH,如图所示:
1 2 3
则有ΔH=ΔH+ΔH+ΔH。
1 2 3
7.加和法进行计算
(1)计算步骤(2)ΔH与书写方式的关系
①正逆反应的△H、K的关系:△H
正
+△H
逆
=0,K
正
·K
逆
=1
②化学计量数变成n倍,△H变为n 倍,K变为 n 次方 倍
③反应③=反应①+反应②,则:△H= △ H + △ H ,K =K · K
3 1 2 3 1 2
④反应③=反应①-反应②,则:△H= △ H - △ H ,K =
3 1 2 3
1 1
⑤反应③=a×反应①-b ×反应②,则:△H=a△ H -b △ H ,K =
3 1 2 3
(3)反应举例
①A+B=C+D ⊿H
1
②2E+F=2C ⊿H
2
③3D=M+2N ⊿H
3
则:6A+6B=6E+3F+ 2M+4N △H= 6 △ H - 3△ H + 2 △ H
1 2 3
8.根据图像计算
考点4 反应热大小比较
1.与“符号”相关的反应热比较
(1)对于放热反应来说,ΔH=-QkJ·mol-1,虽然“-”仅表示放热的意思
(2)比较ΔH大小时要将其看成真正意义上的“负号”,即放热越多,ΔH反而越小。
2.与“化学计量数”相关的反应热比较
(1)“化学计量数”越大,反应释放或吸收的热量越多
(2)例如:a<b,ΔH>ΔH
1 2
1
①H(g)+2O(g)=HO(l) ΔH=-akJ·mol-1
2 2 2 1
②2H(g)+O (g)=2HO(l) ΔH=-bkJ·mol-1
2 2 2 2
3.与“物质聚集状态”相关的反应热比较
(1)同一反应,生成物状态不同时:
①A(g)+B(g)=C(g)ΔH<0
1
②A(g)+B(g)=C(l)ΔH<0
2
③因为C(g)=C(l)ΔH<0
3
则ΔH= Δ H - Δ H ,所以ΔH<ΔH。
3 2 1 2 1
(2)同一反应,反应物状态不同时
①S(g)+O (g)=SO (g)ΔH<0
2 2 1
②S(s)+O (g)=SO (g)ΔH<0
2 2 2③设计如下途径:
则ΔH= Δ H - Δ H ,因ΔH<0,所以ΔH<ΔH。。
3 1 2 3 1 2
4.与“同素异形体”相关的反应热比较
(1)C(石墨,s)+O (g)=CO(g)ΔH
2 2 1
(2)C(金刚石,s)+O (g)=CO(g)ΔH
2 2 2
(3)因为C(石墨,s)=C(金刚石,s)ΔH>0,所以ΔH>ΔH。
1 2
5.与“反应进行程度”相关的反应热比较
(1)对于燃烧反应,燃烧越充分放出的热量就越多,ΔH越小。
①2C(s)+O (g)=2CO(g)ΔH
2 1
②2C(s)+2O (g)=2CO(g)ΔH
2 2 2
③ΔH>ΔH
1 2
(2)对于可逆反应,
①放热反应:反应正向进行的程度越大,则反应放出的热量就越多。
②吸热反应:反应正向进行的程度越大,则反应吸收的热量就越多。