文档内容
第 19 讲 盐类的水解
知识导航
小杨老师 15521324728 侵权必究
课前引入
NaCO 、俗名 “苏打”,又称为“纯碱”,你还记得它
2 3
的性质吗?
NaCO 的水溶液呈碱性,可用于生活洗涤。
2 3
NaCO 的水溶液为什么呈碱性?
2 3 杨sir化学,侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、盐溶液的酸碱性
实验探究——盐溶液的酸碱性盐溶液 NaCl NaCO NHCl KNO CHCOONa (NH)SO
2 3 4 3 3 4 2 4
酸碱性
盐的类型
【答案】中性 碱性 酸性 中性 碱性 酸性
强酸强碱盐 强碱弱酸盐 强酸弱碱盐 强酸强碱盐 强碱弱酸盐 强酸弱碱盐
盐溶液呈酸碱性的原因分析
杨sir化学,侵权必究
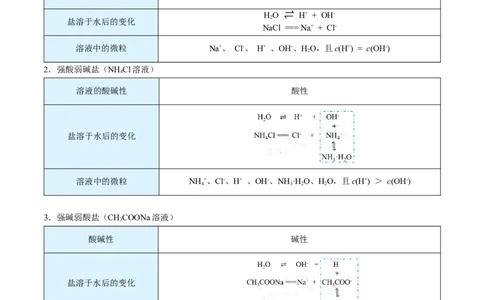
1. 强酸强碱盐(NaCl溶液)
溶液的酸碱性 中性
HO ⇌ H+ + OH-
2
盐溶于水后的变化
NaCl === Na+ + Cl-
溶液中的微粒 Na+、 Cl-、 H+ 、OH-、HO,且c(H+) = c(OH-)
2
2.强酸弱碱盐(NH Cl溶液)
4
溶液的酸碱性 酸性
盐溶于水后的变化
溶液中的微粒 NH +、Cl-、H+ 、OH-、NH ·HO、HO,且c(H+) > c(OH-)
4 3 2 2
3.强碱弱酸盐(CHCOONa溶液)
3
酸碱性 碱性
盐溶于水后的变化
溶液中的微粒 Na+、 CHCOO-、 H+ 、OH-、CHCOOH、HO,且c(H+) < c(OH-)
3 3 2
二、盐类水解的原理及规律
1.定义:在溶液中,盐电离出来的离子跟水电离产生的H+或OH-结合生成____________的反应。
杨sir化学,侵权必究
2. 实质:生成弱酸或弱碱,破坏了水的电离平衡,使得水的电离平衡________,电离程度________,即盐
类的水解________水的电离。
【答案】弱电解质 右移 增大 促进3. 盐类水解的特点
4. 水解规律
有弱才水解;越弱越水解;谁强显谁性;同强显中性;同弱双水解。
杨sir化学,侵权必究
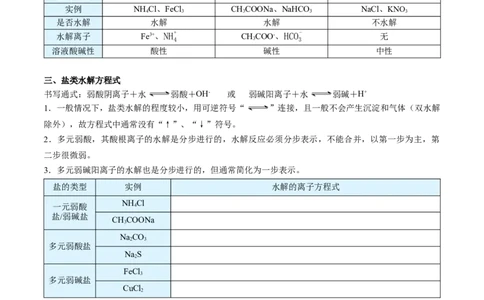
盐的类型 强酸弱碱盐 强碱弱酸盐 强酸强碱盐
实例 NH Cl、FeCl CHCOONa、NaHCO NaCl、KNO
4 3 3 3 3
是否水解 水解 水解 不水解
水解离子
Fe3+、NH+ CHCOO-、HCO-
无
4 3 3
溶液酸碱性 酸性 碱性 中性
三、盐类水解方程式
书写通式:弱酸阴离子+水 弱酸+OH- 或 弱碱阳离子+水 弱碱+H+
1.一般情况下,盐类水解的程度较小,用可逆符号“ ”连接,且一般不会产生沉淀和气体(双水解
除外),故方程式中通常没有“↑”、“↓”符号。
2.多元弱酸,其酸根离子的水解是分步进行的,水解反应必须分步表示,不能合并,以第一步为主,第
二步很微弱。
杨sir化学,侵权必究
3.多元弱碱阳离子的水解也是分步进行的,但通常简化为一步表示。
盐的类型 实例 水解的离子方程式
NH Cl
一元弱酸 4
盐/弱碱盐
CHCOONa
3
NaCO
2 3
多元弱酸盐
NaS
2
FeCl
3
多元弱碱盐
CuCl
2
【答案】 + HO NH ·H O + H+
NH+ 2 ⇌ 3 2
4
CHCOO- + HO ⇌ CHCOOH + OH-
3 2 3
+ HO + OH- ; + HO HCO + OH-
CO2- 2 ⇌ HCO- HCO- 2 ⇌ 2 3
3 3 3
S2- + HO ⇌ HS- + OH- ;HS- + HO ⇌ HS + OH-
2 2 2
Fe3+ + 3HO ⇌ Fe(OH) + 3H+
2 3
Cu2+ + 2HO ⇌ Cu(OH) + 2H+
2 24.双水解:弱酸阴离子与弱碱阳离子相互促进水解,水解程度较大,绝大多数能进行到底,书写时要用
“===”、“↑”、“↓”。
如 Fe3+ 与 :2Fe3+ + 3 + 3H O ===== 2Fe(OH)↓+ 3CO↑
CO2- CO2- 2 3 2 杨sir化学,侵权必究
3 3
对点训练
小杨老师 15521324728 侵权必究
题型一:盐类水解的概念理解
杨sir化学,侵权必究
【例1】下列关于盐类水解反应说法正确的是
A.任何盐都可发生水解反应
B.盐只能发生水解反应而不能发生其他反应
C.盐水解反应肯定能破坏水的电离平衡且促进水的电离
D.盐的水溶液为中性时,则盐一定不发生水解反应
【答案】C
【详解】
A.由弱酸或弱碱形成的盐才可发生水解反应,错误;
B.水解只是某些盐的性质,错误;
C.盐水解反应肯定能破坏水的电离平衡且促进水的电离 ,正确;
D.盐的水溶液为中性时,有两种可能,一是强酸强碱盐不发生水解反应,二是弱酸弱碱盐,水解能力差
不多,错误;
答案选C。
题型二:判断盐溶液的酸碱性
杨sir化学,侵权必究
【例2】下列物质的水溶液因水解而呈碱性的是( )
A.NaCO B.AlCl C.Ca(OH) D.NaNO
2 3 3 2 3
【答案】A
【解析】A项,碳酸钠溶液中存在碳酸根的水解CO2-+H O HCO -+OH-,溶液显碱性,A符合题意;
3 2 3
B项,AlCl 溶液中存在Al3+的水解而显酸性,B不符合题意;C项,Ca(OH) 可以在水溶液中电离出OH-而
3 2
显碱性,与水解无关,C不符合题意;D项,NaNO 为强酸强碱盐,溶液显中性,D不符合题意;故选
3
A。
题型三:水解方程式的正误判断
杨sir化学,侵权必究
【例3】在一定条件下发生下列反应,其中属于盐类水解反应的是
A. +2HO NH ·H O+HO+
2 3 2 3B. +HO HO++
2 3
C.HS H++HS-
2
D.Cl+HO H++Cl-+HClO
2 2
【答案】A
【详解】
A. +2HO NH ·H O+HO+表示 结合水电离的氢氧根离子生成一水合氨,属于铵根的水解,
2 3 2 3
故A符合题意;
B. +H O HO++ 表示 在水溶液中的电离,故B不符题意;
2 3
C.HS H++HS-表示HS的一级电离,故C不符题意;
2 2
D.Cl+HO H++Cl-+HClO表示Cl 溶于水生成HCl和HClO,与盐的水解无关,故D不符题意;
2 2 2
故答案为A。
【变3-2】下列方程式正确的是
A. 的电离:
B. 的水解:
C. 的电离:
杨sir化学,侵权必究
D.向硫酸铝溶液中滴加碳酸钠溶液:
【答案】C
【详解】
A.醋酸铵是强电解质,在水溶液中完全电离,用等号连接,A错误;
B.亚硫酸氢根离子水解生成亚硫酸和氢氧根离子,B错误;
C.氯化铝是强电解质,上述电离方程式正确,C正确;
D.铝离子和碳酸根离子会发生双水解生成氢氧化铝沉淀和二氧化碳气体,D错误。
故选C。
题型四:离子共存(双水解)
杨sir化学,侵权必究
【变4】下列各组离子因发生相互促进的水解反应而不能大量共存的是
A.NH Al(SO ) 溶液中:Na+、Mg2+、HCO -、NO -
4 4 2 3 3
B.pH=1的溶液中:Fe2+、Al3+、NO -、Cl-
3
C.常温下,水电离出的c(H+)=1×10-12 mol·L-1的溶液中:Al3+、Ca2+、NO -、Cl-
3D.加入铝粉产生氢气的溶液中:Cu2+、NH +、HCO -、Br-
4 3
【答案】A
【详解】
A.NH Al(SO ) 溶液中,NH +和Al3+ 水解溶液呈酸性,HCO -水解呈碱性,因发生相互促进的水解反应
4 4 2 4 3
而不能大量共存,故A选;
B. pH=1的溶液中:Fe2+、H+、NO -发生氧化还原反应不能大量共存,故B不选;
3
C.常温下,水电离出的c(H+)=1×10-12 mol·L-1的溶液呈酸性或碱性,在酸性条件下Al3+、Ca2+、NO -、
3
Cl-能大量共存,故C不选;
D.加入铝粉产生氢气的溶液,呈强酸性或强碱性:Cu2+、NH +在碱性条件下不共存,HCO - 在酸性和碱
4 3
性条件下均不能大量共存,与相互促进的水解不能大量共存不符,故D不选;
故选A。
题型五:盐类水解综合
杨sir化学,侵权必究
【例5】向纯水中加入少量下列物质或改变下列条件,能促进水的电离,并能使溶液中c (OH-)>c (H+)的
平 平
操作是
①稀硫酸 ②金属钠 ③氨气 ④FeCl 固体 ⑤NaClO固体 ⑥将水加热煮沸
3
A.②⑤ B.①④ C.③④⑥ D.④
【答案】A
【详解】
使溶液中c (OH-)>c (H+),则溶液呈碱性,
平 平
①稀硫酸能抑制水的电离、溶液呈酸性,不符合;
②金属钠 能消耗水电离的氢离子,能促进水的电离,②符合;
③氨气溶于水呈碱性、但一水合氨电离出的氢氧根离子能抑制水的电离,不符合;
④FeCl 固体进入水中,铁离子能消耗水电离的氢氧根离子生成氢氧化铁,则促进水电离,即氯化铁水解、
3
溶液呈酸性,不符合;
⑤NaClO固体进入水中,次氯酸根离子能和氢离子结合生成次氯酸分子,即次氯酸钠水解促进水电离,溶
液呈碱性,符合;
⑥将水加热煮沸后还是水,呈中性,不符合;
答案选A。
【例7】现有浓度均为0.01 mol∙L−1的五种电解质溶液:①HNO;②NaCO;③NH Cl;
3 2 3 4
④CHCOONH;⑤NaOH。
3 4
(1)25℃时①的pH=_______。
(2)能够促进水的电离的有_______ (填编号)。
(3)所含离子种类最多的是_______ (填编号)。
(4)在上述溶液中分別加入AlCl 溶液,有一种物质能产生大量的气体,该反应的离子方程式为_______。
3
(5)这五种溶液的pH由小到大的顺序是_______(用编号表述)。【答案】2 ②③④ ② ①③④②⑤
【详解】
(1)25℃时0.01 mol∙L−1的HNO 的c(H+) =0.01 mol∙L−1,因此pH=2;故答案为:2。
3
(2)酸碱都是抑制水的电离,而要水解的盐会促进水的电离,因此能够促进水的电离的有②③④;故答案为:
②③④。
(3)①HNO 中含有三种离子;②NaCO 中含有五种离子;③NH Cl中含有四种离子;④CHCOONH 中含
3 2 3 4 3 4
有四种离子;⑤NaOH中含有三种离子;所含离子种类最多的是②;故答案为②。
(4)加入AlCl 溶液,有一种物质能产生大量的气体,该物质的碳酸钠,则反应的离子方程式为
3
;故答案为: 。
(5)①HNO,③NH Cl都显酸性,但酸电离的氢离子浓度大,酸性强,pH小,②NaCO,⑤NaOH都显碱
3 4 2 3
性,但强碱电离出的氢氧根浓度大,碱性强,pH大,④CHCOONH 显中性,因此这五种溶液的pH由小
3 4
到大的顺序是①③④②⑤;故答案为:①③④②⑤。
提分特训
小杨老师 15521324728 侵权必究
【题1】关于盐类水解反应的说法正确的是( )
A.溶液呈中性的盐一定是强酸强碱生成的盐
B.盐溶液的酸碱性主要决定于形成盐的酸、碱性的相对强弱
C.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同
3 4
D.除去CuCl 中的Fe3+,可以加入NaOH固体
2 杨sir化学,侵权必究
【答案】B
【详解】
A.如果弱酸、弱碱的电离程度相当,生成的盐的水溶液呈中性,例如醋酸铵显中性,故A不符合题意;
B. 酸和碱反应生成的盐溶液的酸碱性取决于酸根离子和弱碱阳离子的水解程度,弱离子的水解程度与酸、
碱的强弱有关,则盐溶液的酸碱性主要决定于形成盐的酸、碱性的相对强弱,故B符合题意;
C.醋酸铵是弱酸弱碱盐,水溶液中发生水解,CHCOONH 促进水的电离,醋酸根离子水解程度和铵根离
3 4
子水解程度相近溶液呈中性,NaCl是强酸强碱盐对水的电离无影响,所以两溶液中水的电离程度不同,故
C不符合题意;
D.铜离子、铁离子均能与氢氧化钠反应,所以加NaOH不能除去CuCl 中的Fe3+,故D不符合题意;
2
答案选B。
【题2】下列物质能促进水的电离的是
A.醋酸 B.醋酸钠 C.乙醇 D.氯化钡
【答案】B
【详解】A.醋酸电离会生成H+,因此对水的电离有抑制作用,A项错误;
B.醋酸钠中的醋酸根会发生水解,消耗水电离生成的H+,因此会对水的电离产生促进作用,B项正确;
C.乙醇属于非电解质,溶于水不发生电离,对于水的电离无影响,C项错误;
D.BaCl 溶于水电离出的Ba2+和Cl-不会发生水解,对于水的电离无影响,D项错误;
2
答案选B。
【点睛】
一般来讲,能够抑制水的电离的物质有:酸,碱等;能够促进水的电离的物质有:能水解的盐,金属钠等。
【题3】下列反应中,属于水解反应且使溶液显酸性的是
A.
B.
C.
D.
【答案】D
【详解】
A. 是氨水的电离方程式,使溶液呈碱性,故不选A;
B. 是碳酸氢根离子的电离方程式,故不选B;
C. 是硫离子的水解方程式,但使溶液呈碱性,故不选C;
D. 是铵根离子的水解方程式,溶液呈酸性,故选D;
选D。
【题4】下列各组离子中因发生相互促进的水解反应而不能大量共存的是( )
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
杨sir化学,侵权必究
【答案】C
【详解】
A. 与 反应生成硫酸钡沉淀,但不是因水解反应不能大量共存的,故不选;
B. 、 与 因发生氧化还原反应不能大量共存,但不是因水解反应不能大量共存的,故不选;C. 和 发生相互促进的水解反应生成二氧化碳和氢氧化铝而不能大量共存,故C选;
D. 与 生成二氧化碳不能大量共存, 与 生成碳酸钙沉淀不能大量共存,但不是因水解反
应不能大量共存的,故不选;
故选:C。
【题5】碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)Na CO 俗称___________,可作为碱使用的原因是___________(用离子方程式表示),其水溶液中各离子
2 3
的浓度从大到小的顺序为 ___________
(2)现有下列物质①100 ℃ 纯水;②25 ℃ 0.1 mol/L HCl溶液;③25 ℃ 0.1 mol/L KOH溶液;④25 ℃
pH=5的NH Cl溶液。这些物质与25 ℃纯水相比,能促进水电离的是___________(填序号),其中②由水电
4
离的c(OH-)=___________,③的pH=___________ ,④中由水电离的c(H+)=___________。
【答案】苏打或纯碱 +H
2
O⇌ +OH− c(Na+)>c( )>c(OH−)>c( )>c(H+)
①④ 1.0×10-13mol/L 13 1.0×10-5mol/L
【详解】
(1)Na CO 俗称纯碱,碳酸钠水解使溶液呈碱性,所以可作为碱使用,离子方程式是 +H O⇌
2 3 2
+OH−,其水溶液中各离子的浓度从大到小的顺序为c(Na+)>c( )>c(OH−)>c( )>c(H+);
(2)电离吸热,加热能促进水电离;酸、碱抑制水电离;盐水解促进水电离,这些物质与25 ℃纯水相比,
能促进水电离的是①100 ℃ 纯水、④25 ℃ pH=5的NH Cl溶液;②25 ℃ 0.1 mol/L HCl溶液中,
4
c(H+)=0.1 mol/L、c(OH-)= mol/L,盐酸抑制水电离,由水电离的c(OH-)=1.0×10-13mol/L;③25
℃ 0.1 mol/L KOH溶液,c(OH-)=0.1 mol/L、c(H+)= mol/L,pH=13,④25 ℃ pH=5的NH Cl
4
溶液,c(H+)=1.0×10-5mol/L、c(OH-)= mol/L,NH Cl水解促进水电离,由水电离的的c(H+)=
4
1.0×10-5mol/L。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列物质的水溶液因水解而呈碱性的是( )
A.NH NO B.NaCO C.NaCl D.Al (SO )
4 3 2 3 2 4 3【答案】B
【解析】A项,NH NO 溶液中铵根离子水解使溶液显酸性,故A不符合题意;B项,NaCO 溶液中碳酸
4 3 2 3
根离子水解使溶液显碱性,故B符合题意;C项,NaCl不水解,显中性,故C不符合题意;D项,
Al (SO ) 溶液中铝离子水解使溶液显酸性,故D不符合题意;故选B。
2 4 3
【练2】下列方程式属于水解反应方程式的是( )
A.HCO HCO -+H+ B.HCO -+H OH O++CO 2-
2 3 3 3 2 3 3
C.HCO -+OH-=H O+CO2- D.CO2-+ H O HCO -+ OH-
3 2 3 3 2 3
【答案】D
【解析】A项,碳酸是一种二元弱酸,选项所给为碳酸的第一步电离方程式,A不符合题意;B项,碳酸
氢根水解生成碳酸和氢氧根,选项所给为碳酸氢根的电离方程式,B不符合题意;C项,碳酸氢根水解生
成碳酸和氢氧根,选项所给为碳酸氢根和氢氧根的反应,C不符合题意;D项,碳酸根水解生成碳酸氢根
和氢氧根,方程式为CO2-+ H O HCO -+ OH-,D符合题意;故选D。
3 2 3
【练3】下列有关盐类水解的叙述正确的是
⇌
A.所有的盐溶液均呈中性
B.盐只能发生水解反应而不能发生其他反应
C.盐类的水解反应是吸热反应
D.任何盐都可发生水解反应
【答案】C
【详解】
A.NH Cl溶液呈酸性,CHCOONa溶液呈碱性,不是所有的盐溶液均呈中性,故A错误;
4 3
B.某些盐可以和酸、碱、盐等发生复分解反应,某些具有氧化性或还原性的盐还可以和具有还原性或氧
化性的物质发生氧化还原反应,故B错误;
C.盐类的水解反应是酸碱中和反应的逆反应,酸碱中和反应是放热的,所以盐的水解反应是吸热的,故
C正确;
D.强酸强碱盐如NaCl不发生水解反应,故D错误;
故选C。
【练4】下列物质中,能促进水的电离且溶液中c(H+)>c(OH-)的是
A.NaHSO B.CHCOONa C.HCl D.CuSO
4 3 4杨sir化学,侵权必究
【答案】D
【解析】
NaHSO 在溶液中电离出大量的氢离子,对水的电离起到抑制作用,选项A错误。CHCOONa是强碱弱酸
4 3
盐,水解显碱性,选项B错误。HCl在溶液中电离出大量的氢离子,对水的电离起到抑制作用,选项C错
误。CuSO 是强酸弱碱盐,水解溶液显酸性,同时水解会促进水电离,所以选项D正确。
4
点睛:物质对于水电离的影响可总结为:加酸加碱对于水的电离都起到抑制作用,加入可以水解的盐对水
的电离起到促进作用,加入不水解的盐对水的电离无影响。另外如果加入酸式盐,NaHCO 这样水解大于
3
电离的应该促进水电离,NaHSO 这样电离大于水解的应该抑制水电离。
3
【练5】下列离子方程式中,属于水解反应的是A.HCOOH HCOO-+H+
B.HCO +HO HCO+OH-
2 2 3
C.HO+HO HO++OH-
2 2 3
D.HCO CO +H+
【答案】B
【详解】
A.HCOOH HCOO-+H+是甲酸的电离方程式,故不选A;
B.HCO +HO HCO+OH-是碳酸氢根离子的水解方程式,故选B;
2 2 3
C.HO+HO HO++OH-是水的电离方程式,故不选C;
2 2 3
D.HCO CO +H+是碳酸氢根离子的电离方程式,故不选D;
选B。
【练6】(1)AlCl 水溶液呈___________性,原因是___________(用离子方程式表示,下同);NaCO 水溶液
3 2 3
呈___________性,原因是___________。二者均___________(填“促进”或“抑制”)水的电离。
(2)常温下,有两种溶液:0.1mol·L-1CHCOOH溶液;0.1mol·L-1CHCOONa溶液。
3 3
①0.1mol·L-1CHCOONa溶液呈___________(填“酸”“碱”或“中”)性。其原因是___________(用离子
3
方程式和适当的叙述说明)。
②下列说法正确的是___________(填序号)。
杨sir化学,侵权必究
A.两种溶液中c(CHCOO﹣)都等于0.1mol·L-1
3
B.两种溶液中c(CHCOO﹣)都小于0.1mol·L-1
3
C.CHCOOH溶液中c(CHCOO﹣)小于CHCOONa溶液中c(CHCOO﹣)
3 3 3 3
【答案】酸 Al3++3H O Al(OH) +3H+ 碱 CO +H O HCO +OH﹣ 促进 碱
2 3 2
CHCOO﹣+H O CHCOOH+OH﹣,CHCOO﹣水解使溶液显碱性 BC
3 2 3 3
【详解】
(1)氯化铝为强酸弱碱盐,铝离子在溶液中发生水解反应生成氢氧化铝和盐酸,促进水的电离,使溶液呈酸
性,水解的离子方程式为Al3++3H O Al(OH) +3H+;碳酸钠是强碱弱酸盐,碳酸根离子在溶液中分步
2 3
水解,促进水的电离,使溶液呈碱性,碳酸根离子在溶液中以一级水解为主,水解的离子方程式为CO+H O HCO +OH﹣,故答案为:酸;Al3++3H O Al(OH) +3H+;碱;CO +H O HCO +OH
2 2 3 2
﹣;促进;
(2) ①醋酸钠是强碱弱酸盐,醋酸根离子在溶液中发生水解反应生成醋酸和氢氧化钠,促进水的电离,使
溶液呈酸性,水解的离子方程式为CHCOO﹣+H O CHCOOH+OH﹣,故答案为:碱;CHCOO﹣+H O
3 2 3 3 2
CHCOOH+OH﹣,CHCOO﹣水解使溶液显碱性;
3 3
②醋酸是弱酸,在溶液中部分电离出氢离子和醋酸根离子,0.1mol·L-1醋酸溶液中c(CHCOO﹣)小于
3
0.1mol·L-1,醋酸钠是强碱弱酸盐,醋酸根离子在溶液中发生水解反应生成醋酸和氢氧化钠,0.1mol·L-1醋
酸钠溶液中c(CHCOO﹣)小于0.1mol·L-1,由于醋酸的电离和醋酸钠的水解都微弱,则醋酸溶液中
3
c(CHCOO﹣)小于醋酸钠溶液中c(CHCOO﹣),故选BC。
3 3倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育