文档内容
《海水中的重要元素——钠和氯》单元测试(培优提升)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共34分)
1.(本题2分)氯气有毒,在气泄露防范演习中,下列逃逸办法错误的是
A.向高处转移 B.迎着风撤离
C.顺风向低凹处转移 D.用肥皂液或水浸湿毛巾捂住口鼻
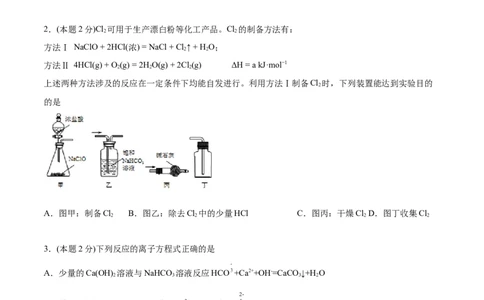
2.(本题2分)Cl 可用于生产漂白粉等化工产品。Cl 的制备方法有:
2 2
方法Ⅰ NaClO + 2HCl(浓) = NaCl + Cl ↑ + H O;
2 2
方法Ⅱ 4HCl(g) + O (g) = 2HO(g) + 2Cl (g) ΔH = a kJ·mol−1
2 2 2
上述两种方法涉及的反应在一定条件下均能自发进行。利用方法Ⅰ制备Cl 时,下列装置能达到实验目的
2
的是
A.图甲:制备Cl B.图乙:除去Cl 中的少量HCl C.图丙:干燥Cl D.图丁收集Cl
2 2 2 2
3.(本题2分)下列反应的离子方程式正确的是
A.少量的Ca(OH) 溶液与NaHCO 溶液反应HCO +Ca2++OH-=CaCO ↓+H O
2 3 3 2
B.稀HSO 滴入Ba(OH) 溶液中:Ba2++OH-+H++SO =BaSO ↓+H O
2 4 2 4 2
C.NaHCO 溶液滴入NaHSO 溶液中:HCO +H+=H O+CO↑
3 4 2 2
D.在漂白粉溶液中通入过量的CO:Ca2++2ClO-+CO +H O=CaCO ↓+2HClO
2 2 2 3
4.(本题2分)下列判断正确的是( )
①足量金属Na与标准状况下11.2 L O 反应时一定转移2 mol电子
2②某元素由化合态转化为游离态,这种元素一定被还原
③钠与硫酸铜溶液反应,可置换出铜
④NaO 与足量HO反应时,每生成1 mol O 转移电子的数目为2N
2 2 2 2 A
⑤NaO 遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
2 2
⑥向饱和烧碱溶液中加入2 g Na O,充分反应完后,恢复至室温,溶液中c(Na+)不变
2 2
A.①②③ B.②③⑤ C.④⑥ D.④
5.(本题2分)下列说法正确的是
A.NaO 遇到湿润的红色石蕊试纸后,石蕊试纸最终变成蓝色
2 2
B.NaO 与CO 反应生成0.1 mol O 时转移电子0.4 mol
2 2 2 2
C.将NaO 投入到CuCl 溶液中有蓝色沉淀及气泡产生
2 2 2
D.向饱和烧碱溶液中加入2 g Na O 充分反应完时,溶液中c(Na+)不变
2 2
6.(本题2分)下列对于NaO、NaO 的比较正确的一项是
2 2 2
A.NaO、NaO都是钠的氧化物,都是碱性氧化物
2 2 2
B.NaO、NaO 都是易溶于水(与水反应)的白色固体
2 2 2
C.NaO 在和CO 的反应中既是氧化剂又是还原剂
2 2 2
D.NaO 与水反应时,1 mol Na O 转移2 mol电子
2 2 2 2
7.(本题2分)下列有关NaCO 和NaHCO 性质的说法,不正确的是
2 3 3
A.NaCO 固体溶于水放热,而NaHCO 固体溶于水吸热
2 3 3
B.相同温度下,0.1 mol·L-1盐溶液的pH:NaCO > NaHCO
2 3 3
C.等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应放出气体的量:NaCO>NaHCO
2 3 3
D.与澄清石灰水反应:NaCO 、NaHCO 溶液中均有沉淀生成
2 3 3
8.(本题2分)为研究Na的性质,进行如下实验
装置 实验
液体a 现象
蒸馏水 Ⅰ.Na浮在液面上,剧烈反应,产生少量白雾
0.1 mol·L-1 盐酸 Ⅱ.Na浮在液面上,反应比Ⅰ中剧烈,产生白雾Ⅲ.Na浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白
浓盐酸
色固体
下列说法中,不正确的是
A.Ⅰ中现象说明Na与水反应放热
B.Ⅰ中反应的离子方程式为
C.Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多
D.推测Ⅲ中反应缓慢可能与c(Cl-)以及生成的白色固体有关
9.(本题2分)下列有关实验的说法不正确的是
A.中学实验室中可以将未用完的钠放回原试剂瓶
B.纯净的氢气在氯气中安静燃烧,发出苍白色火焰
C.干燥的氯气可以使有色鲜花变色,说明干燥的氯气有漂白性
D.配制480 mL 0.1 mol/L硫酸铜溶液时,需要用到500 mL容量瓶
10.(本题2分)下列关于实验室制 Cl 的认识正确的是
2
A.还原剂是 MnO
2
B.发生氧化反应的是 Cl-
C.向含有 4 mol HCl 的浓盐酸中加入足量 MnO 并加热,反应过程中转移电子数为 2 N
2 A
D.收集 Cl 宜采用向下排空气法收集
2
11.(本题2分)在一密闭容器中有CO、H 和O 共28.5 g,用电火花引燃,使其完全燃烧,再将燃烧后的气
2 2
体用NaO 充分吸收,固体增重12.5 g,则原混合气体中O 的物质的量为
2 2 2
A.0.35 mol B.0.45 mol C.0.50 mol D.1.00 mol
12.(本题2分)1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物
质后冷却,残留的固体物质是
A.NaCO B.NaO、NaCO
2 3 2 2 2 3
C.NaOH、NaCO D.NaO、NaOH、NaCO
2 3 2 2 2 3
13.(本题2分)有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06 g Na CO 和0.84 g NaHCO,
2 3 3
试管中各有10 mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各自的试管中,下列叙述正确的是
A.甲装置的气球膨胀速率小
B.若最终两气球体积相同,则一定有c(HCl)≥2 mol·L-1
C.若最终两气球体积不同,则一定有c(HCl)≤1 mol·L-1
D.最终两溶液中Na+、Cl-的物质的量相同
14.(本题2分)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.标准状况下,2.24 L H O的原子总数为0.1N B.常温常压下,1 mol N 的体积是22.4 L
2 A 2
C.1 mol -OH中电子数为10N D.18 g HO中含有的氢原子总数为2N
A 2 A
15.(本题2分)a mol HSO 中含有b个氧原子,则阿伏加德罗常数可以表示为
2 4
A. mol-1 B. mol-1 C. mol-1 D. mol-1
16.(本题2分)把V L含有Fe (SO ) 和KSO 的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰
2 4 3 2 4
好使铁离子完全沉淀为氢氧化铁;另一份加入含b mol BaCl 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。
2
则原混合溶液中钾离子的浓度为
A.(b-a)/V mol·L-1 B.(2b-a)/V mol·L-1
C.2(2b-a)/V mol·L-1 D.2(b-a)/V mol·L-1
17.(本题2分)设N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.0.5 mol·L-1的MgCl 溶液中,含有Cl-个数为N
2 A
B.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,生成H 的体积为1 120 mL
2
C.常温常压下,3.2 g O 所含的原子数为0.2N
2 A
D.标准状况下,2.24 L H O含有的HO分子数为0.1N
2 2 A
二、双选题(共12分)18.(本题4分)下列叙述中,正确的是
A.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水,距刻度线1
~2 cm处时再改用胶头滴管滴加蒸馏水至刻度线
B.向久置的氯水中滴入紫色石蕊试液,溶液可能只变红
C.检验Cl 中是否混有HCl气体的方法是将气体通入硝酸银溶液
2
D.10 mL0.2 mol/L氯化钾溶液与100 mL0.1 mol/L硫酸钾溶液里钾离子物质的量浓度相同
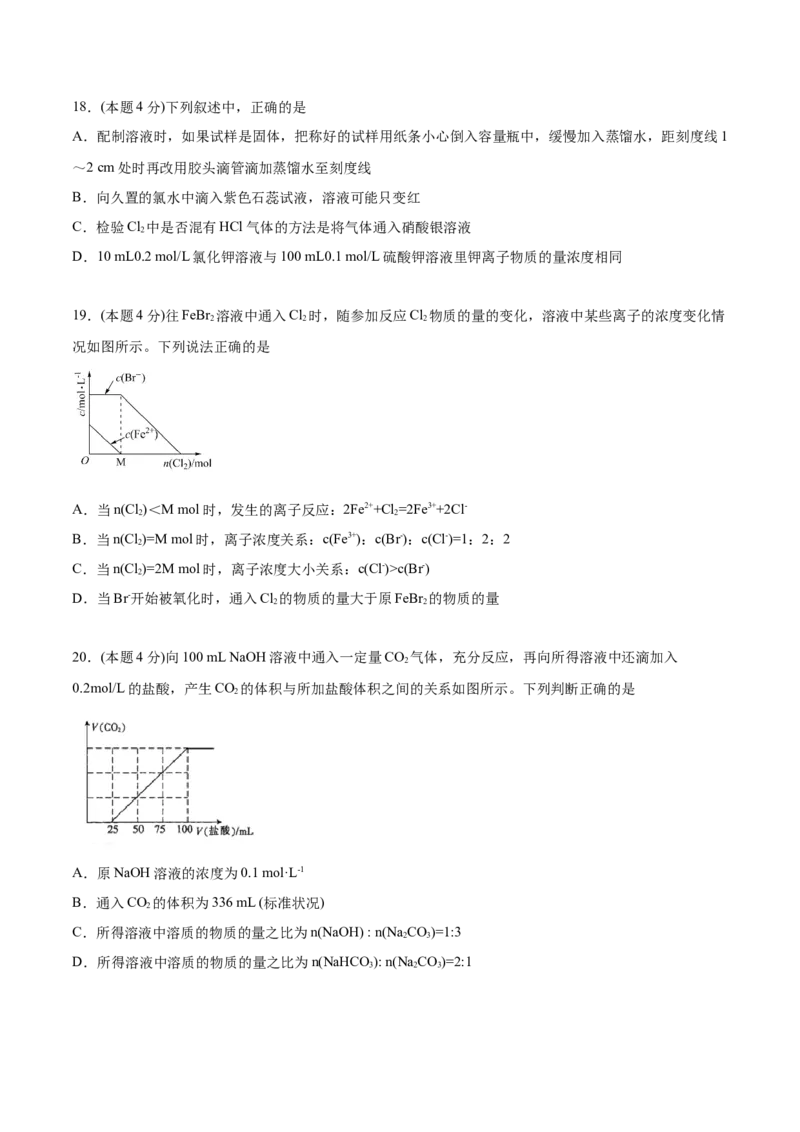
19.(本题4分)往FeBr 溶液中通入Cl 时,随参加反应Cl 物质的量的变化,溶液中某些离子的浓度变化情
2 2 2
况如图所示。下列说法正确的是
A.当n(Cl )<M mol时,发生的离子反应:2Fe2++Cl=2Fe3++2Cl-
2 2
B.当n(Cl )=M mol时,离子浓度关系:c(Fe3+):c(Br-):c(Cl-)=1:2:2
2
C.当n(Cl )=2M mol时,离子浓度大小关系:c(Cl-)>c(Br-)
2
D.当Br-开始被氧化时,通入Cl 的物质的量大于原FeBr 的物质的量
2 2
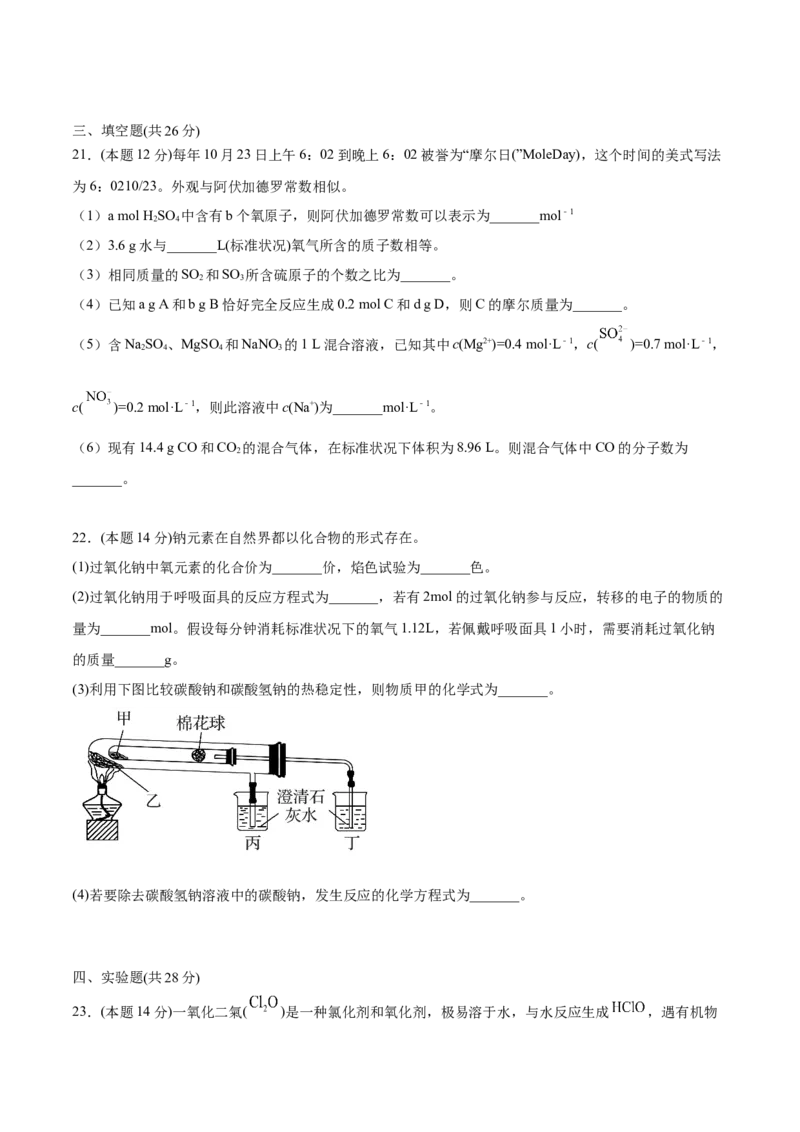
20.(本题4分)向100 mL NaOH溶液中通入一定量CO 气体,充分反应,再向所得溶液中还滴加入
2
0.2mol/L的盐酸,产生CO 的体积与所加盐酸体积之间的关系如图所示。下列判断正确的是
2
A.原NaOH溶液的浓度为0.1 mol·L-1
B.通入CO 的体积为336 mL (标准状况)
2
C.所得溶液中溶质的物质的量之比为n(NaOH) : n(Na CO)=1:3
2 3
D.所得溶液中溶质的物质的量之比为n(NaHCO ): n(Na CO)=2:1
3 2 3三、填空题(共26分)
21.(本题12分)每年10月23日上午6:02到晚上6:02被誉为“摩尔日(”MoleDay),这个时间的美式写法
为6:0210/23。外观与阿伏加德罗常数相似。
(1)a mol H SO 中含有b个氧原子,则阿伏加德罗常数可以表示为_______mol﹣1
2 4
(2)3.6 g水与_______L(标准状况)氧气所含的质子数相等。
(3)相同质量的SO 和SO 所含硫原子的个数之比为_______。
2 3
(4)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为_______。
(5)含NaSO 、MgSO 和NaNO 的1 L混合溶液,已知其中c(Mg2+)=0.4 mol·L﹣1,c( )=0.7 mol·L﹣1,
2 4 4 3
c( )=0.2 mol·L﹣1,则此溶液中c(Na+)为_______mol·L﹣1。
(6)现有14.4 g CO和CO 的混合气体,在标准状况下体积为8.96 L。则混合气体中CO的分子数为
2
_______。
22.(本题14分)钠元素在自然界都以化合物的形式存在。
(1)过氧化钠中氧元素的化合价为_______价,焰色试验为_______色。
(2)过氧化钠用于呼吸面具的反应方程式为_______,若有2mol的过氧化钠参与反应,转移的电子的物质的
量为_______mol。假设每分钟消耗标准状况下的氧气1.12L,若佩戴呼吸面具1小时,需要消耗过氧化钠
的质量_______g。
(3)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为_______。
(4)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为_______。
四、实验题(共28分)
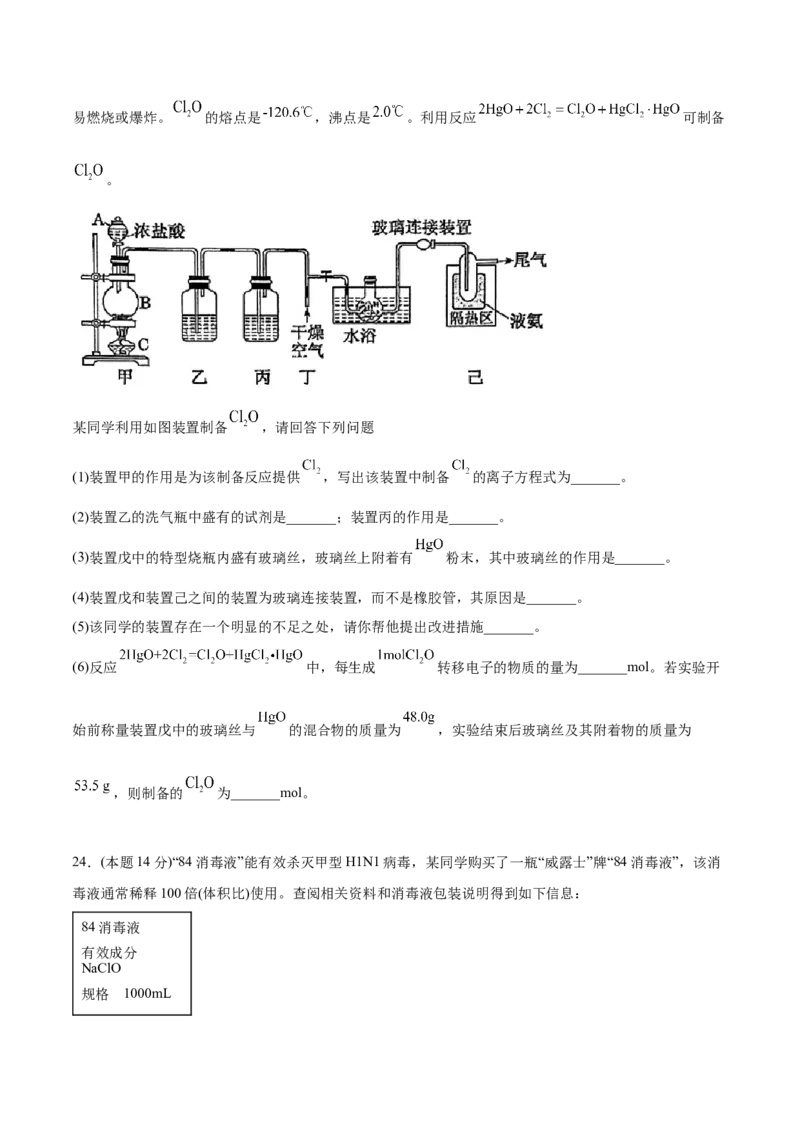
23.(本题14分)一氧化二氣( )是一种氯化剂和氧化剂,极易溶于水,与水反应生成 ,遇有机物易燃烧或爆炸。 的熔点是 ,沸点是 。利用反应 可制备
。
某同学利用如图装置制备 ,请回答下列问题
(1)装置甲的作用是为该制备反应提供 ,写出该装置中制备 的离子方程式为_______。
(2)装置乙的洗气瓶中盛有的试剂是_______;装置丙的作用是_______。
(3)装置戊中的特型烧瓶内盛有玻璃丝,玻璃丝上附着有 粉末,其中玻璃丝的作用是_______。
(4)装置戊和装置己之间的装置为玻璃连接装置,而不是橡胶管,其原因是_______。
(5)该同学的装置存在一个明显的不足之处,请你帮他提出改进措施_______。
(6)反应 中,每生成 转移电子的物质的量为_______mol。若实验开
始前称量装置戊中的玻璃丝与 的混合物的质量为 ,实验结束后玻璃丝及其附着物的质量为
,则制备的 为_______mol。
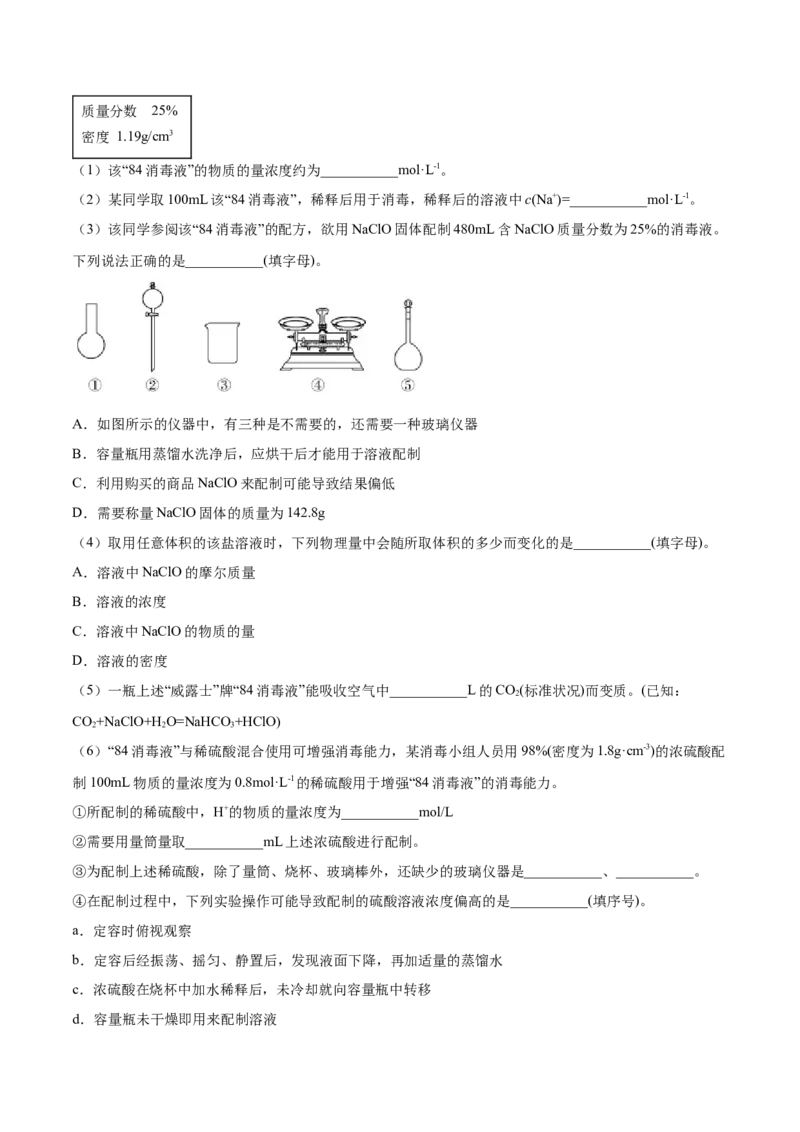
24.(本题14分)“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消
毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
84消毒液
有效成分
NaClO
规格 1000mL质量分数 25%
密度 1.19g/cm3
(1)该“84消毒液”的物质的量浓度约为___________mol·L-1。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___________mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。
下列说法正确的是___________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
D.需要称量NaClO固体的质量为142.8g
(4)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是___________(填字母)。
A.溶液中NaClO的摩尔质量
B.溶液的浓度
C.溶液中NaClO的物质的量
D.溶液的密度
(5)一瓶上述“威露士”牌“84消毒液”能吸收空气中___________L的CO(标准状况)而变质。(已知:
2
CO+NaClO+H O=NaHCO +HClO)
2 2 3
(6)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8g·cm-3)的浓硫酸配
制100mL物质的量浓度为0.8mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为___________mol/L
②需要用量筒量取___________mL上述浓硫酸进行配制。
③为配制上述稀硫酸,除了量筒、烧杯、玻璃棒外,还缺少的玻璃仪器是___________、___________。
④在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是___________(填序号)。
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液e.往容量瓶转移时,有少量液体溅出
f.未洗涤稀释浓硫酸的烧杯关注更新免费领取,淘宝唯一每月更新店铺:知二教育