文档内容
《海水中的重要元素——钠和氯》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共48分)
1.(本题2分)下列说法中正确的是
A.摩尔是表示物质质量的单位
B.物质的量适用于计量分子、原子、离子等粒子的集合体
C.摩尔是表示物质所含微粒个数的物理量
D.物质的量就是指物质的质量
2.(本题2分)下列化学生活常识说法正确的是
A.苹果切开后过一段时间表面变黑,说明苹果发生了氧化反应
B.铅笔芯的主要成分是铅
C.胃酸过多引起的胃溃疡病人可以服用医用
D.家用碱性洗碗剂的主要成分是氢氧化钠
3.(本题2分)下列实验现象的描述正确的是
A.氢气在氧气中燃烧,发生苍白色火焰,瓶口上方形成白色烟雾
B.铁丝在氯气中燃烧,产生红棕色的烟,产物溶于水,溶液呈浅绿色
C.铜丝在氯气中燃烧,产生棕黄色的烟,产物溶于水,溶液呈蓝绿色
D.钠在空气中燃烧,发出黄色火焰,生成白色固体
4.(本题2分)有两试管分别装有NaCO 和NaHCO 溶液,下列操作或判断正确的是
2 3 3
方案 操作 判断
A 分别加入澄清石灰水 产生沉淀者为NaCO
2 3
B 分别加入等浓度的稀盐酸 反应较剧烈者为NaCO
2 3
C 分别加入CaCl 溶液 产生沉淀者为NaCO
2 2 3
D 逐渐加入等浓度的盐酸 立即产生气泡者为NaCO
2 3
A.A B.B C.C D.D
5.(本题2分)与50mL0.1mol·L-1NaCO 溶液中Na+的物质的量浓度相同的溶液是
2 3A.50mL0.2mol·L-1的NaCl溶液 B.100mL0.1mol·L-1的NaPO 溶液
3 4
C.25mL0.2mol·L-1的NaSO 溶液 D.10mL0.5mol·L-1的NaCO 溶液
2 4 2 3
6.(本题2分)下列关于金属钠的描述中,不正确的是
A.有银白色金属光泽 B.在空气中燃烧发出黄色火焰
C.具有很强的还原性 D.钠与水反应生成氢氧化钠和氧气
7.(本题2分)将一小块金属钠投入到CuSO 溶液中,不可能观察到的现象是
4
A.溶液中有蓝色沉淀生成
B.有气体生成
C.有红色物质析出
D.钠熔成小球,在CuSO 溶液底部
4
8.(本题2分)下列有关NaCO 和NaHCO 的性质,叙述错误的是
2 3 3
A.鉴别NaCO 和NaHCO 既可以用BaCl 溶液,不可用Ba(OH) 溶液
2 3 3 2 2
B.NaCO、NaHCO 的水溶液均呈碱性,它们都可以用作食用碱
2 3 3
C.向NaCO 粉末和NaHCO 晶体中滴入少量水,前者温度升高,后者温度下降
2 3 3
D.除去NaCO 溶液中混有的少量NaHCO ,用加热法
2 3 3
9.(本题2分)下列关于NaO和NaO 的叙述,正确的是
2 2 2
A.NaO比NaO 稳定 B.均可与CO、HO反应产生氧气
2 2 2 2 2
C.NaO、NaO 均是碱性氧化物 D.阴、阳离子个数比均为1:2
2 2 2
10.(本题2分)下列有关钠及其化合物的叙述错误的是
A. 吸收 产生 ,可用作呼吸面具供氧剂
B.高压钠灯发出的黄光透雾能力强,可用于道路和广场照明
C.氢氧化钠具有强碱性,可用于制胃酸中和剂
D.钠着火可以用干燥的沙土来灭火
11.(本题2分)下列反应的离子方程式正确的是A.少量的Ca(OH) 溶液与NaHCO 溶液反应HCO +Ca2++OH-=CaCO ↓+H O
2 3 3 2
B.稀HSO 滴入Ba(OH) 溶液中:Ba2++OH-+H++SO =BaSO ↓+H O
2 4 2 4 2
C.NaHCO 溶液滴入NaHSO 溶液中:HCO +H+=H O+CO↑
3 4 2 2
D.在漂白粉溶液中通入过量的CO:Ca2++2ClO-+CO +H O=CaCO ↓+2HClO
2 2 2 3
12.(本题2分)下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是
A.CuCl B.FeCl C.MgCl D.FeCl
2 2 2 3
13.(本题2分)下列关于氯水的叙述,正确的是
A.新制氯水中只含Cl 和HO分子
2 2
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是O
2
D.氯水久置后,由于Cl 挥发,酸性减弱
2
14.(本题2分)下列过程不涉及化学变化的是
A.钠在空气中表面生成白色物质 B.铜器生铜绿
C.用氯化钠溶液做焰色试验 D.光照氯水,溶液褪色
15.(本题2分)下列有关物质保存的说法错误的是
A.钠保存在煤油中
B.过氧化钠需密封保存
C.氯水密封保存在无色试剂瓶中
D.漂白粉不能露置在空气中保存
16.(本题2分)下列关于氯及其化合物的叙述正确的是
① 实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
② 氯气易液化,液氯可以保存在钢瓶中
③ 氯气的性质很活泼,它与氢气混合后立即发生爆炸
④ 检验HCl气体中是否混有Cl 的方法是将气体通入硝酸银溶液
2
⑤ 氯水、氯气、液氯均能与碳酸氢钠溶液反应产生无色无味的气体A.①② B.②⑤ C.③⑤ D.③④
17.(本题2分)同温同压下,具有相同体积的气体一定具有
A.相同的分子数 B.相同的质量 C.相同的原子数 D.相同的密度
18.(本题2分)下列说法正确的是
A.O 的摩尔质量是32g
2
B.Fe2+的摩尔质量是54g/mol
C.摩尔质量数值上等于相对分子质量
D.利用丁达尔效应可以区别溶液与胶体
19.(本题2分)铅笔芯主要成分是石墨和黏土。假设铅笔芯质量的一半是石墨(其余组成物质中不含碳),用
铅笔写一个汉字消耗的质量约为 ,那么这个汉字中含有的碳原子数约为
A. B. C. D.
20.(本题2分)若 与 按质量比1:4混合时极易爆炸,此时 与 的体积比为
A.1:4 B.1:2 C.1:1 D.2:1
21.(本题2分)下列数量的各物质所含原子数按由大到小序排列是
① 时 水 ② 氨气 ③标准状况下 氢气 ④ 硫酸
A.④③②① B.①②③④ C.③①④② D.①③②④
22.(本题2分)下列叙述正确的是
A.金属钠长期置于空气中,最后变为NaOH
B.“84”消毒液可用作漂白剂,过氧化钠可用作供氧剂
C.Na的金属活动性比Cu强,可用Na与CuCl 溶液反应制Cu
2
D.常温下,称取5.9g NaCl溶于100ml水配成1 mol·L-1的溶液
23.(本题2分)用1 L 0.5 mol/LNaOH溶液吸收0.4 mol CO,反应后溶液中的 和 的物质的量浓度
2之比约是
A.3:1 B.1:2 C.2:3 D.1:3
24.(本题2分)下列与Cl 有关的说法正确的是
2
A.Cl 具有很强的氧化性,在化学反应中只作氧化剂
2
B.铁丝在氯气中燃烧,产生棕褐色的烟,加水溶解后,溶液呈浅绿色
C.0.1 mol Cl 与足量NaOH溶液反应,转移0.2 mol电子
2
D.Cl 虽然是一种有毒气体,但控制用量,可以用于自来水的消毒、杀菌
2
二、填空题(共24分)
25.(本题12分)完成下列填空:
(1)分子数为3.01×1023个NH 的物质的量约为___________。
3
(2)标准状况下,2.24LCl 的质量为___________g,标准状况下,将aL HCl气体溶于水配成
2
500mL0.4mol∙L-1的溶液,则a=___________;
(3)在一定的温度和压强下,1体积气体X 跟3体积气体Y 化合生成2体积化合物C,则该化合物的化
2 2
学式是___________。
(4)在标准状况下,由CO和CO 组成的混合气体11.2L,质量为20g,该混合气体中,CO和CO 物质的
2 2
量之比为___________, 碳与氧两种原子的数目之比为___________。
(5)已知溶液Y由20mL0.1 mol∙L-1AlCl 溶液和30ml0.2 mol∙L-1MgCl 溶液混合而成,则Y中
3 2
c(Cl-)=___________mol∙L-1 (假设混合溶液的体积等于混合前两种溶液的体积之和)。
26.(本题12分)钠及其化合物是重要的化学物质。回答下列问题:
(1)少量的钠保存在___________中,如果露置在空气中会迅速变成___________(填化学式)。
(2)钠很活泼,一定条件下,它能置换出TiCl 中Ti,写出该反应的化学方程式:___________。
4
(3)Na O 属于___________(填物质类别),可用蒸馏水检验NaO中混有少量NaO,试用化学方程式解释含
2 2 2 2 2
有NaO 的现象:___________。
2 2
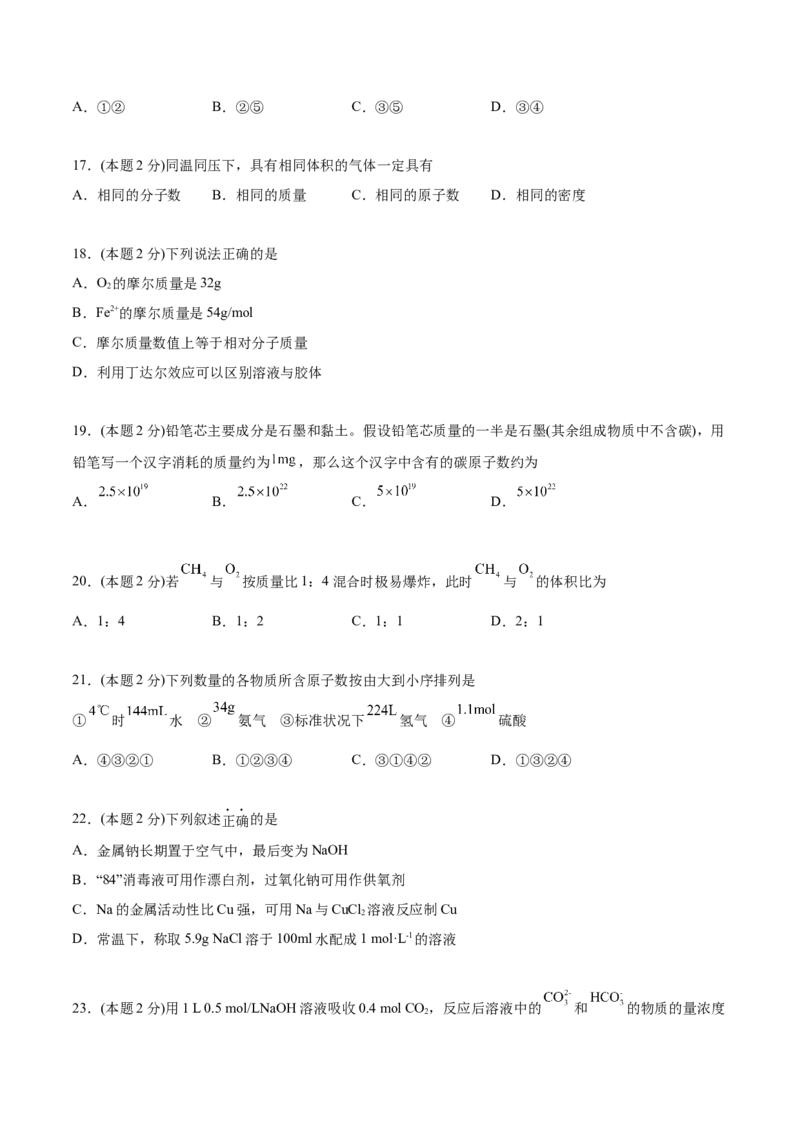
(4)热稳定性:NaHCO ___________(填“>”或“<”)Na CO,实验室可用如图装置验证,试管B中应装入的固
3 2 3
体是___________。(5)1 mL 0.1 mol·L-1 NaHCO 溶液与1 mL 0.01 mol·L-1 Ca(OH) 溶液混合产生CaCO 白色沉淀。
3 2 3
①请用离子方程式表示生成CaCO 的反应过程:___________。
3
②同学们设计了如图实验方案,验证上述反应过程,请将方案补充完整:
实验步骤 实验现象
ⅰ.取1mL0.1mol L-1NaHCO 溶液,向其中加入
3 无明显现象
1mL0.01mol L-1CaCl 溶液
2
ⅱ.向上述溶液中滴加________ ___________
三、实验题(共28分)
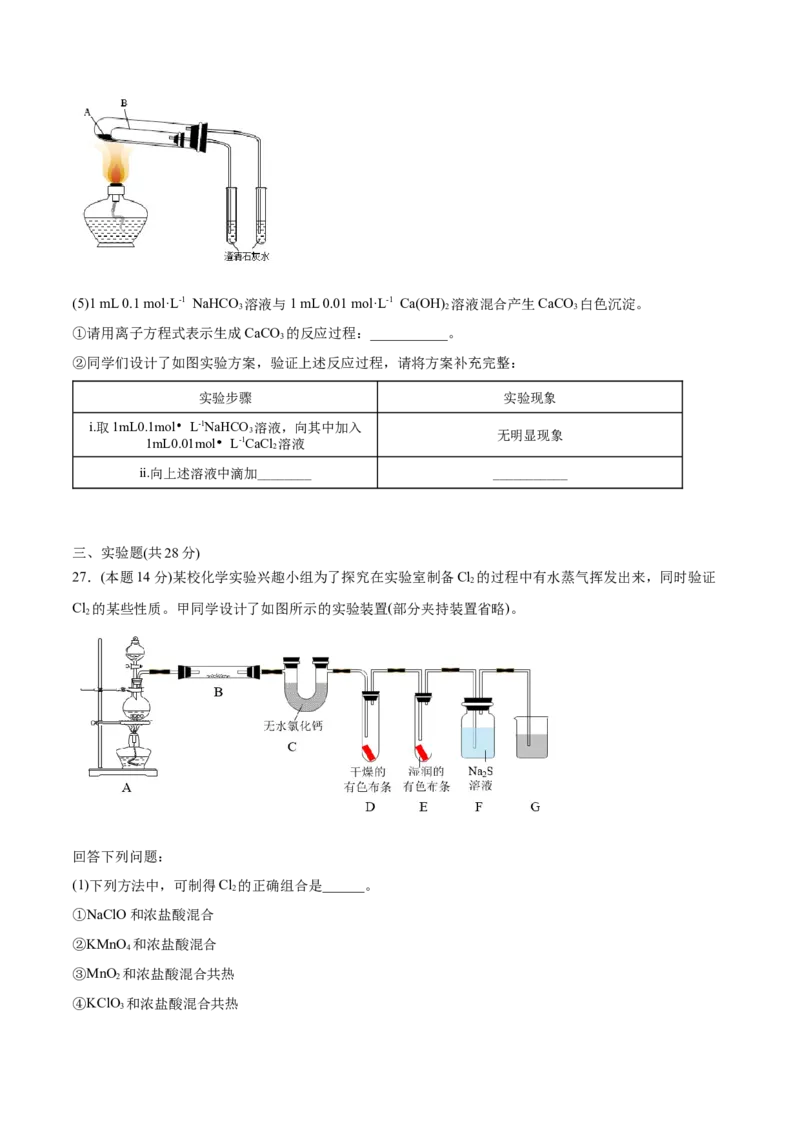
27.(本题14分)某校化学实验兴趣小组为了探究在实验室制备Cl 的过程中有水蒸气挥发出来,同时验证
2
Cl 的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。
2
回答下列问题:
(1)下列方法中,可制得Cl 的正确组合是______。
2
①NaClO和浓盐酸混合
②KMnO 和浓盐酸混合
4
③MnO 和浓盐酸混合共热
2
④KClO 和浓盐酸混合共热
3A.①② B.②④ C.③④ D.全部可以
(2)若用含0.2 mol HCl的浓盐酸与足最的MnO 反应制取Cl,制得Cl 体积______(填“>”“<”或“=”)1.12 L(标
2 2 2
准状况)。
(3)①装置B中盛放无水CuSO ,若看到______现象,说明生成Cl 含有水蒸气。
4 2
②由装置D和E中出现的不同现象得出的结论是______。其中装置E中氯气与水发生反应的离子方程式为
______。
③装置F中可观察到的现象为______,由此得出非金属性:Cl______(填“>”、“<”)S。
④装置G中应放入______,吸收多余Cl,防止污染环境。
2
28.(本题14分)某化学实验室需要0.5 mol/L硫酸溶液450 mL。根据溶液的配制情况回答下列问题:
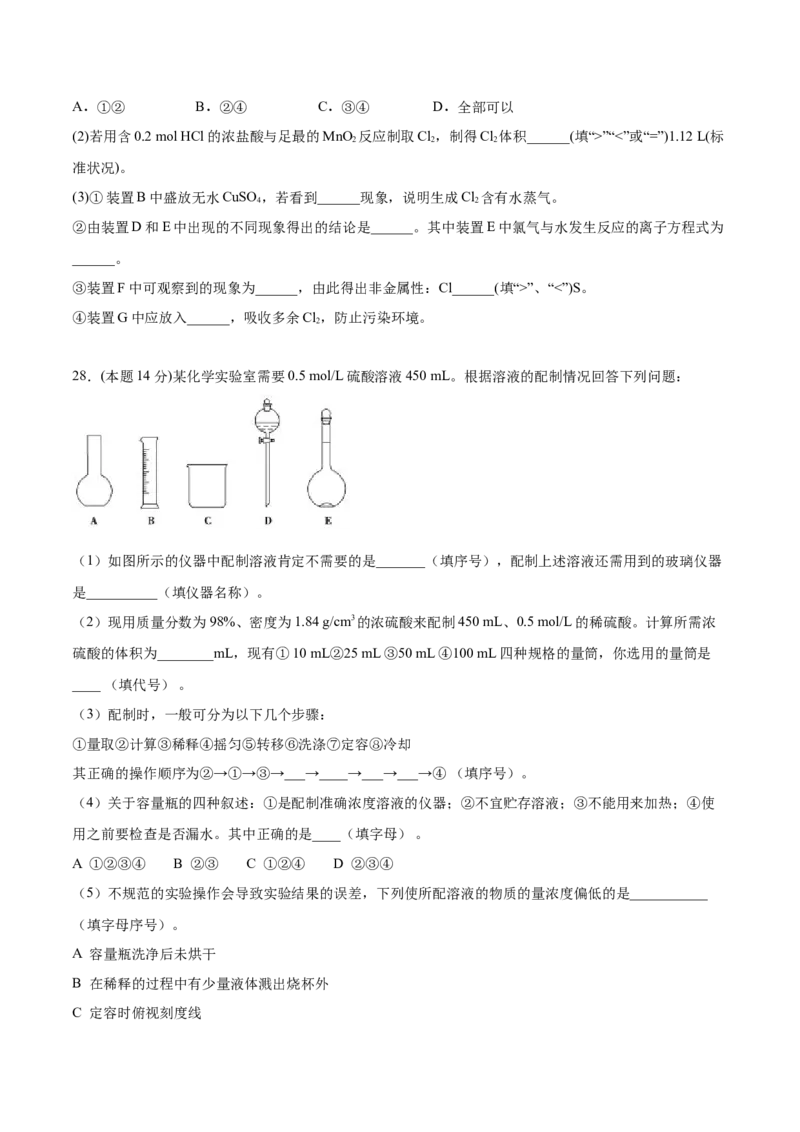
(1)如图所示的仪器中配制溶液肯定不需要的是_______(填序号),配制上述溶液还需用到的玻璃仪器
是__________(填仪器名称)。
(2)现用质量分数为98%、密度为1.84 g/cm3的浓硫酸来配制450 mL、0.5 mol/L的稀硫酸。计算所需浓
硫酸的体积为________mL,现有①10 mL②25 mL ③50 mL ④100 mL四种规格的量筒,你选用的量筒是
____ (填代号) 。
(3)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇匀⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为②→①→③→___→____→___→___→④ (填序号)。
(4)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使
用之前要检查是否漏水。其中正确的是____(填字母) 。
A ①②③④ B ②③ C ①②④ D ②③④
(5)不规范的实验操作会导致实验结果的误差,下列使所配溶液的物质的量浓度偏低的是___________
(填字母序号)。
A 容量瓶洗净后未烘干
B 在稀释的过程中有少量液体溅出烧杯外
C 定容时俯视刻度线D 将稀释好的溶液,未经冷却立即转移到容量瓶中并定容
E 定容后,将容量瓶振荡掘匀后,静置发现液面低于刻度线,又加入少量水至刻度线关注更新免费领取,淘宝唯一每月更新店铺:知二教育