文档内容
3.1 卤代烃(精练)
题组一 卤代烃
1.(2021·广东荔湾·高二期末)卤代烃(CH)C=CHCl能发生的反应有
3 2
①取代反应②加成反应③消去反应④氧化反应⑤加聚反应⑥与AgNO 溶液生成白色沉淀
3
A.以上反应均可发生 B.只有③⑥不能发生
C.只有①③不能发生 D.只有②⑥不能发生
【答案】B
【解析】卤代烃(CH)C=CHCl中含有Cl原子可以发生水解反应,属于取代反应;含有碳碳双键故可以发
3 2
生加成反应;含有Cl但是由于与其相邻的碳原子上没有H,故不能发生消去反应;含有碳碳双键可以使酸
性高锰酸钾溶液褪色而发生氧化反应;含有碳碳双键故可以发生加聚反应;氯代烃属于非电解质,不能电
离出卤素离子,故加入AgNO 溶液后不产生白色沉淀;综上所述可知,该卤代烃能够发生的反应有:
3
①②④⑤,即只有③⑥不能发生,故答案为:B。
2.(2021·安徽·定远县育才学校高二期末)下列说法正确的是
A.卤代烃均不溶于水,且浮于水面上
B.C HC1在浓硫酸的作用下发生消去反应生成乙烯
2 5
C.卤代烃在NaOH水溶液中发生的取代反应
D.向C HC1中加硝酸酸化的AgNO 溶液可以检验C HC1中的氯元素
2 5 3 2 5
【答案】C
【解析】A.卤代烃均不溶于水,但不是都浮于水面上,密度大于水的,在水的下层,如CCl 的密度比水
4
大,和水混合后,在下层,A错误;
B.C HCl在NaOH醇溶液的作用下加热发生消去反应生成乙烯,B错误;
2 5
C.卤代烃在NaOH水溶液中加热发生水解反应生成醇,属于取代反应,C正确;
D.C HCl是非电解质,在水溶液中不发生电离产生不了Cl-,故向C HCl与NaOH水溶液共热后的溶液
2 5 2 5
中先加硝酸酸化,再加入AgNO 溶液来检验C HCl中的氯元素,D错误;
3 2 5
故答案为:C。
3(2022·全国·高二专题练习)下列关于卤代烃的说法错误的是
A.常温下,卤代烃中除个别是气体外,大多是液体或固体
B.某些卤代烃可用作有机溶剂
C.一氯代烃的密度一般随着烃基中碳原子数的增加而增大
D.一氯代烃的沸点一般随着烃基中碳原子数的增加而升高【答案】C
【解析】A.常温下,卤代烃中除CHCl是气体外,其余的大多是液体或固体物质,A正确;
3
B.卤代烃中CHCl 、CCl 是常用的有机溶剂,B正确
3 4
C.一氯代烃的密度一般随着烃基中碳原子数的增加而减小,C错误;
D.一氯代烃都是分子晶体,分子间作用力随物质相对分子质量的增大而增强,分子间作用力越大,克服
分子间作用力使物质熔化或气化消耗的能量就越多,物质的物质熔点、沸点就越高,所以卤代烃的熔沸点
一般随着烃基中碳原子数的增加而升高,D正确;
故合理选项是C。
4.(2021·陕西·咸阳市实验中学高二阶段练习)下列关于卤代烃的叙述中正确的是
A.通过卤代烃水解反应可制得多种烃的含氧衍生物
B.所有卤代烃在适当条件下都能发生消去反应
C.所有卤代烃都是难溶于水, 密度比水小的液体
D.所有卤代烃都是通过取代反应制得的
【答案】A
【解析】A.通过卤代烃水解反应可制得醇、酚、醛、酮和羧酸等多种烃的含氧衍生物,如溴乙烷水解可
以制得乙醇、1,1—二溴乙烷水解可以制得乙醛、1,1,1—三溴乙烷水解可以制得乙酸,故A正确;
B.卤素原子所连碳原子必须有邻碳原子,邻碳原子上必须有氢原子的卤代烃才可发生消去反应,如
CHCl、(CH)CCHCl不能发生消去反应,故B错误;
3 3 3 2
C.所有卤代烃不一定都是液体,如一氯甲烷是气体,密度不一定比水小,如四氯化碳的密度比水大,故
C错误;
D.卤代烃不一定通过取代反应制得,烯烃与卤素单质或卤化氢发生加成反应也可制得卤代烃,故D错误;
答案选A。
5(2020·江苏省苏州实验中学高二阶段练习)下列关于卤代烃的叙述正确的是
A.所有卤代烃都是难溶于水,比水密度大的液体
B.所有卤代烃都是通过取代反应制得的
C.所有卤代烃在适当条件下都能发生消去反应
D.所有卤代烃都含有卤原子
【答案】D
【解析】A.一般卤代烃难溶于水,卤代烃不一定为液体,如CHCl为气体,卤代烃的密度不一定比水的
3
密度大,如一氯乙烷的密度比水的密度小,A项正确;
B.卤代烃也可利用烯烃加成反应制备,如乙烯与HCl可发生加成反应生成氯乙烷,B项错误;C.与−X相连C的邻位C上有H才可以发生消去反应,如CH
3
Cl、(CH
3
)
3
CCH
2
Cl不能发生消去反应,C项
错误;
D.卤代烃可以看做是烃分子中的氢原子被卤素原子取代后生成的化合物,所有的卤代烃都含有卤原子,D
项正确;答案选D。
题组二 溴乙烷的水解反应
1.(2021·福建省建瓯市芝华中学高二期中)下列物质中,既能发生水解反应,又能发生加成反应,但不
能发生消去反应的是
A.CHCHCHCHCl B.CHCHCl
3 2 2 2 3 2
C.CHBr D.
3
【答案】D
【解析】A.该物质属于氯代烃,可以发生水解反应,与氯相连碳的邻位碳有H,能发生消去反应,但由
于没有不饱和键,故不能发生加成反应,故A不符合题意;
B.该物质属于氯代烃,可以发生水解反应,与氯相连碳的邻位碳有H,能发生消去反应,但由于没有不
饱和键,故不能发生加成反应,故B不符合题意;
C.该物质属于氯代烃,可以发生水解反应,但由于只有一个碳原子上,所以不能发生消去反应,也不能
发生加成反应,故C不符合题意;
D.该物质属于不饱和氯代烃,可以发生水解、加成反应,由于和官能团相连的邻位碳原子上没有氢原子,
不能发生消去反应,故D符合题意;
故答案选D。
2.(2022·全国·高二专题练习)在卤代烃RCHCHX中化学键如图所示,则下列说法正确的是
2 2
A.发生水解反应时,被破坏的键是①和③
B.发生消去反应时,被破坏的键是①和④
C.发生水解反应时,被破坏的键是①
D.发生消去反应时,被破坏的键是②和③【答案】C
【解析】卤代烃水解反应是卤素原子被羟基取代生成醇,只断①键;消去反应是卤代烃中卤素原子和卤素
原子相连碳原子的邻位碳上的氢原子共同去掉,断①③键,综上所述故选C。
3.(2022·全国·高二专题练习)下列化合物中,既能发生水解反应,又能发生消去反应。且消去反应只生
成一种烯烃的是
A. B. C. D.
【答案】B
【解析】A. 分子中含有氯原子,能在氢氧化钠溶液中共热发生水解反应,但与氯原子相连的碳原
子没有邻碳原子,不能发生消去反应,故A错误;
B. 分子中含有氯原子,能在氢氧化钠溶液中共热发生水解反应,与氯原子相连的碳
原子的邻碳原子上连有氢原子,能在氢氧化钠醇溶液中发生消去反应生成1种烯烃,故B正确;
C. 分子中含有氯原子,能在氢氧化钠溶液中共热发生水解反应,与氯原子相连的碳
原子的邻碳原子上不连有氢原子,不能在氢氧化钠醇溶液中发生消去反应,故C错误;
D. 分子中含有氯原子,能在氢氧化钠溶液中共热发生水解反应,与氯原子相连的
碳原子的邻碳原子上连有氢原子,能在氢氧化钠醇溶液中发生消去反应生成2种烯烃,故D错误;
故选B。
4.(2022·全国·高二专题练习)下列有关溴乙烷的叙述正确的是
A.在溴乙烷中滴入 溶液,立即有淡黄色沉淀生成
B.溴乙烷在加热、 水溶液作用下可生成乙烯C.溴乙烷在加热、 的醇溶液作用下可生成乙醇
D.溴乙烷可用乙烯与溴化氢加成来制取
【答案】D
【解析】A.溴乙烷不能电离出溴离子,所以在溴乙烷中滴入 溶液,不会有淡黄色沉淀生成,A项
错误;
B.溴乙烷在加热、 的醇溶液作用下发生消去反应,生成乙烯,B项错误;
C.溴乙烷在加热、 水溶液作用下发生取代反应,可生成乙醇,C项错误;
D.乙烯与溴化氢发生加成反应生成溴乙烷,故D正确;
故选D。
5.(2021·全国·高二)下列化合物中能发生消去反应生成两种烯烃,又能发生水解反应的是
A.CHCl B. C. D.
3
【答案】D
【解析】A.CHCl分子中含有氯原子,能发生水解反应,但与氯原子相连的碳原子没有邻碳原子,不能
3
发生消去反应,故A错误;
B. 分子中含有氯原子,能发生水解反应,与氯原子相连的碳原子有连有氢原子的邻
碳原子,能发生消去反应,但发生消去反应只能生成一种烯烃,故B错误;
C. 分子中含有氯原子,能发生水解反应,与氯原子相连的碳原子有连有氢原子的邻碳原子,
能发生消去反应,但发生消去反应只能生成一种烯烃,故B错误;
D. 分子中含有氯原子,能发生水解反应,与氯原子相连的碳原子有连有氢原子的邻碳原
子,能发生消去反应生成两种烯烃,故D正确;故选D。
题组三 溴乙烷的消去反应
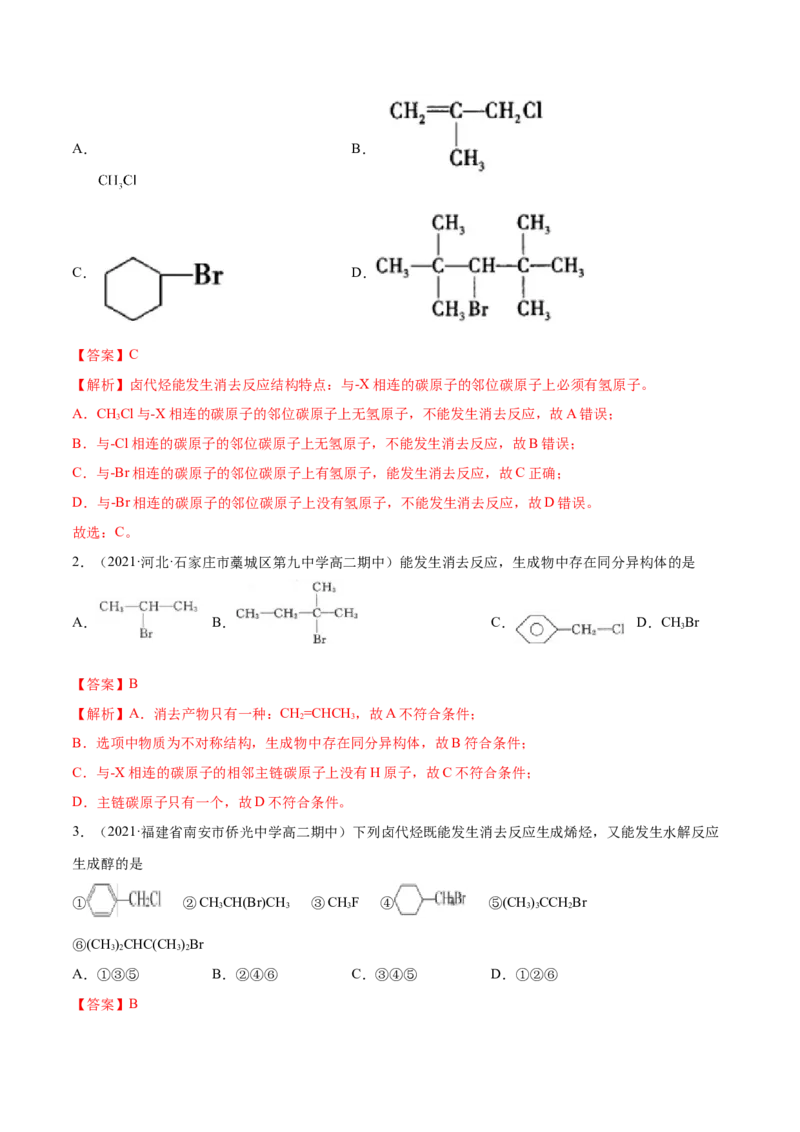
1.(2021·福建省永泰县第一中学高二期末)能在KOH的醇溶液中发生消去反应的是A. B.
C. D.
【答案】C
【解析】卤代烃能发生消去反应结构特点:与-X相连的碳原子的邻位碳原子上必须有氢原子。
A.CHCl与-X相连的碳原子的邻位碳原子上无氢原子,不能发生消去反应,故A错误;
3
B.与-Cl相连的碳原子的邻位碳原子上无氢原子,不能发生消去反应,故B错误;
C.与-Br相连的碳原子的邻位碳原子上有氢原子,能发生消去反应,故C正确;
D.与-Br相连的碳原子的邻位碳原子上没有氢原子,不能发生消去反应,故D错误。
故选:C。
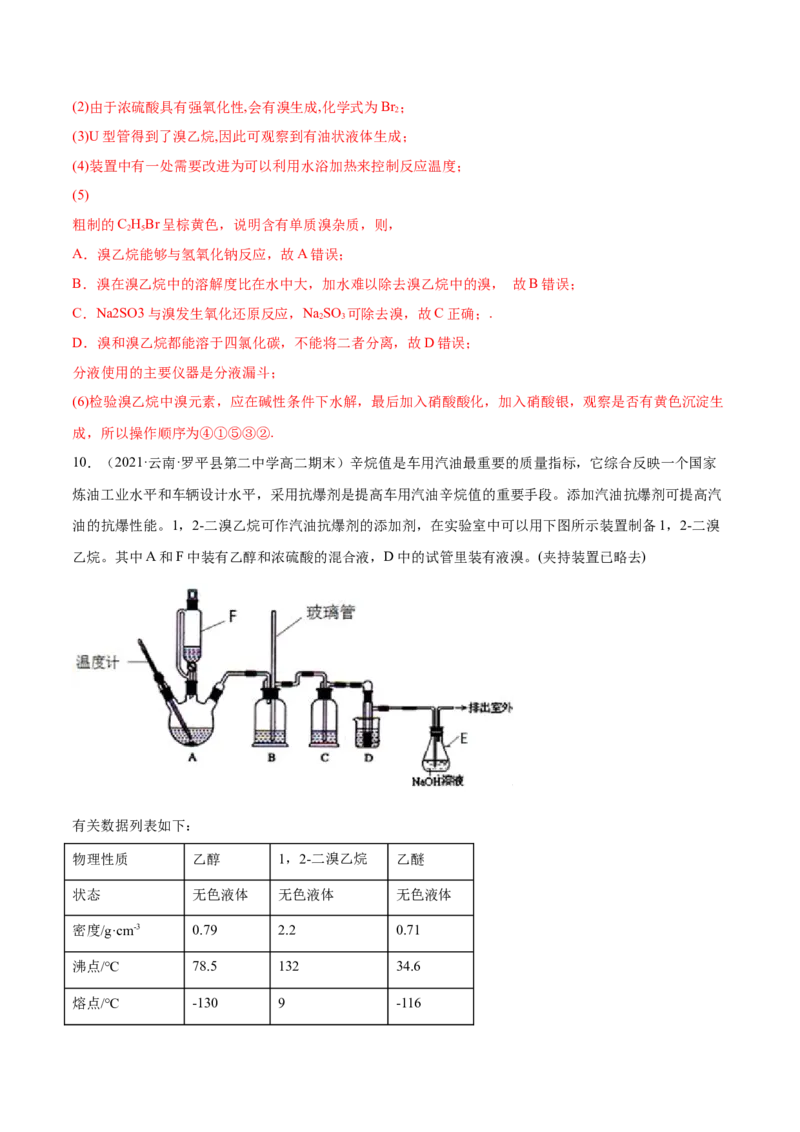
2.(2021·河北·石家庄市藁城区第九中学高二期中)能发生消去反应,生成物中存在同分异构体的是
A. B. C. D.CHBr
3
【答案】B
【解析】A.消去产物只有一种:CH=CHCH,故A不符合条件;
2 3
B.选项中物质为不对称结构,生成物中存在同分异构体,故B符合条件;
C.与-X相连的碳原子的相邻主链碳原子上没有H原子,故C不符合条件;
D.主链碳原子只有一个,故D不符合条件。
3.(2021·福建省南安市侨光中学高二期中)下列卤代烃既能发生消去反应生成烯烃,又能发生水解反应
生成醇的是
① ②CHCH(Br)CH ③CHF ④ ⑤(CH)CCHBr
3 3 3 3 3 2
⑥(CH)CHC(CH )Br
3 2 3 2
A.①③⑤ B.②④⑥ C.③④⑤ D.①②⑥
【答案】B【解析】①与氯原子相连接的碳原子的邻位碳上没有氢原子,所以不能发生消去反应,故①不符合题意;
②含有溴原子,并且与溴原子相连接的碳原子的邻位碳原子上含有氢原子,可以发生消去反应和水解反应,
故②符合题意;
③只有一个碳原子,不能发生消去反应,故③不符合题意;
④含有溴原子,并且与溴原子相连接的碳原子的邻位碳原子含有氢原子,可以发生消去反应和水解反应,
故④符合题意;
⑤与溴原子相连接的碳原子的邻位碳原子没有氢原子,不能发生消去反应,故⑤不符合题意;
⑥含有溴原子,并且与溴原子相连接的碳原子的邻位碳原子含有氢原子,可以发生消去反应和水解反应,
故⑥符合题意,所以②④⑥符合题意。
故A、C、D不符合题意,B符合题意。
故选:B。
4.(2021·辽宁·辽河油田第二高级中学高二阶段练习)下列卤代烃在 醇溶液中加热不反应的是
① ② ③ ④ ⑤
A.①③ B.②③⑤ C.②④ D.全部
【答案】A
【解析】① 中Cl与苯环相连,在 醇溶液中加热不能发生消去反应,①符合题意;
② 中与Cl相连的C的邻位C上有H,在 醇溶液中加热可以发生消去反应,②不符题
意;
③ 中与Cl相连的C的邻位C上没有H,在 醇溶液中加热不可以发生消去反应, ③
符合题意;
④ 中与Br、Cl相连的C的邻位C上有H,在 醇溶液中加热可以发生消去反应,④不符
题意;
⑤ 中与Cl相连的C的邻位C上有H,在 醇溶液中加热可以发生消去反应,⑤不符题意;
综上所述,符合题意的有①③,A满足题意;
答案选A。
5.(2021·江苏·涟水县第一中学高二阶段练习)2-溴丁烷在氢氧化钠的醇溶液中发生消去反应后的产物有几种
A.1 B.2 C.3 D.4
【答案】B
【解析】2-溴丁烷结构简式是 ,在该物质分子中Br原子连接的C原子有两种不同位置的H
原子,因此2-溴丁烷与NaOH的乙醇溶液共热,发生消去反应产生的有机物有CH=CHCHCH、
2 2 3
CHCH=CH-CH 两种不同结构,故合理选项是B。
3 3
6.(2021·河北·曹妃甸一中高二阶段练习)分子式为 的同分异构体中,不能发生消去反应的有
A.1种 B.2种 C.3种 D.4种
【答案】A
【解析】分子式为 C H Br 的有机物为卤代烃,不能发生消去反应的卤代烃的分子结构的特点是连接卤素
5 11
原子的碳原子的邻位碳原子上没有氢原子,分子式为 C H Br 的8种同分异构体中,不能发生消去反应的
5 11
只有(CH)CCHBr,故选A。
3 3 2
7.(2021·全国·高二课时练习)下列卤代烃在KOH醇溶液、加热条件下不能发生消去反应的是
①CHC≡CBr;② ;③(CH)CCHCl;④CHCl CHBr ;⑤ ;⑥CHCl
3 3 3 2 2 2 3
A.①③⑥ B.②③⑤ C.全部 D.②④
【答案】A
【解析】①溴原子所连碳原子的相邻碳原子上没有氢原子,因此该有机物不能发生消去反应,符合题意;
②氯原子所连碳原子的相邻碳原子上有氢原子,该有机物可以发生消去反应,不符合题意;
③该有机物的结构简式为 ,氯原子所连碳原子的相邻碳原子上没有氢原子,因此该有机物
不能发生消去反应,符合题意;
④氯、溴原子所连碳原子的相邻碳原子上均有氢原子,该有机物可以发生消去反应,不符合题意;
⑤溴原子所连碳原子的相邻碳原子上有氢原子,该有机物可以发生消去反应,不符合题意;
⑥ 没有邻位碳原子,不符合发生消去反应的条件,符合题意;
选A。7.(2021·全国·高二课时练习)已知乙烯能按下列反应流程进行一系列转化,其中属于消去反应的是
A.① B.② C.③ D.④
【答案】C
【解析】题给反应流程中①是加成反应;②是水解反应(取代反应);③是消去反应;④是氧化反应。故正
确答案为:C
题组四 卤族元素检验
1.(2021·江苏淮安·高二期中)能够证明某氯代烃中存在氯元素的操作及现象是
A.在氯代烃中直接加入稀硝酸酸化的AgNO 溶液,产生白色沉淀
3
B.加入NaOH的醇溶液,加热后加入稀硝酸酸化,然后加入AgNO 溶液,产生白色沉淀
3
C.加蒸馏水,充分搅拌后,加入AgNO 溶液,产生白色沉淀
3
D.加入NaOH溶液,加热后加入AgNO 溶液,产生白色沉淀
3
【答案】B
【解析】A.氯代烃中不含有氯离子,不能直接与稀硝酸酸化的硝酸银溶液反应产生白色沉淀,故A错误;
B.氯代烃在氢氧化钠醇溶液中共热发生消去反应生成氯化钠,加热后加入稀硝酸酸化排出氢氧根离子的
干扰,然后加入硝酸银溶液,产生白色沉淀说明该烃为氯代烃,故B正确;
C.氯代烃中不含有氯离子,不能直接与硝酸银溶液反应产生白色沉淀,则加入蒸馏水充分搅拌后,加入
硝酸银溶液不能产生白色沉淀,故C错误;
D.氯代烃在氢氧化钠溶液中共热发生水解反应生成氯化钠,溶液中的氢氧化钠会干扰氯离子的检验,加
热后加入硝酸银溶液不能产生白色沉淀,故D错误;故选B。
2.(2022·全国·高二专题练习)要检验某卤乙烷中的卤素是不是溴元素。正确的实验方法是
①加入氯水振荡,观察水层是否变为红棕色
②滴入 溶液,再加入稀硝酸,观察有无淡黄色沉淀生成
③加入 溶液共热,冷却后加入稀硝酸至溶液呈酸性,再滴入 溶液,观察有无淡黄色沉淀生成
④加入 的醇溶液共热,冷却后加入稀硝酸至溶液呈酸性,再滴入 溶液,观察有无淡黄色沉淀
生成
A.①③ B.②④ C.①② D.③④【答案】D
【解析】
①卤乙烷不能电离出卤离子,加入氯水振荡,卤乙烷与氯水不反应,水层没有颜色变化,不能检验某卤乙
烷中的卤素是不是溴元素,故错误;
②卤乙烷不能电离出卤离子,滴入硝酸银溶液,再加入稀硝酸,卤乙烷与硝酸银溶液不反应,不可能有淡
黄色沉淀生成,不能检验某卤乙烷中的卤素是不是溴元素,故错误;
③有机物分子中含有溴原子,能在氢氧化钠溶液中共热发生水解反应生成溴化钠,若加入氢氧化钠溶液共
热,冷却后加入稀硝酸至溶液呈酸性,再滴入硝酸银溶液,有淡黄色沉淀生成,说明卤乙烷中的卤素是溴
元素,若没有淡黄色沉淀生成,说明卤乙烷中的卤素不是溴元素,故正确;
④有机物分子中含有溴原子且与溴原子相连的碳原子的邻碳原子上不连有氢原子,能在氢氧化钠醇溶液中
共热发生消去反应生成溴化钠,若加入氢氧化钠醇溶液共热,冷却后加入稀硝酸至溶液呈酸性,再滴入硝
酸银溶液,有淡黄色沉淀生成,说明卤乙烷中的卤素是溴元素,若没有淡黄色沉淀生成,说明卤乙烷中的
卤素不是溴元素,故正确;
③④正确,故选D。
3.(2020·云南省下关第一中学高二阶段练习)为证明溴乙烷中溴元素的存在,现有以下操作:①加入硝
酸银溶液;②加入氢氧化钠溶液;③加热;④加入蒸馏水;⑤加入稀硝酸至溶液呈酸性;⑥加入氢氧化钠
的醇溶液,下列按一定顺序进行的操作步骤正确的是
A.⑥③①⑤ B.④③⑤① C.④⑥③① D.②③⑤①
【答案】D
【解析】证明溴乙烷中溴元素的存在,先发生②加入氢氧化钠溶液,然后③加热,发生水解反应生成
NaBr,再发生⑤加入稀硝酸至溶液呈酸性,最后①加入硝酸银溶液,生成淡黄色沉淀,则证明含溴元素,
即操作顺序为②③⑤①,故合理选项是D。
4.(2021·全国·高二期末)要检验某溴乙烷中的溴元素,正确的实验方法是
A.加入氯水振荡,观察水层是否有棕红色出现
B.滴入AgNO 溶液,再加入稀硝酸,观察有无浅黄色沉淀生成
3
C.加入NaOH溶液共热,然后加入稀硝酸使溶液呈酸性,再滴入AgNO 溶液,观察有无浅黄色沉淀生成
3
D.加入NaOH溶液共热,冷却后加入AgNO 溶液,观察有无浅黄色沉淀生成
3
【答案】C
【解析】A.在溴乙烷中溴元素以Br原子形式存在,不是Br-,加入氯水不能发生置换反应产生Br ,因此
2
不能观察到水层变为棕红色,A不符合题意;
B.在溴乙烷中溴元素以Br原子形式存在,不是Br-,因此加入AgNO 溶液丙再加入稀硝酸,不能观察到
3有浅黄色沉淀生成,B不符合题意;
C.在溴乙烷中溴元素以Br原子形式存在,向其中加入NaOH溶液共热,溴乙烷发生取代反应产生Br-,
然后加入稀硝酸溶液消耗溶液中的NaOH,使溶液呈酸性,再滴入AgNO 溶液,Ag+与溶液中的Br-反应产
3
生AgBr浅黄色沉淀,因此可以证明其中含有Br元素,C符合题意;
D.向溴乙烷中加入NaOH溶液共热,溴乙烷发生取代反应产生Br-,由于溶液中可能含有过量的NaOH,
OH-会与加入AgNO 溶液的Ag+变为AgOH沉淀,AgOH分解产生Ag O,也会观察到有浅黄色沉淀产生,
3 2
因而会影响Br元素的检验,D不符合题意;
故合理选项是C。
5.(2021·宁夏·平罗中学高二期中)为检验某卤代烃(R-X)中的卤元素,进行如下操作,正确的顺序是
①加热
②加入AgNO 溶液
3
③取少量该卤代烃
④加入足量稀硝酸酸化
⑤加入NaOH溶液⑥冷却
A.③①⑤⑥②④ B.③⑤①⑥④② C.③②①⑥④⑤ D.③⑤①⑥②④
【答案】B
【解析】检验卤代烃(R-X)中的X元素,先取少量卤代烃,卤代烃的水解需在碱性条件下,所以向卤代
烃中加入氢氧化钠溶液,然后进行加热加快反应速率,溶液冷却后,由于碱性条件下,氢氧根离子干扰银
离子与卤素的反应现象,所以应先向溶液中加入稀硝酸使溶液酸化,再加入硝酸银溶液观察是否生成沉淀,
所以正确的操作顺序为:③⑤①⑥④②,故选:B。
6.(2021·河北·张家口市第一中学高二阶段练习)下列过程最终能得到白色沉淀的是
A.C HCl中加入硝酸酸化的AgNO 溶液
2 5 3
B.NH Cl中加入硝酸酸化的AgNO 溶液
4 3
C.KClO 中加入硝酸酸化的AgNO 溶液
3 3
D.C HCl与过量NaOH醇溶液共热后加入AgNO 溶液
2 5 3
【答案】B
【解析】A.C HCl分子中是氯原子,该有机物难溶于水,不电离,所以不会有白色沉淀产生,描述错误,
2 5
不符题意;
B.NH Cl溶于水可电离出 和Cl-,所以溶液中会出现白色沉淀,描述正确,符合题意;
4
C.KClO 溶于水会电离出K+和 ,没有Cl-,所以溶液中不会出现白色沉淀,描述错误,不符题意;
3D.C HCl在醇溶液中与过量NaOH反应会生成Cl-,但是溶液未经稀硝酸酸化,有剩余NaOH,故溶液中
2 5
会出现AgCl白色沉淀及Ag O黑色沉淀,描述错误,不符题意;
2
综上,本题选B。
7.(2021·辽宁葫芦岛·高二阶段练习)下列关于甲、乙、丙、丁四种有机物的说法正确的是
甲:CHCl 乙:CH-CHBr-CH 丙:CH-C(CH)-CHCl 丁:
3 3 3 3 3 2 2
A.甲、乙、丙、丁中分别滴入AgNO 溶液,均有沉淀生成
3
B.甲、乙、丙、丁中分别加入NaOH的醇溶液,共热,然后加入稀硝酸至溶液呈酸性,再滴入AgNO 溶
3
液,均有沉淀生成
C.丙发生消去反应生成2, 二甲基丙烯
D.甲、乙、丙、丁中分别加入NaOH的水溶液,共热,然后加入稀硝酸至溶液呈酸性,再滴入AgNO 溶
3
液,均有沉淀生成
【答案】D
【解析】A.卤代烃和硝酸银不反应,甲、乙、丙、丁中分别滴入AgNO 溶液,均没有沉淀生成,故A错误;
3
B.甲、丙、丁不能发生消去反应生成HX,所以甲、丙、丁和氢氧化钠的醇溶液共热后,再加入HNO 酸化
3
的AgNO 溶液不能生成沉淀,故B错误;
3
C.丙不能发生消去反应生成烯烃,故C错误;
D.卤代烃和NaOH的水溶液发生取代反应生成NaX,检验卤素离子,应在酸性条件下,因此加入稀硝酸至
溶液呈酸性,再滴入AgNO 溶液,均有沉淀生成,故D正确;
3
故选D。
8.(2022浙江)某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
NaBr+HSO HBr+NaHSO CHCHOH+HBr CHCHBr+HO
2 4 4 3 2 3 2 2
化学兴趣小组根据实验原理设计如图装置。根据题意完成下列填空,有关数据列表如下:
乙醇 溴乙烷无色液
状态 无色液体
体
密度/g · cm-3 0.8 1.4
沸点/℃ 78.5 119.0
熔点/℃ -l30 38.4
(1)配制体积比2:1的硫酸所用的仪器为___________(选填编号)
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶 e.滴定管
(2)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第
___________层;
(3)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质应加入___________(选填编号)
然后再进行___________一步操作即可,反应时生成的液态有机副产物可能是___________(写结构简式)。
a.无水氯化钙 b.硝酸银溶液 c.四氯化碳 d.亚硫酸钠溶液
(4)实验过程中,同学发现仪器连接部分有漏气现象,老师建议把上述装置中的仪器连接部分都改成标准玻
璃接口,其原因是:___________。
【答案】(1)abc
(2)3
(3) d 分液 C HOC H 或CHBrCHBr
2 5 2 5 2 2
(4)反应产生的溴单质会腐蚀橡胶
【解析】
(1)配制体积比2:1的硫酸所用的仪器有烧杯、玻璃棒和量筒,故答案为abc;
(2)生成的溴乙烷和水互不相溶,并且溴乙烷的密度比水大,在冰水混合物的下层,故答案为:3;
(3)试管A中获得的有机物呈棕黄色,是由于浓硫酸具有强氧化性,将HBr氧化物Br ,产物为溴乙烷,混
2
有单质溴,蒸馏不能完全除去杂质,并且操作麻烦,氢氧化钠溶液易使溴乙烷水解,四氯化碳会引入新的
杂质,而亚硫酸钠和溴发生氧化还原反应生成HBr和硫酸钠,易与溴乙烷分离,两者分层,用分液的方法
分离,在浓硫酸并加热的条件下乙醇可能发生分子间脱水生成乙醚,也可能发生分子内脱水生成乙烯,乙
烯与单质溴会发生加成反应,所以反应时生成的液态有机副产物可能是C HOC H 或CHBrCHBr,故答
2 5 2 5 2 2
案为:d;分液;C HOC H 或CHBrCHBr;
2 5 2 5 2 2
(4)浓硫酸具有强氧化性,将HBr氧化为Br ,生成的Br 具有强氧化性,会腐蚀橡胶,应用玻璃导管,故答
2 2
案为:反应产生的溴单质会腐蚀橡胶。
9.(2021·广东·广州市培正中学高二期中)实验室制备溴乙烷(C HBr)的装置和步骤如图(已知溴乙烷的沸
2 5
点38.4℃):①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水:
②在圆底烧瓶中加入10 ml 95%乙醇.28mL 78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热。使其充分反应。
回答下列问题:
(1)该实验制取溴乙烷分为两步,分别写出这两步的化学方程式_______
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为_______
(3)U形管内可观察到的现象是_______
(4)装置中有一处需要改进:_______
(5)反应结束后,U形管内粗制的C HBr呈棕黄色。为了除去粗产品中的杂质,最好选择下列试剂中的
2 5
_______(填序号)。除杂过程所需的主要玻璃仪器为_______
A.NaOH 溶液 B.HO C.NaSO 溶液 D.CCl
2 2 3 4
(6)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后
_______(填代号)。
①加热:②加入AgNO 溶液;③加入稀HNO 酸化:④加入NaOH溶液: ⑤冷却
3 3
【答案】(1)NaBr+ H SO (浓) NaHSO+HBr,HBr+C HOH C HBr+H O ;
2 4 4 2 5 2 5 2
(2)Br ;
2
(3)油状物生成;
(4)利用水浴加热来控制反应温度
(5) C; 分液漏斗;
(6)④①⑤③②;
【解析】(1)溴化钠、浓硫酸和乙醇制取溴乙烷的化学方程式为NaBr+ H SO (浓) NaHSO+HBr,
2 4 4
HBr+C HOH C HBr+H O ;
2 5 2 5 2(2)由于浓硫酸具有强氧化性,会有溴生成,化学式为Br ;
2
(3)U型管得到了溴乙烷,因此可观察到有油状液体生成;
(4)装置中有一处需要改进为可以利用水浴加热来控制反应温度;
(5)
粗制的C HBr呈棕黄色,说明含有单质溴杂质,则,
2 5
A.溴乙烷能够与氢氧化钠反应,故A错误;
B.溴在溴乙烷中的溶解度比在水中大,加水难以除去溴乙烷中的溴, 故B错误;
C.Na2SO3与溴发生氧化还原反应,NaSO 可除去溴,故C正确;.
2 3
D.溴和溴乙烷都能溶于四氯化碳,不能将二者分离,故D错误;
分液使用的主要仪器是分液漏斗;
(6)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生
成,所以操作顺序为④①⑤③②.
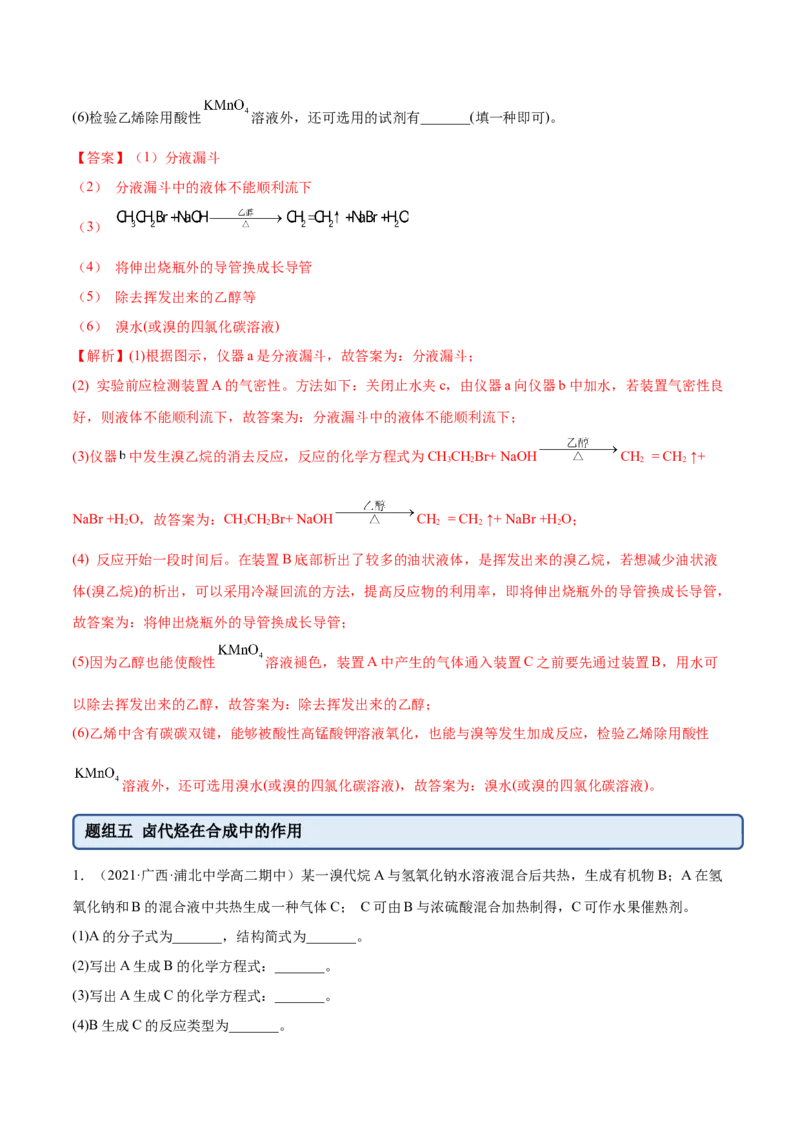
10.(2021·云南·罗平县第二中学高二期末)辛烷值是车用汽油最重要的质量指标,它综合反映一个国家
炼油工业水平和车辆设计水平,采用抗爆剂是提高车用汽油辛烷值的重要手段。添加汽油抗爆剂可提高汽
油的抗爆性能。1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2-二溴
乙烷。其中A和F中装有乙醇和浓硫酸的混合液,D中的试管里装有液溴。(夹持装置已略去)
有关数据列表如下:
物理性质 乙醇 1,2-二溴乙烷 乙醚
状态 无色液体 无色液体 无色液体
密度/g·cm-3 0.79 2.2 0.71
沸点/℃ 78.5 132 34.6
熔点/℃ -130 9 -116填写下列空白:
(1)仪器F的名称为:___________,A中主要反应的化学方程式:___________。
(2)安全瓶B可以防止倒吸,并可以检查实验进行时导管是否发生堵塞。请写出发生堵塞时瓶B中的现象
___________。
(3)在装置C中应加入___________(填字母),其目的是吸收反应中可能生成的杂质气体:A.水 B.碱石
灰 C.氢氧化钠溶液 D.饱和亚硫酸氢钠溶液
(4)容器E中NaOH溶液的作用是___________。
(5)若产物中有少量副产物乙醚。可用___________(填操作名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又
不能过度冷却(如用冰水),其原因是___________。
(7)检验1,2-二溴乙烷中溴元素:取少量1,2-二溴乙烷,然后___________(按正确的操作顺序填序号)。
①加热;②加入AgNO 溶液;③加入稀HNO 酸化;④冷却;⑤加入NaOH溶液
3 3
【答案】(1) 恒压分液漏斗 CHCHOH CH=CH ↑+H O
3 2 2 2 2
(2)b中水面会下降,玻璃管中的水柱会上升,甚至溢出
(3)C
(4)吸收挥发出来的溴,防止污染环境
(5)蒸馏
(6)1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞
(7)⑤①④③②
【解析】(1)根据仪器构造可判断仪器F的名称为恒压分液漏斗,A中主要发生的是乙醇在浓硫酸、170℃
条件下发生消去反应生成乙烯,反应方程式为:CHCHOH CH=CH ↑+H O;
3 2 2 2 2
(2)当导管堵塞时,B中压强增大,将水压入直玻璃管中,玻璃管中水柱会上升,甚至溢出玻璃管,B中水
面会下降;
(3)乙烯中可能含有的杂质气体有二氧化碳、二氧化硫,装置C中溶液可以吸收二氧化碳、二氧化硫,因此
是NaOH溶液,故答案为:C;
(4)D中反应后尾气中含有挥发出的溴等,直接排放会污染大气,装置E中氢氧化钠溶液的作用是:吸收挥
发出来的溴,防止污染环境;
(5)1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离;
(6)冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞,故不能过度冷却(如用冰水);
(7)检验1,2-二溴乙烷中溴元素,需要首先水解,然后酸化,即取少量1,2-二溴乙烷,然后加入NaOH溶
液、加热、冷却、加入稀HNO 酸化、加入AgNO 溶液,即正确的操作顺序为⑤①④③②。
3 3
11.(2021·广东·广州市为明学校高二阶段练习)某兴趣小组在实验室用加热乙醇、浓硫酸、溴化钠和少
量水的混合物来制备溴乙烷,检验反应的部分副产物,并探究溴乙烷的性质。
(一)溴乙烷的制备及产物的检验:装置如图1,其中夹持仪器、加热仪器及冷却水管没有画出。请根据实验
步骤,回答下列问题:
(1)关闭活塞a,将上述物质加入仪器A中,还需加入__。浓硫酸的作用是_(用化学方程式表示)。
(2)上述反应的副产物可能有:乙醚(CHCH—O—CH CH)、乙烯、溴化氢等。
3 2 2 3
①检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子,打开a,利用余热继续反应
直至冷却,通过B、C装置检验。B、C中应盛放的试剂分别是____、____(填编号)
a.苯 b.水 c.NaOH溶液 d.硝酸银溶液
②检验副产物中是否含有乙醚:通过红外光谱仪鉴定所得产物中含有“—CHCH”基团,来确定副产物中
2 3
存在乙醚。该方法____(填“是”或“否”)合理,原因是____。
(3)加热片刻后,A中的混合物出现橙红色,该橙红色物质可能是____,欲除去溴乙烷中的该杂质,方法正
确的是____(填编号)
a.用KI溶液洗涤 b.用水洗涤 c.用CCl 萃取 d.用亚硫酸钠溶液洗涤
4
(二)溴乙烷性质的探究:用如图2实验装置(铁架台、酒精灯等未画出)来探究溴乙烷的性质。\
(4)在试管中加入10mL6mol/LNaOH水溶液和5mL溴乙烷,振荡,水浴加热,当观察到的现象为___时,表
明溴乙烷与NaOH水溶液已完全反应,该反应的化学方程式为____;
(5)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,将生成的气体通入如图3装置。A试管中水的作
用是__,若无A试管,B试管中的试剂应为____。
【答案】(1)沸石(或碎瓷片) CH CHOH CH=CH +H O、2NaBr+HSO (浓)
3 2 2 2 2 2 4
2HBr+Na SO
2 4
(2)① a d 否 溴乙烷中也含有乙基
(3) Br d
2
(4)液体不分层 CHCHBr+NaOH CHCHOH+NaBr
3 2 3 2
(5)吸收挥发出的乙醇 溴水(或溴的四氯化碳溶液)
【解析】(一)(1)该反应中反应物大部分为液态,所需温度高于某些液体的沸点,所以还需要加入沸石(或碎
瓷片)防止暴沸;乙醇在浓硫酸加热的条件下发生消去反应生成乙烯,化学方程式为CHCHOH
3 2
CH=CH +H O,同时还能和溴化钠得到HBr:2NaBr+HSO (浓) 2HBr+Na SO ;
2 2 2 2 4 2 4
(2)①由于浓硫酸具有强氧化性,能将溴离子氧化为Br ,而Br 会对HBr的检验造成影响,所以应先用苯吸
2 2
收生成溴单质,然后再通入硝酸银溶液中,若生成淡黄色沉淀,则有HBr生成,所以B、C中盛放的试剂
分别为a、d;
②由于溴乙烷中也含有-CHCH 基团,所以该方法不合理,无法鉴别乙醚;
2 3
(3)浓硫酸具有强氧化性,能将溴离子氧化为Br ,所以该橙红色物质可能是Br ;
2 2
a.KI虽然能和溴反应,但生成的碘单质会成为新的杂质,a不符合题意;b.溴在水中的溶解度较小,无法水洗除去,b不符合题意;
c.溴乙烷同样会溶解在四氯化碳中,c不符合题意;
d.溴单质可以和亚硫酸钠溶液发生氧化还原反应,生成易溶于水的盐,而溴乙烷不反应,且难溶于水,
所以可以除去杂质溴,d符合题意;
综上所述答案为d;
(二)(4)溴乙烷在NaOH水溶液中加热水解生成乙醇,溴乙烷不溶于水,和水混合时溶液分层,水解产物易
溶于水而和水混合时不分层,所以观察到液体不分层现象时,表明溴乙烷与NaOH溶液已完全反应,化学
方程式为CHCHBr+NaOH CHCHOH+NaBr;
3 2 3 2
(5)若溴乙烷在NaOH乙醇溶液中发生的是消去反应,则生成乙烯和NaBr,挥发出的乙醇也可以是酸性高
锰酸钾溶液,所以先用水将其吸收,然后再通入酸性高锰酸钾溶液;若无A试管,乙烯可以和溴水发生加
成反应使其褪色,而乙醇不行,所以试管B中试剂应为溴水(或溴的四氯化碳溶液)。
12.(2021·西藏·拉萨中学高二阶段练习)已知溴乙烷( )是无色液体,其沸点为 ,密度比水
的大,难溶于水,可溶于多种有机溶剂。有人设计了如图所示的装置,并用酸性 溶液来检验生成
的气体是否为乙烯。请回答下列问题:
(1)仪器a的名称为_______。
(2)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若_______,则证
明装置A不漏气。
(3)仪器b中发生反应的化学方程式为_______。
(4)反应开始一段时间后。在装置B底部析出了较多的油状液体,若想减少油状液体的析出,可对装置A作
何改进?_______。
(5)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为_______。(6)检验乙烯除用酸性 溶液外,还可选用的试剂有_______(填一种即可)。
【答案】(1)分液漏斗
(2) 分液漏斗中的液体不能顺利流下
(3)
(4) 将伸出烧瓶外的导管换成长导管
(5) 除去挥发出来的乙醇等
(6) 溴水(或溴的四氯化碳溶液)
【解析】(1)根据图示,仪器a是分液漏斗,故答案为:分液漏斗;
(2) 实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若装置气密性良
好,则液体不能顺利流下,故答案为:分液漏斗中的液体不能顺利流下;
(3)仪器 中发生溴乙烷的消去反应,反应的化学方程式为CHCHBr+ NaOH CH = CH ↑+
3 2 2 2
NaBr +H O,故答案为:CHCHBr+ NaOH CH = CH ↑+ NaBr +H O;
2 3 2 2 2 2
(4) 反应开始一段时间后。在装置B底部析出了较多的油状液体,是挥发出来的溴乙烷,若想减少油状液
体(溴乙烷)的析出,可以采用冷凝回流的方法,提高反应物的利用率,即将伸出烧瓶外的导管换成长导管,
故答案为:将伸出烧瓶外的导管换成长导管;
(5)因为乙醇也能使酸性 溶液褪色,装置A中产生的气体通入装置C之前要先通过装置B,用水可
以除去挥发出来的乙醇,故答案为:除去挥发出来的乙醇;
(6)乙烯中含有碳碳双键,能够被酸性高锰酸钾溶液氧化,也能与溴等发生加成反应,检验乙烯除用酸性
溶液外,还可选用溴水(或溴的四氯化碳溶液),故答案为:溴水(或溴的四氯化碳溶液)。
题组五 卤代烃在合成中的作用
1.(2021·广西·浦北中学高二期中)某一溴代烷A与氢氧化钠水溶液混合后共热,生成有机物B;A在氢
氧化钠和B的混合液中共热生成一种气体C; C可由B与浓硫酸混合加热制得,C可作水果催熟剂。
(1)A的分子式为_______,结构简式为_______。
(2)写出A生成B的化学方程式:_______。
(3)写出A生成C的化学方程式:_______。
(4)B生成C的反应类型为_______。【答案】(1) C HBr CH CHBr
2 5 3 2
(2)CH CHBr+NaOH CHCHOH+ NaBr
3 2 3 2
(3)CH CHBr +NaOH CH =CH ↑+NaBr+H O
3 2 2 2 2
(4)消去反应
【解析】(1)据分析,A为溴乙烷、分子式为C HBr,结构简式为CHCHBr。
2 5 3 2
(2)A生成B 即加热下CHCHBr在NaOH水溶液中发生水解反应得到CHCHOH和 NaBr,化学方程式:
3 2 3 2
CHCHBr+NaOH CHCHOH+ NaBr。
3 2 3 2
(3)A生成C 即加热下CHCHBr 在NaOH乙醇溶液中发生消去反应生成 CH =CH 、NaBr和HO,化学
3 2 2 2 2
方程式:CHCHBr +NaOH CH =CH ↑+NaBr+H O。
3 2 2 2 2
(4)B生成C即乙醇在浓硫酸迅速加热到170°C时发生反应生成乙烯和水,反应类型为消去反应。
2.(2021·全国·高二课时练习)卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,
请回答下列问题:
Ⅰ.氟利昂 ,即二氟二氯甲烷,分子式为 ,氟利昂 ,即一氟三氯甲烷,分子式为 。氟
利昂是破坏臭氧层的元凶,也是地球变暖的罪魁祸首,它所产生的温室效应是二氧化碳的数千倍。禁止使
用氟利昂对保护地球环境具有极为重要的意义。 破坏臭氧层的机理为 ;
; 。
(1)活性氯( )的作用是___________。
(2)下列关于氟利昂 ( )、氟利昂 ( )的推测不正确的有___________。
A.两种氟利昂在 醇溶液中均可发生消去反应
B.两种氟利昂均不存在同分异构体
C.直接用 溶液均可检验两种氟利昂中的氯元素
Ⅱ.已知二氯烯丹是一种除草剂,其合成路线如下:(二氯烯丹)
已知: 在反应⑤中所生成的E的结构只有一种。
(3)写出下列反应类型:反应①是___________,反应③是___________,反应⑥是___________。
(4)写出下列物质的结构简式:A___________,E___________。
(5)写出反应③的化学方程式:___________。
(6)写出有机物 所有同分异构体的结构简式:___________。
【答案】(1)作催化剂
(2) AC
(3) 取代反应 消去反应 取代反应
(4)
(5)
(6) 、 、 、
【解析】I.(1)第一步反应产生的活性氯( )导致后续反应发生,且最后又产生活性氯( ),可见活性氯(
)在反应中起催化作用。
(2)A项,这两种氟利昂分子中均只有一个 原子,在 醇溶液中均不能发生消去反应,错误。C项,
氟利昂分子不能电离出 ,不能直接用 溶液检验,错误。甲烷是正四面体结构,所以两种氟利昂
均不存在同分异构体,B正确,故选AC。
Ⅱ.此题突破口在B与氯气加成得到 ,从而逆向推出B为 、A为
。 通过反应③得到C。反应⑥为E与 发生取代反应而得到二氯烯丹,故E为 ,D的消去产物E只有一种结构,所以D为
,再进一步联系反应③,可推知C为 。
(1)反应①是A和氯气在高温下的取代反应,反应③是卤代烃在NaOH醇溶液中的消去反应,反应⑥是E中
的CH 上的Cl被 取代了,是取代反应。
2
(2)由以上分析可知,A为 ,E为 。
(3)反应③是消去反应,从CHCl-CHCl-CH Cl中消去一个小分子,生成不饱和化合物,化学方程式为:
2 2
。
(4)CH ClCHClCH Cl的同分异构体即为丙烷分子中的3个氢原子被氯原子代替,3个氯原子可以取代一个
2 2
碳原子上的三个氢原子,也可以一个碳原子上的2个氢原子被取代,另一个碳原子上的1个氢原子被取代,
共有4种: 、 、 、 。
2.(2021·宁夏·中宁县中宁中学高二阶段练习)根据下面的反应路线及所给信息,回答下列问题:
(1)有机物A为异丁烷,则A的结构简式是___。
(2)B和C均为一氯代烃,B的名称(系统命名)为___。
(3)E的一个同分异构体的结构简式是___。
(4)①、②、③的反应类型依次是___、___、___。
(5)写出②、③反应的化学方程式:___、___。
【答案】(1)CHCH(CH )CH
3 3 3
(2)2-甲基-1-氯丙烷
(3) CHBrCH(CH)CHBr
2 3 2
(4) 消去反应 加成反应 取代反应(5) CH=C(CH )+Br →CHBrCBr(CH ) CH BrCBr(CH )+2NaOH CHOHCOH(CH )+2NaBr
2 3 2 2 2 3 2 2 3 2 2 3 2
【解析】(1)异丁烷 A的结构简式是CHCH(CH )CH;
3 3 3
(2)B和C均为一氯代烃,取代后的产物为2-甲基-1-氯丙烷和2-甲基-2-氯丙烷,B的名称为2-甲基-1-氯丙
烷;
(3)E为CHBrCBr(CH ),E的同分异构体的结构简式是CHBrCH(CH )CHBr、CHBr CH(CH )、
2 3 2 2 3 2 2 3 2
CHBrCHBrCH CH、CHBrCHCHBrCH 、CHBrCHCHCHBr、CHBr CHCHCH、CHCBr CHCH、
2 2 3 2 2 3 2 2 2 2 2 2 2 3 3 2 2 3
CHCHBrCHBrCH ,同分异构体的结构简式是CHBrCH(CH )CHBr;
3 3 2 3 2
(4)①、②、③的反应类型依次是消去反应、加成反应、取代反应;
(5) 反应②的化学方程式为CH=C(CH )+Br →CHBrCBr(CH ),反应③的化学方程式为
2 3 2 2 2 3 2
CHBrCBr(CH )+2NaOH CHOHCOH(CH )+2NaBr。
2 3 2 2 3 2
3.(2022·重庆市)烯烃A在一定条件下可以按如图所示进行反应。
已知:CHCHCHCHCHCHBr CHCHCHCHCH=CH [D是 , 和
3 2 2 2 2 2 3 2 2 2 2
互为同分异构体, 和 互为同分异构体。]
(1)A的结构简式是___________ 。
(2)框图中属于取代反应的是(填数字代号)___________ 。
(3)框图中①、③、⑥属于___________ 反应。
(4)G 的结构简式是___________ 。
1
(5) 的化学反应方程式 ___________。(6)上述10种化合物中,属于二烯烃的是 ___________(填符号)。
【答案】(1)(CH)C=C(CH)
3 2 3 2
(2) ②
(3) 加成反应;
(4)
(5) CH=C(CH)C(CH)=CH +Br →CHBrCBr(CH)C(CH)=CH ;
2 3 3 2 2 2 3 3 2
(6) A、E
【解析】由D可知A为(CH)C=C(CH),E为CH=C(CH)C(CH)=CH ,则B为(CH)
3 2 3 2 2 3 3 2 3
CHCH(CH),C为(CH)CHCBr(CH),CH=C(CH)C(CH)=CH 可与溴发生1,2加成或
2 3 2 3 2 3 2 2 3 3 2
1,4加成,且F 可F 都可生成G,则F 为CHBrC(CH)=C(CH)CHBr,F 为CHBrCBr(CH)C
1 2 1 1 2 3 3 2 2 2 3
(CH)=CH ,G 为 ,G 为CHBrCBr(CH)CBr(CH)CH,
3 2 1 2 2 3 3 3
(1)由以上分析可知A为(CH)C=C(CH), 故答案为:(CH)C=C(CH);
3 2 3 2 3 2 3 2
(2)反应②为B在光照条件下与溴发生取代反应,故答案为:②;
(3)反应①为加成反应,②为取代反应,③为加成反应,④为加成反应,⑤为消去反应,⑥为加成反应,
⑦为加成反应,⑧为加成反应,故答案为:加成反应;
(4)由分析可知G 为 ,故答案为: ;
1
(5)E→F 发生的是1,2加成,其化学反应方程式为CH=C(CH)C(CH)=CH +Br →CHBrCBr
2 2 3 3 2 2 2
(CH)C(CH)=CH ,属于加成反应;故答案为:CH=C(CH)C(CH)=CH +Br →CHBrCBr
3 3 2 2 3 3 2 2 2
(CH)C(CH)=CH ;
3 3 2
(6)由分析的结构简式可知A为(CH)C=C(CH),E为CH=C(CH)C(CH)=CH ,所以属于
3 2 3 2 2 3 3 2
二烯烃的是A、E,故答案为:A、E,
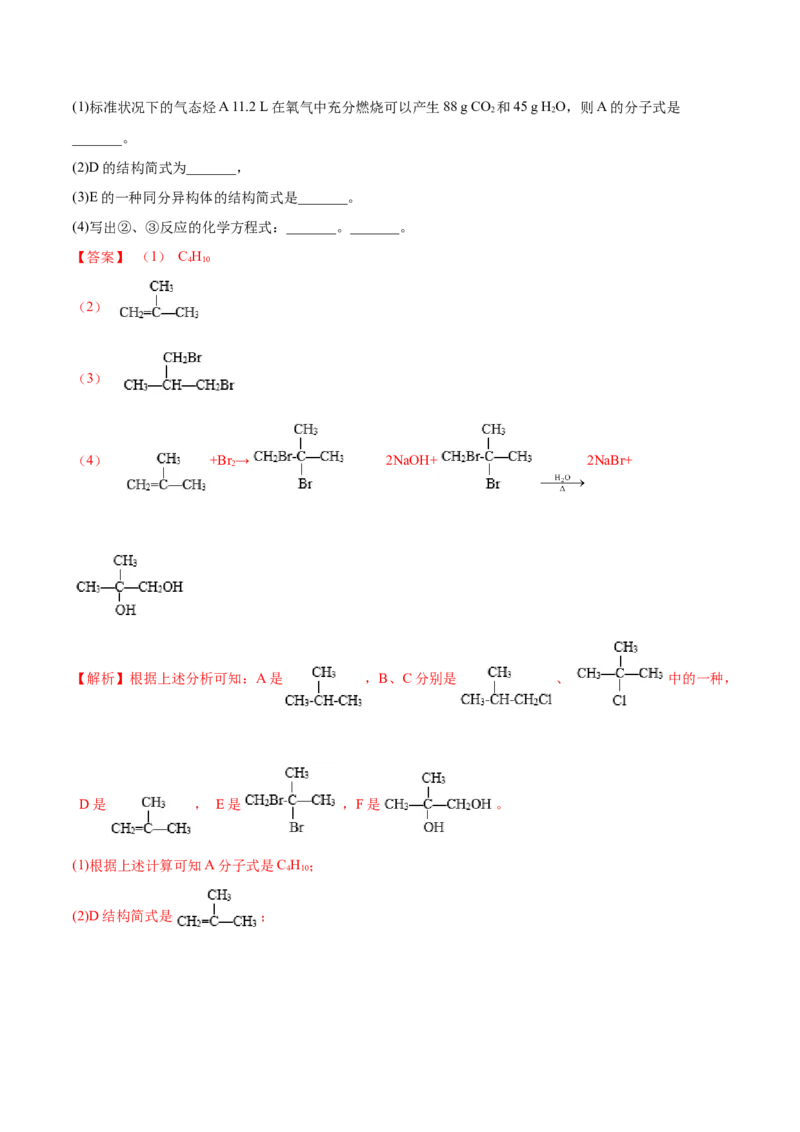
3.(2021·江苏·涟水县第一中学高二阶段练习)根据图中的反应路线及所给信息,回答下列问题:(1)标准状况下的气态烃A 11.2 L在氧气中充分燃烧可以产生88 g CO 和45 g HO,则A的分子式是
2 2
_______。
(2)D的结构简式为_______,
(3)E的一种同分异构体的结构简式是_______。
(4)写出②、③反应的化学方程式:_______。_______。
【答案】 (1) C H
4 10
(2)
(3)
(4) +Br → 2NaOH+ 2NaBr+
2
【解析】根据上述分析可知:A是 ,B、C分别是 、 中的一种,
D是 , E是 ,F是 。
(1)根据上述计算可知A分子式是C H ;
4 10
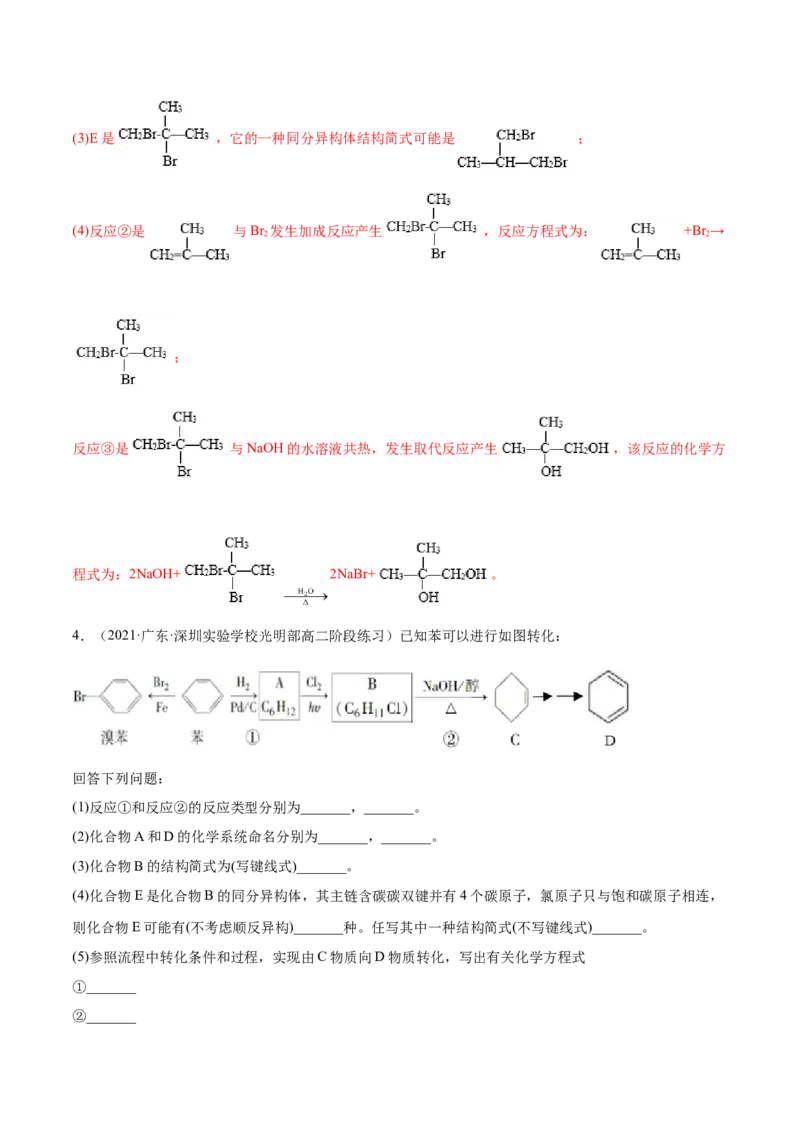
(2)D结构简式是 ;(3)E是 ,它的一种同分异构体结构简式可能是 ;
(4)反应②是 与Br 发生加成反应产生 ,反应方程式为: +Br →
2 2
;
反应③是 与NaOH的水溶液共热,发生取代反应产生 ,该反应的化学方
程式为:2NaOH+ 2NaBr+ 。
4.(2021·广东·深圳实验学校光明部高二阶段练习)已知苯可以进行如图转化:
回答下列问题:
(1)反应①和反应②的反应类型分别为_______,_______。
(2)化合物A和D的化学系统命名分别为_______,_______。
(3)化合物B的结构简式为(写键线式)_______。
(4)化合物E是化合物B的同分异构体,其主链含碳碳双键并有4个碳原子,氯原子只与饱和碳原子相连,
则化合物E可能有(不考虑顺反异构)_______种。任写其中一种结构简式(不写键线式)_______。
(5)参照流程中转化条件和过程,实现由C物质向D物质转化,写出有关化学方程式
①_______
②_______【答案】 (1) 加成反应或还原反应 消去反应
(2) 环己烷 1,3-环己二烯
(3)
(4) 7 CH =CHC(CH )CHCl
2 3 2 2
(5) +Cl→ +2NaOH 2NaCl+2H O+
2 2
【解析】(1)反应①和反应②的反应类型分别为加成反应,消去反应。
(2)化合物A (C H )的结构简式为 ,D的结构简式为 ,化学系统命名分别为,环己烷、1,3-
6 12
环己二烯。
(3) 与氯气发生取代反应生成化合物B,B的结构简式为 。
(4)化合物E是化合物B的同分异构体,其主链含碳碳双键并有4个碳原子,氯原子只与饱和碳原子相连,
则化合物E可能有(不考虑顺反异构) :CH=CHC(CH )CHCl、CH=C(CH Cl)CH(CH )、
2 3 2 2 2 2 3 2
CH=C(CH )CCl(CH )、CH=C(CH )CH(CH )CHCl、(CH)C =C (CH ) CH Cl、CH=C(CH CH)CHClCH 、
2 3 3 2 2 3 3 2 3 2 3 2 2 2 3 3
CH=C(CH CH)CHCHCl。
2 2 3 2 2
(5)参照流程中转化条件和过程,实现由C物质向D物质转化,写出有关化学方程式
① +Cl→ 。
2
② +2NaOH 2NaCl+2H O+ 。
2