文档内容
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
一、物质的聚集状态
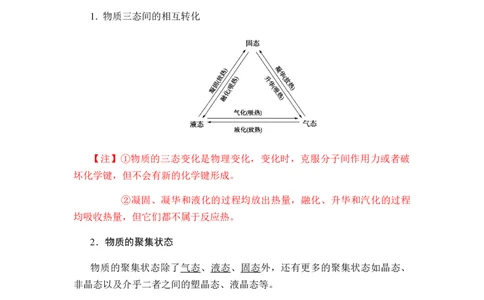
1. 物质三态间的相互转化
【注】①物质的三态变化是物理变化,变化时,克服分子间作用力或者破
坏化学键,但不会有新的化学键形成。
②凝固、凝华和液化的过程均放出热量,融化、升华和汽化的过程
均吸收热量,但它们都不属于反应热。
2.物质的聚集状态
物质的聚集状态除了气态、液态、固态外,还有更多的聚集状态如晶态、
非晶态以及介乎二者之间的塑晶态、液晶态等。
【拓展】
1.等离子体
①概念:由电子、阳离子和电中性粒子(分子或原子)组成的整体上电
中性的气态物质。
②是一种特殊的气体,存在于我们周围。③存在:日光灯和霓虹灯的灯管里、蜡烛火焰里、极光和雷电里。
2.液晶:介于液态和晶态之间的物质状态。
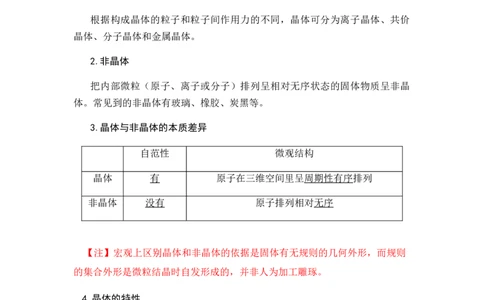
二、晶体与非晶体
1.晶体
把内部微粒(原子、离子或分子)在三维空间里呈周期性有序排列的固体
物质称为晶体。常见晶体有食盐、冰、铁、铜等。
根据构成晶体的粒子和粒子间作用力的不同,晶体可分为离子晶体、共价
晶体、分子晶体和金属晶体。
2.非晶体
把内部微粒(原子、离子或分子)排列呈相对无序状态的固体物质呈非晶
体。常见到的非晶体有玻璃、橡胶、炭黑等。
3.晶体与非晶体的本质差异
自范性 微观结构
晶体 有 原子在三维空间里呈周期性有序排列
非晶体 没有 原子排列相对无序
【注】宏观上区别晶体和非晶体的依据是固体有无规则的几何外形,而规则
的集合外形是微粒结晶时自发形成的,并非人为加工雕琢。
4.晶体的特性
(1)自范性
①定义:晶体能自发地呈现多面体外形的性质。
②形成条件:晶体生长的速率适当。
③本质原因:晶体中粒子在微观空间里呈现周期性有序排列。
(2)各向异性:晶体的某些物理性质在不同方向上的差异。(3)晶体有固定的熔点。
(4)外形和内部质点排列的高度有序性。
(5)X射线衍射:晶体能使X射线衍射,而非晶体对X射线只能产生散射。
【注】非晶体排列相对无序,无自范性、无各向异性、无固定熔点。
5.获得晶体的途径
(1)熔融态物质凝固。
①凝固速率适当,可得到规则晶体。
②凝固速率过快,得到没有规则外形的块状固体或看不到多面体外形粉
末。
(2)气态物质冷却不经液态直接凝固(凝华)。
(3)溶质从溶液中析出。
三、晶胞
1.概念:晶胞是描述晶体结构的基本单元。晶胞是晶体中最小的重复结构
单元。
2.结构:常规的晶胞都是平行六面体,晶体可以看作是数量巨大的晶胞无
隙并置而成。
(1)“无隙”:相邻晶胞之间没有任何间隙。
(2)“并置”:所有晶胞都是平行排列的,取向相同。
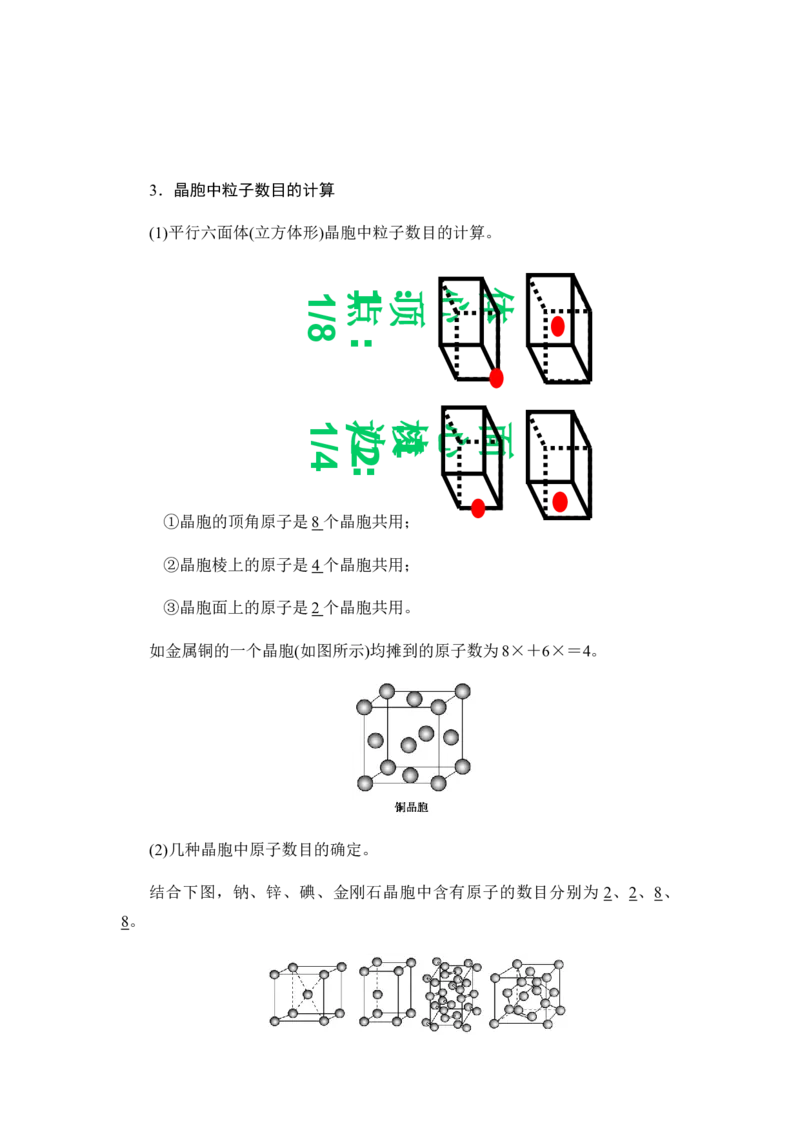
(3)所有晶胞的形状及其内部的原子种类、个数及几何排列是完全相同的。3.晶胞中粒子数目的计算
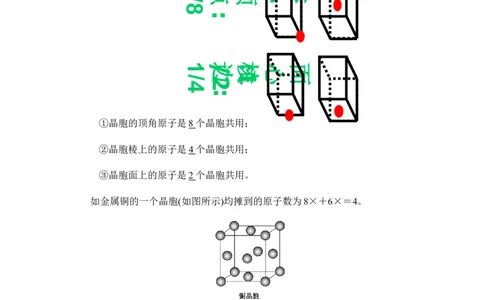
(1)平行六面体(立方体形)晶胞中粒子数目的计算。
1 点1 顶: 心 体
/
8
:
1/边:棱 心 面
1
/2
4
:
①晶胞的顶角原子是8 个晶胞共用;
②晶胞棱上的原子是4 个晶胞共用;
③晶胞面上的原子是2 个晶胞共用。
如金属铜的一个晶胞(如图所示)均摊到的原子数为8×+6×=4。
(2)几种晶胞中原子数目的确定。
结合下图,钠、锌、碘、金刚石晶胞中含有原子的数目分别为 2、2、8、
8。钠、锌、碘、金刚石晶胞示意图
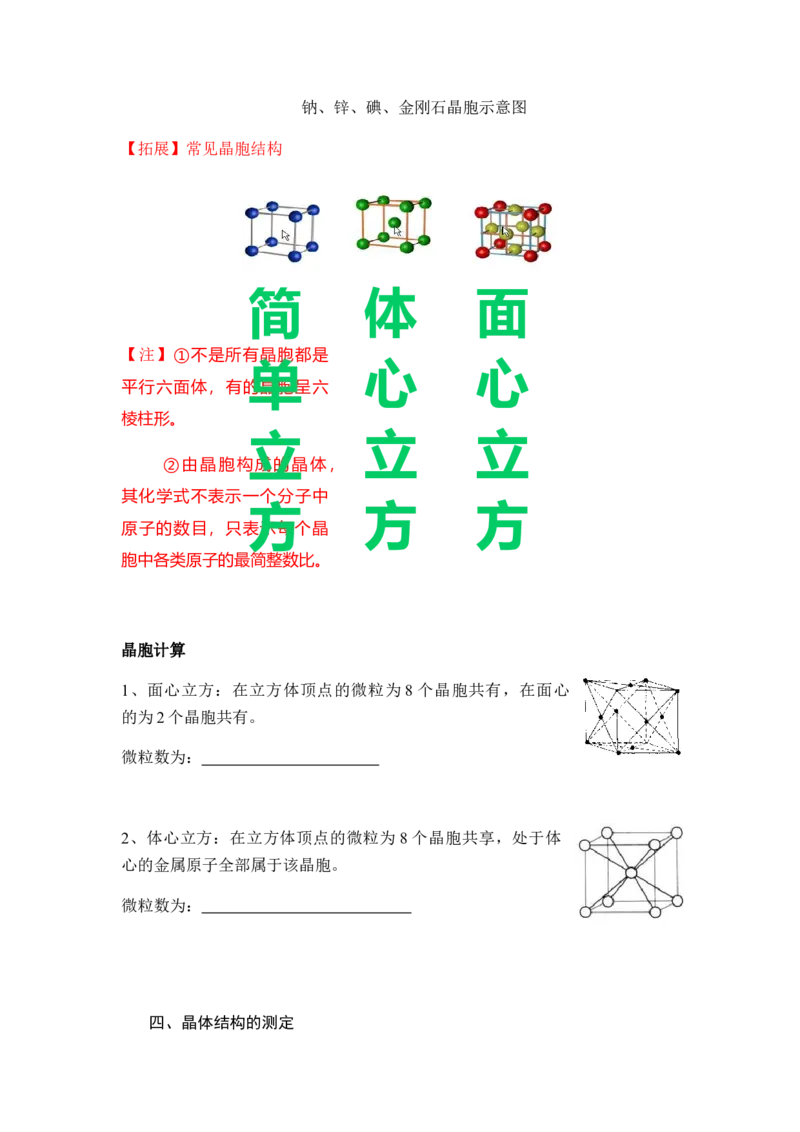
【拓展】常见晶胞结构
简 体 面
【注】①不是所有晶胞都是
单 心 心
平行六面体,有的晶胞呈六
棱柱形。
立 立 立
②由晶胞构成的晶体,
其化学式不表示一个分子中
方 方 方
原子的数目,只表示每个晶
胞中各类原子的最简整数比。
晶胞计算
1、面心立方:在立方体顶点的微粒为 8 个晶胞共有,在面心
的为2个晶胞共有。
微粒数为:
2、体心立方:在立方体顶点的微粒为 8个晶胞共享,处于体
心的金属原子全部属于该晶胞。
微粒数为:
四、晶体结构的测定1.测定晶体结构最常用的仪器是 X 射线衍射仪 。在X射线通过晶体时,X
射线和晶体中的电子相互作用,会在记录仪上产生分立的斑点或明锐的衍射峰。
2.由衍射图形获得晶体结构的信息包括晶胞形状和大小、分子或原子在微
观空间有序排列呈现的对称类型、原子在晶胞里的数目和位置等。
【总结】
晶体与非晶体的比较
晶体 非晶体
微观结构特征 粒子周期性有序排列 粒子排列相对无序
自范性 有 无
性质
熔点 固定 不固定
特征
各向异性 有 无
鉴别 间接方法 看是否具有固定的熔点或根据某些物理性质的各向异性
方法 科学方法 对固体进行X-射线衍射实验
举例 NaCl、I 、SiO 、Na晶体等 玻璃、橡胶等
2 2
【注】关于晶体与非晶体的认识误区
1同一物质可以是晶体,也可以是非晶体,如晶体SiO 和非晶体SiO 。
2 2
2有着规则几何外形或者美观、对称外形的固体,不一定是晶体。例如,
玻璃制品可以塑造出规则的几何外形,也可以具有美观对称的外观。
3具有固定组成的物质也不一定是晶体,如某些无定形体也有固定的组成。
4晶体不一定都有规则的几何外形,如玛瑙。