文档内容
第三章 水溶液中的离子反应与平衡
课题
第一节 电离平衡
1、了解弱电解质的概念;
知识与技
2、了解弱电解质电离平衡的影响因素
能
教 3、了解弱电解质电离平衡的平衡常数计算
学
过程与方 通过实验,培养学生观察、分析能力,掌握推理、归纳、演绎和
目
法 类比等科学方法
标
情感态度 通过本节课的学习,意识到整个自然界实际就是各类物种相互依
与价值观 存、各种变化相互制约的复杂的平衡体系
教学
重点 弱电解质电离平衡的影响因素
教学
难点 弱电解质电离平衡的平衡常数计算
教
学
设
本章是上一章化学平衡理论的延伸和扩展。第一节弱电解质的电离的课标要求主要是认
教 识电解质的强弱和能用化学平衡理论描述电解质在水溶液中的电离平衡。本节理论性较
材
强,是理论与实践相结合的一节,掌握方法是学好本节知识的关键。在具体的学习中,注
分
析 意与初中和高中必修内容的衔接,增强知识的逻辑性,以化学平衡理论为指导,引出一系
列新知识点;同时通过实验加强科学方法、科学态度的学习,加强能力和技能培养。
学
情 学生已经学过弱电解质的知识,在上一章学习了化学平衡,已经建立了平衡思
分
想,在此基础上进一步学习弱电解质电离平衡是比较容易理解的。
析
教
法
想 情景教学法与启发式教学相结合
设
计
教学 教 学 内 容 设计
环节 意图
教师活动 学生活动【复习提问】什么是弱电解质?电离方程式存在什
复习并引入
么?
新课
【学生回答】在水溶液中部分电离出离子的电解 思考 回答
质,电离方程式存在可逆性
【引入】本节课我们来学习弱电解质的电离平衡
【板书】第一节 弱电解质的电离平衡
【讲解】回想化学平衡建立来学习弱电解质的电离 讨论、分析
平衡
以CH COOH电离为例来分析并画图像
3
CH COOH CH COOˉ + H+ 培养学生分
3 3
析问题和总
v 结总题 的能
力
0 总结
t
【引导】通过分析可知什么是电离平衡?
【板书】1、定义:在一定条件下,当弱电解质分子
导 电离成离子的速率与离子重新结合生成分
学
达 子的速率相等时,溶液中分子和离子的浓
标
度保持不变的状态。
【引导】类比化学平衡总结电离平衡的特征
【板书】2、特征:1) 逆 —— 电离过程是可逆
2)等 —— 达到平衡状态时,v = v 回答
(电离) (结合)
3)动 —— 在一定条件下,达到平衡状态,v =
(电离)
v ≠0,是一生种动态平衡
(结合)
4)定 —— 外界条件一定,达到平衡时溶液中分子
浓度、压强、
和离子的浓度保持一定
温度 让学生用类
5)变 —— 外界条件改变,电离平衡发生移动
比的方法来
【提问】影响化学平衡的因素有哪些? 学习,有利
于知识的巩
【讲述】影响电离平衡的因素又有哪些?
固
【板书】3、影响因素:
1)温度:弱电解质电离过程为吸热过程,升温促进
电离;降温抑制电离。
2) 浓度:浓度越大,电离程度越小;浓度越小,
电离程度越大。
3) 酸碱度:加入酸或碱,促进或抑制电离。【讲述】电离平衡CH
3
COOH CH
3
COO- + H+ ,各种因素对平衡的影响可归纳为下表:
平衡移 导电 电离
n(H+) c(H+) c(CHCOO -)
3
动方向 能力 程度
导 加冰醋酸
学
达 加NaOH(s)
标
加HCl(g)
加金属Mg
加水稀释
升高温度
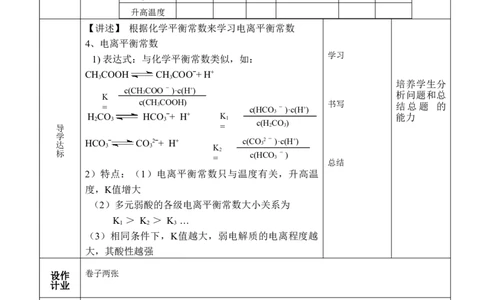
【讲述】 根据化学平衡常数来学习电离平衡常数
4、电离平衡常数
学习
1) 表达式:与化学平衡常数类似,如:
CH COOH CH COOˉ+ H+
3 3
培养学生分
析问题和总
书写 结总题 的
H CO HCO ˉ+ H+ 能力
2 3 3
导
学
达 HCO 3 ˉ CO 3 2ˉ+ H+
标
总结
2)特点:(1)电离平衡常数只与温度有关,升高温
度,K值增大
(2)多元弱酸的各级电离平衡常数大小关系为
K > K > K …
1 2 3
(3)相同条件下,K值越大,弱电解质的电离程度越
大,其酸性越强
设作 卷子两张
计业
板
书
设
c(CH COOˉ)·c(H+)
K
3
c(CH COOH) = 3 c(HCO ˉ)·c(H+)
K
3
1
c(H CO )
= 2 3
c(CO 2ˉ)·c(H+) K 3
2
=
c(HCO
3
ˉ)
第一节 弱电解质的电离平衡
1、定义
2、特征:逆、等、动、定、变
3、影响因素:浓度、温度
4、电离平衡常数
计