文档内容
第一节 电离平衡
一、强电解质和弱电解质
(一)电解质与非电解质
1、电解质:在水溶液或熔融状态下能够导电的化合物。例如:酸、碱、盐、活泼金属氧化
物、少数有机物、HO
2
2、非电解质:在水溶液或熔融状态下都不能导电的化合物。例如:非金属氧化物、大部分
的有机物、NH
3
注:(1)必须是化合物,单质和混合物既不是电解质也不是非电解质。例如:铜、氯化钠
水溶液
(2)电解质不一定导电,导电的不一定是电解质。例如:氯化钠固体、氯化钠水溶液
(3)非电解质不导电,不导电的不一定是非电解质。例如:氢气
(4)电解质必须是化合物本身能电离出离子,否则不属于电解质。例如:NH 、SO 、
3 2
CO
2
(二)强弱电解质
1、强电解质:(1)定义:在水溶液中能够全部电离的电解质。
(2)特点:完全电离,只有离子,无分子,不可逆,电离方程式用“=”连
接
(3)类别:强酸:HCl、HSO 、HNO、HBr、HI、HClO
2 4 3 4
强碱:NaOH、KOH、Ca(OH) 、Ba(OH)
2 2
大部分盐(包括难溶盐)、活泼金属氧化物
2、弱电解质:(1)定义:在水溶液中能够部分电离的电解质。
(2)特点:不完全电离,既有分子又有离子,可逆,存在电离平衡,电离方
程式用“ ”连接
(3)类别:弱酸、弱碱、水、极少的盐(醋酸铅Pb(CH COO) 、HgCl )
3 2 2
注:①电解质的强弱与溶解性无关,与溶液的导电性无必然联系
②电解质的导电性与溶液中自由移动的离子浓度有关,自由移动的离子浓度越大,离
子所带电荷数越多,导电性越强
(三)电离方程式的书写
1、原则:遵循质量守恒、电荷守恒、客观事实
2、书写:①强电解质:“=”、弱电解质:“ ”
②多元弱酸分步电离,以第一步电离为主,分步书写;多元弱碱分步电离,一步
书写
③两性氢氧化物:Al3++3OH- Al(OH) H++AlO -+H O
3 2 2
碱式 酸式
④强酸酸式盐的电离:NaHSO=Na++H++SO2- (水中) NaHSO=Na+
4 4 4
+HSO -(熔融状态)
4
⑤弱酸酸式盐的电离:NaHCO = Na++HCO- HCO - H++CO2-
3 3 3 3
二、弱电解质的电离平衡
(一)定义:在一定条件(如温度、压强)下,当弱电解质分子电离成离子的速率与离
子重新结合成弱电解质分子的速率相等时,电离过程就达到平衡状态,这种平衡状态叫做弱电解质的电离平衡
(二)特征:逆、等、动、定、变
逆——可逆过程 等——v =v 动——动态平衡 定——离子、分子的浓度保持一
电离 结合
定 变——条件变、平衡动
(三)影响因素
1、内因:物质本身的性质
2、外因:
(1)温度:由于电离过程是吸热的过程,所以升高温度,平衡向电离方向移动,电离程度
增大
(2)浓度:①加水稀释→平衡向电离的方向移动→电离程度增大→但离子浓度减小
②增大弱电解质的浓度→平衡向电离方向移动→但电离程度减小
③加入同浓度的弱电解质溶液→平衡不移动→各微粒浓度不变、电离程度不变
④加入其它试剂,减小或增大弱电解质电离出的某离子的浓度,可促进或抑制
电离
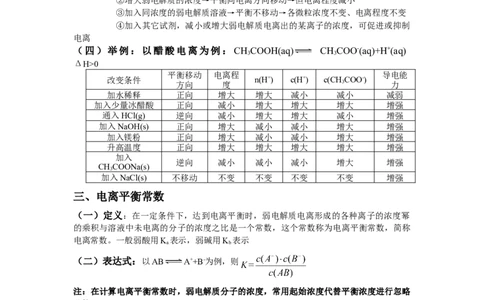
(四)举例:以醋酸电离为例:CH COOH(aq) CH COO-(aq)+H+(aq)
3 3
ΔH>0
平衡移动 电离程 导电能
改变条件 n(H+) c(H+) c(CHCOO-)
方向 度 3 力
加水稀释 正向 增大 增大 减小 减小 减弱
加入少量冰醋酸 正向 减小 增大 增大 增大 增强
通入HCl(g) 逆向 减小 增大 增大 减小 增强
加入NaOH(s) 正向 增大 减小 减小 增大 增强
加入镁粉 正向 增大 减小 减小 增大 增强
升高温度 正向 增大 增大 增大 增大 增强
加入
逆向 减小 减小 减小 增大 增强
CHCOONa(s)
3
加入NaCl(s) 不移动 不变 不变 不变 不变 增强
三、电离平衡常数
(一)定义:在一定条件下,达到电离平衡时,弱电解质电离形成的各种离子的浓度幂
的乘积与溶液中未电离的分子的浓度之比是一个常数,这个常数称为电离平衡常数,简称
电离常数。一般弱酸用K 表示,弱碱用K 表示
a b
(二)表达式:以AB A++B-为例,则
注:在计算电离平衡常数时,弱电解质分子的浓度,常用起始浓度代替平衡浓度进行忽略
计算
(三)影响因素:1、物质本身的性质决定
2、只受温度影响,升高温度,电离平衡常数增大,电离程度越大
(四)意义:相同条件下,K值越大,表示该弱电解质越易电离,所对应溶液的酸性或
碱性越强
(五)说明:
1、K越大,只能说明其分子发生电离的程度越大,但其溶液中的离子浓度不一定大,导电
能力也不一定强
2、多元弱酸是分步电离的,每一步都有相应的K,对于同一种弱酸的K 、K 、K ,总有
1 2 3
K 》K 》K ,即电离程度逐渐减弱。这是因为上一级电离产生的H+,对下一级电离起
1 2 3到抑制作用。所以计算多元弱酸溶液的c(H+)或比较弱酸酸性相对强弱时,通常只考虑
第一步电离