文档内容
第三章 晶体结构与性质
第二节 分子晶体与共价晶体
第一课时 分子晶体
一.选择题
1.下列晶体由原子直接构成,且属于分子晶体的是( )
A. 固态氢 B. 固态氖 C. 磷 D. 三氧化硫
【答案】B
【解析】稀有气体分子都属于单原子分子,因此稀有气体形成的晶体属于分子晶体且由原子直接构
成。其他分子晶体一般由分子构成,如干冰、冰等。
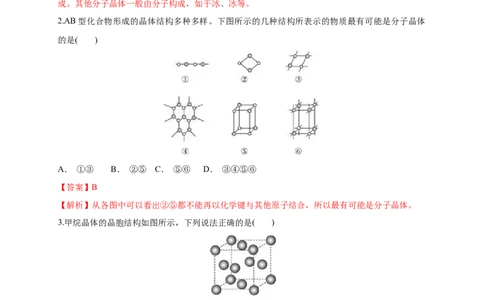
2.AB型化合物形成的晶体结构多种多样。下图所示的几种结构所表示的物质最有可能是分子晶体
的是( )
A. ①③ B. ②⑤ C. ⑤⑥ D. ③④⑤⑥
【答案】B
【解析】从各图中可以看出②⑤都不能再以化学键与其他原子结合,所以最有可能是分子晶体。
3.甲烷晶体的晶胞结构如图所示,下列说法正确的是( )
A. 甲烷晶胞中的球只代表1个C原子
B. 晶体中1个CH 分子有12个紧邻的CH 分子
4 4
C. 甲烷晶体熔化时需克服共价键
D. 1个CH 晶胞中含有8个CH 分子
4 4
【答案】B
【解析】题图所示的甲烷晶胞中的球代表的是1个甲烷分子,并不是1个C原子,A错误;由甲烷
晶胞分析,位于晶胞顶点的某一个甲烷分子与其距离最近的甲烷分子有 3个,而这3个甲烷分子在晶胞的面上,因此每个都被2个晶胞共用,故与1个甲烷分子紧邻的甲烷分子数目为3×8× =12,
B正确;甲烷晶体是分子晶体,熔化时克服范德华力,C错误;甲烷晶胞中甲烷分子的个数为8×
+6× =4,D错误。
4.二茂铁[(C H ) Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属
5 5 2
化合物研究的新领域。已知二茂铁的熔点是1 73 ℃(在100 ℃以上能升华),沸点是249 ℃,
不溶于水,易溶于苯、乙醚等有机溶剂。下列说法不正确的是( )
A. 二茂铁属于分子晶体
B. 在二茂铁中,C H 与Fe2+之间形成的化学键类型是离子键
5
C. 已知环戊二烯的结构式为 ,则其中仅有1个碳原子采取sp3杂化
D. C H 中一定含有π键
5
【答案】B
【解析】根据二茂铁的物理性质,如熔点低、易升华、易溶于有机溶剂等,可知二茂铁为分子晶体,
A项正确;碳原子含有孤电子对,铁离子含有空轨道,故二者形成配位键,B项错误;1号碳原子
含有4个σ键,无孤电子对,杂化类型为sp3,2、3、4、5号碳原子有3个σ键,无孤电子对,杂
化类型为sp2,因此仅有1个碳原子采取sp3杂化,C项正确;C H 中碳原子没有达到饱和,故存在
5
碳碳双键,而碳碳双键中只有一个σ键,另一个必然为π键,D项正确。
5.如果分子间作用力只是范德华力,则该分子晶体将采取密堆积,原因是分子晶体中( )
A. 范德华力无方向性和饱和性
B. 占据晶格结点的微粒是原子
C. 化学键是共价键
D. 三者都是
【答案】A
【解析】分子晶体中分子间以范德华力结合在一起,由于范德华力没有方向性和饱和性,所以分子
在堆积成晶体时将采取分子密堆积,A项正确。
6.下列有关分子晶体熔点的高低叙述中,正确的是( )
A. Cl>I B. SiCl >CCl
2 2 4 4
C. PH >NH D. C(CH)>CHCHCHCHCH
3 3 3 4 3 2 2 2 3
【答案】B【解析】NH 分子间存在氢键,分子间作用力大,PH 分子间不存在氢键,分子间作用力弱,NH
3 3 3
的熔点高于PH ,C不正确;A、B选项中均无氢键,且固态时都为分子晶体,物质组成结构相似,
3
相对分子质量大的熔点高,故A不正确,B正确;相对分子质量相同的烷烃的同分异构体,支链越
多,熔点越低,故D不正确。
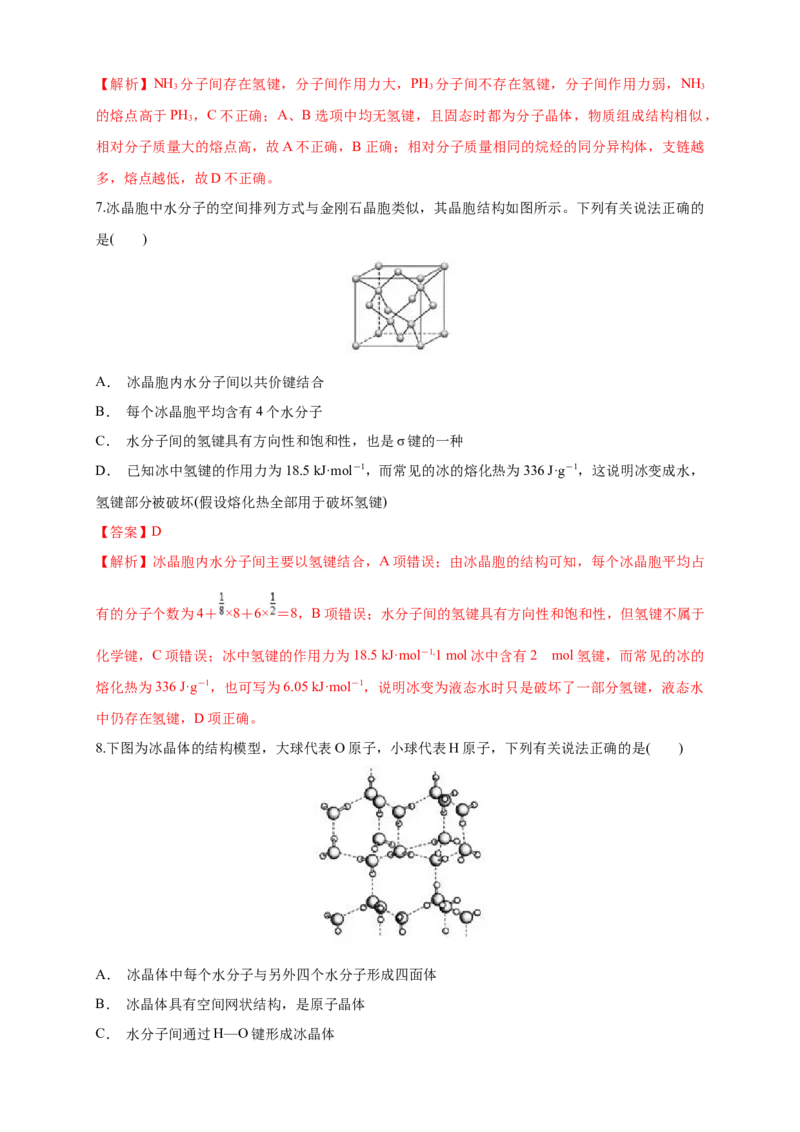
7.冰晶胞中水分子的空间排列方式与金刚石晶胞类似,其晶胞结构如图所示。下列有关说法正确的
是( )
A. 冰晶胞内水分子间以共价键结合
B. 每个冰晶胞平均含有4个水分子
C. 水分子间的氢键具有方向性和饱和性,也是σ键的一种
D. 已知冰中氢键的作用力为18.5 kJ·mol-1,而常见的冰的熔化热为336 J·g-1,这说明冰变成水,
氢键部分被破坏(假设熔化热全部用于破坏氢键)
【答案】D
【解析】冰晶胞内水分子间主要以氢键结合,A项错误;由冰晶胞的结构可知,每个冰晶胞平均占
有的分子个数为4+ ×8+6× =8,B项错误;水分子间的氢键具有方向性和饱和性,但氢键不属于
化学键,C项错误;冰中氢键的作用力为18.5 kJ·mol-1,1 mol冰中含有2 mol氢键,而常见的冰的
熔化热为336 J·g-1,也可写为6.05 kJ·mol-1,说明冰变为液态水时只是破坏了一部分氢键,液态水
中仍存在氢键,D项正确。
8.下图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是( )
A. 冰晶体中每个水分子与另外四个水分子形成四面体
B. 冰晶体具有空间网状结构,是原子晶体
C. 水分子间通过H—O键形成冰晶体D. 冰晶体熔化时,水分子之间的空隙增大
【答案】A
【解析】 B项,冰晶体属于分子晶体;C项,水分子间通过分子间作用力形成晶体;D项,冰熔
化,氢键部分断裂,空隙减小。
9.下列性质适合于分子晶体的是( )
A. 熔点1070 ℃,易溶于水,水溶液导电
B. 熔点2853 ℃,液态不导电,水溶液也不导电
C. 能溶于CS,熔点112.8 ℃,沸点444.6 ℃
2
D. 熔点97.81 ℃,质软导电,密度为0.97 g·cm-3
【答案】C
【解析】A选项熔点高,不是分子晶体,分子晶体熔点低;B选项是原子晶体的性质;D选项是金
属钠的性质。
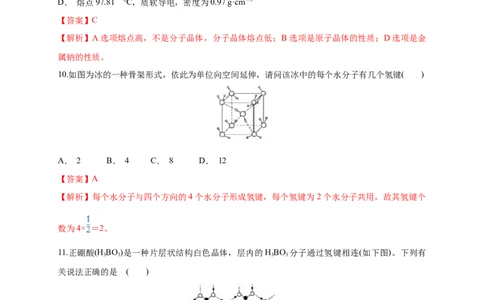
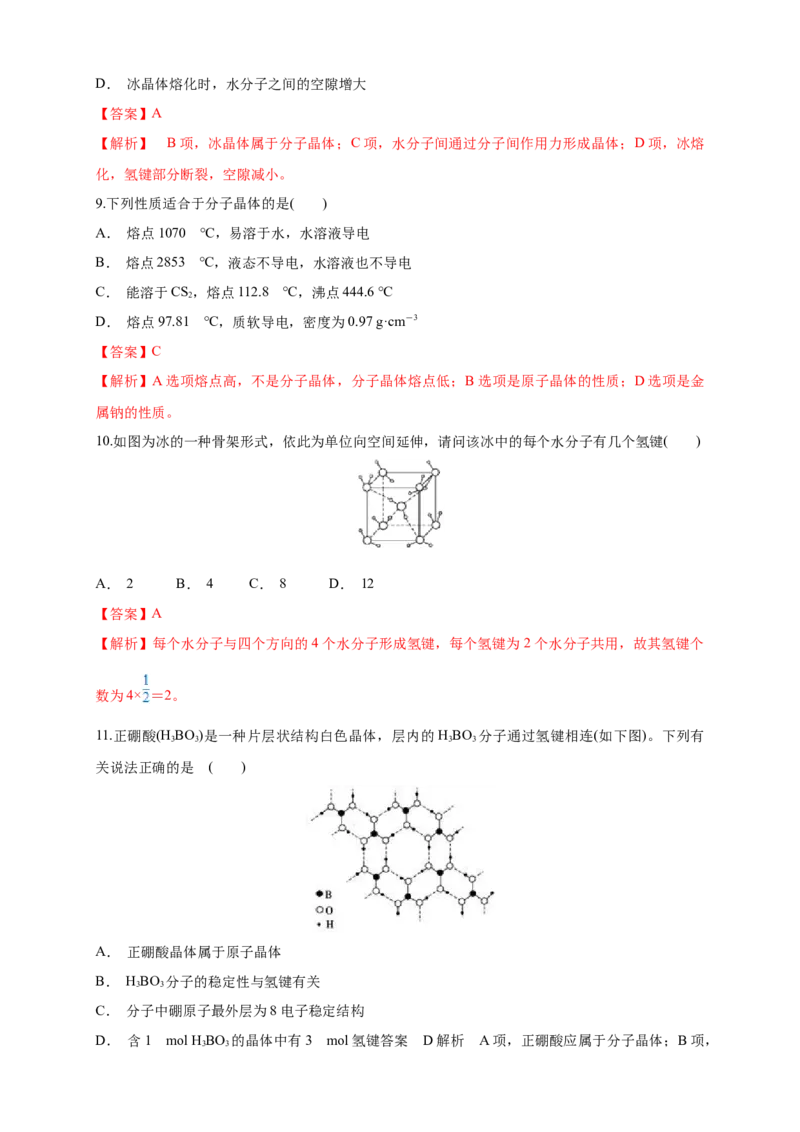
10.如图为冰的一种骨架形式,依此为单位向空间延伸,请问该冰中的每个水分子有几个氢键( )
A. 2 B. 4 C. 8 D. 12
【答案】A
【解析】每个水分子与四个方向的4个水分子形成氢键,每个氢键为2个水分子共用,故其氢键个
数为4× =2。
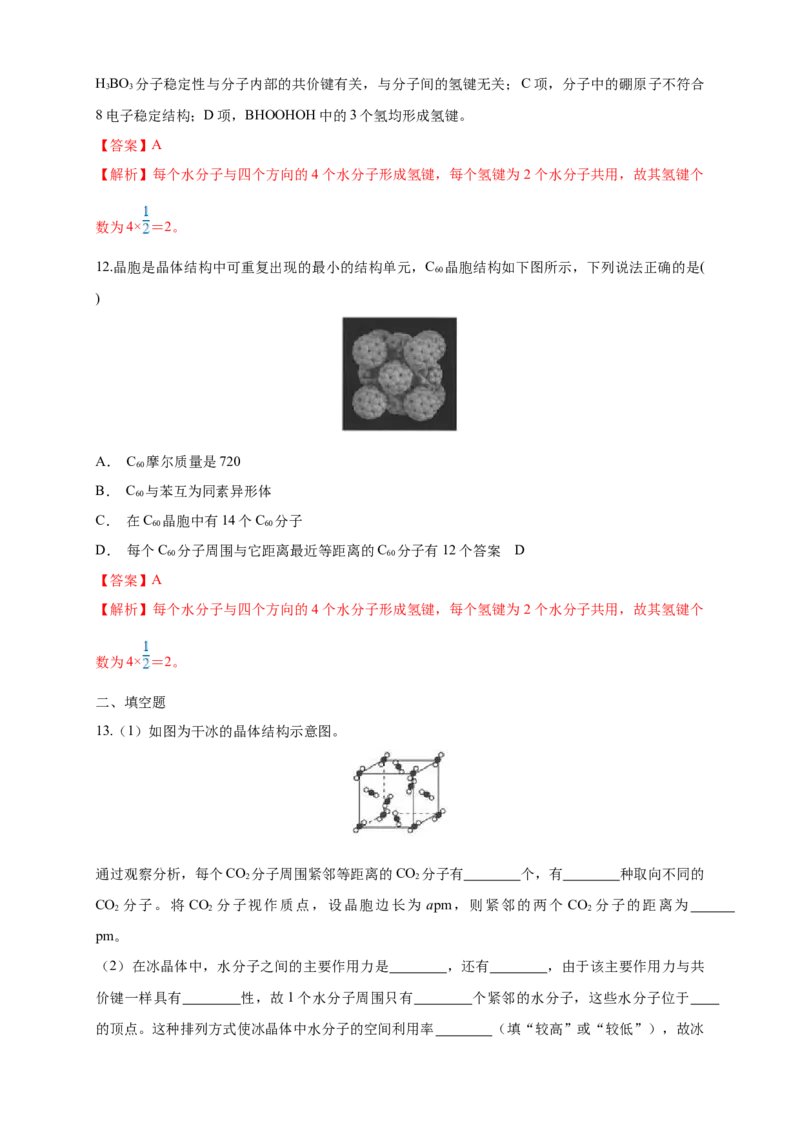
11.正硼酸(H BO)是一种片层状结构白色晶体,层内的HBO 分子通过氢键相连(如下图)。下列有
3 3 3 3
关说法正确的是 ( )
A. 正硼酸晶体属于原子晶体
B. HBO 分子的稳定性与氢键有关
3 3
C. 分子中硼原子最外层为8电子稳定结构
D. 含1 mol H BO 的晶体中有3 mol氢键答案 D解析 A项,正硼酸应属于分子晶体;B项,
3 3HBO 分子稳定性与分子内部的共价键有关,与分子间的氢键无关;C项,分子中的硼原子不符合
3 3
8电子稳定结构;D项,BHOOHOH中的3个氢均形成氢键。
【答案】A
【解析】每个水分子与四个方向的4个水分子形成氢键,每个氢键为2个水分子共用,故其氢键个
数为4× =2。
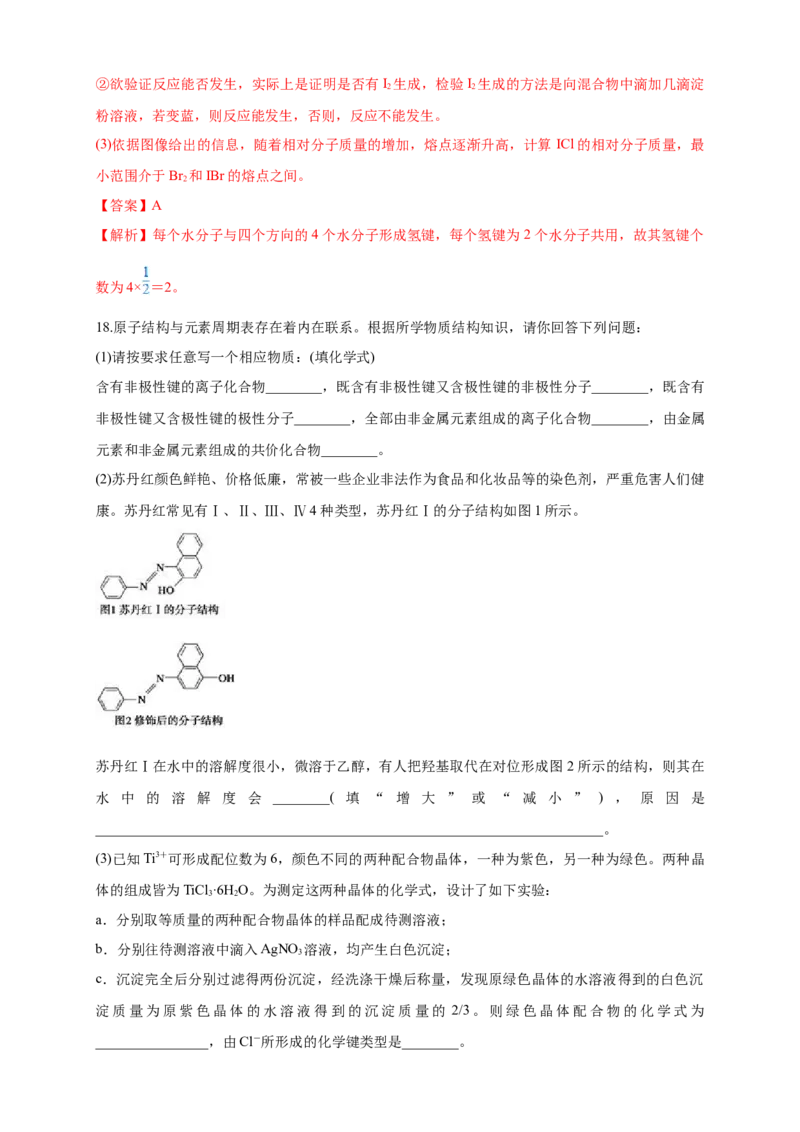
12.晶胞是晶体结构中可重复出现的最小的结构单元,C 晶胞结构如下图所示,下列说法正确的是(
60
)
A. C 摩尔质量是720
60
B. C 与苯互为同素异形体
60
C. 在C 晶胞中有14个C 分子
60 60
D. 每个C 分子周围与它距离最近等距离的C 分子有12个答案 D
60 60
【答案】A
【解析】每个水分子与四个方向的4个水分子形成氢键,每个氢键为2个水分子共用,故其氢键个
数为4× =2。
二、填空题
13.(1)如图为干冰的晶体结构示意图。
通过观察分析,每个CO 分子周围紧邻等距离的CO 分子有 个,有 种取向不同的
2 2
CO 分子。将 CO 分子视作质点,设晶胞边长为 apm,则紧邻的两个 CO 分子的距离为
2 2 2
pm。
(2)在冰晶体中,水分子之间的主要作用力是 ,还有 ,由于该主要作用力与共
价键一样具有 性,故1个水分子周围只有 个紧邻的水分子,这些水分子位于
的顶点。这种排列方式使冰晶体中水分子的空间利用率 (填“较高”或“较低”),故冰的密度比水的密度要 (填“大”或“小”)。
【答案】(1)12 4 a (2)氢键 范德华力 方向 4 四面体 较低 小
【解析】观察并分析干冰和冰的晶体结构,可知在干冰晶体中,CO 分子排列为面心立方堆积,顶
2
点为一种取向,三对平行面分别为三种不同取向。离顶点的CO 分子最近的是面心的分子,两者的
2
距离为面对角线的一半,即 apm。每个CO 分子周围紧邻且等距离的CO 分子共有12个。
2 2
在冰晶体中,水分子间的主要作用力是氢键,氢键具有方向性,1个水分子周围只有4个紧邻的水
分子,使冰晶体中水分子的空间利用率较低,分子的间距较大,结构中有许多空隙,造成冰的密度
小于水的密度。
14.在我国南海300~500 m海底深处沉积物中存在着大量的“可燃冰”,其主要成分为甲烷水合物
在常温、常压下它会分解成水和甲烷,因而得名。请回答下列问题:
(1)甲烷晶体的晶胞结构如图所示,下列说法正确的是 (填序号)。
A.甲烷晶胞中的球只代表一个C原子
B.晶体中1个CH 分子中有12个紧邻的CH 分子
4 4
C.CH 熔化时需克服共价键
4
D.1个CH 晶胞中含有8个CH 分子
4 4
E.CH 是非极性分子
4
(2)水在不同的温度和压强条件下可以形成多种不同结构的晶体,冰晶体结构有多种。其中冰Ⅶ
的晶体结构如下图所示。
①水分子的立体结构是 形,在酸性溶液中,水分子容易得到一个 H+,形成水合氢离子
(HO+),水分子能与H+形成配位键,其原因是在氧原子上有 ,应用价层电子
3
对互斥理论(或模型)推测HO+的形状为 。
3
②实验测得冰中氢键的作用能为 18.5 kJ·mol-1,而冰的熔化热为 5.0 kJ·mol-1,这说明___________________________________________________________
___________________________________________________________。
(3)用x、y、z分别表示HO、HS、HSe的沸点(℃),则x、y、z的大小关系是 ,其
2 2 2
判断依据是___________________________________
___________________________________________________________。
【答案】(1)BE (2)①V 孤电子对 三角锥形 ②冰熔化为液态水时只破坏了一部分氢键,
液态水中仍存在氢键 (3)x>z>y 水分子间可以形成氢键,HSe的相对分子质量大于HS,故
2 2
有沸点:HO>HSe>HS
2 2 2
【解析】(1)CH 是分子晶体,熔化时克服范德华力。晶胞中的球体代表的是一个甲烷分子,并
4
不是一个C原子。以该甲烷晶胞分析,位于顶点的某一个甲烷分子与其距离最近的甲烷分子有3个
而这3个甲烷分子在面上,因此每个都被共用2次,故与1个甲烷分子紧邻的甲烷分子有3×8× =
12(个)。甲烷晶胞属于面心立方晶胞,该晶胞中甲烷分子的个数为8× +6× =4(个)。CH 分
4
子为正四面体结构,C原子位于正四面体的中心,结构对称,CH 是非极性分子。
4
(2)①水分子中O原子的价电子对数= =4,孤电子对数为2,所以水分子为V形,HO分子
2
能与H+形成配位键,其原因是在O原子上有孤电子对,H+有空轨道。HO+价电子对数 =
3
4,含有1对孤电子对,故HO+为三角锥形。②冰中氢键的作用能为18.5 kJ·mol-1,而冰的熔化
3
热为5.0 kJ·mol-1,说明冰熔化为液态水时只是破坏了一部分氢键,并且液态水中仍存在氢键。
(3)水分子间存在氢键,HSe与HS分子间不存在氢键,但HSe的相对分子质量大于HS相对分
2 2 2 2
子质量,HSe分子间范德华力大于HS分子间范德华力。
2 2
15.下表数据是对应物质的熔点:
(1)BCl 分子构型为平面三角形,则BCl 分子为 (填“极性”或“非极性”,下同)分
3 3子,其分子中的共价键类型为 键。
(2)BF 的熔点比BCl (填“高”、“低”或“无法确定”);下列化学用语中,能正
3 3
确表示BF 分子的是 (填编号)。
3
(3)氯化铝是 (填“离子”或“共价”)化合物,AlCl 属于 (填“强”或
3
“弱”)电解质,它的晶体类型为 ,AlCl (填“难”或“易”)溶于苯和
3
CCl 。设计一个可靠的实验,判断氯化铝是离子化合物还是共价化合物。你设计的实验是
4
_________________________________
___________________________________________________________。
(4)AlCl 在177.8 ℃时升华,气态或熔融态以Al Cl 形式存在,则可推知Al Cl 在固态属于
3 2 6 2 6
晶体,Al Cl 中 (填“存在”或“不存在”)配位键。
2 6
【答案】(1)非极性 极性 (2)低 bd
(3)共价 强 分子晶体 难 在熔融状态下,验证其是否导电,若不导电是共价化合物
(4)分子 存在
【解析】
16.据报道科研人员应用计算机模拟出结构类似C 的物质N 。
60 60
已知:①N 分子中每个氮原子均以N—N键结合三个N原子而形成8电子稳定结构;
60
②N—N键的键能为167 kJ·mol-1。
请回答下列问题:
(1)N 分子组成的晶体为________晶体,其熔、沸点比N________(填“高”或“低”),原因是
60 2
________________________________________________________________________。
(2)1 mol N 分解成N 时________(填“吸收”或“放出”)的热量是______kJ(已知N≡N键的键能为
60 2
942 kJ·mol-1),表明稳定性N ______(填“>”“<”或“=”)N 。
60 2
(3)由(2)列举N 的用途(举一种):_____________________________________________。
60
【答案】(1)分子 高 N 、N 均形成分子晶体,且N 的相对分子质量大,分子间作用力大,故熔、
60 2 60
沸点高
(2)放出 13 230 <
(3)N 可作高能炸药(其他合理答案也可)
60
【解析】(1)N 、N 形成的晶体均为分子晶体,因M(N )>M(N ),故N 晶体中分子的范德华力比
60 2 r 60 r 2 60N 晶体大,N 晶体的熔、沸点比N 晶体高。
2 60 2
(2)因N 中每个氮原子形成三个N—N键,每个N—N键被2个N 原子共用,故1 mol N 中存在N
60 60
—N键:1 mol×60×3× =90 mol。发生的反应为N ==30N ,故ΔH=90 mol×167 kJ·mol-1-30
60 2
mol×942 kJ·mol-1=-13 230 kJ<0,为放热反应,表明稳定性:N>N 。
2 60
(3)由于反应放出大量的热,同时生成大量气体,因此N 可用作高能炸药。
60
17.卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX′型卤素互化物与卤素单质结
构相似、性质相近。试回答下列问题:
(1)如图是部分
卤素单质和XX′型卤素互化物的熔点与其相对分子质量的关系图。它们的熔点随着相对分子质量的
增大而升高,其原因是____________________________________________________
________________________________________________________________。
(2)卤素互化物可发生的反应:
HO+BrCl===HBrO+HCl
2
KBr+BrCl===KCl+Br
2
①写出KI与IBr反应的化学方程式__________________________________________________
____________。
②若要验证①反应能否发生,请你设计一个简单的实验:______________________
________________________________________________________________________。
(3)试推测ICl的熔点所处的最小范围________________________________________
________________________________________________________________________。
答案 (1)相对分子质量越大,分子间的作用力越强
(2)①KI+IBr===KBr+I ②向反应物混合液中滴加几滴淀粉溶液,若变蓝,证明能反应,否则不
2
能反应
(3)介于Br 的熔点和IBr的熔点之间
2
解析 (1)卤素单质及XX′型卤素互化物都是双原子分子,组成和结构相似,其相对分子质量越大,
范德华力越大,熔、沸点越高。
(2)①主要考查学生运用信息、模拟信息的能力,KI+IBr===KBr+I。
2②欲验证反应能否发生,实际上是证明是否有I 生成,检验I 生成的方法是向混合物中滴加几滴淀
2 2
粉溶液,若变蓝,则反应能发生,否则,反应不能发生。
(3)依据图像给出的信息,随着相对分子质量的增加,熔点逐渐升高,计算 ICl的相对分子质量,最
小范围介于Br 和IBr的熔点之间。
2
【答案】A
【解析】每个水分子与四个方向的4个水分子形成氢键,每个氢键为2个水分子共用,故其氢键个
数为4× =2。
18.原子结构与元素周期表存在着内在联系。根据所学物质结构知识,请你回答下列问题:
(1)请按要求任意写一个相应物质:(填化学式)
含有非极性键的离子化合物________,既含有非极性键又含极性键的非极性分子________,既含有
非极性键又含极性键的极性分子________,全部由非金属元素组成的离子化合物________,由金属
元素和非金属元素组成的共价化合物________。
(2)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健
康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ的分子结构如图1所示。
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在
水 中 的 溶 解 度 会 ________( 填 “ 增 大 ” 或 “ 减 小 ” ) , 原 因 是
________________________________________________________________________。
(3)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶
体的组成皆为TiCl ·6H O。为测定这两种晶体的化学式,设计了如下实验:
3 2
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO 溶液,均产生白色沉淀;
3
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉
淀质量为原紫色晶体的水溶液得到的沉淀质量的 2/3。则绿色晶体配合物的化学式为
________________,由Cl-所形成的化学键类型是________。(4)下图中A,B,C,D四条曲线分别表示第ⅣA、ⅤA、ⅥA、ⅦA族元素的氢化物的沸点,其
中表示ⅦA族元素氢化物沸点的曲线是________;表示ⅣA族元素氢化物沸点的曲线是________;
同 一 族 中 第 3 、 4 、 5 周 期 元 素 的 氢 化 物 沸 点 依 次 升 高 , 其 原 因 是
________________________________________________________________________;
A,B,C曲线中第二周期元素的氢化物的沸点显著高于第三周期元素的氢化物的沸点,其原因是
________________________________________________________________________。
【答案】(1)Na O C H HO NH Cl AlCl
2 2 2 2 2 2 4 3
(2)增大 因为苏丹红Ⅰ形成分子内氢键,而修饰后的分子可形成分子间氢键,与水分子间形成氢键
后有利于增大化合物在水中的溶解度
(3)[TiCl(H O) ]Cl ·H O 离子键、配位键(或共价键)
2 5 2 2
(4)B D 组成和结构相似的物质,相对分子质量越大,范德华力越大,沸点越高 HO、NH 、
2 3
HF分子之间存在氢键,沸点较高
【解析】(1)含有非极性键的离子化合物可以是NaO 、CaC 等;既含极性键又含非极性键的非极性
2 2 2
分子可以是C H 、C H 等;既含有非极性键又含极性键的极性分子是 H2O ;全部由非金属元素组
2 6 2 4 2
成的离子化合物是铵盐;由金属元素和非金属元素组成的共价化合物是AlCl 、AlBr 等。
3 3
(2)苏丹红Ⅰ形成分子内氢键,羟基取代对位后,则易形成分子间氢键,与 HO之间形成氢键后会
2
增大其溶解度。
(3)根据实验步骤c,绿色配合物外界有2个Cl-,紫色配合物外界有3个Cl-,其化学式分别为
[TiCl(H O) ]Cl ·H O、[Ti(HO) ]Cl ,由Cl-形成的化学键是离子键、配位键。
2 5 2 2 2 6 3
(4)因为沸点:HO>HF>NH >CH ,所以A、B、C、D分别代表ⅥA、ⅦA、ⅤA、ⅣA元素氢
2 3 4
化物的沸点变化趋势;形成分子间氢键的氢化物的沸点高,不能形成分子间氢键的,对于组成和结
构相似的物质,相对分子质量越大,范德华力越大,沸点越高。