文档内容
3.2.2 共价晶体(导学案)
1. 知道共价晶体的结构特点,能辨识常见的共价晶体。
2. 认识金刚石晶体中碳原子的三维骨架结构,能借助共价晶体的晶体结构模型说明共价晶
体中粒子间的相互作用,促进“证据推理与模型认知”化学核心素养的发展。
重点:共价晶体的结构与物理性质。
难点:共价晶体的结构与物理性质。
1.共价晶体
(1)相邻原子间以共价键结合形成 结构的晶体,不存在单个的小分
子。
(2)
(3)物理性质
共价晶体由于原子间以较强的共价键相结合,熔化时必需破坏共价键,而破坏它们需要很
高的温度,所以一般熔点 ,硬度 。
2.金刚石的晶体结构
(1)金刚石是典型的 ,天然的金刚石经常呈现规则多面体的外形。C—C—C
夹角为 ,即金刚石中的碳以 杂化轨道形成共价键。
(2)金刚石里的C—C共价键的键长 ,键能很大,这一结构使金刚石在所有已知
晶体中硬度 ,而且熔点也 。
3.SiO2的结构及应用
(1)SiO 是另一种典型的共价晶体,熔点为 1713 ℃,有多种结构,最常见的是
2
,其结构中有顶角相连的 形成螺旋上升的长链,这一结构决定了它具有
,被广泛用作压电材料。
(2)SiO2具有许多重要用途,是制造水泥、玻璃、单晶硅、硅光电池、芯片和光导纤维的原料。
4.其他常见的共价晶体
(1)某些单质,如硼、 、锗和灰锡等。
(2)某些非金属化合物,如 (俗称金刚砂)、氮化硼(BN)等。
1.判断正误,正确的画“√”,错误的画“×”。
(1)共价晶体中共价键越强,熔点越高。( )
(2)共价晶体可能含有离子键。( )
(3)共价晶体的原子间只存在共价键,而分子晶体内只存在范德华力。( )
(4)SiO 的晶体结构中,每个Si原子与2个O原子直接相连。( )
2
(5)通常状况下,60 g SiO 晶体中含有的分子数为N (N 表示阿伏加德罗常数的值)。(
2 A A
)
(6)由原子直接构成的晶体一定是共价晶体。( )
2.根据下表中给出的有关数据,判断下列说法中错误的是( )
AlCl SiCl 晶体硼 金刚石 晶体硅
3 4
熔点/℃ 190 -60 2300 3550 1410
沸点/℃ 183 57 2550 4827 2355
A.SiCl 是分子晶体
4
B.晶体硼是共价晶体
C.AlCl 是分子晶体,加热能升华
3
D.金刚石中的C—C键比晶体硅中的Si—Si键弱
3.有下列几种晶体:A.无色水晶,B.冰醋酸,C.白磷,D.金刚石,E.晶体氩,F.干冰。
(1)属于分子晶体的是________(填字母,下同)。
(2)属于共价晶体的化合物是________。
(3)受热熔化时化学键不发生变化的晶体是________,受热熔化时需克服共价键的晶体
是________。
(4)晶体中存在氢键的是________。
(5)晶体中不存在化学键的是________。
考点1分子晶体的结构特点和物理性质1. 典型共价晶体的结构模型
物质 晶体结构 结构特点
a.在晶体中每个碳原子以4个共价单键对称地与相邻的4个碳
原子相结合,形成正四面体结构
b.晶体中C—C—C夹角为
金刚
石 109°28′,碳原子采取sp3杂化
c.最小环上有6个碳原子且六个碳原子不在同一平面内
d.晶体中C原子个数与C—C键个数之比为1∶=1∶2
a.每个Si与4个O以共价键结合,形成正四面体结构
二氧
b.每个正四面体占有1个Si,4个“O”,n(Si)∶n(O)=1∶2
化硅
c.最小环上有12个原子,即6个O,6个Si
注意:(1)二氧化硅晶体中,没有独立存在的SiO 分子,所以SiO 仅是代表二氧化硅晶
2 2
体的元素组成的化学式,而不是二氧化硅晶体的分子式。
(2)金刚石、晶体硅、碳化硅、二氧化硅等共价晶体中的成键数目:①金刚石(或晶体
硅)中,1 mol C(或Si)形成2 mol C—C(或Si—Si)键;②碳化硅晶体中,1 mol碳或1 mol硅
均形成4 mol C—Si键;③SiO 晶体中,1 mol SiO 晶体中有4 mol Si—O键。
2 2
2. 共价晶体的物理特性及熔点比较
(1)共价晶体的物理性质
①一般熔点都很高、硬度都很大。
②一般不导电,但晶体硅是半导体。
③难溶于常见的溶剂。
(2)共价晶体熔点比较
对结构相似的共价晶体来说,原子半径越小,键长越短,键能越大,晶体的熔点越高。如
金刚石、碳化硅、晶体硅的物理性质见下表:
晶体 键能/(kJ·mol-1) 熔点/℃ 硬度
金刚石 (C—C)347 3350 10
碳化硅 (C—Si)301 2600 9
晶体硅 (Si—Si)226 1415 7
由于金刚石、碳化硅、晶体硅的结构相似,C原子半径小于Si原子半径,键能:C—C
键>C—Si键>Si—Si键,所以三者的熔点:金刚石>碳化硅>晶体硅。氮化碳部分结构如下图所示,其中β-氮化碳的硬度超过金刚石晶体,成为首屈一指
的超硬新材料。下列有关氮化碳的说法错误的是( )
A.β氮化碳属于共价晶体,其化学键比金刚石的更稳定
B.该晶体中碳原子和氮原子的最外层都满足8电子稳定结构
C.β氮化碳的化学式为C N,其中氮显-3价,碳显+4价
3 4
D.该晶体与金刚石结构相似,都是原子间以非极性键形成的空间网状结构
下列关于C、Si及其化合物结构与性质的论述错误的是
A.键能 C-C>Si-Si、C-H>Si-H ,因此C H 稳定性大于Si H
2 6 2 6
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度和熔点
C.常温下C、Si的最高价氧化物晶体类型相同,性质相同。
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成 键
一、选择题(每小题只有1个选项符合题意)
1.下列物质属于共价晶体的是( )
①干冰 ②SiO ③晶体硅 ④白磷 ⑤氨基乙酸 ⑥固态He
2
A.①③④⑤⑥ B.②③④⑥
C.②③ D.①②⑤⑥
2.下列关于共价晶体和分子晶体的说法不正确的是( )
A.共价晶体硬度通常比分子晶体大
B.共价晶体的熔点较高
C.分子晶体中有的水溶液能导电
D.金刚石、水晶和干冰都属于共价晶体
3. 为阿伏加德罗常数的值,下列说法正确的是
A.1 mol 被CO还原成Fe,转移 个电子B.标准状况下,11.2 L HO含有的共价键总数为
2
C.常温下,将0.5 mol Fe投入浓硫酸中,反应转移的电子数为
D.2 mol 中含 个 分子
4.下列说法正确的是
A.相同条件下,PH 比 NH 易溶于水、易液化
3 3
B.NCl 的空间结构和 VSEPR 模型都为四面体形
3
C.基态气态 Mn2+再失去1个电子比基态气态 Fe2+再失去1个电子难
25 26
D.AlN 和 GaN的成键结构与金刚石相似,为共价晶体,GaN 的熔点高于AlN
5.氮氧化铝(AlON)属于共价晶体,是一种高强度透明材料,下列叙述错误的是( )
A.AlON和SiO 所含化学键的类型相同
2
B.电解熔融AlON可得到Al
C.AlON中N元素的化合价为-1
D.AlON和SiO 的晶体类型相同
2
6.下列晶体性质的比较中错误的是( )
A.熔点:金刚石>碳化硅>晶体硅
B.沸点:NH >PH
3 3
C.硬度:白磷>冰>二氧化硅
D.熔点:SiI >SiBr >SiCl
4 4 4
7.下列说法正确的是(N 代表阿伏加德罗常数的值)( )
A
A.在含2 mol Si—O键的二氧化硅晶体中,氧原子的数目为4N
A
B.30 g二氧化硅晶体中含有0.5N 个二氧化硅分子
A
C.金刚石的熔点高与C—C键的键能有关
D.晶体硅、晶体氖均是由相应原子直接构成的共价晶体
8.将SiCl 与过量的液氨反应可生成化合物 Si(NH ) 。将该化合物在无氧条件下高温灼
4 2 4
烧,可得到氮化硅(Si N)固体,氮化硅是一种新型耐高温、耐磨材料,在工业上有广泛的
3 4
应用。下列推断可能正确的是( )
A.SiCl 、Si N 的晶体类型相同
4 3 4
B.Si N 晶体是立体网状结构
3 4
C.C N 的熔点比Si N 的低
3 4 3 4D.SiCl 晶体在熔化过程中化学键断裂
4
9.已知C N 晶体很可能具有比金刚石更大的硬度,且原子间均以单键结合,下列关于晶
3 4
体说法正确的是
A.C N 晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子
3 4
B.C N 晶体中,C—N键的键长比金刚石中C—C键的键长要长
3 4
C.C N 晶体是分子晶体
3 4
D.C N 晶体中微粒间通过离子键结合
3 4
10.中外科学家团队共同合成了T碳。T碳是将金刚石中的每个碳原子用一个由4个碳原子
形成的正四面体结构单元取代形成的碳的一种新型三维立方晶体,结构如图 1所示。下列
说法错误的是( )
A.每个T碳晶胞中含32个碳原子
B.T碳结构中的最小夹角为109°28′
C.T碳属于共价晶体
D.如图2是T碳晶胞的俯视图
11.已知SiC晶体具有较大的硬度,且原子间均以单键结合,下列关于SiC晶体的说法正确
的是( )
A.SiC晶体是分子晶体
B.SiC晶体中C—Si键的键长比金刚石中C—C键的键长要短
C.SiC晶体中粒子间通过离子键结合
D.SiC晶体中每个C原子连接4个Si原子,而每个Si原子连接4个C原子
12.单质硼有无定型和晶体两种,参考下表数据,回答下列问题:
物质 金刚石 晶体硅 晶体硼
熔点/K 大于3 828 1 683 2 573
沸点/K 5 100 2 628 2 823
硬度/Mob 10 7.0 9.5
(1)晶体硼的晶体类型属于________晶体,理由是________________
___________________________________________________________
_____________________________________________________________________________________________________________________。
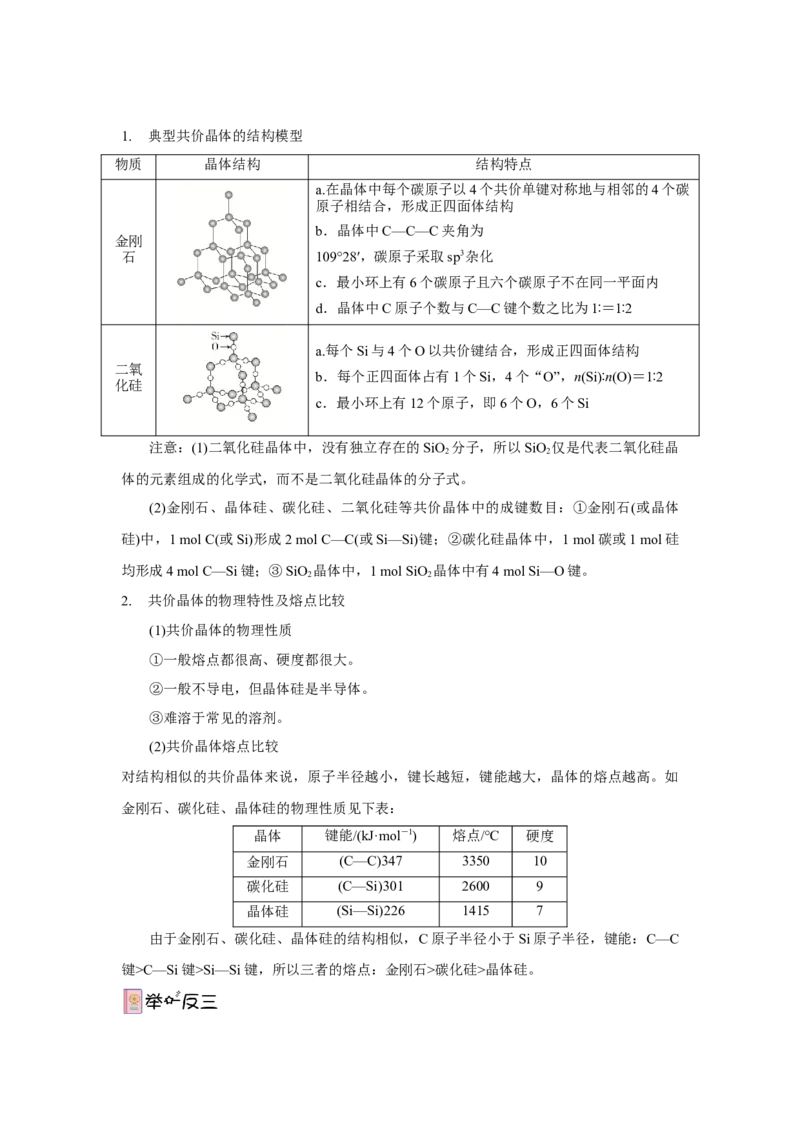
(2)已知晶体硼的基本结构单元是由硼原子组成的正二十面体,如图。其中有 20个等边三
角形的面和一定数目的顶点,每个顶点上各有一个硼原子。通过观察及推算,此基本结构
单元由________个硼原子构成,其中 B—B 键的键角为________,B—B 键的键数为
________。
13.请回答下列问题:
(1) Ga基态原子的核外电子排布式是________________。某种半导体材料由Ga和As
31
两种元素组成,该半导体材料的化学式是________,其晶体结构类型可能为________。
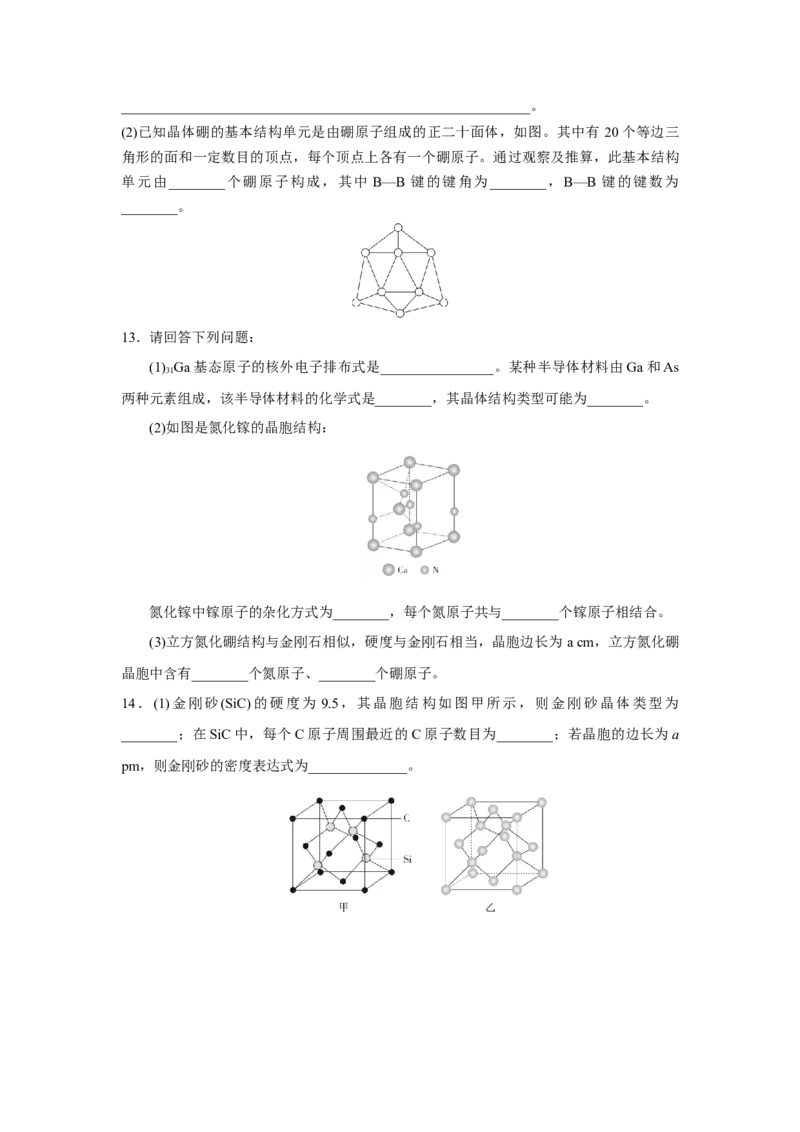
(2)如图是氮化镓的晶胞结构:
氮化镓中镓原子的杂化方式为________,每个氮原子共与________个镓原子相结合。
(3)立方氮化硼结构与金刚石相似,硬度与金刚石相当,晶胞边长为 a cm,立方氮化硼
晶胞中含有________个氮原子、________个硼原子。
14.(1)金刚砂(SiC)的硬度为 9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为
________;在SiC中,每个C原子周围最近的C原子数目为________;若晶胞的边长为a
pm,则金刚砂的密度表达式为______________。