文档内容
《分子晶体与共价晶体》第二课时 教学设计
课题 《分子晶体与共 单 3 学科 化学 年 高二
价晶体》 元 级
本章内容比较系统地介绍了晶体结构与性质,内容比较丰富。第三章作
为选修性必修2结尾章,与前两章一起构成“原子、分子、晶体的结构与性
质”三位一体的物质结构与性质模块的基本内容。本节教学内容是人教版高中
化学选择性必修第二册第三章《晶体结构与性质》第二节《分子晶体与共价晶
教材
体》第二课时。
分析
本节安排了“共价晶体”这部分内容。学生通过学习这部分知识,能辨识
常见的共价晶体,并能从微观角度分析共价晶体中各构成微粒之间的作用对共
价晶体物理性质的影响。能利用共价晶体的通性推断常见的共价晶体,并能利
用均摊法对晶胞进行分析。
教学 宏观辨识与微观探析:能辨识常见的共价晶体,并能从微观角度分析共价
目标 晶体中各构成微粒之间的作用对共价晶体物理性质的影响。
与核
证据推理与模型认知:能利用共价晶体的通性推断常见的共价晶体,并能
心素
利用均摊法对晶胞进行分析。
养
重点 共价晶体
难点
教学过程
教学环节 教师活动 学生活动 设计意图
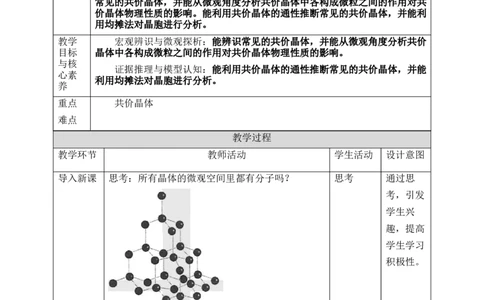
导入新课 思考:所有晶体的微观空间里都有分子吗? 思考 通过思
考,引发
学生兴
趣,提高
学生学习
积极性。讲授新课 第一节 分子晶体与共价晶体
第二课时 共价晶体
一、共价晶体
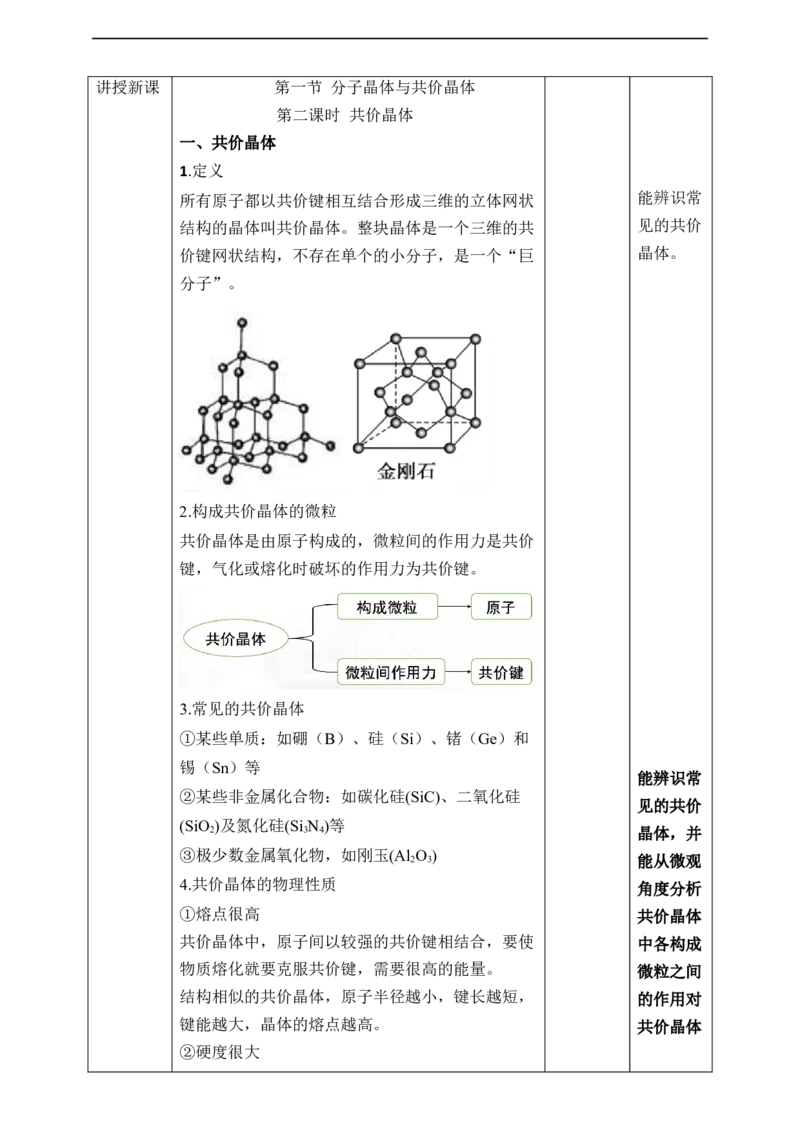
1.定义
所有原子都以共价键相互结合形成三维的立体网状 能辨识常
结构的晶体叫共价晶体。整块晶体是一个三维的共 见的共价
价键网状结构,不存在单个的小分子,是一个“巨 晶体。
分子”。
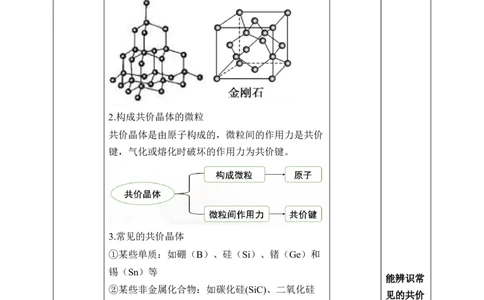
2.构成共价晶体的微粒
共价晶体是由原子构成的,微粒间的作用力是共价
键,气化或熔化时破坏的作用力为共价键。
3.常见的共价晶体
①某些单质:如硼(B)、硅(Si)、锗(Ge)和
锡(Sn)等
能辨识常
②某些非金属化合物:如碳化硅(SiC)、二氧化硅
见的共价
(SiO )及氮化硅(Si N )等
2 3 4 晶体,并
③极少数金属氧化物,如刚玉(Al O )
2 3 能从微观
4.共价晶体的物理性质
角度分析
①熔点很高 共价晶体
共价晶体中,原子间以较强的共价键相结合,要使 中各构成
物质熔化就要克服共价键,需要很高的能量。 微粒之间
结构相似的共价晶体,原子半径越小,键长越短, 的作用对
键能越大,晶体的熔点越高。 共价晶体
②硬度很大③一般不导电,但晶体硅是半导体 物理性质
④难溶于一般溶剂 的影响。
二、典型的共价晶体 思考
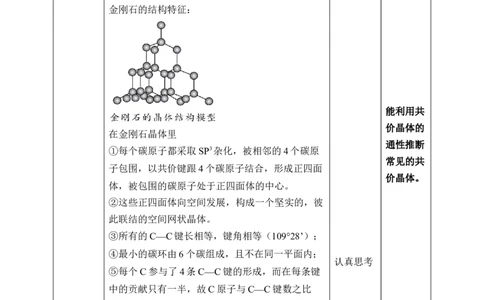
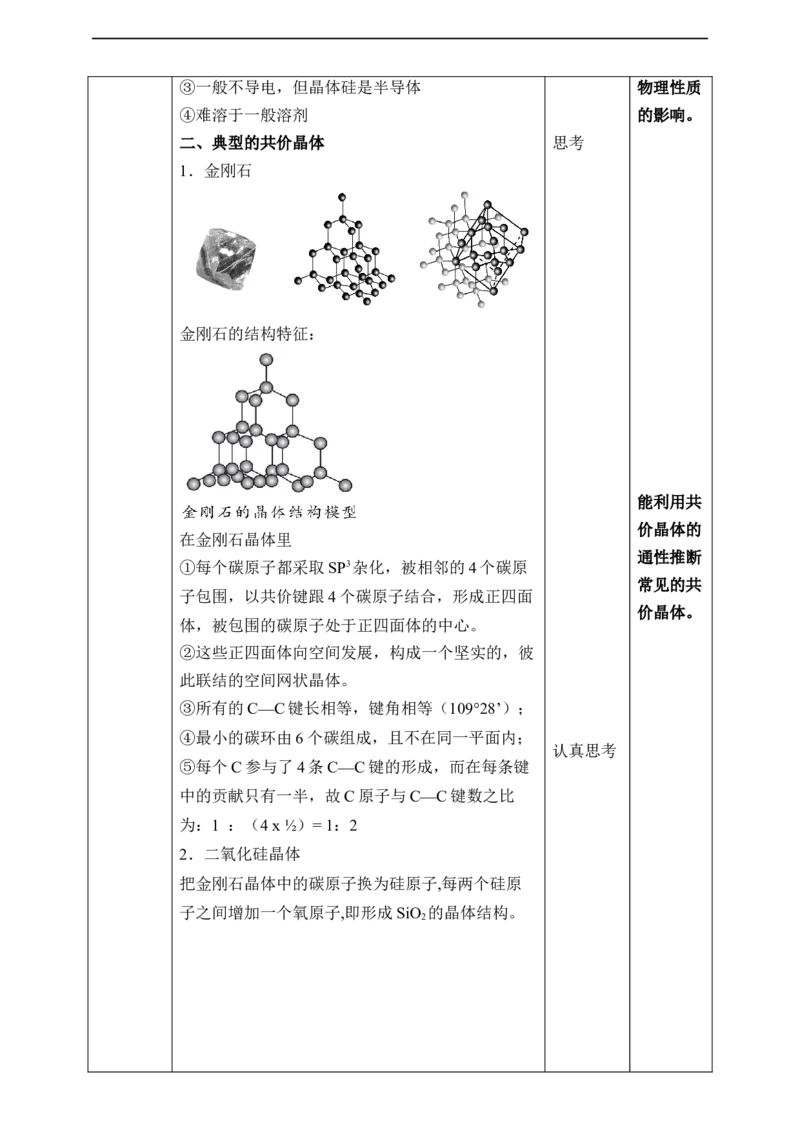
1.金刚石
金刚石的结构特征:
能利用共
价晶体的
在金刚石晶体里
通性推断
①每个碳原子都采取SP3杂化,被相邻的4个碳原
常见的共
子包围,以共价键跟4个碳原子结合,形成正四面
价晶体。
体,被包围的碳原子处于正四面体的中心。
②这些正四面体向空间发展,构成一个坚实的,彼
此联结的空间网状晶体。
③所有的C—C键长相等,键角相等(109°28’);
④最小的碳环由6个碳组成,且不在同一平面内;
认真思考
⑤每个C参与了4条C—C键的形成,而在每条键
中的贡献只有一半,故C原子与C—C键数之比
为:1 :(4 x ½)= 1:2
2.二氧化硅晶体
把金刚石晶体中的碳原子换为硅原子,每两个硅原
子之间增加一个氧原子,即形成SiO 的晶体结构。
2能利用均
摊法对晶
胞进行分
析。
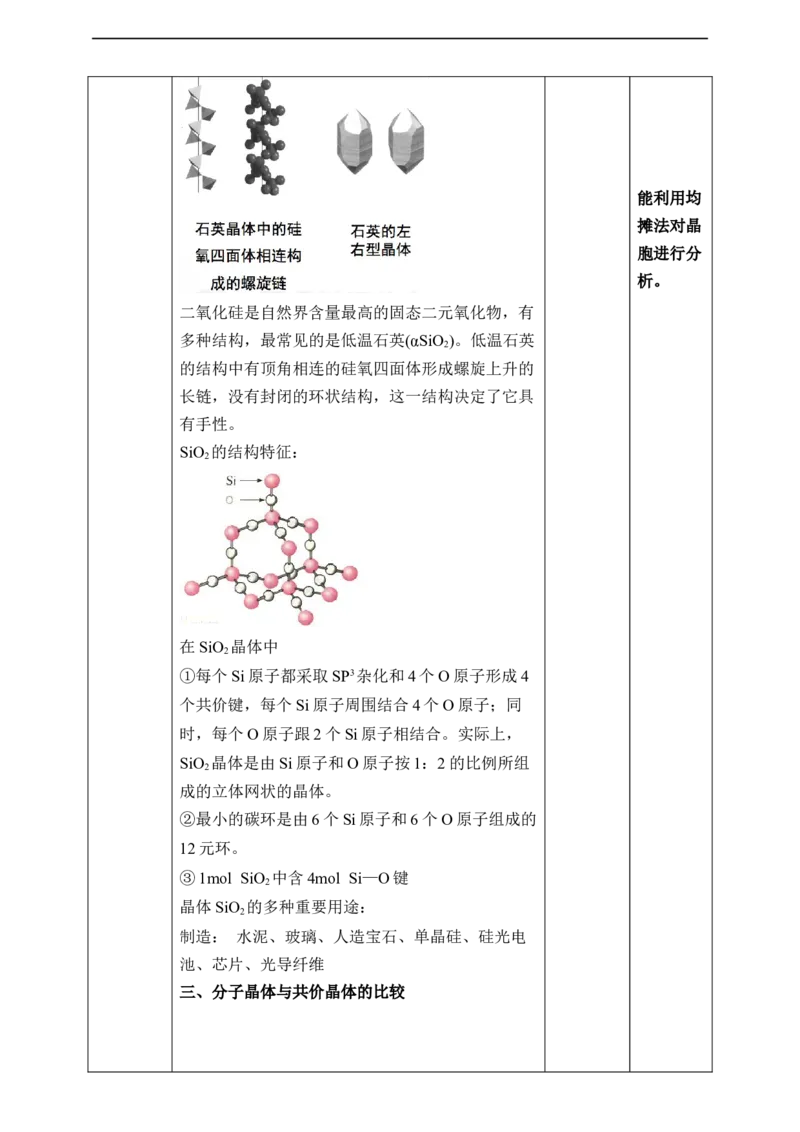
二氧化硅是自然界含量最高的固态二元氧化物,有
多种结构,最常见的是低温石英(αSiO )。低温石英
2
的结构中有顶角相连的硅氧四面体形成螺旋上升的
长链,没有封闭的环状结构,这一结构决定了它具
有手性。
SiO 的结构特征:
2
在SiO 晶体中
2
①每个Si原子都采取SP3杂化和4个O原子形成4
个共价键,每个Si原子周围结合4个O原子;同
时,每个O原子跟2个Si原子相结合。实际上,
SiO 晶体是由Si原子和O原子按1:2的比例所组
2
成的立体网状的晶体。
②最小的碳环是由6个Si原子和6个O原子组成的
12元环。
③1mol SiO 中含4mol Si—O键
2
晶体SiO 的多种重要用途:
2
制造: 水泥、玻璃、人造宝石、单晶硅、硅光电
池、芯片、光导纤维
三、分子晶体与共价晶体的比较四、分子晶体与共价晶体的判断方法
(1)依据构成晶体的微粒和微粒间的作用力判断。
构成共价晶体的微粒是原子,微粒间的作用力是共
价键;构成分子晶体的微粒是分子或原子(稀有气体),
微粒间的作用力是分子间作用力。
(2)依据晶体的熔点判断。
共价晶体的熔点高,常在1000℃以上;而分子晶体熔
点低,常在数百摄氏度以下甚至更低。
(3)还可以依据晶体的硬度与机械性能判断。
共价晶体硬度大,分子晶体硬度小且较脆。
(4)依据导电性判断。
分子晶体为非导体,但部分溶于水后能导电;原子晶
体多数为非导体,但晶体硅、锗是半导体。
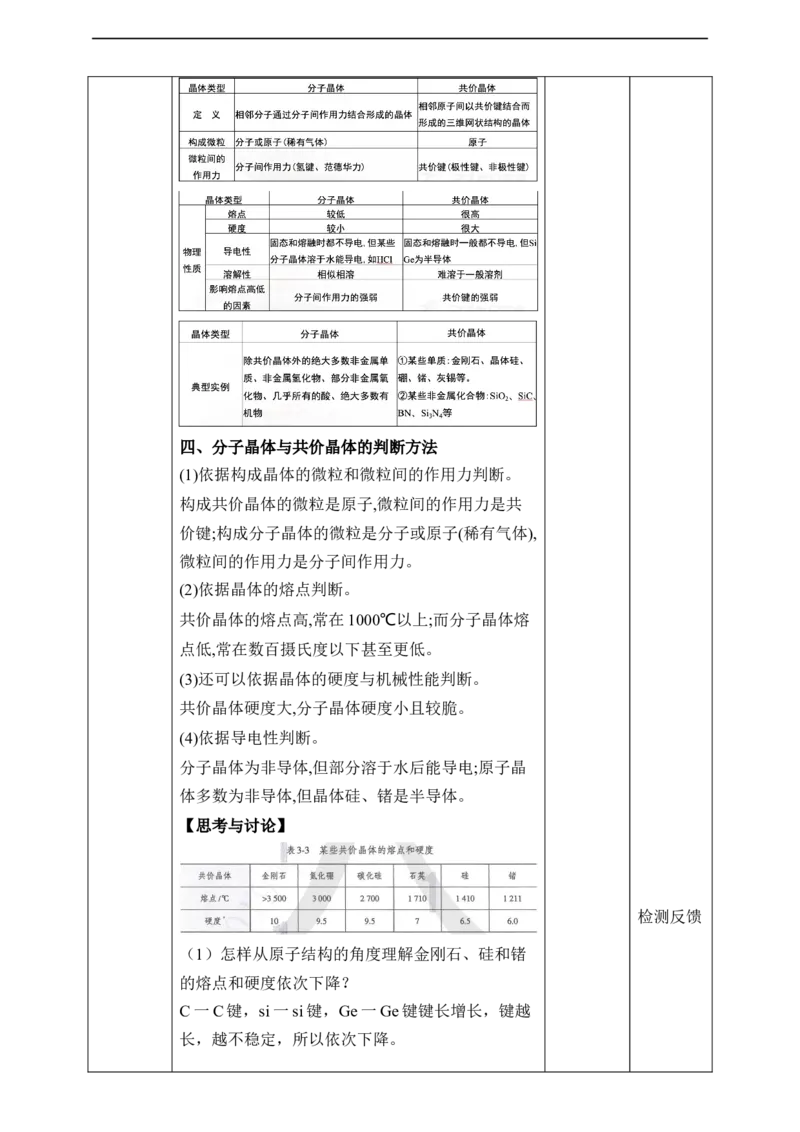
【思考与讨论】
检测反馈
(1)怎样从原子结构的角度理解金刚石、硅和锗
的熔点和硬度依次下降?
C一C键,si一si键,Ge一Ge键键长增长,键越
长,越不稳定,所以依次下降。(2)“具有共价键的晶体叫做共价晶体”,这种
说法对吗?为什么?
不对,共价晶体的网状结构是共价键形成的,而有
的分子晶体中也存在共价键,比如干冰、冰等。
【课堂练习】
1.判断正误(对的在括号内打“√”,错的在括号
内打“×”。)
1.分子晶体中一定存在共价键。 ( )
2.干冰升华的过程中破坏了共价键。( )
3.二氧化硅和干冰虽然是同一主族元素形成的氧化
物,但属于不同的晶体类型。( )
4.分子晶体的熔、沸点比较低,共价晶体的熔、沸点
比较高。( )
5.含有共价键的晶体都是共价晶体。( )
6.SiO 是二氧化硅的分子式。( )
2
答案:(1)× (2)× (3) √ (4)√ (5)× (6) ×
2.下列有关共价晶体的叙述错误的是( )
A.共价晶体中,只存在共价键
B.共价晶体具有空间网状结构
C.共价晶体中不存在独立的分子
D.共价晶体熔化时不破坏共价键
解析:选D。A项,共价晶体中原子之间通过共价键
相连;B项,共价晶体是相邻原子之间通过共价键
结合而成的空间网状结构;C项,共价晶体是由原
子以共价键相结合形成的,不存在独立的分子;D
项,共价晶体中原子是通过共价键连接的,熔化时
需要破坏共价键。
3.3.下列说法正确的是( )
A.共价晶体中只存在非极性共价键
B.因为HCl的相对分子质量大于HF,所以HCl晶体
的熔点高于HF
C.干冰升华时,分子内共价键不会发生断裂D.金属元素和非金属元素形成的化合物一定是离子
化合物
解析:选C。共价晶体中可能存在极性共价键,如
SiO 、SiC等,A项不正确;HF晶体中存在氢键,熔点
2
高于HCl晶体,B项不正确;干冰升华是物理变化,分
子间作用力被破坏,但分子内共价键不断裂,C项正
确;金属元素和非金属元素形成的化合物不一定是
离子化合物,也可能是共价化合物,如AlCl 等,D项不
3
正确。
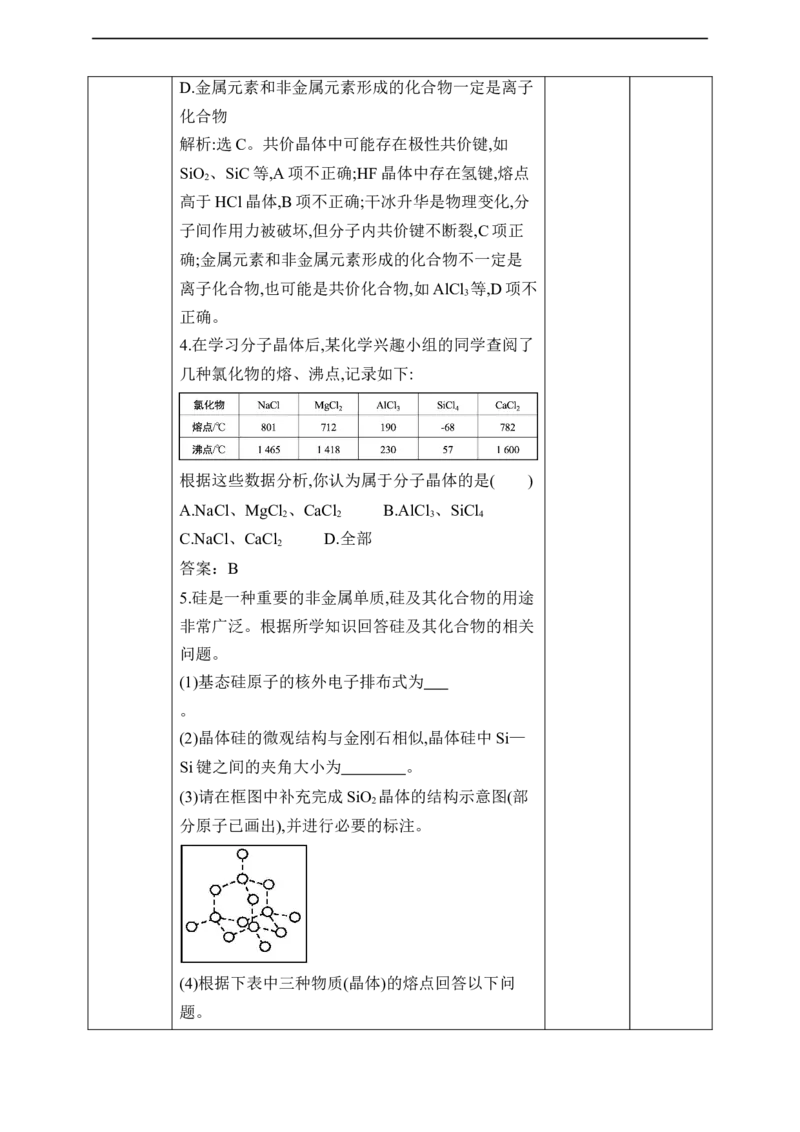
4.在学习分子晶体后,某化学兴趣小组的同学查阅了
几种氯化物的熔、沸点,记录如下:
根据这些数据分析,你认为属于分子晶体的是( )
A.NaCl、MgCl 、CaCl B.AlCl 、SiCl
2 2 3 4
C.NaCl、CaCl D.全部
2
答案:B
5.硅是一种重要的非金属单质,硅及其化合物的用途
非常广泛。根据所学知识回答硅及其化合物的相关
问题。
(1)基态硅原子的核外电子排布式为
。
(2)晶体硅的微观结构与金刚石相似,晶体硅中Si—
Si键之间的夹角大小为 。
(3)请在框图中补充完成SiO 晶体的结构示意图(部
2
分原子已画出),并进行必要的标注。
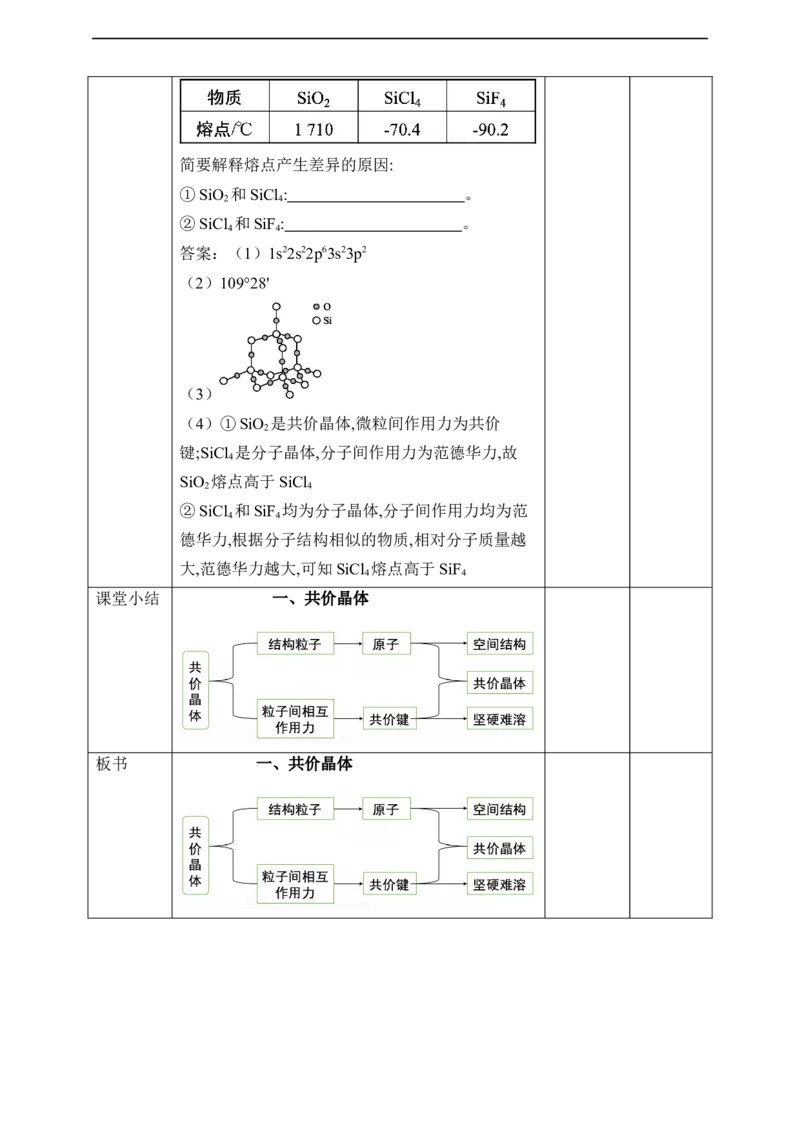
(4)根据下表中三种物质(晶体)的熔点回答以下问
题。简要解释熔点产生差异的原因:
①SiO 和SiCl : 。
2 4
②SiCl 和SiF : 。
4 4
答案:(1)1s22s22p63s23p2
(2)109°28'
(3)
(4)①SiO 是共价晶体,微粒间作用力为共价
2
键;SiCl 是分子晶体,分子间作用力为范德华力,故
4
SiO 熔点高于SiCl
2 4
②SiCl 和SiF 均为分子晶体,分子间作用力均为范
4 4
德华力,根据分子结构相似的物质,相对分子质量越
大,范德华力越大,可知SiCl 熔点高于SiF
4 4
课堂小结 一、共价晶体
板书 一、共价晶体