文档内容
第三章 铁 金属材料
第二节 金属材料 课时作业
第二课时 新型合金 物质的量在化学方程式计算中的应用
基础达标
1.下列不属于新型合金的是( )
A.储氢合金 B.钛合金
C.铁合金 D.形状记忆合金
2.下列说法正确的是( )
A.用来制造储存氢气所用钢瓶的合金是储氢合金
B.不锈钢是最常见的新型合金
C.新型合金主要应用于航天航空﹑生物工程等领域
D.碳纤维复合材料属于新型合金材料
3.科学技术的迅猛发展促进了社会的进步。下列科技成果涉及的材料中,主要成分不
属于金属材料的是( )
选项 A B C D
科技
成果
“蛟龙”号耐压球
C919飞机外壳 宇航服 地铁列车车体
壳
成分 铝锂合金 钛合金 聚酯纤维 不锈钢
4.2019年12月17日,我国国产航母——山东舰正式列装服役。下列用于制造该舰的
材料属于无机非金属材料的是( )
A.舰身无磁镍铬钛合金钢 B.甲板耐磨SiC涂层
C.舰载机起飞挡焰板铝合金 D.舰底含硅有机涂层
5.钛和钛的合金具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,尤
其是钛合金与人体器官具有很好的“生物相容性”。根据它们的主要性能,下列用途不切
合实际的是( )
A.用来做保险丝 B.用于制造航天飞机杨sir化学,侵权必究C.用来制造人造骨 D.用于家庭装修,做钛合金装饰门
6.下列关于金属材料的说法不正确的是( )
A.镧镍合金能大量吸收H 形成金属氢化物,可作储氢材料杨sir化学,侵权必究
2
B.任何两种金属都能形成合金
C.金属材料中可能含有非金属元素
D.不锈钢中的主要合金元素为Cr和Ni
7.已知30 mL浓度为0.5 mol·L-1的NaSO 溶液恰好与50 mL浓度为0.1 mol·L-1的KRO
2 3 4
溶液完全反应转化为NaSO 。则R元素在产物中的化合价是( )
2 4
A.+1 B.+2 C.+3 D.+4
8.等质量的两份铝分别与适量的稀HSO 和NaOH溶液完全反应,若消耗两溶液的体
2 4
积相同,则稀HSO 与NaOH溶液的物质的量浓度之比为( )
2 4
A.3∶2 B.2∶3 C.2∶1 D.1∶2
9.若加热5.00 g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减
少了0.31 g,则原混合物中碳酸钠的质量为
A.1.68 g B.3.32 g C.4.16 g D.4.38 g
10. 甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液中,向两烧杯中
分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲∶乙=1∶2,则加入的铝粉
质量为( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
能力提升
11.28 g铁粉溶于稀盐酸中,然后加入足量的NaO 固体,充分反应后过滤,将滤渣
2 2
加强热,最终得到的固体质量为( )
A.36 g B.40 g C.80 g D.160 g
12.16.3 g由NaO、NaO、NaCO、NaOH组成的混合物与200 g质量分数为7.3%的
2 2 2 2 3
盐酸恰好反应,蒸干反应后的溶液,最终得到的固体的质量为( )
A.8 g B.15.5 g C.11.7 g D.23.4 g
13.某同学研究铝及其化合物 性的质时设计了如下两个实验方案。方案①:2.7 g Al\s\up 2(100 mL HCl)\s\up 4()X溶液N H— a — O\s\up 4()Al(OH) 3 沉淀
方案②:2.7 g Al\s\up 2(100 mLNaOH)\s\up 4()Y溶液H —— C → l\s\up 4()Al(OH) 3 沉淀
NaOH和HCl的浓度均是3 mol·L-1,如图是向X溶液和Y溶液中分别加入NaOH和
HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确
的是
A.b曲线表示的是向X溶液中加入NaOH溶液
B.在O点时两方案中所得溶液浓度相等
C.a、b曲线表示的反应都是非氧化还原反应
D.X溶液是ACl 溶液,Y溶液显碱性
3
14.取27.4 g由NaCO 和NaHCO 组成的固体混合物,加热至质量不再减少,冷却后
2 3 3
称得剩余固体质量为21.2 g;再将该剩余固体加入到 500 mL足量稀盐酸中,充分反应。
(忽略溶液体积变化)
(1)加热时,生成HO的质量是___________g。
2
(2)原混合物中NaCO 的物质的量是___________mol。
2 3
(3)所得溶液中Na+的物质的量浓度是___________mol·L-1。
(4)整个过程中,生成CO 的总体积是___________L(标准状况)。
2
直击高考
15.取A、B两份等物质的量浓度的NaOH溶液,每份100 mL,先分别向A、B中通
入不等量的CO,再继续向两溶液中逐滴加入0.l mol·L-1的盐酸,产生如图所示关系。下
2
列说法不正确的是( )
A.A曲线中的P点发生的离子反应为H++CO2-=HCO -
3 3
B.加盐酸之前B溶液中的溶质是氢氧化钠和碳酸钠
C.B曲线最终产生的CO 体积为33.6 mL
2
D.原NaOH溶液的物质的量浓度为0.075 mol·L-1
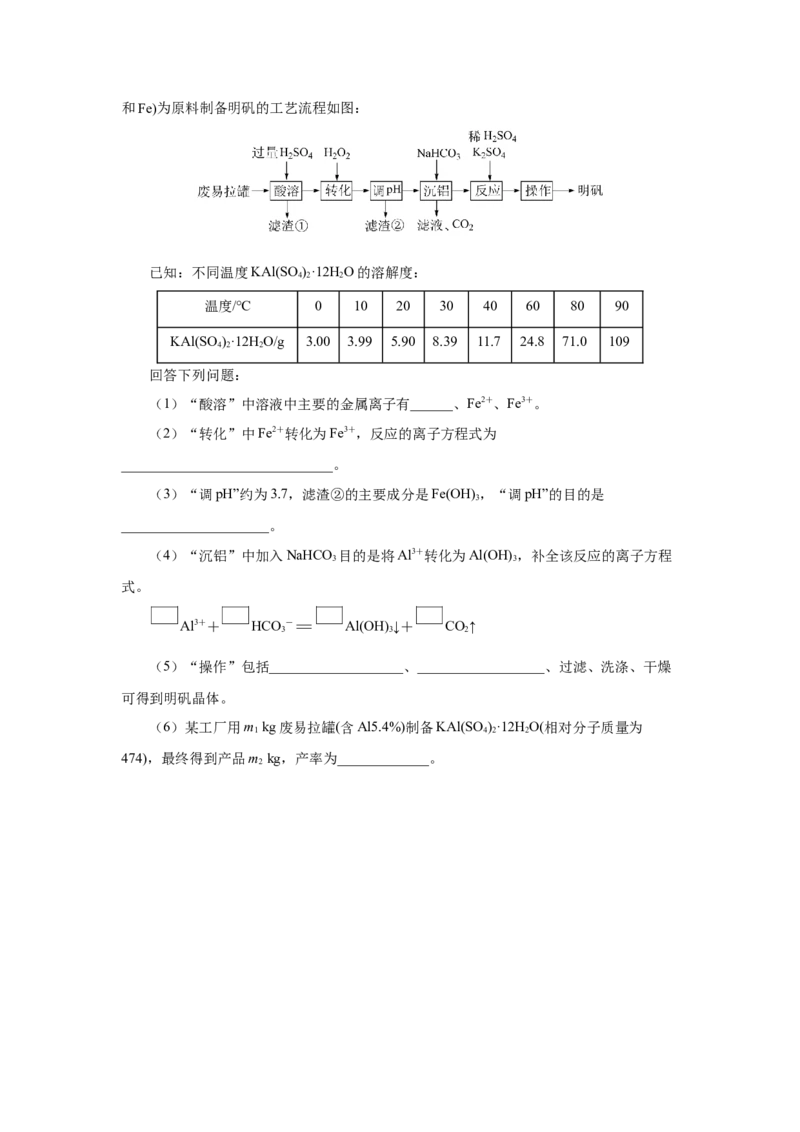
16.明矾[KAl(SO)·12H O]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为Al
4 2 2和Fe)为原料制备明矾的工艺流程如图:
已知:不同温度KAl(SO )·12H O的溶解度:
4 2 2
温度/℃ 0 10 20 30 40 60 80 90
KAl(SO )·12H O/g 3.00 3.99 5.90 8.39 11.7 24.8 71.0 109
4 2 2
回答下列问题:
(1)“酸溶”中溶液中主要的金属离子有______、Fe2+、Fe3+。
(2)“转化”中Fe2+转化为Fe3+,反应的离子方程式为
______________________________。
(3)“调pH”约为3.7,滤渣②的主要成分是Fe(OH) ,“调pH”的目的是
3
_____________________。
(4)“沉铝”中加入NaHCO 目的是将Al3+转化为Al(OH) ,补全该反应的离子方程
3 3
式。
Al3++ HCO -= Al(OH) ↓+ CO↑
3 3 2
(5)“操作”包括___________________、__________________、过滤、洗涤、干燥
可得到明矾晶体。
(6)某工厂用m kg废易拉罐(含Al5.4%)制备KAl(SO )·12H O(相对分子质量为
1 4 2 2
474),最终得到产品m kg,产率为_____________。
2