文档内容
3.2 醇 酚 (精讲)
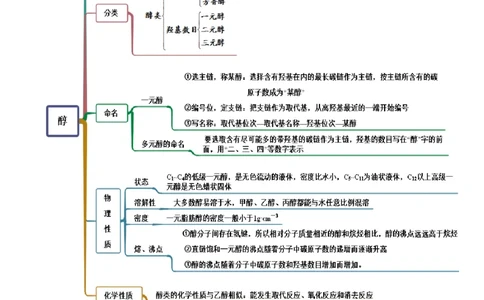
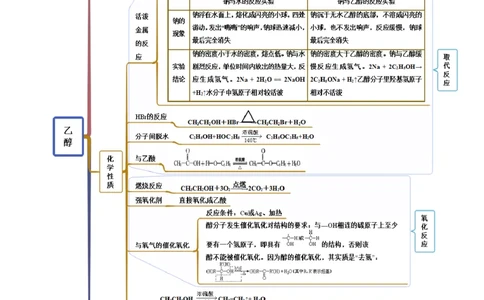
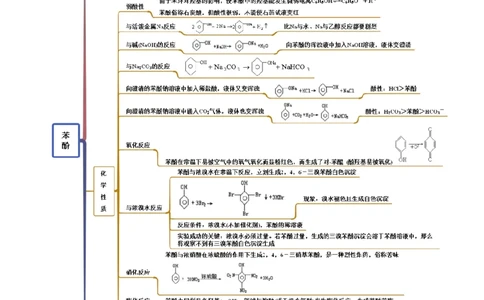
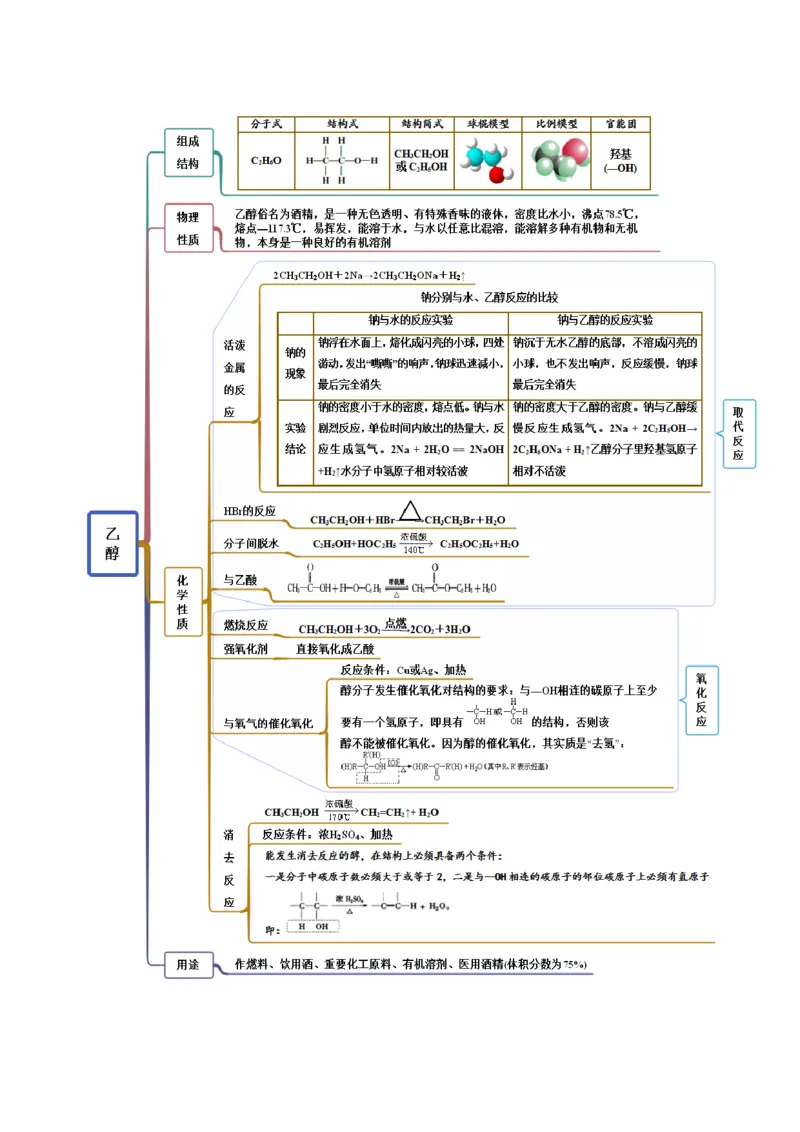
思维导图常见考点
考点一 醇类
【例1-1】(2021·甘肃·静宁县第一中学高二阶段练习)下列物质既能发生消去反应,又能催化氧化生成醛
的是
A.CHCHCHOH B.CHOH
3 2 2 3
C. D.
【答案】A
【解析】A.CHCHCHOH与羟基相连的邻位碳上有H原子,可发生消去反应,含有-CHOH,能催化氧
3 2 2 2
化生成醛,A正确;
B.CHOH与羟基相连的邻位碳上没有H原子,不能发生消去反应,B错误;
3
C. 与羟基相连的邻位碳上有H原子,可发生消去反应,与羟基之间相连的碳只有1个H
原子,只能催化氧化生成酮,C错误;
D. 与羟基之间相连的碳没有H原子,不能发生催化氧化反应,D错误;
故选:A。
【例1-2】(2022·甘肃张掖)足量的金属钠分别与甲醇、乙二醇、丙三醇反应,放出等体积的氢气,消耗这三种醇的物质的量之比是
A.6:3:2 B.2:3:6 C.3:2:1 D.1:2:3
【答案】A
【解析】足量的金属钠分别与甲醇、乙二醇、丙三醇反应,放出等体积的氢气,说明这3种醇中所含的羟
基的总量是相同的。因为甲醇、乙二醇、丙三醇分子中分别有1个、2个、3个羟基,所以消耗这三种醇的
物质的量之比为6:3:2,A正确,本题选A。
【一隅三反】
1.(2021·全国·高二课时练习)下列物质中,不属于醇类的是
A. B.
C. D.
【答案】C
【解析】A. 是丙烷中的氢原子被羟基取代,属于醇,故A错误;
B. 是甲苯中的氢原子被羟基取代,属于醇,故B错误;
C. 是羟基取代苯环上的氢原子,属于酚,故C正确;
D. 是丙烷中的三个氢原子被羟基取代,属于醇,故D错误;
故选C。
2.(2022·全国·高二专题练习)下列物质中,沸点最高的是
A.CHCHCH B.CHCHCHOH
3 2 3 3 2 2
C.CHOH D.CHCHCHCHOH
3 3 2 2 2
【答案】D
【解析】因为醇的分子之间有通过醇羟基相连的氢键,所以稳定性高于CHCHCH,一元正醇,C原子数
3 2 3
越多,沸点也越高,沸点越高D为4个碳原子,碳原子最多,相对分子量最大,沸点最高,综上所述故选
D。3.(2021·黑龙江·哈九中高二开学考试)已知分子中含有羟基的物质都能与钠反应产生氢气。乙醇、乙二
醇( )、丙三醇( )分别与足量金属钠作用,产生氢气在相同条件下体积之比为
6∶2∶3。则这三种醇的物质的量之比为
A.6∶3∶2 B.1∶3∶2
C.3∶2∶1 D.6∶1∶1
【答案】D
【解析】羟基个数与被置换的氢原子个数之比为1:1,三种醇与钠反应放出氢气的体积比为6:2:3(相同条件
下),则三种醇提供的羟基数之比为6:2:3,因此三种醇的物质的量之比为(6×1): : =6:1:1;
故选D。
4.(2021·安徽·蚌埠二中高二期中)有两种饱和一元醇的混合物37.6 g,与23g Na充分反应,生成的H
2
在标准状态下的体积为11.2L,这两种醇分子中相差一个碳原子。则这两种可能醇是
A.甲醇和乙醇 B.乙醇和1-丙醇
C.2-丙醇和1-丁醇 D.无法确定
【答案】A
【解析】饱和一元醇与钠按物质的量比1:1反应,生成的H 在标准状况下的体积为11.2L,则氢气的物质
2
的量为 =0.5mol,由 :需要金属Na的物质的量为1mol,参加反应的钠的质量为
1mol×23g/mol=23g,故Na完全反应,故饱和一元醇混合物的平均摩尔质量= =37.6g/mol,由于两种
醇分子中相差一个碳原子,设醇中碳原子数目分别为n、n+1,则:14n+2+16 75.2
12(n+1)+2(n+1)+2+16,可得n=1,综上所述这两种可能醇是甲醇和乙醇,故A正确;选A。
考点二 乙醇
【例2-1】(2021·海南·琼中中学高二阶段练习)(多选)乙醇分子结构中各种化学键如图所示。关于乙醇
在各种反应中断裂键的说法,不正确的是A.与金属钠反应时键①断裂
B.和浓硫酸共热到170℃时,键②与⑤断裂
C.和浓硫酸共热到140℃时,仅有键②断裂
D.在铜催化下与O 反应时,键①和⑤断裂
2
【答案】CD
【解析】A.乙醇与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键,即①断裂,故A正确;
B.乙醇和浓硫酸共热到170℃时发生消去反应,断裂碳氧键、与羟基所连的碳的相邻的碳上的碳氢键,即
②⑤断裂,故B正确;
C.乙醇和浓硫酸共热至140℃时,发生分子间脱水生成乙醚和水,故乙醇断键的位置为①和②,故C错
误;
D.乙醇在铜催化下与O 反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的氢,即①③断
2
裂,故D错误;
故选CD。
【例2-2】(2022·云南绥江·高二期末)一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO和HO的
2 2
总质量为26.8g,其中HO的质量为10.8g,则CO的质量是
2
A.1.4g B.2.8g
C.4.4g D.在2. 8g和4.4g之间
【答案】B
【解析】一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO和HO的总质量为26.8g,其中HO的质
2 2 2
量为10.8g,则n(H O)= =0.6mol,根据H原子守恒可知,n(H)=2n(H O)=1.2mol,故n(C HOH)=
2 2 2 5
=0.2mol,根据碳原子守恒可知,n(CO)+n(CO )=0.2×2mol=0.4mol,根据质量守恒可知,28n(CO)
2
+44n(CO )=26.8-10.8=16g,联合解得,n(CO)=0.1mol,m=n(CO)M(CO)=0.1mol×28g/mol=2.8g,故答案为:
2
B。【一隅三反】
1.(2022·江苏苏州·高一期末)乙醇(C HOH)是一种优质的液体燃料,一种由二甲醚(CHOCH )与合成气
2 5 3 3
制乙醇的反应为CHOCH +CO+2H = CHOH+C HOH。下列说法正确的是
3 3 2 3 2 5
A.CHOCH 和C HOH互为同分异构体
3 3 2 5
B.CHOH和C HOH互为同素异形体
3 2 5
C.C HOH与H 属于非电解质
2 5 2
D.CHOCH 与CO属于有机物
3 3
【答案】A
【解析】A. CHOCH 和C HOH的分子式相同都是C HO而结构不同互为同分异构体,故A正确;
3 3 2 5 2 6
B. CHOH和C HOH的结构相似,分子组成相差一个-CH-,都属于饱和一元醇,互为同系物,故B错
3 2 5 2
误;
C. C HOH属于非电解质,H 是单质,既不是电解质也不是非电解质,故C错误;
2 5 2
D. CHOCH 属于有机物,CO属于无机物,故D错误;
3 3
故答案为:A
2.(2021·全国·高二课时练习)写出下列物质间转化的化学方程式,并注明反应条件___________。
【答案】①CHCHBr+NaOH CHCHOH+NaBr,;
3 2 3 2
②CHCHOH CH=CH ↑+H O;
3 2 2 2 2
③CH=CH +HBr CHCHBr;
2 2 3 2
④CHCHBr+NaOH CH=CH ↑+NaBr+H O;
3 2 2 2 2
⑤CH=CH +H O CHCHOH;
2 2 2 3 2
⑥CHCHOH+HBr CHCHBr+ H O;
3 2 3 2 2
⑦2C HOH+O 2CHCHO+2H O
2 5 2 3 2【解析】①溴乙烷在NaOH水溶液中水解生成乙醇,反应的方程式为CHCHBr+NaOH
3 2
CHCHOH+NaBr,;
3 2
②乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯,反应的化学方程式为:CHCHOH
3 2
CH=CH ↑+H O;
2 2 2
③乙烯含有不饱和C=C双键,能与溴化氢发生加成反应生成溴乙烷,反应的化学方程式为:
CH=CH +HBr CHCHBr;
2 2 3 2
④溴乙烷和氢氧化钠醇溶液中共热生成乙烯、溴化钠和水,反应的化学方程式为:CHCHBr+NaOH
3 2
CH=CH ↑+NaBr+H O;
2 2 2
⑤乙烯含有不饱和C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇,反应的化学方程式为:
CH=CH +H O CHCHOH;
2 2 2 3 2
⑥乙醇和HBr在催化剂下发生取代反应得到溴乙烷,反应的化学方程式为:CHCHOH+HBr
3 2
CHCHBr+ H O;
3 2 2
⑦乙醇能发生催化氧化生成乙醛和水,反应的化学方程式为:2C HOH+O 2CHCHO+2H O。
2 5 2 3 2
考点三 苯酚
【例3-1】(2021·内蒙古·北京八中乌兰察布分校高二阶段练习)能证明苯酚具有弱酸性的实验是
A.加入浓溴水生成白色沉淀 B.苯酚钠溶液中通入 CO 后,溶液由澄清变浑浊
2
C.浑浊的苯酚加热后变澄清 D.苯酚的水溶液中加NaOH溶液,生成苯酚钠
【答案】B
【解析】A.浓溴水与苯酚发生取代反应,生成白色沉淀,无法说明苯酚的酸性,故A错误;
B.碳酸是弱酸,与苯酚钠溶液反应生成苯酚,说明苯酚酸性比碳酸弱,故B正确;
C.苯酚的浑浊液加热后变澄清,说明温度升高苯酚溶解度增大,无法说明苯酚的酸性,故C错误;
D.苯酚的水溶液中加NaOH溶液,生成苯酚钠,只能说明苯酚溶液呈酸性,故D错误。
故选:B。
【例3-2】(2021·北京理工大学附属中学分校高二期中)下列有关苯酚的说法不正确的是
A.纯净的苯酚是无色晶体B.苯酚有特殊气味
C.常温时苯酚易溶于有机溶剂和蒸馏水
D.苯酚沾到皮肤上可用酒精清洗
【答案】C
【解析】A.纯净的苯酚是无色晶体,故A正确;
B.苯酚有特殊气味,故B正确;
C.常温时苯酚易溶于有机溶剂,在蒸馏水中溶解度不大,65℃以上时与水混溶,故C错误;
D.苯酚有毒,对皮肤有腐蚀性,苯酚沾到皮肤上可用酒精清洗,故D正确;故选:C。
【一隅三反】
1.(2021·宁夏长庆高级中学高二期末)下列关于苯酚的叙述中,正确的是
A.苯酚呈弱酸性,能使石蕊溶液显浅红色
B.苯酚分子中的13个原子不可能处于同一平面上
C.苯酚有强腐蚀性,沾在皮肤上可用酒精洗涤
D.苯酚能与FeCl 溶液反应生成紫色沉淀
3
【答案】C
【解析】A.苯酚的酸性很弱,不能使石蕊试液变色,故A错误;
B.苯环为平面结构,酚−OH与苯环直接相连,C−O可在空间旋转,则13个原子可能共面,故B错误;
C.苯酚有毒,可溶于酒精,则沾在皮肤上可用酒精洗涤,故C正确;
D.苯酚能与FeCl 溶液发生显色反应,溶液为紫色,故D错误;
3
故选C。
2.(2021·河北·曹妃甸一中高二阶段练习)下列关于苯酚的叙述正确的是
A.纯净的苯酚是粉红色晶体,65℃以上时能与水混溶
B.苯酚溅在皮肤上应用酒精洗涤
C.苯酚的酸性很弱,不能使酚酞指示剂变色,但可以与碳酸氢钠反应放出
D.苯酚比苯难发生苯环上的取代反应
【答案】B
【解析】A.纯净的苯酚是无色晶体,65℃以上时能与水混溶,故A错误;
B.苯酚易溶于苯酚,苯酚溅在皮肤上应用酒精洗涤,故B正确;
C.苯酚的酸性弱于碳酸,不能使酚酞指示剂变色,也不能与碳酸氢钠反应放出 CO,只能生成碳酸氢钠,
2
故C错误;
D.苯酚能和溴水发生取代反应生成三溴苯酚,苯和液溴发生取代反应一般生成溴苯,所以苯比苯酚难发生苯环上的取代反应,故D错误;
故选B。
3.(2021·全国·高二课时练习)苯酚具有弱酸性的原因是
A.苯环使羟基中的 极性变强 B.羟基使苯环活化
C.苯酚能与 溶液反应 D.苯酚与溴水反应
【答案】A
【解析】A.苯环的存在使羟基中的O-H极性变强,H可以电离出来,使苯酚显弱酸性,故A选;
B.羟基也能使苯环活化,但不是苯酚具有弱酸性的原因,故B不选;
C.苯酚有弱酸性,能与NaOH溶液反应生成盐,这是苯酚具有弱酸性的结果,故C不选;
D.苯酚与溴水反应是羟基使苯环活化的结果,故D不选;
故选A。
4.(2021·河北·张家口市第一中学高二阶段练习)苯中可能混有少量的苯酚,下列实验能证明苯中是否混
有少量苯酚的是
A.取样品,加入少量高锰酸钾酸性溶液,振荡,看酸性高锰酸钾溶液是否褪色,褪色则有苯酚,不褪色
则无苯酚
B.取样品,加入氢氧化钠溶液,振荡,观察样品是否分层
C.取样品,加入过量的浓溴水,观察是否产生白色沉淀,若产生白色沉淀则有苯酚,没有白色沉淀则无
苯酚
D.取样品,滴加少量的 溶液,观察溶液是否显紫色,若显紫色则有苯酚,若不显紫色则无苯酚
【答案】AD
【解析】A.苯酚能使锰酸钾褪色,但是苯不能,所以取样品,加入少量高锰酸钾酸性溶液,振荡,看酸
性高锰酸钾溶液是否褪色,褪色则有苯酚,不褪色则无苯酚,A正确;
B.不管苯中是否有苯酚,加入NaOH溶液都会产生分层,因此无法鉴别,B错误;
C.产生的三溴苯酚能溶于苯因此不能鉴别,C错误;
D.苯酚遇到氯化铁显示紫色,但是苯不能,取样品,滴加少量的FeCl 溶液,观察溶液是否显紫色,若显
3
紫色则有苯酚,若不显紫色则无苯酚,D正确;
故选AD。
考点四 醇 酚的综合运用【例4-1】(2021·北京昌平·高二期末)传统中草药金银花对治疗“新冠肺炎”有效,其有效成分“绿原
酸”的结构简式如图所示。下列有关该物质的说法不正确的是
A.分子式是C H O
16 18 9
B.绿原酸易被氧化,需密封保存
C.1mol绿原酸最多能与3molBr 发生反应
2
D.绿原酸有顺反异构
【答案】C
【解析】A.根据结构简式确定分子式为C H O,A正确;
16 18 9
B.该分子中的酚羟基易被氧化,所以绿原酸需要密封保存,B正确;
C.苯环上酚羟基邻对位H原子能和溴以1:1发生取代反应,碳碳双键和溴以1 : 1发生加成反应,1mol绿
原酸能和3mol Br 发生取代反应、1mol Br 发生加成反应,所以1mol绿原酸最多能消耗4molBr ,C错误;
2 2 2
D.该分子中碳碳双键两端连接不同的原子或原子团,所以存在顺反异构,D正确;
答案选C。
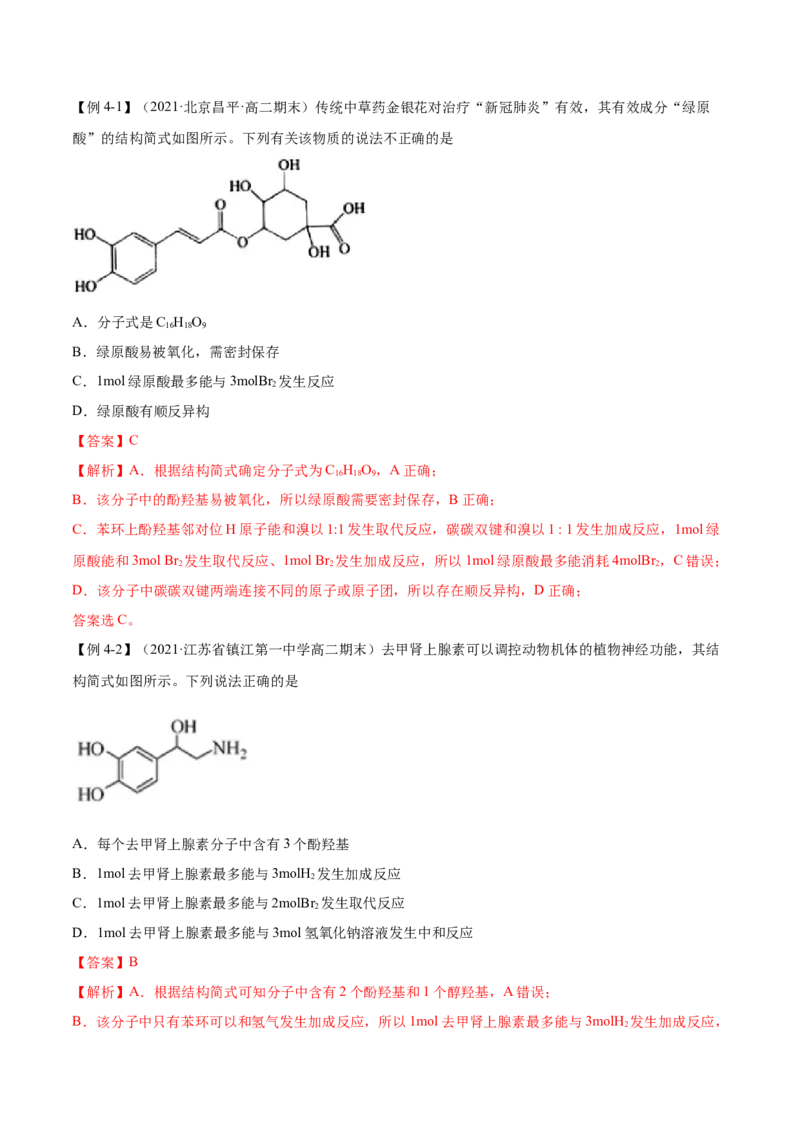
【例4-2】(2021·江苏省镇江第一中学高二期末)去甲肾上腺素可以调控动物机体的植物神经功能,其结
构简式如图所示。下列说法正确的是
A.每个去甲肾上腺素分子中含有3个酚羟基
B.1mol去甲肾上腺素最多能与3molH 发生加成反应
2
C.1mol去甲肾上腺素最多能与2molBr 发生取代反应
2
D.1mol去甲肾上腺素最多能与3mol氢氧化钠溶液发生中和反应
【答案】B
【解析】A.根据结构简式可知分子中含有2个酚羟基和1个醇羟基,A错误;
B.该分子中只有苯环可以和氢气发生加成反应,所以1mol去甲肾上腺素最多能与3molH 发生加成反应,
2B正确;
C.酚羟基的邻对位氢原子易被取代,所以1mol去甲肾上腺素最多能与3molBr 发生取代反应,C错误;
2
D.只有酚羟基能和NaOH发生中和反应,所以1mol去甲肾上腺素最多能与2mol氢氧化钠溶液发生中和
反应,D错误;
综上所述答案为B。
【一隅三反】
1.(2021·黑龙江·宾县第一中学高二阶段练习)有机物A的结构简式如图,下列A的性质叙述中,错误的
是
A.A不能发生水解反应
B.A能与碳酸钠溶液反应
C.A既有与羧酸反应,又能与醇反应
D.A与氢氧化钠溶液完全反应时,两者物质的量之比是1:3
【答案】D
【解析】A.不含卤原子和酯基,所以不能发生水解反应,故A正确;
B.含有羧基和酚羟基,所以能和碳酸钠溶液反应,故B正确;
C.含有羟基和羧基,所以A既能与羧酸反应,又能与醇反应,故C正确;
D.羧基和酚羟基都能和NaOH反应,且以1:1反应,A与氢氧化钠溶液完全反应时,两者物质的量之比
是1:2,故D错误;
故答案为D。
2.(2021·全国·高二)某医药中间体的结构简式如图所示。当与等量该有机物反应时,最多消耗Na、
Br 、NaOH的物质的量之比为
2
A.1:1:1 B.4:4:3 C.5:4:3 D.3:5:1
【答案】C
【解析】含有3个酚羟基、2个醇羟基,可与5molNa反应;分子中含有3个酚羟基,1个碳碳双键,其中1mol有机物可与3mol溴发生取代反应,与1mol溴发生加成反应,共4mol溴;含有3个酚羟基,可与
3molNaOH反应,最多消耗Na、Br 、NaOH的物质的量之比为5:4:3,故选:C。
2
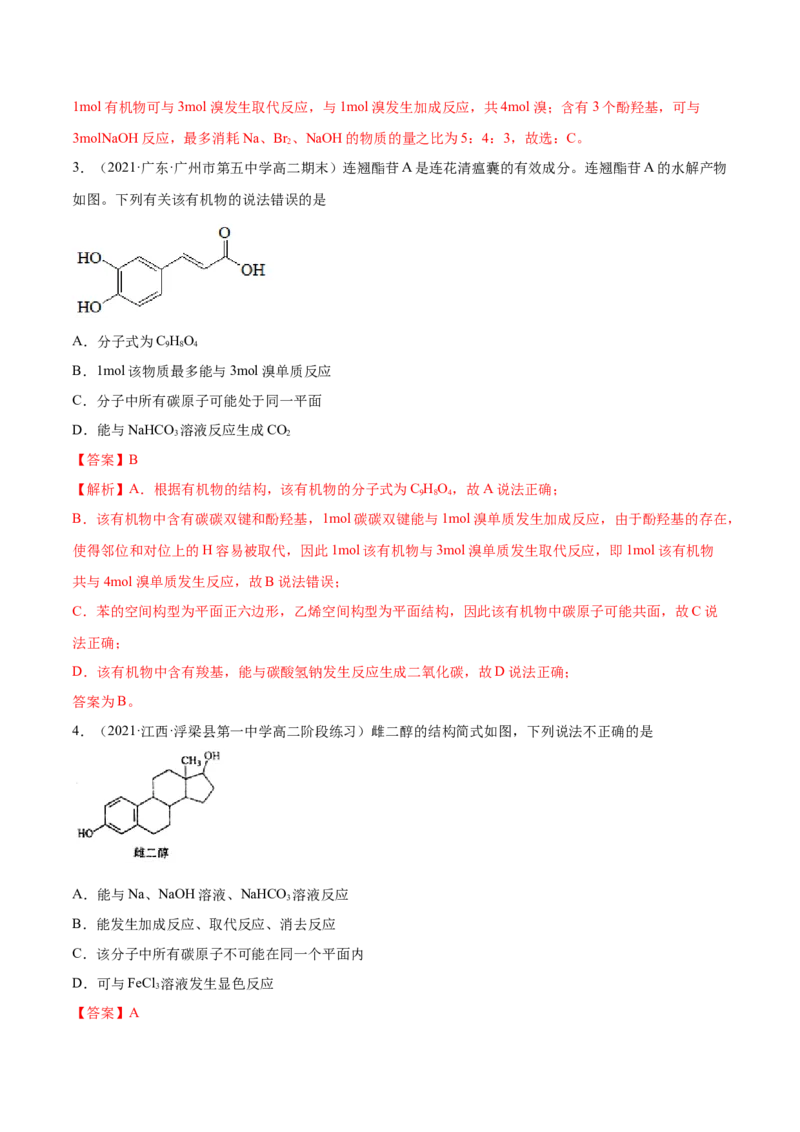
3.(2021·广东·广州市第五中学高二期末)连翘酯苷A是连花清瘟囊的有效成分。连翘酯苷A的水解产物
如图。下列有关该有机物的说法错误的是
A.分子式为C HO
9 8 4
B.1mol该物质最多能与3mol溴单质反应
C.分子中所有碳原子可能处于同一平面
D.能与NaHCO 溶液反应生成CO
3 2
【答案】B
【解析】A.根据有机物的结构,该有机物的分子式为C HO,故A说法正确;
9 8 4
B.该有机物中含有碳碳双键和酚羟基,1mol碳碳双键能与1mol溴单质发生加成反应,由于酚羟基的存在,
使得邻位和对位上的H容易被取代,因此1mol该有机物与3mol溴单质发生取代反应,即1mol该有机物
共与4mol溴单质发生反应,故B说法错误;
C.苯的空间构型为平面正六边形,乙烯空间构型为平面结构,因此该有机物中碳原子可能共面,故C说
法正确;
D.该有机物中含有羧基,能与碳酸氢钠发生反应生成二氧化碳,故D说法正确;
答案为B。
4.(2021·江西·浮梁县第一中学高二阶段练习)雌二醇的结构简式如图,下列说法不正确的是
A.能与Na、NaOH溶液、NaHCO 溶液反应
3
B.能发生加成反应、取代反应、消去反应
C.该分子中所有碳原子不可能在同一个平面内
D.可与FeCl 溶液发生显色反应
3
【答案】A【解析】A. 由有机物的结构简式可知,含有酚羟基和醇羟基,故能与Na、NaOH溶液,但不含羧基,故
不能与NaHCO 溶液反应,A错误;
3
B. 该有机物中含有苯环,故能发生加成反应,含有酚羟基且邻位上有H,故能发生取代反应,含有醇羟基
且邻碳上有H,故能发生消去反应和取代反应,B正确;
C. 由于该分子中含有多个sp3杂化的碳原子,且该碳原子连有多个碳原子,故该分子中所有碳原子不可能
在同一个平面内,C正确;
D. 由有机物的结构简式可知,含有酚羟基,故可与FeCl 溶液发生显色反应,D正确;
3
故答案为:A。
5.(2021·广东荔湾·高二期末)环己烯是重要的化工原料。其实验室制备与提纯流程如下:
可能用到的有关数据如下:
名称 相对分子质量 密度/( ) 沸点/℃ 溶解性
环己醇 100 0.96 161 能溶于水
环己烯 82 0.81 83 难溶于水
回答下列问题:
(1)原料环己醇中若含苯酚杂质,检验试剂为___________,现象为___________。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为___________,浓硫酸也可作该反应的催化剂,选择
而不用浓硫酸的优点为___________(任答一点即可)。
②加热过程中,温度控制在90℃以下,蒸馏温度不宜过高的原因是___________。(3)下列仪器中,操作2需使用的有___________(填字母)。
(4)蒸馏操作的正确顺序为___________(填序号)。
①加热
②安装装置,加入待蒸馏的物质和沸石
③弃去前馏分,收集83℃的馏分
④通冷凝水
(5)以下区分环烯纯品和粗品的方法,合理的是___________(填标号)。
A.用酸性高锰酸钾溶液 B.用金属钠 C.测定沸点
(6)根据蒸馏最后得到的产品,计算反应的产率为___________(只列出计算式)。
【答案】(1) FeCl 溶液 溶液呈紫色
3
(2) +H O 浓硫酸易使原料碳化,并放出二氧化硫气体 减少未反应的环己醇
2
蒸出
(3)ad
(4)②④①③
(5)BC
(6)
【解析】环己醇在 z作用下发生消去反应生成环己烯、水,蒸出的环己烯粗产品含有环己醇,
粗产品中加入饱和食盐水,环己烯不溶于饱和食盐水,液体分层,有机相为环己烯,通过干燥、过滤、蒸
馏得到纯净的环己烯。
(1)苯酚能与FeCl 溶液发生显色反应,溶液呈紫色,环己醇不能,原料环己醇中若含苯酚杂质,检验试剂
3
为FeCl 溶液;
3(2)①烧瓶A中进行的可逆反应是环己醇在 z作用下发生消去反应生成环己烯、水,化学方程式
为 +H O;浓硫酸具有脱水性、强氧化性,浓硫酸易使原料碳化,并放出二氧化硫气
2
体,所以选择 而不用浓硫酸作催化剂;
②加热过程中,温度控制在90℃以下,可以减少未反应的环己醇蒸出;
(3)操作2使两种互不相溶的液体分离,操作名称为分液,用的有玻璃仪器有分液漏斗和烧杯,选ad。
(4)蒸馏操作的正确顺序为:②安装装置,加入待蒸馏的物质和沸石;④通冷凝水;①加热;③弃去前馏分,
收集83℃的馏分;
(5)环己烯精品和粗品都能使高锰酸钾褪色,不能用酸性高锰酸钾溶液区分环己醇和环己烯;环己烯粗品中
含有环己醇,环己醇能与钠产生氢气,而环己稀不能,能用金属钠区分环己烯精品和粗品;混合物没有固
定的沸点,而纯净物有固定的沸点,通过测定环己烯粗品和环己烯精品的沸点,可以区分环己烯精品和粗
品;选BC。
(6)环己醇的物质的量是 ,理论上生成环己烯的物质的量是 ,所以环己烯的产
率是 。