文档内容
第2讲 盐类水解的应用
1.了解影响盐类水解平衡的因素,能分析外界条件对盐类水解平衡的影响。
2.了解盐类水解在生产生活、化学实验、科学研究中的应用。
重点:影响盐类水解平衡的因素。
难点:盐类水解的应用。
一 、影响盐类水解的因素
研究盐类水解时,一般从两个方面来探究:一是 ,二是 。
(1)内因
是影响盐类水解的主要因素。组成盐的酸根离子对应的弱酸酸性越弱(或阳离
子对应的弱碱碱性越弱),盐的水解程度就 。
(2)外因
①温度:盐类的水解可看作酸碱中和反应的 ,中和反应是 反应,盐类的水
解是 反应,因此加热可促使平衡向水解反应的方向移动,盐的水解程度 。
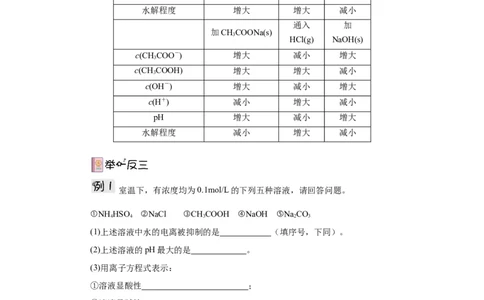
②浓度:加水稀释可促使平衡向 的方向移动,盐的水解程度 。
③外加酸碱:在盐溶液中加入适量酸或碱,会引起盐类水解平衡的移动和水解程度的
改变。
二、盐类水解的应用
(1)盐溶液的配制:配制FeCl 溶液时,可加入少量盐酸,目的是 。
3
(2)热碱去油污:用纯碱溶液清洗油污时,加热可增强去污效果,是由于CO2- 水解:
3
,加热平衡 ,碱性 。
(3)作净水剂:铝盐、铁盐等部分盐类水解生成的 有较强的吸附性,常用作净水
剂。如明矾可以用来净水,其反应的离子方程式为Al3++3HO Al(OH) (胶体)+3H+。
2 3
(4)制备物质
用 TiCl 制取 TiO 发生反应的化学方程式为 、
4 2
TiO·xHO△,TiO +xHO。
2 2 2 2
1.判断正误,正确的打“√”,错误的打“×”。
(1)用热的NaCO 溶液清洗油污,效果更佳。( )
2 3(2)实验室配制FeCl 溶液时,常将FeCl 晶体溶于稀硫酸中。( )
3 3
(3)铝盐、铁盐可用作净水剂,是因为Al3+、Fe3+水解生成的胶体具有杀菌作用。(
)
(4)盐溶液浓度越大,K 越大。( )
w
考点1影响盐类水解的因素
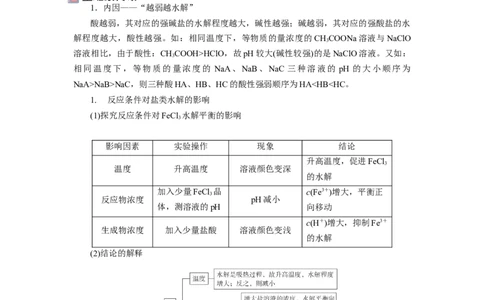
1.内因——“越弱越水解”
酸越弱,其对应的强碱盐的水解程度越大,碱性越强;碱越弱,其对应的强酸盐的水
解程度越大,酸性越强。如:相同温度下,等物质的量浓度的CHCOONa溶液与NaClO
3
溶液相比,由于酸性:CHCOOH>HClO,故pH较大(碱性较强)的是NaClO溶液。又如:
3
相同温度下,等物质的量浓度的 NaA、NaB、NaC 三种溶液的 pH 的大小顺序为
NaA>NaB>NaC,则三种酸HA、HB、HC的酸性强弱顺序为HA②>③
3 2 3
7.NaCO 溶液中存在水解平衡:CO2- +H O⇌HCO- +OH-。下列说法错误的是
2 3 3 2 3
A.通入CO,溶液pH减小 B.升高温度,平衡常数增大
2
c(HCO−
)
3
C.加水稀释,溶液中所有离子的浓度都减小 D.加入NaOH固体, 减小
c(CO2−
)
3
8.在一定条件下,NaCO 溶液存在水解平衡:CO2- +H O⇌HCO- +OH-。下列说法正
2 3 3 2 3
确的是
A.稀释溶液,各物质浓度均减小,平衡不移动
B.加入少量NaHCO 固体,平衡向正反应方向移动
3
c(HCO−
)
3
C.升高温度, 减小
c(CO2−
)
3
D.加入NaOH固体,溶液pH增大
9.0.1 mol/L 的①NaOH溶液 ②NaCO 溶液 ③NH Cl溶液 ④NaCl溶
2 3 4
液,按pH由大到小的顺序,排列正确的是
A.②①③④ B.①②④③ C.③④②① D.④③②①
10.化学与社会、生产、生活密切相关,下列说法错误的是
A.热的纯碱溶液可以去油污
B.发生煤气中毒时需要及时将中毒者转移至空气流通处
C.人体中 缓冲体系起到稳定血液 的作用
D.为增强肥效,可以将草木灰和铵态氮肥按照一定比例混合使用
11.以下有关物质用途的叙述正确的是
A.废旧钢材焊接前,可依次用饱和NaCO 溶液、饱和NH Cl溶液处理焊点
2 3 4
B.金属钠、金属镁等活泼金属着火时,可以使用干粉灭火器来灭火C.食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质
D.中国蓝是古代人工合成的蓝色化合物,其化学式为BaCuSi O ,可改写成
4 10
BaO·4SiO ·CuO
2
12.下列实验操作能达到实验目的的是
选项 实验操作 实验目的
A 将NaS溶液在空气中直接加热蒸干 制备无水NaS晶体
2 2
B 将饱和FeCl 溶液滴入沸水中,边加热边搅拌 制备Fe(OH) 胶体
3 3
C 将Fe(NO ) 固体加入少量浓硝酸中,然后稀释到所需浓度 配制Fe(NO ) 溶液
3 2 3 2
D 将浓氨水滴入盛有氧化钙固体的锥形瓶中 制备氨气
A.A B.B C.C D.D
13.下列说法不正确的是
A.明矶能水解生成Al(OH) 胶体,可用作净水剂
3
B.焊接时用NH Cl溶液除锈与盐类水解有关
4
C.在配制氯化铁溶液时,加入少量的盐酸是为了抑止Fe3+的水解
D.草木灰和铵态氮肥混合使用,肥效增强
14.合理利用某些盐能水解的性质,能解决许多生产、生活中的问题,下列叙述的事
实与盐水解的性质无关的是
A.金属焊接时可用NH Cl溶液作除锈剂
4
B.用NaCO 溶液处理锅炉水垢中的CaSO
2 3 4
C.配制FeCl 溶液时,常将FeCl 晶体溶于较浓的盐酸中
3 3
D.用TiCl 制备TiO
4 2
二、填空题
15.研究电解质在水溶液中的平衡能了解它的存在形式。已知部分弱酸的电离常数如
表:
化学式 HF HCO HS HCN
2 3 2
K =4.4×10-7 K =9.1×10-8
a1 a1
电离平衡常数K(25℃) 7.2×10-4 K=4.9×10-10
K =9.1×10-11 K =1.1×10-11
a2 a2
(1)①常温下,pH相同的三种溶液NaF、NaCO、NaS,物质的量浓度最小的是
2 3 2
。
②将过量HS通入NaCO 溶液,反应的离子方程式是 。
2 2 3(2)25℃时,向NaCN溶液中通入少量CO,所发生反应的离子方程式为 。
2
(3)pH相同、体积相同的盐酸和氢氟酸两种溶液盐酸分别与足量的锌粉发生反应,下
列关于氢气体积(V)随时间(t)变化的示意图正确的是 (填字母)。(①表示盐酸,②表
示氢氟酸)
a. b. c. d.
16.有下列五种盐溶液:①NaClO、②(NH )SO 、③NaCO、④AlCl 、⑤KNO 回答
4 2 4 2 3 3 3.
下列问题:
(1)不能破坏水的电离平衡的是 ,溶液呈酸性的是 ,pH>7的
是 。
(2)写出下列盐类水解的离子方程式:
①NaClO: ;
②(NH )SO : ;
4 2 4
③Na CO: 、 ;
2 3
④AlCl : 。
3