文档内容
第2讲 盐类水解的应用
1.了解影响盐类水解平衡的因素,能分析外界条件对盐类水解平衡的影响。
2.了解盐类水解在生产生活、化学实验、科学研究中的应用。
重点:影响盐类水解平衡的因素。
难点:盐类水解的应用。
一 、影响盐类水解的因素
研究盐类水解时,一般从两个方面来探究:一是反应物的性质,二是反应条件。
(1)内因
盐的性质是影响盐类水解的主要因素。组成盐的酸根离子对应的弱酸酸性越弱(或阳离
子对应的弱碱碱性越弱),盐的水解程度就越大。
(2)外因
①温度:盐类的水解可看作酸碱中和反应的逆反应,中和反应是放热反应,盐类的水
解是吸热反应,因此加热可促使平衡向水解反应的方向移动,盐的水解程度增大。
②浓度:加水稀释可促使平衡向水解反应的方向移动,盐的水解程度增大。
③外加酸碱:在盐溶液中加入适量酸或碱,会引起盐类水解平衡的移动和水解程度的
改变。
二、盐类水解的应用
(1)盐溶液的配制:配制FeCl 溶液时,可加入少量盐酸,目的是 抑制 FeC l 的水解。
3 3
(2)热碱去油污:用纯碱溶液清洗油污时,加热可增强去污效果,是由于CO2- 水解:
3
CO2- + H O⇌HCO- + OH - ,加热平衡正向移动,碱性增强。
3 2 3
(3)作净水剂:铝盐、铁盐等部分盐类水解生成的胶体有较强的吸附性,常用作净水
剂。如明矾可以用来净水,其反应的离子方程式为Al3++3HO⇌Al(OH) (胶体)+3H+。
2 3
(4)制备物质
用TiCl 制取TiO 发生反应的化学方程式为TiCl + ( x + 2)H O == =TiO · x H O↓ + 4HCl 、
4 2 4 2 2 2
TiO·xHO△,TiO +xHO。
2 2 2 2
1.判断正误,正确的打“√”,错误的打“×”。
(1)用热的NaCO 溶液清洗油污,效果更佳。( )
2 3(2)实验室配制FeCl 溶液时,常将FeCl 晶体溶于稀硫酸中。( )
3 3
(3)铝盐、铁盐可用作净水剂,是因为Al3+、Fe3+水解生成的胶体具有杀菌作用。(
)
(4)盐溶液浓度越大,K 越大。( )
w
答案 (1)√ (2)× (3)× (4)×
考点1影响盐类水解的因素
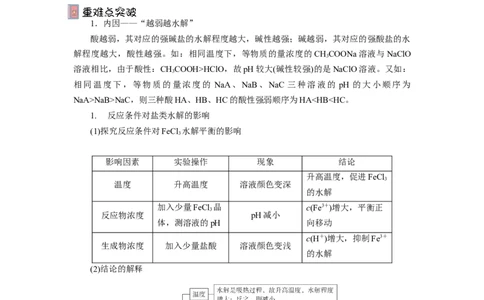
1.内因——“越弱越水解”
酸越弱,其对应的强碱盐的水解程度越大,碱性越强;碱越弱,其对应的强酸盐的水
解程度越大,酸性越强。如:相同温度下,等物质的量浓度的CHCOONa溶液与NaClO
3
溶液相比,由于酸性:CHCOOH>HClO,故pH较大(碱性较强)的是NaClO溶液。又如:
3
相同温度下,等物质的量浓度的 NaA、NaB、NaC 三种溶液的 pH 的大小顺序为
NaA>NaB>NaC,则三种酸HA、HB、HC的酸性强弱顺序为HA④>③>①>②
解析 NH在溶液中存在水解平衡:NH+HO⇌NH ·H O+H+。第1组选①②③,以
2 3 2
①为参照物,②中CHCOO-水解显碱性,与NH的水解相互促进,所以c(NH)为②<①。
3
③中NH HSO 电离出H+,会抑制NH的水解,所以c(NH)为③>①。第2组选④⑤,未水
4 4
解前④中NH浓度为①②③中的2倍,以④为参照物,⑤中Fe2+的水解呈酸性,对NH的
水解起抑制作用,所以c(NH)为⑤>④,综上,c(NH)由大到小的顺序为⑤>④>③>①>②。
考点2盐类水解的应用
1.某些物质的水溶液的配制
配制FeCl 的水溶液,FeCl 溶于水后发生如下水解反应:Fe3++3HO⇌Fe(OH) +3H
3 3 2 3
+,因Fe(OH) 的生成而使溶液变浑浊,通常先将 FeCl 溶于浓盐酸中,可抑制Fe3+的水
3 3
解,使溶液保持澄清,再加水稀释至所需浓度。
若配制强碱弱酸盐的水溶液,应加入少量强碱,抑制弱酸根离子的水解。如配制硫化
钠的水溶液时,应先滴入几滴氢氧化钠溶液,再加水稀释至所需浓度。
2.某些化肥的施用
草木灰不能与铵态氮肥混用,因草木灰的主要成分为 KCO ,溶于水时 CO+
2 3
HO⇌HCO+OH-,生成的OH-与NH发生反应:NH+OH-===NH↑+HO,使氮肥肥效
2 3 2
降低。
3.利用盐的水解去除杂质
如两种盐的水解程度不一样,可利用水解反应将一种盐转化为氢氧化物沉淀而除去。
例如:MgCl 溶液中混有少量FeCl 杂质,因Fe3++3HO⇌Fe(OH) +3H+水解程度比
2 3 2 3
Mg2+水解程度大,可加入MgO或Mg(OH) 、MgCO 等,使Fe3+的水解平衡正向移动,生
2 3
成Fe(OH) 沉淀而除去Fe3+。
3
4.明矾等物质净水的原理
明矾在水中发生电离:KAl(SO )===K++Al3++2SO2- ,其中Al3+发生水解:Al3++
4 2 4
3HO⇌Al(OH) +3H+,生成的Al(OH) 胶体有较强吸附性,可吸附杂质下沉,以达到净水
2 3 3
的目的。FeCl 也能净水,原理与明矾相同。
3
5.泡沫灭火器灭火的原理
泡沫灭火器内装饱和的Al (SO ) 溶液和NaHCO 溶液,它们分装在不同的容器中。当
2 4 3 3
两溶液混合后,发生相互促进的水解反应:Al3++3HCO===Al(OH) ↓+3CO↑。灭火器内
3 2
压强增大,CO、HO、Al(OH) 一起喷出覆盖在着火物质上使火焰熄灭。
2 2 36.作除锈剂
NH Cl、ZnCl 溶液因NH、Zn2+水解而显酸性,金属表面的氧化膜可与H+反应,因此
4 2
均可作焊接时的除锈剂。
7.判断离子能否大量共存
相互促进程度很大、水解很彻底的离子不能大量共存,如 Al3++3HCO===Al(OH) ↓+
3
3CO↑,这类离子组合常见的有
2
这类相互促进水解且几乎进行完全的水解方程式的书写要用“===”且标“↑”
“↓”。例如2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑。
2 3 2
在生产、生活和科学研究中,常常需要促进或抑制盐的水解。试回答下列问
题:
(1) 溶液呈 (填“酸”“中”或“碱”)性,原因是(用离子方程式表
示): 。实验室在配制 溶液时,常将 固体先溶于较浓的盐酸中,以
(填“促进”或“抑制”)其水解,然后用蒸馏水稀释到所需的浓度。
(2)普通泡沫灭火器是利用 溶液跟 溶液混合,产生大量的气体和沉
淀,气体将混合物压出灭火器,相关反应的离子方程式是 。
(3)将 溶液加热蒸干所得主要固体为 ,灼烧所得到固体为 。
【答案】(1) 酸 Fe3++3H O⇌Fe(OH) +3H+ 抑制
2 3
(2)Al3++3HCO- =Al(OH) ↓+3CO ↑
3 3 2
(3) Fe(OH) Fe O
3 2 3
【解析】(1)氯化铁是强酸弱碱盐,水解显酸性,增大氢离子浓度,能抑制其水解。
(2)硫酸铝水解显酸性,碳酸氢钠水解显碱性,二者混合时水解相互促进,生成氢氧化
铝沉淀和CO 气体。(3)氯化铁溶液中存在水解平衡FeCl +3H O⇌Fe(OH) +3HCl,加热促
2 3 2 3
进水解,同时生成物氯化氢易挥发,进一步促进水解,得到氢氧化铁沉淀,灼烧得到氧化铁。
回答下列问题:
(1)室温下,pH=12的NaOH溶液100mL,要使它的pH为11,如果加0.01mol/LHCl,
应加 mL。(体积变化忽略不计)
(2)现有常温下0.1mol·L-1NH Cl溶液。
4
①你认为该溶液呈 性,原因是(用离子方程式表示): 。
②该溶液中离子浓度大小顺序为: 。
(3)氯化铁水溶液呈酸性,原因是(用离子方程式表示) 。实验室在临时配制
一些氯化铁溶液时,常将氯化铁固体先溶于较浓的 中,然后再用蒸馏水稀释到
所需要的浓度,是为了抑制其水解。
(4)泡沫灭火器(里面装饱和NaHCO 溶液和Al (SO ))的工作原理是 (用离子方程
3 2 4 3
式表示)。
(5)不断加热FeCl 溶液蒸干其水分并灼烧,得到的固体是 。
3
【答案】(1)81.8/82
(2) 酸 NH+ +H O⇌NH ·H O+H+ Cl->NH+ >H+>OH-
4 2 3 2 4
(3) Fe3++3H O⇌Fe(OH) +3H+ 盐酸
2 3
(4) Al3++3HCO- =Al(OH) ↓+3CO ↑
3 3 2
(5) Fe O
2 3
K 10−14
w
【解析】(1)室温下,pH=12的NaOH溶液c(OH-)= = mol/
c(H+ ) 10−12
K 10−14
w
L=0.01mol/L,混合溶液的pH=11,混合溶液中c(OH-)= = mol/L=0.001mol/L,
c(H+ ) 10−11
0.01mol/L×0.1L−0.0.1mol×xL
设V(HCl)=xL,混合溶液中c(OH-)= =0.001mol/L,
(0.1+x)L
x≈0.082,溶液体积为82mL;
(2)①NH Cl为强酸弱碱盐,NH+ 水解导致溶液呈酸性,水解离子方程式为NH
4 4
+ +H O⇌NH •H O+H+;
4 2 3 2
②NH+ 水解导致溶液呈酸性,c(H+)>c(OH-),Cl-不水解,则c(Cl-)>c(NH+ ),但其水解
4 4
程度较小,则存在c(Cl-)>c(NH+ )>c(H+)>c(OH-);
4(3)氯化铁水溶液呈酸性,原因是Fe3++3H O⇌Fe(OH) +3H+,实验室在临时配制一
2 3
些氯化铁溶液时,常将氯化铁固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需要的
浓度,是为了抑制其水解;
(4)泡沫灭火器中NaHCO 溶液和Al (SO ) 发生双水解反应的离子方程式为Al3+
3 2 4 3
+3HCO- ═Al(OH)↓+3CO ↑,产生大量泡沫覆盖可燃物,达到灭火效果;
3 3 2
(5)加热蒸干FeCl 溶液时,FeCl 水解生成氢氧化铁和HCl,加热促进HCl挥发,从
3 3
而促进FeCl 水解,蒸干时得到氢氧化铁固体,灼烧氢氧化铁固体,氢氧化铁分解生成氧化
3
铁和水,所以最终得到Fe O 固体。
2 3
一、单选题
1.漂白粉在溶液中存在平衡:ClO-+H O⇌HClO+OH-,下列措施能增强漂白能力是
2
A.加HO稀释 B.加少量纯碱 C.通入SO D.滴加适量食醋
2 2
【答案】D
【解析】A.加水稀释,ClO-+H O⇌HClO+OH-平衡正向移动,但是次氯酸的浓度会
2
降低漂白能力减弱,故A错误;
B.加入少量纯碱,次氯酸的酸性比碳酸氢根离子酸性强,碳酸根离子的水解程度更
大,溶液中氢氧根离子浓度增大导致ClO-+H O⇌HClO+OH-平衡逆向移动,漂白性减弱,
2
故B错误;
C.通入二氧化硫,二氧化硫有较强还原性会还原次氯酸,溶液中次氯酸浓度降低,
溶液漂白性减弱,故C错误;
D.加入食醋,醋酸的酸性比次氯酸强,溶液中次氯酸浓度增大,漂白性增强,故D
正确;
故答案为:D。
2.下列事实不能用勒夏特列原理解释的是
A.将红棕色NO 压缩体积后颜色变深
2
B.FeCl +3KSCN⇌Fe(SCN) +3KCl的平衡体系,加入少量KSCN固体后溶液颜色加
3 3
深
C.新制氯水在光照条件下变浅
D.热的纯碱溶液碱性强,去油污的能力强【答案】A
【解析】A.增大压强,气体体积减小,导致二氧化氮浓度增大,颜色加深,与平衡
移动无关,不能用勒夏特列原理解释,故A符合题意;
B.FeCl +3KSCN⇌Fe(SCN) +3KCl的平衡体系,加入少量KSCN固体,平衡正向移
3 3
动,Fe(SCN) 浓度增大,颜色加深,能用勒夏特列原理解释,故B不选;
3
C.新制氯水在光照条件下变浅,氯水中存在化学平衡,Cl+H O⇌HCl+HClO,次氯
2 2
酸见光分解,使化学平衡正向进行,氯水颜色变浅,能用勒夏特列原理解释,故C不选;
D.纯碱水解为吸热反应,升高温度促进纯碱水解,导致溶液碱性增强,去油污能力
增强,能用勒夏特列原理解释,故D不选。
答案选A。
3.现代洗涤液问世前,纯碱(Na CO)常用来洗涤油性物质,以下是纯碱水解的化学方
2 3
程式:NaCO+H O⇌NaHCO +NaOH(吸热反应),纯碱水解后呈碱性,能除去油污,以下
2 3 2 3
措施中能提高纯碱的去污能力的是
A.用热水 B.用冷水 C.加小苏打(NaHCO ) D.加入大量的水
3
【答案】A
【解析】A.已知碳酸钠水解反应NaCO+H O⇌NaHCO +NaOH是一个吸热反应,
2 3 2 3
故用热水即升高温度上述水解平衡正向移动,溶液碱性增强,去污能力增强,A符合题
意;
B.已知碳酸钠水解反应NaCO+H O⇌NaHCO +NaOH是一个吸热反应,用冷水即
2 3 2 3
升高温度上述水解平衡逆向移动,溶液碱性减弱,去污能力减弱,B不合题意;
C.已知碳酸钠水解反应NaCO+H O⇌NaHCO +NaOH,加小苏打(NaHCO )则增大
2 3 2 3 3
了碳酸氢根离子浓度,上述水解平衡逆向移动,溶液碱性减弱,去污能力减弱,C不合题
意;
D.加入大量的水,水解平衡虽然正向移动,但OH-浓度减小即溶液碱性减小,去污能
力减弱,D不合题意;
故答案为:A。
4.25℃时,关于CHCOONa溶液的分析,说法错误的是
3
A.CHCOONa溶液对水的电离起促进作用
3
B.pH=9的CHCOONa溶液中,水电离产生的H+浓度为
3
C.升高温度,促进CHCOO-的水解
3D.向CHCOONa溶液中加入少量NaOH固体,抑制CHCOO-的水解
3 3
【答案】B
【解析】A.CHCOONa溶液中CHCOO-发生水解,促进水的电离,故A正确;
3 3
B.pH=9的CHCOONa溶液呈碱性,水电离产生的H+浓度等于c(OH-)=
3
K 10−14
w
= mol/L=10-15mol/L,故B错误;
c(H+ ) 10−9
C.CHCOO-的水解是吸热的,升高温度,促进CHCOO-的水解,故C正确;
3 3
D.CHCOONa溶液中CHCOO-发生水解:CHCOO-+H O⇌CHCOOH+OH-,加入少
3 3 3 2 3
量NaOH固体,增大OH-的浓度,抑制CHCOO-的水解,故D正确;
3
故选B。
5.25℃时,下列有关电解质溶液的说法正确的是
c(H+
)
A.加水稀释0.1mol·L-1氨水,溶液中 减小
c(OH−
)
c(Na+
)
B.向CHCOONa溶液中加入少量水稀释,溶液中 的值增大
3 c(CH COO− )
3
c(HS−
)
c(S2−
)
C.将等物质的量浓度的NaS和NaHS溶液等体积混合后: <
2 c(H S) c(HS− )
2
c(F−
)
D.将浓度为0.1mol·L-1HF溶液加水不断稀释过程中, 始终增大
c(OH−
)
【答案】B
【解析】A.氨水加水稀释时,溶液中氢氧根离子浓度减小,水的离子积常数不变,
c(H+
)
则溶液中的氢离子浓度增大,溶液中 的值增大,故A错误;
c(OH−
)
B.醋酸钠是强碱弱酸盐,醋酸根离子在溶液中水解生成醋酸和氢氧根离子,加水稀
释时,水解平衡向正反应方向移动,溶液中钠离子的物质的量不变,醋酸根离子的物质的
c(Na+
)
量减小,则溶液中 的值增大,故B正确;
c(CH COO− )
3c(HS− ) K
a1
C.等体积等物质的量浓度的硫化钠和硫氢化钠溶液混合溶液中 = 、
c(H S) c(H+ )
2
c(S2− ) K
a2
= ,溶液中氢离子浓度相等,一级电离常数远远大于二级电离常数,则溶
c(HS− ) c(H+ )
c(HS−
)
c(S2−
)
液中 > ,故C错误;
c(H S) c(HS− )
2
D.氢氟酸加水稀释时,氟离子、氢离子浓度浓度减小,水的离子积常数不变,则溶
c(F−
)
液中氢氧根离子浓度增大, 的值减小,故D错误;
c(OH−
)
故选B。
6.下列叙述错误的是
A.NaCO 稀溶液加水稀释,溶液的碱性减弱
2 3
B.稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强
C.在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐褪去
2 3 2
D.pH相等的①NaHCO ②NaCO ③NaOH溶液的物质的量浓度大小:①>②>③
3 2 3
【答案】B
【解析】A.NaCO 稀溶液因碳酸根离子发生水解呈碱性,加水稀释氢氧根离子浓度
2 3
减小,溶液的碱性减弱,故A正确;
B.根据水解反应的规律‘越稀越水解’,稀溶液中,盐的浓度越小,水解程度越
大,但由于浓度减小,其溶液酸性(或碱性)也越弱,故B错误;
C.NaCO 溶液中碳酸根离子和BaCl 溶液中钡离子结合生成硫酸钡沉淀,使水解平衡
2 3 2
CO2- +H O⇌HCO- +OH-逆向移动,溶液碱性减弱,酚酞溶液的红色逐渐褪去,故C正确;
3 2 3
D.常温下,pH相等的①NaHCO 、②NaCO、③NaOH溶液,碱性③>②>①,碱
3 2 3
性越强需要的浓度越小,溶液的物质的量浓度大小为①>②>③,故D正确;
故选B。
7.NaCO 溶液中存在水解平衡:CO2- +H O⇌HCO- +OH-。下列说法错误的是
2 3 3 2 3
A.通入CO,溶液pH减小 B.升高温度,平衡常数增大
2c(HCO−
)
3
C.加水稀释,溶液中所有离子的浓度都减小 D.加入NaOH固体, 减小
c(CO2−
)
3
【答案】C
【解析】A.CO 能与水、CO2- 反应生成碳酸氢根,平衡左移,溶液pH减小,故A正
2 3
确;
B.因水解是吸热的,则升温可以促进水解,平衡正向移动,平衡常数增大,故B正
确;
C.因稀释NaCO 时,碳酸根离子、碳酸氢根、氢氧根离子的浓度变小,因K 不变,
2 3 w
则氢离子的浓度增大,故C错误;
c(HCO−
)
D.加入NaOH固体,平衡向左移动,n(HCO- )减小、n(CO2- )增大, 3 =
3 3 c(CO2−
)
3
n(HCO−
)
3
减小,故D正确;
n(CO2−
)
3
故选:C。
8.在一定条件下,NaCO 溶液存在水解平衡:CO2- +H O⇌HCO- +OH-。下列说法正
2 3 3 2 3
确的是
A.稀释溶液,各物质浓度均减小,平衡不移动
B.加入少量NaHCO 固体,平衡向正反应方向移动
3
c(HCO−
)
3
C.升高温度, 减小
c(CO2−
)
3
D.加入NaOH固体,溶液pH增大
【答案】D
【解析】A.稀释溶液,c(CO2- )、c(HCO- )、c(OH-)均减小,平衡正向移动,A错误;
3 3
B.加入少量NaHCO 固体,c(HCO- )增大,平衡向逆反应方向移动,B错误;
3 3
C.水解反应吸热,升高温度,平衡正向移动,c(HCO- )增大,c(CO2- )减小,则
3 3
c(HCO−
)
3
增大,C错误;
c(CO2−
)
3
D.加入NaOH固体,溶液氢氧根离子的浓度增大,pH增大,D正确;故答案为:D。
9.0.1 mol/L 的①NaOH溶液 ②NaCO 溶液 ③NH Cl溶液 ④NaCl溶
2 3 4
液,按pH由大到小的顺序,排列正确的是
A.②①③④ B.①②④③ C.③④②① D.④③②①
【答案】B
【解析】①NaOH为强碱完全电离,0.1 mol/L 的NaOH溶液pH为13;②NaCO 属
2 3
于强碱弱酸盐,0.1mol/L Na CO 溶液都呈弱碱性,pH小于13;③NH Cl属于强酸弱碱
2 3 4
盐,NH Cl溶液呈酸性;④NaCl为强碱强酸盐,溶液显中性,pH=7,溶液pH由大到小的
4
顺序是①②④③,故选B。
10.化学与社会、生产、生活密切相关,下列说法错误的是
A.热的纯碱溶液可以去油污
B.发生煤气中毒时需要及时将中毒者转移至空气流通处
C.人体中 缓冲体系起到稳定血液 的作用
D.为增强肥效,可以将草木灰和铵态氮肥按照一定比例混合使用
【答案】D
【解析】A.热纯碱溶液中,碳酸根水解生成较多的氢氧根,油脂与氢氧根反应,发
生水解反应,生成脂肪酸钠和甘油,这二者都易溶于水,所以,热纯碱溶液可去油污,故
A正确;
B.煤气中毒时应立即打开门窗通风,迅速将患者转移至空气新鲜流通处,故B正
确;
C.血液中含有许多对对酸碱度起缓冲作用的物质,如HCO-NaHCO ,起到稳定血液
2 3 3
pH的作用,故C正确;
D.草木灰和铵态氮肥混合后会发生双水解反应,此时氨气容易逸出,导致平衡向右
移动,土壤中铵根离子浓度降低,继而使得肥效下降,故D错误;
故答案选D。
11.以下有关物质用途的叙述正确的是
A.废旧钢材焊接前,可依次用饱和NaCO 溶液、饱和NH Cl溶液处理焊点
2 3 4
B.金属钠、金属镁等活泼金属着火时,可以使用干粉灭火器来灭火
C.食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质
D.中国蓝是古代人工合成的蓝色化合物,其化学式为BaCuSi O ,可改写成
4 10BaO·4SiO ·CuO
2
【答案】A
【解析】A.NaCO 和NH Cl中溶液中水解,溶液分别呈碱性和酸性,饱和NaCO 溶
2 3 4 2 3
液可以除去焊点处的油脂,饱和NH Cl溶液可以除去焊点处金属氧化物,故A正确;
4
B.钠、镁能与CO 反应,所以金属钠、金属镁等活泼金属着火时,不能使用干粉灭
2
火器来灭火,应用干沙子扑灭,故B错误;
C.生石灰不具有还原性,不能防止食品氧化变质,生石灰可用作干燥剂,故C错
误;
D.硅酸盐改写成氧化物形式时,活泼的金属氧化物写在前面,再写 SiO,含氢元素
2
的 HO最后写 , 所以 BaCuSi O 用氧化物形式表示 :BaO·CuO·4SiO ,故D错误;
2 4 10 2
故选A。
12.下列实验操作能达到实验目的的是
选项 实验操作 实验目的
A 将NaS溶液在空气中直接加热蒸干 制备无水NaS晶体
2 2
B 将饱和FeCl 溶液滴入沸水中,边加热边搅拌 制备Fe(OH) 胶体
3 3
C 将Fe(NO ) 固体加入少量浓硝酸中,然后稀释到所需浓度 配制Fe(NO ) 溶液
3 2 3 2
D 将浓氨水滴入盛有氧化钙固体的锥形瓶中 制备氨气
A.A B.B C.C D.D
【答案】D
【解析】A.由于S2-+H O⇌HS-+OH-、HS-+H O⇌HS+OH-,生成的HS受热易挥
2 2 2 2
发,促使上述平衡正向移动,且S2-能被空气中的O 氧化生成S,故不能将NaS溶液在空
2 2
气中直接加热蒸干来制备无水NaS晶体,A不合题意;
2
B.将饱和的FeCl 溶液滴入沸水中,出现红褐色液体时停止加热,不能搅拌,否则可
3
导致胶体聚沉,B不合题意;
C.浓硝酸氧化亚铁离子,不能用此法配制硝酸亚铁溶液,C不合题意;
D.NH +H O⇌NH •H O⇌NH+ +OH-,加入氧化钙固体,能与HO反应,增大氢氧根
3 2 3 2 4 2
离子浓度,平衡逆向移动,有利于氨气的生成,能用此法制备NH ,D符合题意;
3
故答案为:D。
13.下列说法不正确的是
A.明矶能水解生成Al(OH) 胶体,可用作净水剂
3B.焊接时用NH Cl溶液除锈与盐类水解有关
4
C.在配制氯化铁溶液时,加入少量的盐酸是为了抑止Fe3+的水解
D.草木灰和铵态氮肥混合使用,肥效增强
【答案】D
【解析】A.明矾在水中可以电离出Al3+,生成胶状的Al(OH) ,Al(OH) 胶体的吸附
3 3
能力很强,可以吸附水里悬浮的杂质,并形成沉淀,使水澄清,故A正确;
B.NH Cl溶液水解显酸性,可作焊接金属中的除锈剂,与水解有关,故B正确;
4
C.氯化铁是强酸弱碱盐,铁离子水解生成氢氧化铁和HCl,为了抑止氯化铁水解,配
制氯化铁溶液时应加入少量盐酸,故C正确;
D.铵态氮肥不能跟草木灰混合使用,其原因是碱性的草木灰跟铵态氮肥混合使用
后,会产生氨气,氨气易挥发,会降低肥效,故D错误;
故答案选D。
14.合理利用某些盐能水解的性质,能解决许多生产、生活中的问题,下列叙述的事
实与盐水解的性质无关的是
A.金属焊接时可用NH Cl溶液作除锈剂
4
B.用NaCO 溶液处理锅炉水垢中的CaSO
2 3 4
C.配制FeCl 溶液时,常将FeCl 晶体溶于较浓的盐酸中
3 3
D.用TiCl 制备TiO
4 2
【答案】B
【解析】A.NH Cl溶液水解显酸性,能和铁锈反应从而除去铁锈,与盐类水解有
4
关,故A不选;
B.CaCO 、CaSO 的溶度积常数表达式相同,K (CaCO)<K (CaSO),所以碳酸钠和
3 4 sp 3 sp 4
硫酸钙反应生成更难溶的CaCO ,属于难溶物的转化,与盐类水解无关,故B符合题意;
3
C.Fe3+易水解生成氢氧化铁沉淀,盐酸能抑制氯化铁中铁离子水解,与盐类的水解有
关,故C不选;
D.TiCl 水解生成TiO•xH O,TiO•xH O受热分解生成TiO,与盐类水解有关,故D
4 2 2 2 2 2
不选。
答案选B。
二、填空题
15.研究电解质在水溶液中的平衡能了解它的存在形式。已知部分弱酸的电离常数如
表:化学式 HF HCO HS HCN
2 3 2
K =4.4×10-7 K =9.1×10-8
a1 a1
电离平衡常数K(25℃) 7.2×10-4 K=4.9×10-10
K =9.1×10-11 K =1.1×10-11
a2 a2
(1)①常温下,pH相同的三种溶液NaF、NaCO、NaS,物质的量浓度最小的是
2 3 2
。
②将过量HS通入NaCO 溶液,反应的离子方程式是 。
2 2 3
(2)25℃时,向NaCN溶液中通入少量CO,所发生反应的离子方程式为 。
2
(3)pH相同、体积相同的盐酸和氢氟酸两种溶液盐酸分别与足量的锌粉发生反应,下
列关于氢气体积(V)随时间(t)变化的示意图正确的是 (填字母)。(①表示盐酸,②表
示氢氟酸)
a. b. c. d.
【答案】(1) Na S H S+CO2- =HCO- +HS-
2 2 3 3
(2)CN-+CO +H O=HCN+HCO-
2 2 3
(3)c
【解析】(1)①由表格知,K(HF)>K (H CO)>K (H S),酸性越弱,对应的酸根离
a2 2 3 a2 2
子的水解能力越强,故物质的量浓度相同的NaF、NaCO、NaS三种溶液,pH:(Na S)>
2 3 2 2
(Na CO)>(NaF),所以常温下,pH相同的三种溶液NaF、NaCO、NaS,物质的量浓度
2 3 2 3 2
最小的是NaS;
2
②因为K (H CO)>K (H S)>K (H CO)>K (H S),由强酸制弱酸可知,将过量HS
al 2 3 a1 2 a2 2 3 a2 2 2
通入NaCO 溶液,反应的离子方程式:HS+CO2- =HCO- +HS-;
2 3 2 3 3
(2)K (H CO)>K(HCN)>K (H CO),故碳酸的酸性强于HCN,碳酸氢根离子的酸
a1 2 3 a2 2 3
性弱于HCN,向NaCN溶液中通入少量CO,反应生成HCN与NaHCO ,该反应的离子方
2 3
程式为CN-+CO +H O=HCN+HCO- ;
2 2 3
(3)反应开始时,c(H+)相等,随着反应的进行,HF的电离平衡向右移动,产生H+,
故反应速率v(HF)>v(HCl),又因为pH相同时,c(HF)>c(HCl),所以与足量的锌粉发生反
应时,HF产生氢气量多,故选c。
16.有下列五种盐溶液:①NaClO、②(NH )SO 、③NaCO、④AlCl 、⑤KNO 回答
4 2 4 2 3 3 3.下列问题:
(1)不能破坏水的电离平衡的是 ,溶液呈酸性的是 ,pH>7的
是 。
(2)写出下列盐类水解的离子方程式:
①NaClO: ;
②(NH )SO : ;
4 2 4
③Na CO: 、 ;
2 3
④AlCl : 。
3
【答案】(1) ⑤ ②④ ①③
(2) ClO-+HO⇌HClO+OH- NH+ +HO⇌NH ·H O+H+ CO2- +HO⇌
2 4 2 3 2 3 2
HCO- +OH- HCO- +HO⇌HCO+OH- Al3++3HO⇌Al(OH) +3H+
3 3 2 2 3 2 3
【解析】(1)①NaClO是强碱弱酸盐,水解显碱性;
②(NH )SO 是强酸弱碱盐,水解显酸性;
4 2 4
③Na CO 是强碱弱酸盐,水解显碱性;
2 3
④AlCl 是强酸弱碱盐,水解显酸性;
3
⑤KNO 是强酸强碱盐,不水解,溶液显中性;
3
不能破坏水的电离平衡的是硝酸钾,答案选⑤,溶液呈酸性的是硫酸铵和氯化铝,答
案选②④,pH>7的是次氯酸钠和碳酸钠,答案选①③。
(2)①NaClO中次氯酸根离子水解:ClO-+HO⇌HClO+OH-;
2
②(NH )SO 中铵根水解:NH+ +HO⇌NH ·H O+H+;
4 2 4 4 2 3 2
③Na CO 中碳酸根水解,且水解分步进行:CO2- +HO⇌HCO- +OH-、HCO +HO
2 3 3 2 3 2
⇌HCO+OH-;
2 3
④AlCl 中铝离子水解:Al3++3HO⇌Al(OH) +3H+。
3 2 3