文档内容
3.1.1 强电解质和弱电解质 弱电解质的电离平衡(学案)
1.能用平衡移动原理分析沉淀的溶解与生成、沉淀转化的实质,并会解决生产、生活中的实
际问题。
2.明确溶度积和离子积的关系,学会判断反应进行的方向。
1.沉淀转化的实质。
向氯化银的饱和溶液中加入浓硝酸银溶液,现象为:_______________。
知识点一、沉淀溶解平衡的应用
1.沉淀的生成
(1)调节pH法:
如加入氨水调节pH=4,可除去氯化铵中的杂质氯化铁。
反应离子方程式:________________________。
(2)加沉淀剂法:
以NaS、HS等作沉淀剂,使Cu2+、Hg2+等生成极难溶的硫化物CuS、HgS等沉淀。反应离子
2 2
方程式如下:
①加NaS生成CuS:________________________。
2
②通入HS生成CuS:________________________。
2
2.沉淀的溶解
(1)原理:根据平衡移动原理,对于在水中难溶的电解质,只要不断溶解平衡体系中的相应离子,
平衡就向________________________的方向移动,从而使沉淀溶解。
(2)实例:①CaCO 沉淀溶于盐酸中:
3
CO 2-+2H+→CO +H O
3 2 2
CO 气体的生成和逸出,使CaCO 溶解平衡体系中的CO2-浓度不断减小,平衡向______的方向移
2 3 3
动。②分别写出用HCl溶解难溶电解质FeS、Al(OH) 、Cu(OH) 的离子方程式
3 2
FeS+2H+===Fe+H S、Al(OH) +3H+===Al3++3H O
2 3 2
Cu(OH) +2H+===Cu2++2H O
2 2
③向Mg(OH) 悬浊液中分别滴加蒸馏水、稀盐酸、NH Cl溶液,白色沉淀将______、________、
2 4
________(填“溶解”或“不溶解”)。
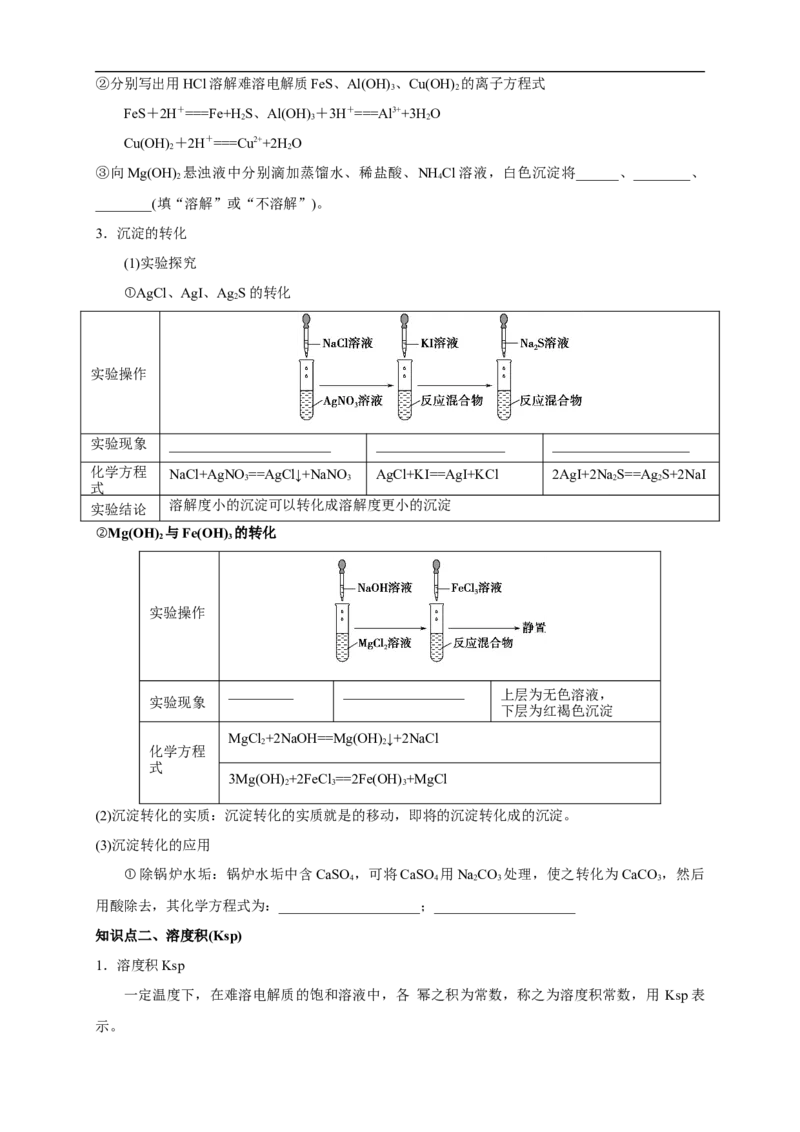
3.沉淀的转化
(1)实验探究
①AgCl、AgI、Ag S的转化
2
实验操作
实验现象 ____________________ ________________ _________________
化学方程 NaCl+AgNO ==AgCl↓+NaNO AgCl+KI==AgI+KCl 2AgI+2Na S==Ag S+2NaI
3 3 2 2
式
溶解度小的沉淀可以转化成溶解度更小的沉淀
实验结论
②Mg(OH) 与Fe(OH) 的转化
2 3
实验操作
________ _______________ 上层为无色溶液,
实验现象
下层为红褐色沉淀
MgCl +2NaOH==Mg(OH) ↓+2NaCl
2 2
化学方程
式
3Mg(OH) +2FeCl ==2Fe(OH) +MgCl
2 3 3
(2)沉淀转化的实质:沉淀转化的实质就是的移动,即将的沉淀转化成的沉淀。
(3)沉淀转化的应用
①除锅炉水垢:锅炉水垢中含CaSO ,可将CaSO 用NaCO 处理,使之转化为CaCO ,然后
4 4 2 3 3
用酸除去,其化学方程式为:____________________;____________________
知识点二、溶度积(Ksp)
1.溶度积Ksp
一定温度下,在难溶电解质的饱和溶液中,各 幂之积为常数,称之为溶度积常数,用 Ksp表
示。2.表达式:AmBn(s)⇌mAn+(aq)+nBm—(aq),Ksp=____________________
例如:Ag SO 的溶度积常数为:Ksp(Ag SO )=____________________
2 4 2 4
3.影响因素
4.溶度积Ksp与离子积Qc的关系
例如:Ag SO 的离子积为:Qc(Ag SO )=____________________
2 4 2 4
通过比较溶度积与溶液中有关离子浓度幂的乘积——离子积 Qc的相对大小,可以判断难溶电
解质在给定条件下沉淀能否生成或溶解。
(1)Qc________Ksp,溶液过饱和,有沉淀析出,直至溶液饱和达到新的平衡;
(2)Qc________Ksp,溶液饱和,沉淀与溶解处于平衡状态;
(3)Qc________Ksp,溶液未饱和,无沉淀析出,若加入过量难溶电解质,难溶电解质溶解直至
溶液饱和。
【练习】1.已知25℃时,AgCl的溶度积K =l.8×10﹣10,则下列说法不正确的是( )
sp
A.温度一定时,当溶液中c(Ag+)•c(Cl﹣)=K 时,此溶液中必有AgCl的沉淀析出
sp
B.AgNO 溶液与NaCl溶液混合后的溶液中,可能有c(Ag+)=c(Cl﹣)
3
C.向饱和AgCl水溶液中加入盐酸,K 不变
sp
D.将AgCl加入到较浓的KI溶液中,部分AgCl可以转化为Agl
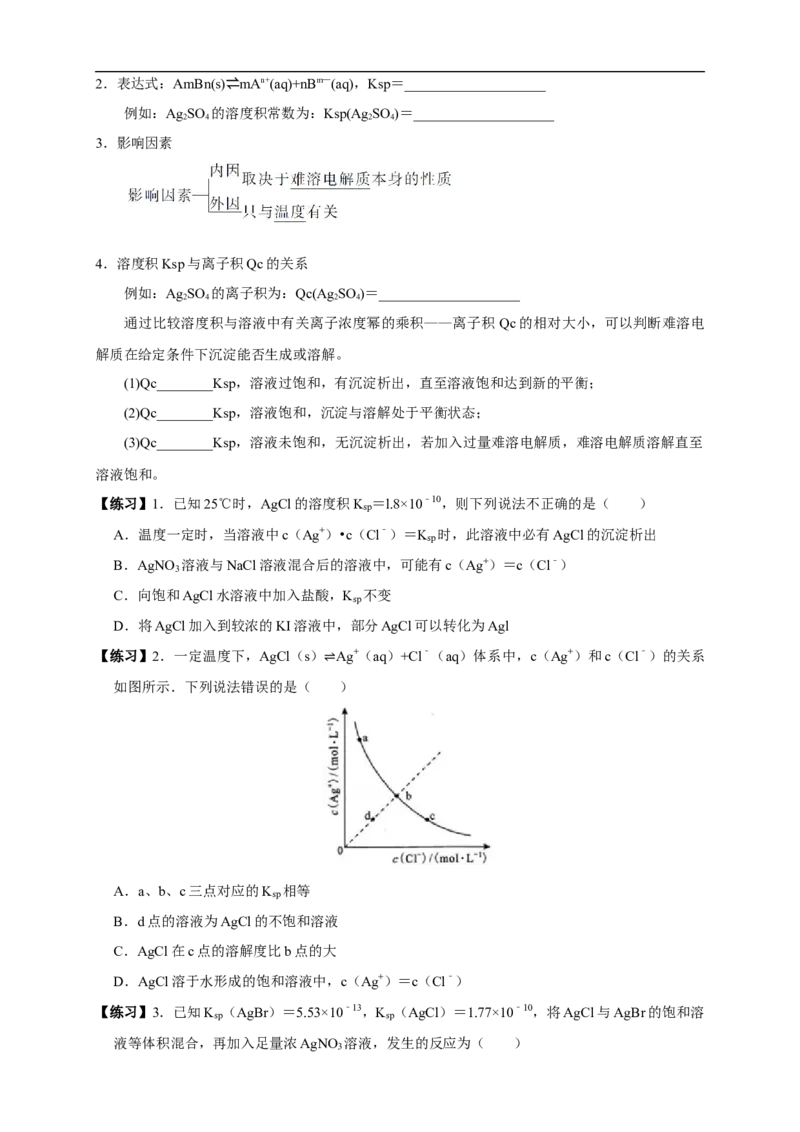
【练习】2.一定温度下,AgCl(s) Ag+(aq)+Cl﹣(aq)体系中,c(Ag+)和c(Cl﹣)的关系
如图所示.下列说法错误的是( ⇌ )
A.a、b、c三点对应的K 相等
sp
B.d点的溶液为AgCl的不饱和溶液
C.AgCl在c点的溶解度比b点的大
D.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl﹣)
【练习】3.已知K (AgBr)=5.53×10﹣13,K (AgCl)=1.77×10﹣10,将AgCl与AgBr的饱和溶
sp sp
液等体积混合,再加入足量浓AgNO 溶液,发生的反应为( )
3A.只有AgBr沉淀生成
B.AgCl和AgBr沉淀等量生成
C.AgCl和AgBr沉淀都有,但以AgCl沉淀为主
D.AgCl和AgBr沉淀都有,但以AgBr沉淀为主
【练习】4.已知部分铅盐的溶度积如表,从溶度积角度分析,沉淀 Pb2+ 时的最佳沉淀剂为(
)
化合物 PbSO PbCO PbS PbCrO
4 3 4
K 1.8×10﹣8 7.4×10﹣14 8.0×10﹣28 2.8×10﹣13
sp
A.硫酸盐 B.碳酸盐 C.硫化物 D.铬酸盐
【练习】5.常温下,K [Fe(OH) ]=4.0×10﹣38,在pH=4的Fe(OH) 饱和溶液中,c(Fe3+)
sp 3 3
为( )
A.1.0×10﹣8mol•L﹣1 B.4.0×10﹣8mol•L﹣1
C.1.0×10﹣26mol•L﹣1 D.1.3×10﹣28mol•L﹣1
【练习】6.25℃时,下列4种盐的溶度积常数(K )分别是如表,结合相关数据分析,下列说法
sp
错误的是( )
Ag SO (白色) Ag S(黑色) FeS(黑色) MnS(肉色)
2 4 2
1.4×10﹣5mol3•L﹣3 6.3×10﹣50mol3•L﹣3 3.3×10﹣18mol2•L﹣2 2.5×10﹣13mol2•L﹣2
A.除去某溶液中的Ag+用Na S溶液比Na SO 溶液效果好
2 2 4
B.25℃时,MnS的溶解度大于FeS的溶解度
C.向少量FeS悬浊液中加入足量饱和MnCl 溶液,沉淀颜色会由黑色变为肉色
2
D.向Ag S(s) 2Ag+(aq)+S2﹣(aq)平衡体系中加入少量Na S固体,溶液中c(Ag+)不
2 2
变 ⇌
【练习】7.取1mL 0.1mol•L﹣1AgNO 溶液进行如下实验(实验中所用试剂浓度均为 0.1mol•L﹣
3
1),下列说法不正确的是( )
A.实验 白色沉淀是难溶的AgCl
B.若按① 顺序实验,能看到白色沉淀
C.若按②①顺序实验,能看到黑色沉淀
D.由实①验③说明AgI比AgCl更难溶
②【练习】8.难溶电解质在水中达到沉淀溶解平衡时,下列说法中不正确的( )
A.溶液中不存在难溶电解质离子
B.沉淀的速率和溶解的速率相等
C.继续加入难溶电解质,溶液中各离子浓度不变
D.一定条件下可以转化为更难溶的物质
1.向含有MgCO 固体的浊液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
3
A.c(Mg2+) B.K (MgCO ) C.c(H+) D.c(CO 2﹣)
sp 3 3
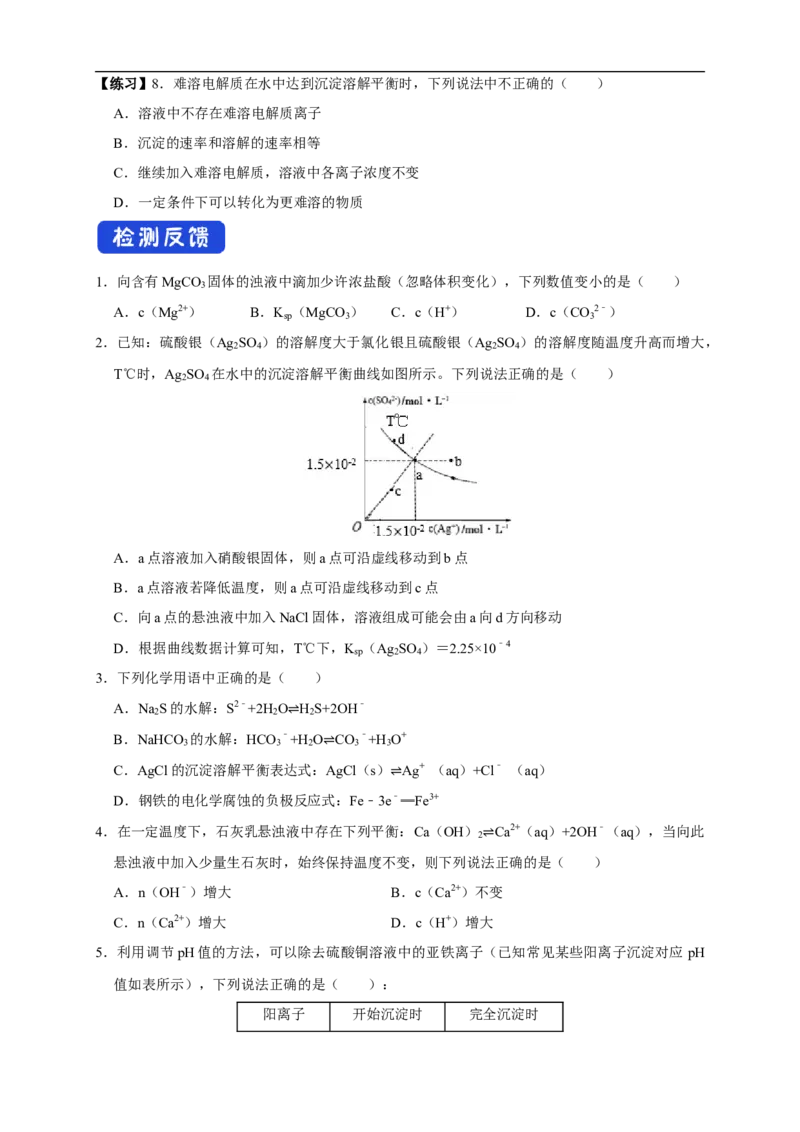
2.已知:硫酸银(Ag SO )的溶解度大于氯化银且硫酸银(Ag SO )的溶解度随温度升高而增大,
2 4 2 4
T℃时,Ag SO 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
2 4
A.a点溶液加入硝酸银固体,则a点可沿虚线移动到b点
B.a点溶液若降低温度,则a点可沿虚线移动到c点
C.向a点的悬浊液中加入NaCl固体,溶液组成可能会由a向d方向移动
D.根据曲线数据计算可知,T℃下,K (Ag SO )=2.25×10﹣4
sp 2 4
3.下列化学用语中正确的是( )
A.Na S的水解:S2﹣+2H O H S+2OH﹣
2 2 2
B.NaHCO 的水解:HCO ﹣ ⇌+H O CO ﹣+H O+
3 3 2 3 3
C.AgCl的沉淀溶解平衡表达式:⇌AgCl(s) Ag+ (aq)+Cl﹣ (aq)
D.钢铁的电化学腐蚀的负极反应式:Fe﹣3e⇌ ﹣═Fe3+
4.在一定温度下,石灰乳悬浊液中存在下列平衡:Ca(OH) Ca2+(aq)+2OH﹣(aq),当向此
2
悬浊液中加入少量生石灰时,始终保持温度不变,则下列说法⇌正确的是( )
A.n(OH﹣)增大 B.c(Ca2+)不变
C.n(Ca2+)增大 D.c(H+)增大
5.利用调节pH值的方法,可以除去硫酸铜溶液中的亚铁离子(已知常见某些阳离子沉淀对应 pH
值如表所示),下列说法正确的是( ):
阳离子 开始沉淀时 完全沉淀时Fe3+ 2.7 3.7
Cu2+ 4.4 6.4
Fe2+ 7.6 9.6
A.调节pH值前,应先将Fe2+氧化为Fe3+,可选择Cl 或H O 作为氧化剂
2 2 2
B.调节pH值可选用Cu(OH) 或Cu(OH) CO
2 2 3
C.调节pH值控制在pH=6.4~7.6效果最好
D.将分离得到硫酸铜溶液蒸干可获得Cu(OH) 固体
2
6.已知:常温下,K (Ag X)=1.4×10﹣5,K (Ag Y)=8.1×10﹣12,K (AgZ)=1.8×10﹣10,
sp 2 sp 2 sp
K (AgR)=8.3×10﹣17.在下列各饱和溶液中,c(Ag+)由小到大的排序是( )
sp
A.AgR<Ag Y<Ag X<AgZ B.AgR<AgZ<Ag Y<Ag X
2 2 2 2
C.AgZ<AgR<Ag X<Ag Y D.AgR<Ag Y<AgZ<Ag X
2 2 2 2
7.工业生产中常用MnS作为沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s) CuS(s)
+Mn2+(aq),下列说法正确的是( ) ⇌
A.该反应达到平衡时,c(Mn2+)=c(Cu2+)
B.该反应达到平衡时,K (CuS)较大
sp
C.往平衡体系中加入少量CuSO 固体后,c(Mn2+)减小
4
D.该反应的平衡常数K=
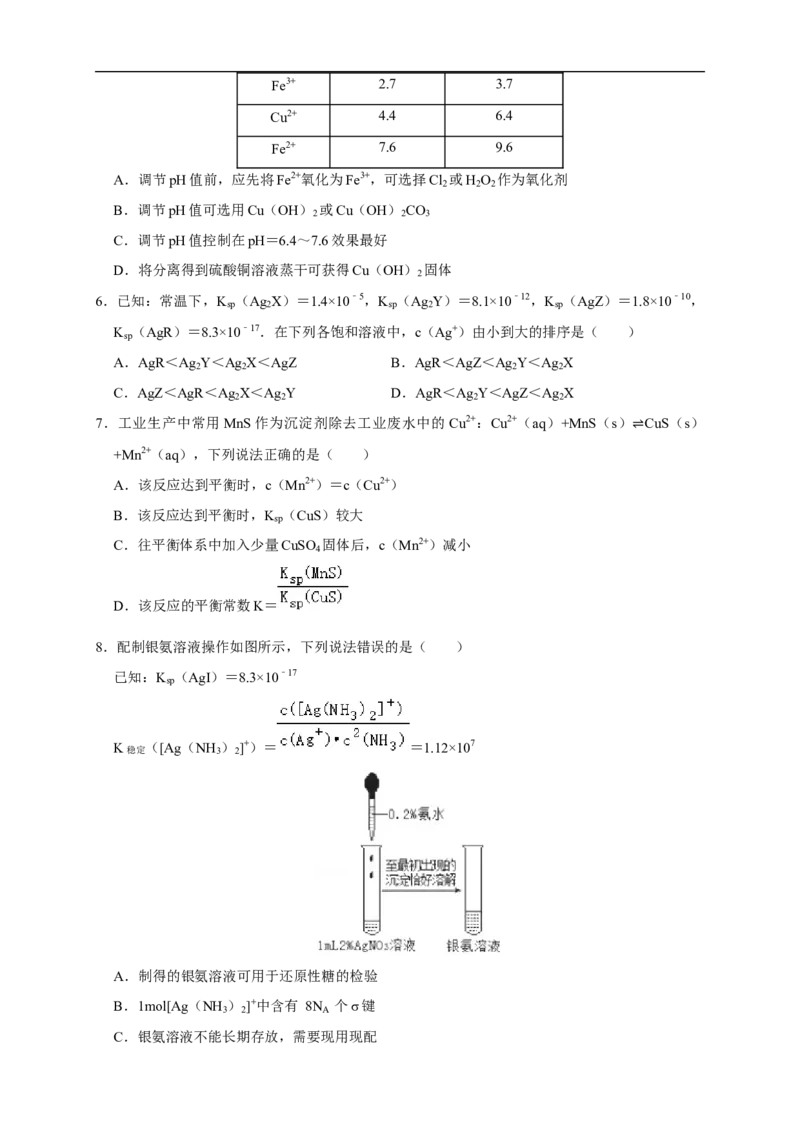
8.配制银氨溶液操作如图所示,下列说法错误的是( )
已知:K (AgI)=8.3×10﹣17
sp
K稳定 ([Ag(NH
3
)
2
]+)= =1.12×107
A.制得的银氨溶液可用于还原性糖的检验
B.1mol[Ag(NH
3
)
2
]+中含有 8N
A
个σ键
C.银氨溶液不能长期存放,需要现用现配D.AgI 固体可溶于氨水得到银氨溶液
【课前复习答案】产生白色沉淀
【知识点填空答案】
Fe3++3NH.H O==Fe(OH) ↓+3NH+;S2-+Cu2+==CuS↓;HS+Cu2+==CuS↓+2H+;沉淀溶解;碳酸钙
3 2 3 2
溶解;溶解;溶解;溶解;有白色沉淀生成;白色沉淀转化为黄色沉淀;黄色沉淀转化为黑色沉淀;
产生白色沉淀;产生红褐色沉淀;CaSO+Na CO==CaCO+Na SO ;CaCO +2H+==Ca2++CO +H O;
4 2 3 3 2 4 3 2 2
Ksp=cm(An+)·cn(Bm-);Ksp(Ag SO )=c2(Ag+)·c (SO 2-);Qc(Ag SO )=c2(Ag+)·c (SO 2-);>;=;
2 4 4 2 4 4
<
【练习答案】ACCCBDBA
【检测反馈答案】DCCBBBDD