文档内容
第三章 铁 金属材料
第二节 金属材料 课时作业
专题 铝及其化合物的转化及图像
基础达标
1.下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
A.K B.Na
C.Fe D.Al
2.有关Al与NaOH溶液反应的说法中,正确的是( )
A.铝是还原剂,其还原产物是Na[Al(OH) ]
4
B.NaOH是氧化剂,其还原产物是H
2
C.铝是还原剂,HO和NaOH都是氧化剂
2
D.HO是氧化剂,Al被氧化
2
3.下列关于铝及其化合物的说法不正确的是( )
A.铝的化学性质不活泼
B.Al(OH) 既能与NaOH溶液反应,也能与盐酸反应
3
C.明矾可用于净水
D.铝合金的硬度比纯铝大
4.下列试剂可除去镁粉中混有的少量铝粉的是( )
A.稀盐酸 B.NaOH溶液
C.BaCl 溶液 D.浓硝酸
2
5.铝、氧化铝、氢氧化铝和硫酸铝与过量强碱溶液的反应,其生成物有一定的规律,
下列说法中正确的是( )
A.都有HO生成 B.都有H 生成
2 2
C.都有[Al(OH) ]-生成 D.都有Al3+生成
4
6.在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸
没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是(
)
A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡B.铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,溶液蓝色变浅,杠
杆右边下沉
C.反应后去掉两烧杯,杠杆仍平衡
D.右边球上出现红色,左边溶液的c(OH-)增大
7.通过一步反应不能实现的是( )
A.Al O→Al(OH) B.Al3+→Al(OH)
2 3 3 3
C.Fe(OH) →Fe(OH) D.FeCl →FeCl
2 3 3 2
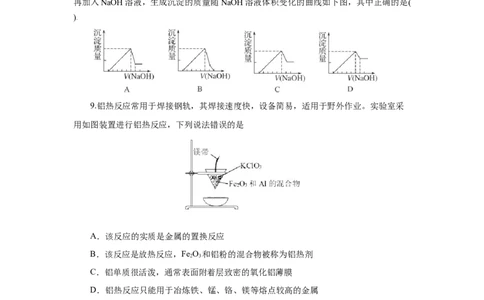
8.有一块镁铝合金,其中镁与铝的质量比是8∶9。加入足量稀HSO 使其完全溶解后,
2 4
再加入NaOH溶液,生成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是(
)
9.铝热反应常用于焊接钢轨,其焊接速度快,设备简易,适用于野外作业。实验室采
用如图装置进行铝热反应,下列说法错误的是
A.该反应的实质是金属的置换反应
B.该反应是放热反应,Fe O 和铝粉的混合物被称为铝热剂
2 3
C.铝单质很活泼,通常表面附着层致密的氧化铝薄膜
D.铝热反应只能用于冶炼铁、锰、铬、镁等熔点较高的金属
10.室温下,在0.2 mol·L-1 Al (SO ) 溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实
2 4 3
验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是( )
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH- Al(OH)
3B.a~b段,溶液pH增大,Al3+浓度不变
C.b~c段,加入的OH-主要用于生成Al(OH) 沉淀
3
D.d点时,Al(OH) 沉淀开始溶解
3
能力提升
11.下列说法正确的是( )
A.向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成
2 3
B.制备Al(OH) 悬浊液:向1 mol·L-1 AlCl 溶液中加过量的6 mol·L-1 NaOH溶液
3 3
C.AlCl 溶液中加入过量稀氨水:Al3++4NH ·H O===[Al(OH) ]-+4NH
3 3 2 4
D.将AlCl 加入Ba(HCO ) 溶液中同时有气体和沉淀产生
3 3 2
12.向含NaCO、NaAl(OH) ]的混合溶液中逐滴加入150 mL 1 mol·L-1 HCl溶液,测得
2 3 4
溶液中的某几种离子物质的量的变化如图所示,则下列说法中不正确的是( )
A.a曲线表示的离子方程式为Al(OH) ]-+H+===Al(OH) ↓+HO
4 3 2
B.b和c曲线表示的离子反应是相同的
C.M点时,溶液中沉淀的质量为3.9 g
D.原混合溶液中的CO与Al(OH) ]-的物质的量之比为1∶2
4
13.将一定质量的Mg和Al的混合物投入250mL2.0mol·L-1的稀硫酸中,固体全部溶解
并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入
NaOH溶液体积的关系如图所示。则下列说法正确的是( )
A.当加入氢氧化钠溶液的体积为20mL时,溶液的pH等于7
B.当加入氢氧化钠溶液的体积为20mL时,溶液中的溶质只有硫酸镁和硫酸铝
C.NaOH溶液的物质的量浓度为5mol·L-1
D.生成的H 在标准状况下的体积为10.08L
2
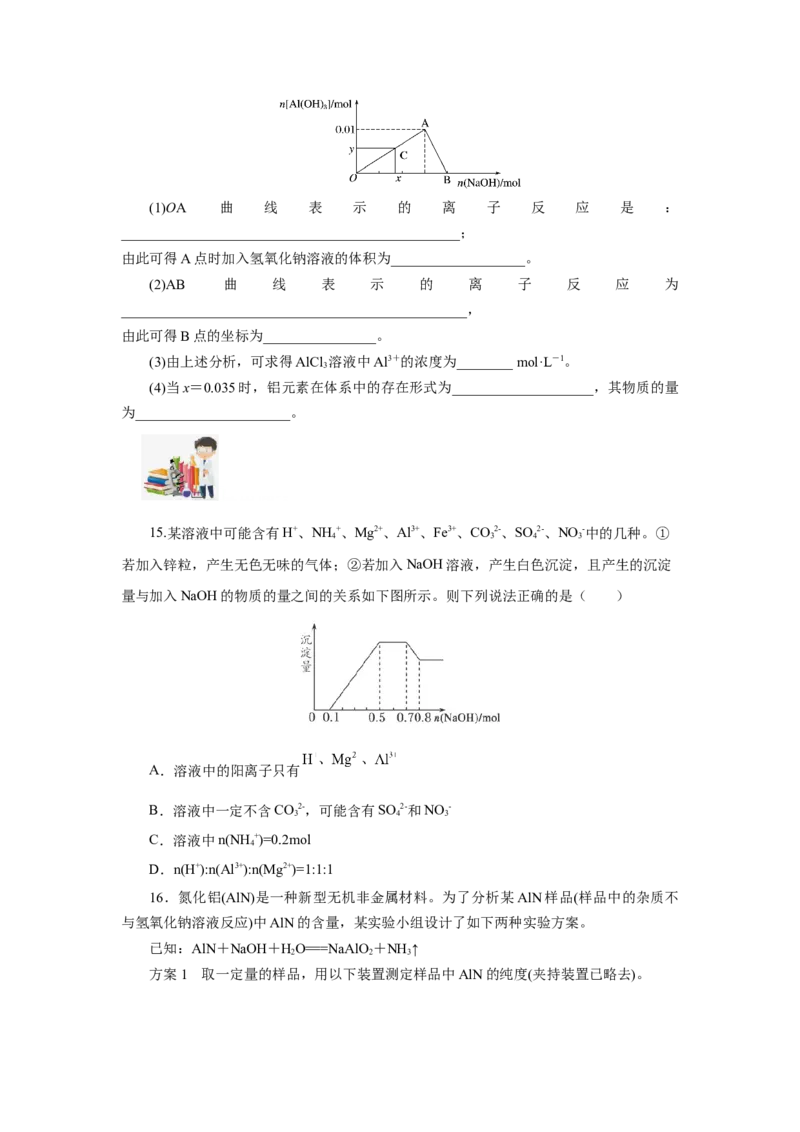
14.将3 mol·L-1 NaOH溶液滴入到25 mL一定浓度的AlCl 溶液中。下图是整个过程的
3
数学分析曲线。其中横轴表示加入OH-的物质的量,纵轴表示产生的Al(OH) 沉淀的物质
3
的量。据图回答:(1)OA 曲 线 表 示 的 离 子 反 应 是 :
________________________________________________;
由此可得A点时加入氢氧化钠溶液的体积为___________________。
(2)AB 曲 线 表 示 的 离 子 反 应 为
_________________________________________________,
由此可得B点的坐标为________________。
(3)由上述分析,可求得AlCl 溶液中Al3+的浓度为________ mol·L-1。
3
(4)当x=0.035时,铝元素在体系中的存在形式为____________________,其物质的量
为______________________。
直击高考
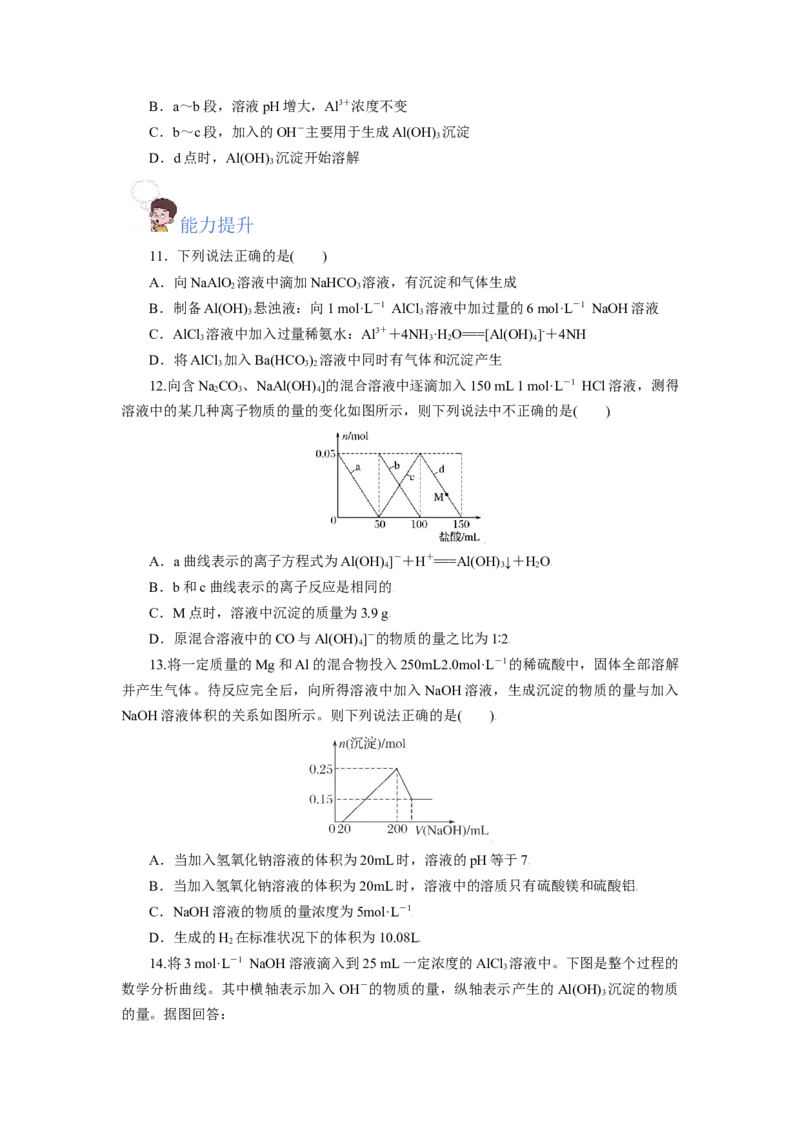
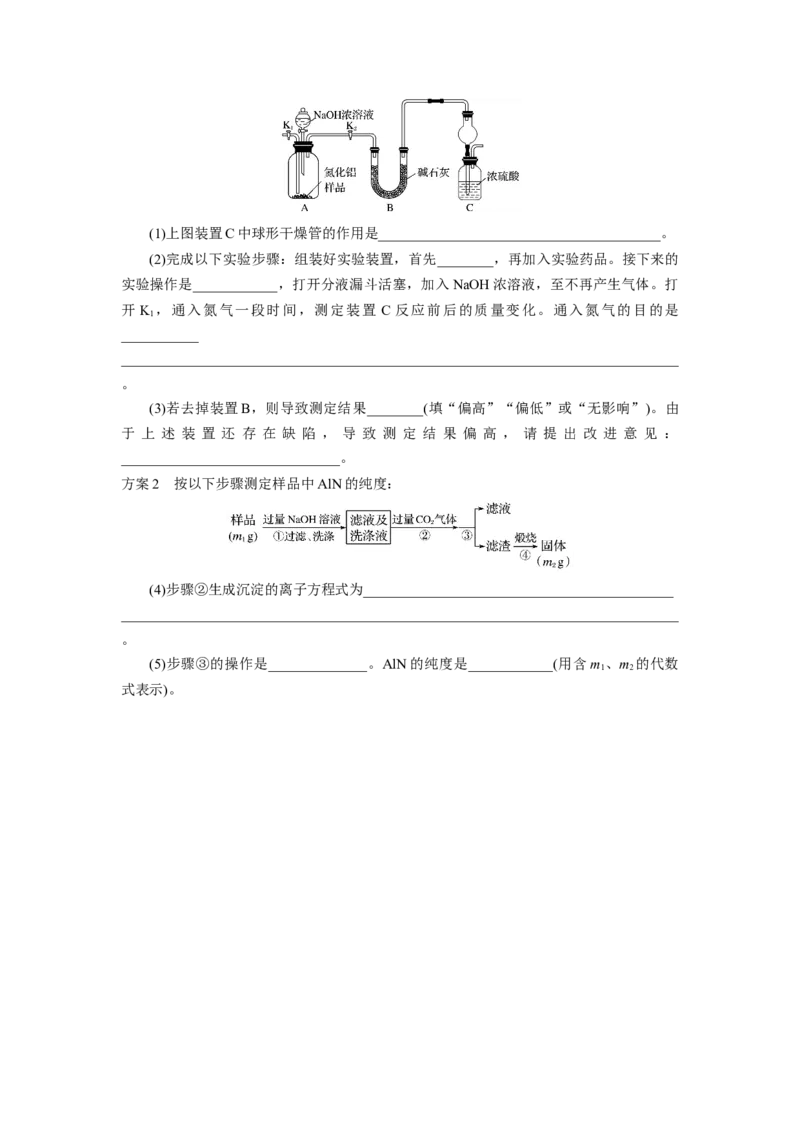
15.某溶液中可能含有H+、NH +、Mg2+、Al3+、Fe3+、CO2-、SO 2-、NO -中的几种。①
4 3 4 3
若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀
量与加入NaOH的物质的量之间的关系如下图所示。则下列说法正确的是( )
A.溶液中的阳离子只有
B.溶液中一定不含CO2-,可能含有SO 2-和NO -
3 4 3
C.溶液中n(NH +)=0.2mol
4
D.n(H+):n(Al3+):n(Mg2+)=1:1:1
16.氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不
与氢氧化钠溶液反应)中AlN的含量,某实验小组设计了如下两种实验方案。
已知:AlN+NaOH+HO===NaAlO+NH ↑
2 2 3
方案1 取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。(1)上图装置C中球形干燥管的作用是________________________________________。
(2)完成以下实验步骤:组装好实验装置,首先________,再加入实验药品。接下来的
实验操作是____________,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打
开 K ,通入氮气一段时间,测定装置 C 反应前后的质量变化。通入氮气的目的是
1
___________
_______________________________________________________________________________
。
(3)若去掉装置B,则导致测定结果________(填“偏高”“偏低”或“无影响”)。由
于 上 述 装 置 还 存 在 缺 陷 , 导 致 测 定 结 果 偏 高 , 请 提 出 改 进 意 见 :
_______________________________。
方案2 按以下步骤测定样品中AlN的纯度:
(4)步骤②生成沉淀的离子方程式为____________________________________________
_______________________________________________________________________________
。
(5)步骤③的操作是______________。AlN的纯度是____________(用含m 、m 的代数
1 2
式表示)。