文档内容
课题: 元素(第二课时)
一、学习目标:
1.知道元素符号所表示的意义
2学会元素符号的正确写法,逐步记住一些常见的元素符号。
重点,难点:元素符号的意义
【课前知识积累】
熟悉读写常见的元素及元素名称
【情境导入】
你知道英语中的26个字母吗?化学物质都是由元素组成的,元素有国际统一符号吗?
二、自主探究:
知识点二:元素符号
【阅读】阅读课本61-62页,完成下列问题:
1.为什么要使用元素符号?国际上对元素符号是怎样规定的?
2.识记课本62页常见的元素名称和符号。写一写看你记住了几个?
3.书写元素符号时应注意什么?
4.一个元素符号能表示几个涵义?
【填空】1.元素符号:国际上统一用来表示元素的一种特定的化学符号。来源于拉丁文。
(1)书写:“一 二 ”
①由一个字母表示的元素符号要 ;
②由两个字母表示的元素符号,第一个字母要 ,第二个字母要
(2)意义:宏观表示一种元素;微观表示这种元素的一个原子。
Fe表示 ;也可以表示
■如果在元素符号前面添上系数,就只表示该元素原子个数,不能表示该元素。
如:H既表示氢元素,又表示一个氢原子;2H只能表示两个氢原子。
【思考交流】
1.P、5P分别表示什么意义?
2.下列两组符号能组成几种元素的符号?Ⅰ:A B C M N Ⅱ:a u e l g
知识点三:元素周期表
【阅读】课本62-63页,完成下列填空:
1.周期表每一横行叫做一个 ,共有7个横行,有7个周期。周期表的18个纵行中(8、9、10三个
纵行),其余15个纵行,每一个纵行叫做一 ,共有16个族。每一横行随着 的递增,开头是
元素(第一周期除外),靠近尾部的是 元素,结尾的是 元素。
2.元素周期表按元素原子核电荷数递增的顺序给元素编了号,叫做_________,________ 与元素原子
核电荷数在数值上相同。
3.从一个元素符号图片你可以获得的信息是:(以铁为例)元素名称 ;元素的
种类 ;元素符号 ;相对原子质量 ;原子序数 ;原子核电荷数 ;
质子数 ;原子的电子数 。
【交流讨论】1.完成课本63页“探究”中的内容。
2.同桌互相检查元素符号的记忆情况。
【课堂小结】通过本节课的学习,你收获了什么?
【我的收获】
1三、自我测评(1-5为必做,6为选做,7为思考)
1、表示4个氢原子的符号是( ) A. 4H B 4H C. 2H D.H
2 2 4
2.下列各组元素符号的第一个字母相同的是( )
A.铁、锌、钠 B.钙、铝、铜 C.铝、银、镁 D.碳、钙、氯
3. 下图是元素周期表中的一格,依据图中的信息得到的下列认识错误的是( )
14 Si
A.该元素原子的质子数为14 B.该元素属于非金属元素
硅
C.该元素一个原子的原子核外有14个电子 D.该元素的相对原子质量为28.09 28.09
4、硒元素的部分信息如右下图,则下列说法中正确的是 。
A.硒元素的相对原子质量为78.96g
B.一个硒原子中有34个中子
C.硒原子结构示意图中的X=18
D.硒元素一个硒原子中有 个质子
5、元素周期表是化学学习和科学研究的重要工具,下列对于元素周期表的使用方法不正确的是 ( )
A.查阅元素的相对原子质量 B.在元素周期表中查找该元素的元素符号及元素名称
C.利用元素周期表中的元素任意组合成我们希望得到的新物质 D确定元素的种类.
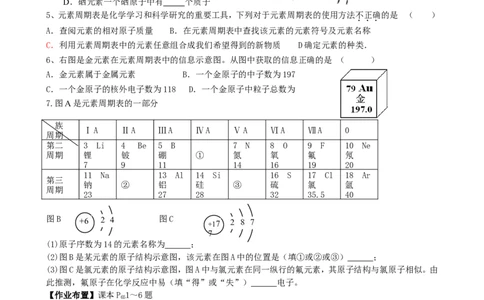
6、右图是金元素在元素周期表中的信息示意图。从图中获取的信息正确的是 ( )
A.金元素属于金属元素 B.一个金原子的中子数为197
C.一个金原子的核外电子数为118 D.一个金原子中粒子总数为
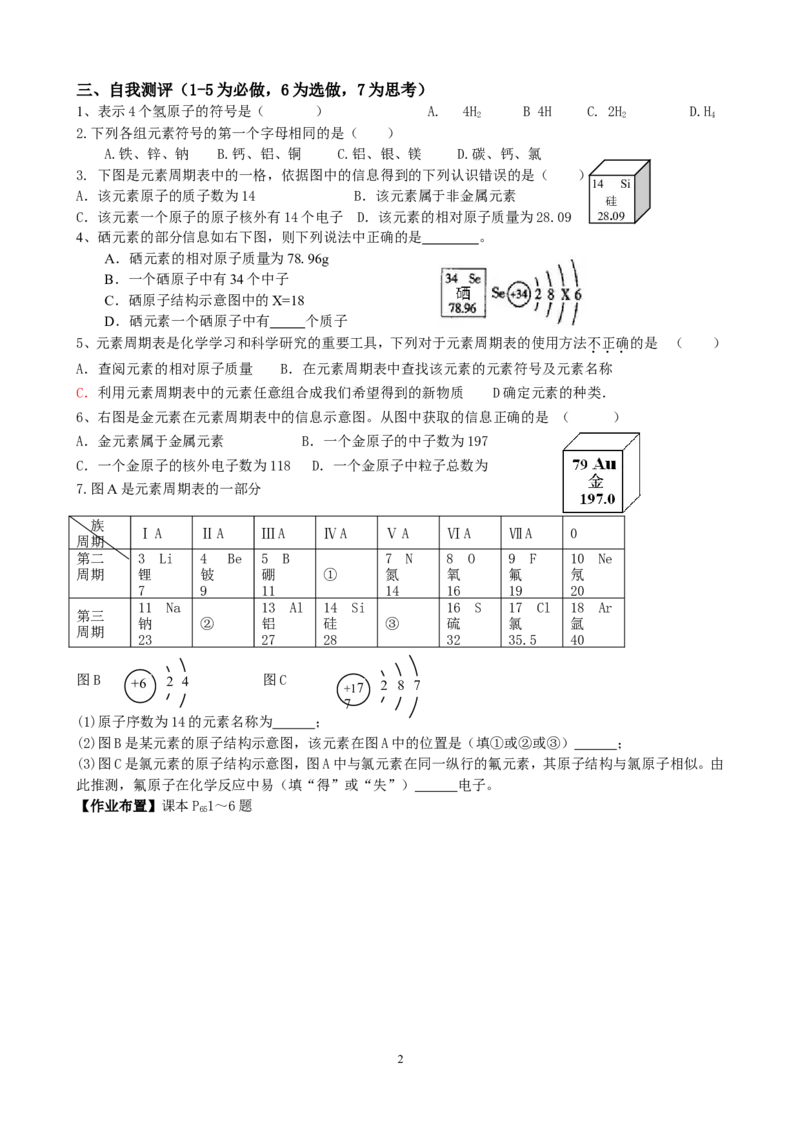
7.图A是元素周期表的一部分
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
第二 3 Li 4 Be 5 B 7 N 8 O 9 F 10 Ne
周期 锂 铍 硼 ① 氮 氧 氟 氖
7 9 11 14 16 19 20
11 Na 13 Al 14 Si 16 S 17 Cl 18 Ar
第三
钠 ② 铝 硅 ③ 硫 氯 氩
周期
23 27 28 32 35.5 40
图B + 6 2 4 图C +17 2 8 7
7
(1)原子序数为14的元素名称为 ;
(2)图B是某元素的原子结构示意图,该元素在图A中的位置是(填①或②或③) ;
(3)图C是氯元素的原子结构示意图,图A中与氯元素在同一纵行的氟元素,其原子结构与氯原子相似。由
此推测,氟原子在化学反应中易(填“得”或“失”) 电子。
【作业布置】课本P 1~6题
65
2